18 серпня, 2021
Ліраглутид у лікуванні ожиріння: огляд і практичні рекомендації
Ожиріння – це хронічне поліетіологічне, зі схильністю до рецидиву метаболічне захворювання, пов’язане з низкою ризиків для здоров’я і серйозними ускладненнями. Незважаючи на те що воно поширене в усьому світі, його недостатньо діагностують і лікують. Як фізіологічний регулятор апетиту і споживання енергії, аналог глюкагоноподібного пептиду‑1 (аГГП‑1) – ліраглутид 3,0 мг схвалений для контролю ваги в осіб з її надлишком або ожирінням. У цій статті представлено огляд клінічних даних ефективності й безпеки використання ліраглутиду 3,0 мг, а також практичні поради щодо застосування препарату.
Ключові слова: метаболічне захворювання, ожиріння, лікування ожиріння, ліраглутид
Ожиріння часто пов’язане зі структурними і функціональними відхиленнями, які збільшують ризики для здоров’я і призводять до серйозних ускладнень. В усьому світі ожиріння є важливою проблемою громадського здоров’я.
Зазвичай оцінку ожиріння в клінічних умовах проводять за допомогою визначення індексу маси тіла (ІМТ). Цей показник відображає наявні ризики для здоров’я і життя пацієнта на рівні популяції. Наприклад, було показано, що при ІМТ >30 кг/м2 тривалість життя зменшується зі збільшенням ІМТ, а при ІМТ 40-45 кг/м2 медіана виживаності знижується на 8-10 років. Дані про смертність мають епідеміологічну значимість і вказують, що ризик смерті пов’язаний із вищим ІМТ, але ці дані не можна застосовувати до окремих пацієнтів.
Також ожиріння асоційоване з різними серйозними ускладненнями, зокрема з розвитком цукрового діабету (ЦД) 2 типу, деяких видів злоякісних пухлин, серцево-судинних захворювань (ССЗ), артеріальної гіпертензії (АГ), неалкогольної жирової хвороби печінки (НАЖХП), апное уві сні, астми, хвороби жовчного міхура, остеоартрозу нижніх кінцівок, депресії і тривожних розладів, а також із порушеннями фертильності, синдромом полікістозних яєчників (СПКЯ) і зниженням якості життя.
У настановах, розроблених Американською асоціацією клінічних ендокринологів і Американським коледжем ендокринології (AACE/ACE), особам з ІМТ ≥25 кг/м2 (або ≥23 кг/м2 у дорослої популяції з Південної, Південно-Східної і Східної Азії) рекомендується щороку проходити скринінг на наявність і тяжкість ускладнень, пов’язаних з ожирінням.
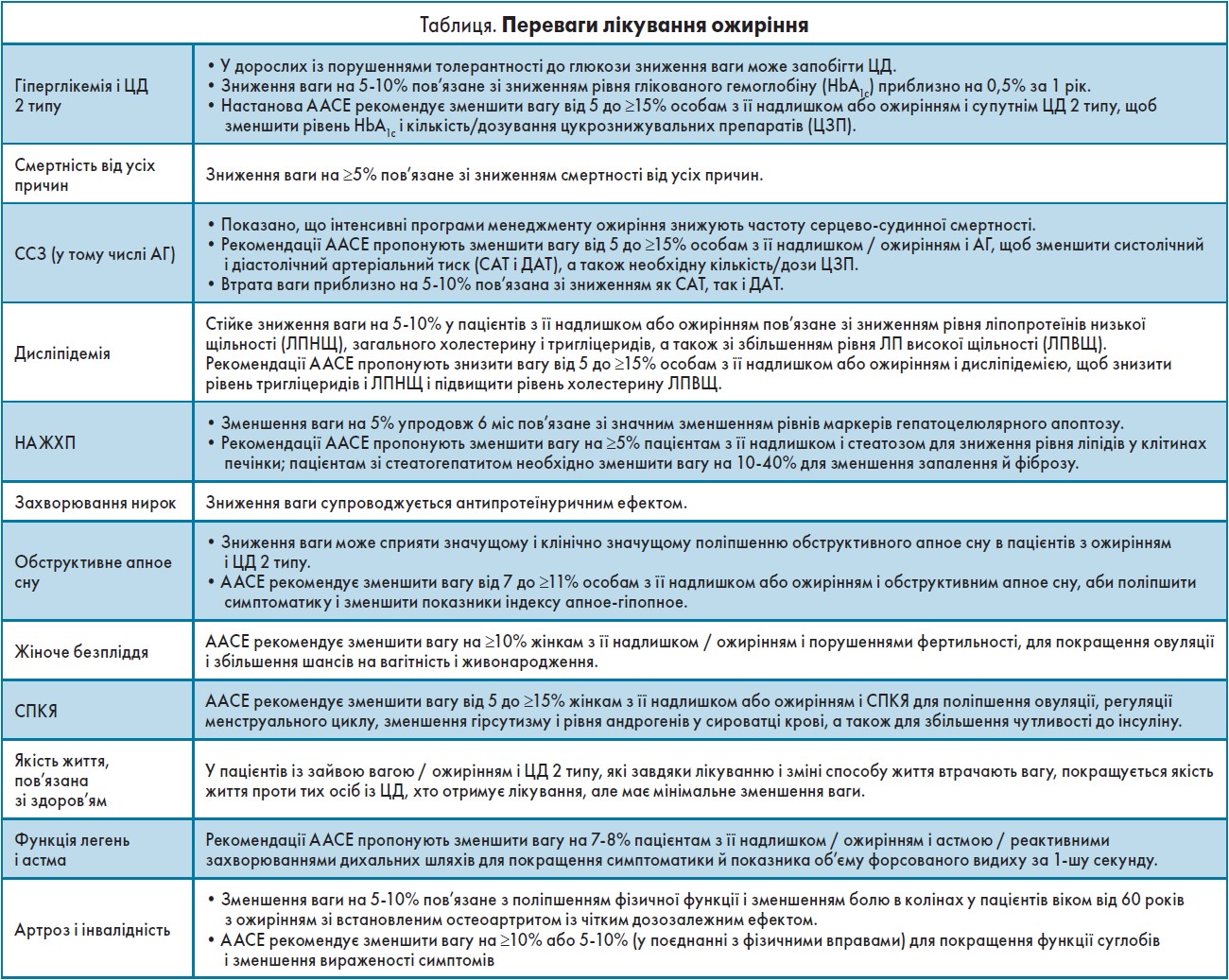
Важливо, що навіть незначне зниження ваги (наприклад, на 5-10%) може мати клінічно значущий вплив на стан здоров’я людини (у тому числі на зменшення гіперліпідемії, гіперглікемії, гіпертонії та апное уві сні) і суттєво покращує якість життя (табл.).
Сучасні настанови щодо лікування ожиріння пропонують низку втручань залежно від ступеня ожиріння, які мають забезпечувати зниження ваги і зменшення довгострокових ризиків для здоров’я пацієнта. Основні рекомендації стосуються модифікації способу життя, а саме зміни харчування і фізичної активності, при цьому фармакотерапія розглядається в осіб з ІМТ ≥27 кг/м2 і супутніми ускладненнями, а також при ІМТ ≥30 кг/м2 без ускладнень. Пацієнтам з ІМТ ≥35 кг/м2 і тяжкими ускладненнями часто рекомендують баріатричну хірургію.
На жаль, зменшення ваги в результаті зміни способу життя часто супроводжується уповільненням швидкості метаболізму в спокої, оскільки організм намагається збалансувати невідповідність між надходженням і витратами енергії. Цей процес відомий як метаболічна адаптація.
Як наслідок, модифікація способу життя далеко не завжди сприяє значущому зменшенню ваги в довгостроковій перспективі – навіть за умови радикальної корекції свого життя. Наприклад, у дослідженні Look AHEAD 33% учасників не досягли мети зменшення ваги на ≥5% упродовж року. До того ж набагато менше пацієнтів дотримуються лікування препаратами проти ожиріння впродовж ≥6 міс, якщо порівняти з тими, хто використовує гіпотензивні засоби або препарати, що знижують рівень холестерину.
Низька частота призначення фармацевтичного лікування ожиріння може бути пов’язана з недостатньою інформованістю щодо ефективності і довгострокової безпеки препаратів.
АГПП‑1 – це клас терапевтичних засобів, які імітують ендогенний ГПП‑1. Вони були розроблені для поліпшення контролю глікемії, тому низку аГПП‑1 схвалено для лікування ЦД 2 типу. Однак ГПП‑1 діє також як фізіологічний регулятор апетиту і споживання енергії.
Завдяки численним метаболічним ефектам аГПП‑1 можуть відігравати важливу роль як частина мультимодальної довгострокової стратегії лікування ожиріння. Ліраглутид 3,0 мг – єдиний препарат цього класу, дозволений сьогодні для довгострокового контролю ваги.
ГПП‑1 і його аналоги
ГПП‑1 є членом родини гормонів інкретинів і виробляється в шлунково-кишковому тракті (ШКТ) у відповідь на надходження їжі. ГПП‑1 переважно секретується L-клітинами в кишечнику, але може виділятися нейронами заднього мозку. Ендогенний ГПП‑1 має короткий період напіввиведення з плазми (приблизно 2 хв), оскільки швидко розкладається ферментом дипептидилпептидазою‑4 (ДПП‑4) і не метаболізується печінкою й нирками. Показано, що в осіб із нормальною вагою постпрандіальний рівень ГПП‑1 відіграє важливу роль у регулюванні апетиту завдяки активації ділянок гіпоталамуса, причетних до споживання енергії. Встановлено, що периферична інфузія нативного ГПП‑1 збільшує відчуття ситості і його тривалість, одночасно зменшуючи відчуття голоду. Через короткий період напіввиведення в результаті швидкої деградації під дією ДПП‑4 нативний ГПП‑1 має обмежений терапевтичний потенціал. Однак аГПП‑1 були розроблені з тривалішим періодом напіввиведення, що робить їх стійкішими до дії ДПП‑4 і придатнішими як терапевтичні засоби. Унаслідок широкого розподілу рецепторів ГПП‑1 у тканинах організму аГПП‑1 мають різноманітні терапевтичні ефекти.
Найактуальнішими для осіб з ожирінням є стимуляція анорексигенних і інгібування орексигенних нейронів, що веде до збільшення відчуття ситості, зменшення відчуття голоду і перспективного споживання їжі.
Крім того, аГПП‑1, особливо препарати короткої дії, затримують спорожнення шлунка, що може бути корисним при ожирінні, але водночас мати несприятливі наслідки для ШКТ.
Препарат тривалої дії ліраглутид 3,0 мг був першим дослідженим і затвердженим засобом для контролю ваги з групи аГПП‑1.
Ефективність ліраглутиду в лікуванні ожиріння
Ефективність і безпечність застосування ліраглутиду 3,0 мг вивчали в рандомізованих контрольованих дослідженнях SCALE фази 3 за участю різних груп осіб із ожирінням або надмірною вагою. В усіх групах початкова доза ліраглутиду становила 0,6 мг на добу. Її збільшували щотижня до досягнення максимальної дози – 3,0 мг. Це дозування базувалося на результатах попереднього дослідження фази 2, яке визначило 3,0 мг ліраглутиду як оптимальну дозу для максимальної втрати ваги проти 1,2; 1,8 і 2,4 мг препарату, яка при цьому має прийнятну переносимість. Кінцевими клінічними точками були безпека/переносимість, зниження ваги і/або підтримання ваги на зниженому рівні (після модифікації способу життя), затримка початку ЦД 2 типу в осіб із ожирінням і предіабетом і покращення обструктивного апное сну.
У дослідженнях SCALE зниження ваги після лікування ліраглутидом 3,0 мг разом із модифікацією способу життя (харчування і фізична активність) становило від 5,7 до 8,0% від початкової маси тіла і було вираженішим, ніж у групі плацебо. Крім того, було показано, що значно більше осіб з ожирінням, які приймали 3,0 мг ліраглутиду, втратили ≥5% ваги (від 46,3 до 63,2%) і >10% ваги (від 23,4 до 33,1%) проти плацебо. У рандомізованому дослідженні учасників випадковим чином було поділено на 3 групи (n=150): учасники першої групи проходили інтенсивну поведінкову терапію (IПT), другої – проходили IПТ + отримували ліраглутид у дозі 3,0 мг, третьої – проходили ІПТ + отримували ліраглутид у дозі 3,0 мг і дотримувалися низькокалорійної дієти. Зниження ваги в групах, учасники яких отримували ліраглутид, було значно вищим за таке при проходженні тільки ІПТ: 44,0%, 70,0% і 74,0% втратили ≥5% ваги і 26,0%, 46,0% і 72,0% втратили ≥10% відповідно. Середня втрата ваги становила 6,1±1,3%, 11,5±1,3% і 11,8±1,3% відповідно. До того ж ліраглутид у дозі 3,0 мг асоціювався з більшою ймовірністю підтримання зниженої ваги після 56 тиж, якщо порівняти з плацебо (81,4 проти 48,9%, відношення шансів 4,8; 95% ДІ 3,0-7,7; р<0,0001).
У канадському дослідженні (n=311) через 6 міс прийому ліраглутиду в дозі 3,0 мг середнє зниження ваги становило 7,3 кг (р<0,001). У тих, хто продовжував лікування впродовж ≥6 міс (n=167), середня вага знизилась на 7,9 кг (p<0,001), або на 7,1%. Серед цих осіб майже дві третини (64,1%) втратили ≥5%, а понад третини (34,5%) – >10% маси тіла. Схожі результати було отримано в італійському дослідженні (n=93): у пацієнтів, які приймали 3,0 мг ліраглутиду впродовж ≥6 міс (n=43), вага знизилася в середньому на 7,9 кг (або на 7,4%). Серед цих осіб 69,8% втратили ≥5%, а 23,2% – ≥10% маси тіла.
Клінічно важливі ефекти ліраглутиду
Показано, що лікування ліраглутидом у дозі 3,0 мг крім зменшення ваги в осіб з ожирінням має численні корисні властивості, зокрема уповільнення розвитку ЦД 2 типу в пацієнтів із предіабетом, поліпшення симптомів обструктивного апное сну і покращення рівнів біомаркерів серцево-судинних ризиків.
В учасників групи ліраглутиду 3,0 мг під час лікування значно рідше діагностували ЦД 2 типу, ніж в осіб із групи плацебо (n=26/1472; 2% проти n=46/738; 6% відповідно). Також при прийомі 3,0 мг ліраглутиду було зазначено поліпшення обструктивного апное сну – стану, який часто супроводжує ожиріння.
В осіб, які отримували 3,0 мг ліраглутиду, спостерігали виражене зменшення кількості випадків апное за годину, ніж при прийомі плацебо (-12,2 проти -6,1 події/год, передбачувана різниця в лікуванні: -6,1 події/год; p=0,015). Ступінь зниження ваги також суттєво корелював із клінічним поліпшенням обструктивного апное сну (р<0,01). Аналіз результатів SCALE показав, що 3,0 мг ліраглутиду не асоціюється з надмірними серцево-судинними ризиками.
Крім того, у процесі досліджень SCALE було продемонстровано статистично значуще поліпшення різних кардіометаболічних і запальних показників на тлі застосування ліраглутиду в дозі 3,0 мг проти плацебо (наприклад, С-реактивного білка, активатора плазміногену, адипонектину, загального холестерину, ліпопротеїнів (ЛП) дуже низької щільности (НЩ), ЛПНЩ, ЛП високої щільності і вільних жирних кислот). Також повідомлялося про статистично значуще зниження систолічного артеріального тиску (АТ) і, меншою мірою, діастолічного АТ.
Ліраглутид і ожиріння: безпека і переносимість
У дослідження безпеки й переносимості ліраглутиду в дозі 3,0 мг було залучено 3384 особи з надмірною вагою або ожирінням, які отримували ліраглутид упродовж періоду лікування, тобто 56 тиж, 52 тиж і 32 тижні. Показано, що ліраглутид у дозі 3,0 мг учасники зазвичай добре переносили; 9,8% з тих, хто отримував ліраглутид 3,0 мг, передчасно припинили лікування через несприятливі явища проти 4,3% на тлі прийому плацебо. Побічні реакції учасників, які відмовилися від терапії через побічні ефекти з боку ШКТ були найпоширенішою причиною припинення лікування, у тому числі нудота (2,9% при прийомі ліраглутиду проти 0,2% у групі плацебо), блювання (1,7 проти <0,1%) і діарея (1,4 проти 0%). Вважається, що більша частота таких побічних ефектів, як нудота, пов’язані із затримкою спорожнення шлунка через вплив ліраглутиду.
У деяких клінічних випробуваннях було показано, що ліраглутид може бути причиною пухлин щитоподібної залози (ЩЗ), тому за відсутності достатньої кількості даних ліраглутид 3,0 мг протипоказаний особам із медулярною карциномою ЩЗ або синдромом множинної ендокринної неоплазії 2 типу в особистому або сімейному анамнезі.
Загалом було зареєстровано 15 випадків гострого панкреатиту в 3291 пацієнта, що приймали ліраглутид у дозі 3,0 мг, проти 2 випадків в осіб, які отримували плацебо.
Також треба бути обережними при збільшенні дози ліраглутиду 3,0 мг у пацієнтів із уже наявною нирковою недостатністю. Хоча ліраглутид специфічно не метаболізується в нирках, деякі пацієнти, які отримували аГПП‑1, у тому числі ліраглутид 3,0 мг, мали гостру ниркову недостатність або погіршення перебігу хронічної ниркової недостатності, що іноді потребувало гемодіалізу. Варто зазначити, що більшість названих подій траплялись у пацієнтів, зневоднених унаслідок блювання або діареї.
Значуще або швидке зниження ваги також пов’язане з підвищеним ризиком проблем із жовчним міхуром. Ліраглутид у дозі 3,0 мг асоціювався з частішим розвитком жовчнокам’яної хвороби і холециститу, якщо порівняти з плацебо (2,2 проти 0,8% і 0,8 проти 0,4% відповідно). Для запобігання розвитку ускладнень з боку жовчного міхура пацієнтам необхідно регулярно проводити УЗД для контролю ситуації.
Оскільки ліраглутид у дозі 3,0 мг стимулює секрецію інсуліну залежно від рівня глюкози, імовірність виникнення гіпоглікемічних епізодів у разі монотерапії препаратом низька. Ризик серйозної гіпоглікемії підвищується при застосуванні ліраглутиду в дозі 3,0 мг у комбінації з інсуліном і секреторами інсуліну, такими як препарати сульфонілсечовини, у пацієнтів із ЦД 2 типу. Тому пацієнтам може знадобитися менша доза сульфонілсечовини або інсуліну в цьому режимі. Пацієнтам без ЦД 2 типу регулярний моніторинг рівня глюкози в крові не потрібний.
У клінічному фармакологічному дослідженні, яке постійно контролювало частоту серцевих скорочень (ЧСС) упродовж 24 год, лікування ліраглутидом у дозі 3,0 мг збільшувало ЧСС у спокої на 4-9 уд./хв вище, ніж плацебо. Пацієнтам, в яких під час лікування спостерігається стійке збільшення ЧСС у спокої, прийом ліраглутиду у дозі 3,0 мг необхідно припинити.
Ожиріння – це хронічне захворювання, яке можна і потрібно лікувати, аби зменшити ризики для здоров’я і життя пацієнта. Завдяки сприятливому профілю ефективності й безпеки ліраглутид у дозі 3,0 мг – привабливий варіант лікування для осіб із надмірною масою тіла, з огляду як на значне зниження ваги, так і на поліпшення інших симптомів, що супроводжують ожиріння.
Практичні поради щодо використання ліраглутиду
Початок терапії ліраглутидом
При застосуванні ліраглутиду в пацієнтів із ожирінням рекомендується повільна ескалація добової дози (1-й тиж – 0,6 мг, 2-й тиж – 1,2 мг, 3-й тиж – 1,8 мг, 4-й тиж – 2,4 мг, 5-й тиж і далі – 3,0 мг). У разі появи нудоти може допомогти використання меншої дози впродовж тривалого періоду з подальшою спробою підвищити дозування. Хоча найчастішою причиною відмови від застосування препарату були побічні ефекти з боку ШКТ, варто нагадати пацієнтам, що більшість (майже 93%) із негативних явищ мають тимчасовий і помірний характер. Для полегшення цих симптомів рекомендовано зменшити розмір порції і збільшити частоту прийомів їжі (приблизно 1/3 звичайного розміру порції 3-5 разів на день). Краще за все харчуватися багатою на білок їжею з овочами і/або фруктами та уникати жирної їжі. За необхідності можуть бути призначені протиблювотні засоби.
У деяких пацієнтів на початку терапії спостерігається посилення гастроезофагеального рефлюксу і закрепів. Такі заходи профілактики рефлюксу, як зменшення об’єму їжі і відмова від неї за 2 год до сну, а також додавання в раціон клітковини – для поліпшення роботи кишечнику, дають можливість запобігти цим негативним явищам або зменшити їх частоту.
Усім пацієнтам, які лікуються ліраглутидом, рекомендується регулярно приймати добавки клітковини, оскільки вона не лише запобігає закрепам, але й дає ефект ситості і може також сприяти зменшенню ваги. Безрецептурні препарати магнію також можуть допомогти полегшити супутні симптоми. Пацієнтам, в яких часто трапляються випадки блювання або діареї, важливо споживати достатньо рідини, аби уникнути ураження нирок.
Щоб заспокоїти пацієнтів на початку лікування, доцільно обговорити план дій у разі пропуску лікування. Якщо пацієнт пропускає прийом препарату один раз на добу, його необхідно відразу відновити, прийнявши наступну заплановану дозу. Якщо з прийому попередньої дози 3,0 мг ліраглутиду минуло понад 3 дні, пацієнти мають знову повернутися до дози 0,6 мг на добу і повільно збільшувати її.
Ручку для ін’єкцій між використанням не варто зберігати в холодильнику. Ручку потрібно зберігати на видному місці, аби не забути нею скористатися, а також не завадило б встановити нагадування про це в телефоні. Дуже важливо провести навчання з користування ручками, особливо якщо людина не мала попереднього досвіду використання подібних ліків.
Лікування ліраглутидом треба припинити, якщо пацієнту не вдалося досягти зниження ваги на 4% після 16 тиж лікування, оскільки малоймовірно, що він зможе досягти і підтримувати клінічно значуще зниження ваги в разі продовження лікування.
Підтримка прихильності до лікування ліраглутидом у дозі 3,0 мг
Для підтримки прихильності до довгострокової терапії ліраглутидом у дозі 3,0 мг важливо нагадати пацієнтам, що фармакотерапія для зниження ваги – це не «швидке рішення», а довгострокове лікування ожиріння як хронічного і складного стану.
Опис способу дії ліраглутиду в дозі 3,0 мг і впливу його довгострокового прийому на ефективність може допомогти заохотити пацієнтів продовжувати лікування. Можливо, варто також нагадати пацієнтам, що зниження ваги на 5-10% має безліч переваг для здоров’я (табл.). Щодо зниження ваги, пацієнти зазвичай бажають знизити її більш як на 5-10%. Але управління цими очікуваннями є найважливішим компонентом лікування ожиріння. Необхідно постійно нагадувати пацієнтам про їхні успіхи в зниженні ваги та обов’язково показувати, як схуднення впливає на поліпшення метаболічних маркерів, таких як рівень глікованого гемоглобіну або ліпідів. Це дасть можливість мотивувати пацієнтів не лише втрачати, але й підтримувати знижену масу тіла. Довгострокове фармацевтичне лікування ожиріння в комплексі зі зміною способу життя, звичайно, є не найшвидшим методом зниження ваги, але дає найбільш стійкий результат.
Реферативний огляд Fitch A., Ingersoll A.B. Patient initiation and maintenance of GLP‑1 RAs for treatment of obesity: a narrative review and practical considerations for primary care providers.
Postgrad Med. 2021 Apr;133(3):310-319.
doi: 10.1080/00325481.2020.1845534.
Підготувала Анастасія Романова