15 листопада, 2021
Фіксована комбінація агоніста рецептора ГПП-1 і базального інсуліну: розбір клінічних випадків
Незважаючи на вагомий арсенал цукрознижувальних препаратів (ЦЗП), більшість пацієнтів із цукровим діабетом (ЦД) 2 типу не досягають контролю захворювання. Зі збільшенням тривалості ЦД 2 типу та подальшим його прогресуванням ситуація тільки погіршується, оскільки ефективність дії пероральних ЦЗП починає знижуватися. Виходом із цієї ситуації є своєчасне призначення інсулінотерапії, але таке лікування асоціюється з підвищеним ризиком гіпоглікемії та збільшенням маси тіла. При цьому контроль захворювання в більшості випадків так і залишається незадовільним.
Покращити контроль діабету в таких пацієнтів дає можливість застосування фіксованої комбінації базального інсуліну й агоніста рецептора глюкагоноподібного пептиду‑1 (ГПП‑1), більш відомої ендокринологам під назвою Ксалтофай. Особливості призначення згаданої комбінації з розбором клінічних випадків обговорювалися на консиліумі експертів під час чергової осінньої «Школи ендокринолога». Як експерти виступили завідувачка відділу діабетології ДУ «Інститут ендокринології та обміну речовин ім. В. П. Комісаренка НАМН України» (м. Київ), доктор медичних наук, професор Любов Костянтинівна Соколова, завідувачка кафедри ендокринології Львівського національного медичного університету ім. Данила Галицького, доктор медичних наук, професор Аліна Мечиславівна Урбанович, керівник науково-організаційного відділу ДУ «Інститут ендокринології та обміну речовин ім. В. П. Комісаренка НАМН України», кандидат медичних наук Юлія Богуславівна Бельчіна. На початку консиліму Юлія Богуславівна представила випадки з власної клінічної практики.
Клінічний випадок 1
Пацієнтка Л., 68 років. ЦД 2 типу діагностовано приблизно у 2007 р. Отримувала таблетовані ЦЗП. Останні 2 роки отримує інсулінотерапію в комбінації з таблетованими ЦЗП. У 2004 р. діагностовано гіпертонічну хворобу. Пацієнтка не курить, алкоголем не зловживає.
Скарги. Надійшла зі скаргами на погіршення самопочуття останніми місяцями. Відзначає загальну слабкість, пітливість уночі, постійне відчуття голоду, збільшення маси тіла, запаморочення, підвищення артеріального тиску (АТ), зниження пам’яті, задишку при фізичному навантаженні, болі в суглобах, болі та парестезії в нижніх кінцівках, судоми в гомілках. Госпіталізована у зв’язку з погіршенням загального стану для проведення клінічного обстеження, лікування та корекції цукрознижувальної терапії.
На момент госпіталізації отримувала: людський інсулін 46 Од/добу, метформін 2000 мг/добу, комбінацію периндоприлу 8 мг й індапаміду 2,5 мг.
Об’єктивно: зріст – 158 см, вага – 88,9 кг, індекс маси тіла (ІМТ) – 35,6 кг/м2 (ожиріння 2 ступеня), АТ – 140/90 (права рука) та 145/90 (ліва рука) мм рт. ст., пульс – 72 уд./хв, частота дихання – 18 р/хв.
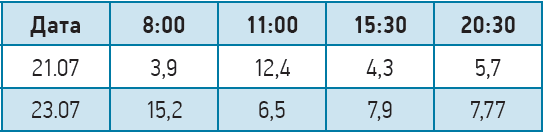
Загальноклінічні дослідження. Показники, які виходили за межі референтних значень: рівень глікованого гемоглобіну – НbА1с (05.07.2021) – 8,4%, рівень 25-гідроксивітаміну D у плазмі крові – 54,2 нмоль/л, електрокардіографія (ЕКГ) – блокада лівої ніжки пучка Гіса, капіляроскопія – мікроангіопатія нижніх кінцівок ІІА-ІІБ ст., реовазографія – зміни судин зі зниженням кровонаповнення. Показники глікемії (ммоль/л) наведено нижче.
Високий показник ранкової глікемії (15,2 ммоль/л) був пов’язаний із нівелюванням нічної гіпоглікемії.
Консультації суміжних фахівців. Кардіолог рекомендував проведення коронарографії. Було виявлено нестабільний стеноз передньої міжшлуночкової гілки лівої коронарної артерії, що має нечіткий ангіографічний контур: ангіографічна картина початкової стадії руйнування бляшки (права бічна проєкція). Множинні ураження правої коронарної артерії. Нестабільний стеноз у дистальному сегменті артерії (ексцентричний 2 типу за Ambrose). Хворій було рекомендовано стентування, котре згодом було успішно виконано в Інституті кардіології ім. М. Д. Стражеска.
Консиліум
Обираючи цукрознижувальну терапію, потрібно враховувати клінічні особливості хворої. Нагадаємо, що пацієнтка Л. страждає на ожиріння, тому їй доцільно призначити саме аналог рецептора ГПП‑1, який здатний пригнічувати апетит і сприяти зниженню маси тіла. Хвора має високий ризик гіпоглікемії, що асоціюється з підвищеним ризиком серцево-судинних катастроф у зв’язку з тяжкою серцево-судинною патологією (проведено стентування та наявні нестабільні атеросклеротичні бляшки коронарних артерій). Отже, запобігання розвитку гіпоглікемії має першочергове значення. Для мінімізації ризику виникнення гіпоглікемії пацієнтка потребує заміни генно-інженерного людського інсуліну на аналог інсуліну пролонгованої дії, як-от деглюдек. Було обрано комбінацію агоніста рецептора ГПП‑1 й інсуліну деглюдек (препарат Ксалтофай).
Наразі Ксалтофай вважають найкращою альтернативою базис-болюсної інсулінотерапії в пацієнтів із ЦД 2 типу. Він дає змогу швидко, безпечно й ефективно знижувати рівень НbА1с до цільових показників, що в підсумку зменшує ризик діабетичних ускладнень і покращує якість життя пацієнтів. Поєднання агоніста рецептора ГПП‑1 із базальним інсуліном сприяє зниженню рівня постпрандіальної глікемії, адже агоніст рецептора ГПП‑1 дає можливість контролювати постпрандіальне підвищення глікемії, з яким зазвичай дуже важко впоратися.
Корекція цукрознижувальної терапії. Стартова доза препарату Ксалтофай становила 16 кроків дози 1 р/день у вечірній час. Титрування препарату проводилося 2 р/тиж з урахуванням середніх показників глікемії натще за 3 попередні дні. Цільовий рівень глікемії натще дорівнював 6,0-7,0 ммоль/л. Титрування пацієнтка переносила добре, скарг на нудоту чи погіршення самопочуття не було.
Запитання, що найчастіше виникають у лікарів у процесі титрування препарату Ксалтофай
Згідно з інструкцією стартова доза препарату Ксалтофай у разі переведення з будь-якої дози іншого інсуліну має становити 16 Од інсуліну деглюдек і 0,6 мг ліраглутиду. Це робиться для того, щоб уникнути передозування агоніста рецептора ГПП-1 та уникнути побічних ефектів, які характерні для препаратів цієї групи.
Часто переведення пацієнта з досить високої дози іншого інсуліну (в нашому випадку пацієнтка отримувала 46 Од інсуліну) викликає в лікаря певні побоювання щодо правильності таких дій. Зниження дози інсуліну в період титрування препарату Ксалтофай може призвести до певного підвищення рівня глікемії. Для профілактики таких явищ у лікаря часто виникає цілком слушне бажання дещо збільшити стартову дозу препарату Ксалтофай, але ця тактика може супроводжуватися розвитком виразних побічних ефектів із боку шлунково-кишкового тракту через вплив ліраглутиду та є помилковою. Загалом можливе підвищення глікемії в період титрування не є настільки тривалим, щоби призвести до розвитку значних змін.
Ще однією ситуацією є розвиток нудоти під час титрування дози препарату Ксалтофай. У такому випадку дозволяється проводити титрування не двічі на тиждень, а лише раз на тиждень. Звісно, тривалість підбору дози препарату Ксалтофай у такому випадку дещо збільшиться, але буде комфортною для пацієнта. Важливо, що нудота спостерігалася лише в 7,8 % пацієнтів на початку титрування і в більшості з них була тимчасовою.
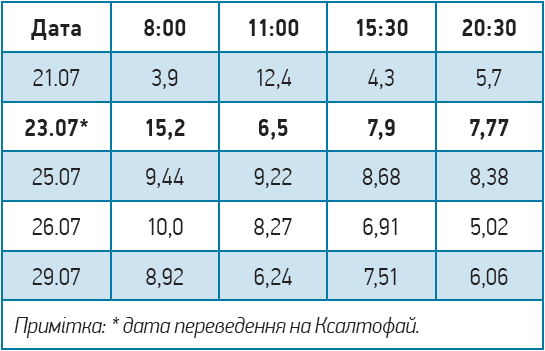
Показники глікемії (ммоль/л) до та після переведення на Ксалтофай наведено нижче.
Лікування. 29.07 пацієнтка була виписана зі стаціонара з такими рекомендаціями: дієта з обмеженням жирів і вуглеводів, рідини та солі; метформін 1000 мг 2 р/добу; Ксалтофай 22 кроки дози 1 р/добу з корекцією дози відповідно до рівня глікемії 2 р/тиж; комбінація периндоприлу 8 мг, індапаміду 2,5 мг й амлодипіну 10 мг зранку; небіволол 2,5 мг зранку; розувастатин 20 мг увечері; ацетилсаліцилова кислота 75 мг 1 р/добу ввечері постійно; вітамін D3 4000 МО; контроль НbА1с через 3 міс.
Подальше спостереження. Через 1,5 міс після виписки хвора отримує Ксалтофай 26 кроків дози 1 р/добу, метформін 1000 мг 2 р/добу. Показники глікемії натще не перевищували 7,2 ммоль/л. Пацієнтка втратила 7,2 кг маси тіла (вага – 81,7 кг, ІМТ – 32,7 кг/м2). Загальний стан і настрій покращилися.
Клінічний випадок 2
Пацієнтка А., 62 роки. ЦД діагностовано приблизно у 2003 р. Отримувала таблетовані ЦЗП. Останні 7 років отримує інсулінотерапію в комбінації з таблетованими ЦЗП. У 2006 р. діагностовано гіпертонічну хворобу, у 2021 р. – лівобічний деформувальний артроз. Пацієнтка курить, алкоголем не зловживає.
Скарги. Останніми місяцями відзначає погіршення самопочуття: наростання загальної слабкості, задишку при незначному фізичному навантаженні, болі в суглобах, обмеження рухової активності, збільшення ваги. Госпіталізована через погіршення загального стану для проведення клінічного обстеження, лікування та корекції цукрознижувальної терапії.
На момент госпіталізації отримувала: інсулін премікс 30/70 у дозі 46 Од/добу, людський інсулін 6-10 Од залежно від рівня глікемії, комбінацію метформіну та ситагліптину 50/1000 мг 1 р/добу зранку, метформін 1000 мг 1 р/добу ввечері.
Об’єктивно: зріст – 176 см, вага – 113 кг, ІМТ – 36,5 кг/м2, АТ – 130/80 (права рука) та 140/90 (ліва рука) мм рт. ст., пульс – 80 уд./хв, частота дихання – 18 р/хв.
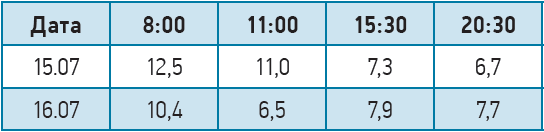
Загальноклінічні дослідження. Показники, які виходили за межі референтних значень: рівень НbА1с (22.07.2021) – 9,8%; концентрація 25-гідроксивітаміну D у плазмі крові – 34,6 нмоль/л; ЕКГ (21.07.2021) – синусовий ритм, відхилення положення електричної осі серця вліво, ознаки збільшення лівих відділів серця; капіляроскопія – мікроангіопатія нижніх кінцівок ІІБ-ІІІ ст.; реовазографія – зміни судин 2 ст. зі зниженням кровонаповнення. Показники глікемії наведено нижче.
Консультація суміжних фахівців. Висновок ортопеда: лівобічний деформувальний гонартроз ІІІ ст., варусна деформація. Гемартроз лівого колінного суглоба. Контрактура правого колінного суглоба.
Консиліум
Які характеристики пацієнтки впливають на вибір цукрознижувальної терапії та який препарат обрати для досягнення контролю ЦД? Використання досить активної болюсної інсулінотерапії в поєднанні з пероральними ЦЗП не давали змогу контролювати діабет. З огляду на такі клінічні характеристики, як гіпертонічна хвороба, малорухливий спосіб життя, макро- та мікросудинні ускладнення ЦД, ризик гіпоглікемічних станів, безпечнішим та ефективнішим є призначення фіксованої комбінації базального інсуліну й агоніста рецептора ГПП-1.
Корекція цукрознижувальної терапії. Пацієнтці було призначено Ксалтофай. Стартова доза становила 16 кроків дози 1 р/день у вечірній час. Титрування препарату проводилося 2 р/тиж з урахуванням середніх показників глікемії натще за 3 попередні дні. Цільовий рівень глікемії натще дорівнював 6,0-7,0 ммоль/л. Титрування пацієнтка переносила добре, скарг на нудоту чи погіршення самопочуття не було.
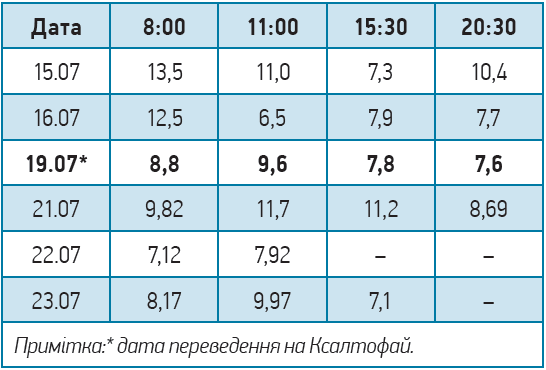
Показники глікемії (ммоль/л) до та після переведення на препарат Ксалтофай представлено нижче.
Через 4 дні після призначення препарату Ксалтофай спостерігалася нормалізація показників глікемії. Пацієнтка була виписана зі стаціонара з відповідними рекомендаціями та скорегованим лікуванням.
Лікування. Дієта з обмеженням жирів і вуглеводів, рідини та солі; метформін 1 р/день 1000 мг 2 р/добу; Ксалтофай 24 кроки дози 1 р/день з корекцією відповідно до рівня глікемії 2 р/тиж; комбінація периндоприлу 8 мг, індапаміду 2,5 мг й амлодипіну 10 мг; розувастатин 20 мг 1 р/добу ввечері; ацетилсаліцилова кислота 75 мг 1 р/добу ввечері постійно; огляд ортопеда-травматолога в динаміці; вітамін D3 8000 МО; контроль рівня НbА1с через 3 міс.
Подальше спостереження. Через 1,5 міс пацієнтка отримує Ксалтофай 44 кроки дози 1 р/день, метформін 1000 мг 2 р/день. Глікемія постпрандіальна – до 10 ммоль/л, натще – 6-9 ммоль/л. Хвора втратила 4 кг маси тіла (вага – 109 кг, ІМТ – 35,2 кг/м2). Загальний стан і настрій покращилися.
Наукове підґрунтя та переваги призначення препарату Ксалтофай порівняно з інсулінотерапією
Добре відомо, що досягнення й підтримання хворими на ЦД 2 типу індивідуальних цільових показників глікемії покращують результати лікування завдяки зниженню частоти мікро- та макросудинних ускладнень. Однак на практиці пацієнти з ЦД 2 типу часто не досягають цільових показників HbA1c. Згідно з даними D. Brixner і співавт. (2019) тільки 22% пацієнтів із ЦД 2 типу досягають мети лікування (HbA1c <7%) при застосуванні базального інсуліну. У разі базис-болюсного режиму інсулінотерапії ситуація з контролем ЦД 2 типу виявляється ще гіршою: цільового рівня HbA1c <7% досягають лише близько 15% осіб, що пов’язано найперше зі складнощами підрахунку потрібної дози інсуліну короткої дії.
Не дивно, що більшість пацієнтів, які застосовують інсулінотерапію, мають підвищений ризик швидкого прогресування серцево-судинних ускладнень унаслідок незадовільного контролю діабету. Знайти вихід із цієї ситуації можна завдяки застосуванню препарату Ксалтофай, який переконливо продемонстрував свої переваги в низці клінічних досліджень.
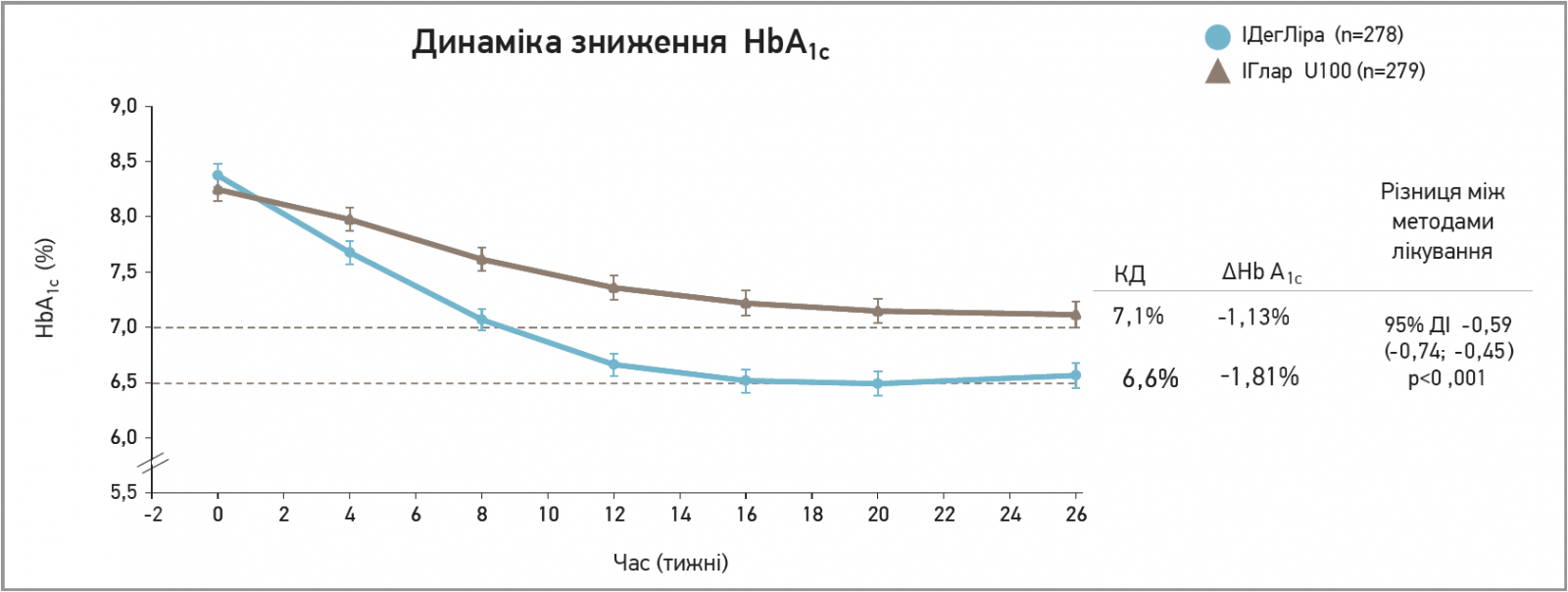
Одним із них є багатоцентрове відкрите 26-тижневе дослідження DUAL V, в якому порівнювали ефективність і безпеку лікування препаратом Ксалтофай із подальшим збільшенням дози базального інсуліну. У дослідження включили 557 пацієнтів із ЦД 2 типу, зіставних за параметрами контролю ЦД 2 типу та його тривалістю, й незадовільним контролем захворювання за допомогою базального інсуліну (HbA1c – від 7 до 10%). Пацієнти були розподілені на отримання комбінації Ксалтофай + метформін або інсулін гларгін U100 + метформін. Середній вихідний рівень HbA1c у групах становив 8,41 та 8,23% відповідно. Через 26 тиж лікування середнє зниження показника HbA1c у групі Ксалтофай + метформін дорівнювало 1,81% (до 6,6%), а в групі інсулін гларгін U100 + метформін – 1,31% (до 7,1%) (рис. 1). Важливо, що в групі Ксалтофай + метформін відзначалося зниження маси тіла в середньому на 1,4 кг, тоді як пацієнти групи порівняння, навпаки, додали 1,8 кг ваги.
Рис. 1. Дослідження DUAL V: інсулін деглюдек/ліраглутид vs подальше збільшення дози базального інсуліну
Примітки. Середні зареєстровані величини з планками похибок (стандартне відхилення на основі розрахованих даних повної вибірки пацієнтів і переносу останнього вимірювання вперед. Різниця між методами лікування оцінюється на основі аналізу ANCOVA, а значення ∆ отримані на основі переносу останнього вимірювання вперед.
Цільовий рівень HbA1c за ADA/EASD <7,0%; цільовий рівень HbA1c за ААCЕ ≤6,5%. КД – кінець дослідження;
ІДегЛіра – інсулін деглюдек/ліраглутид; ІГлар U100 – інсулін гларгін 100 Од/мл.
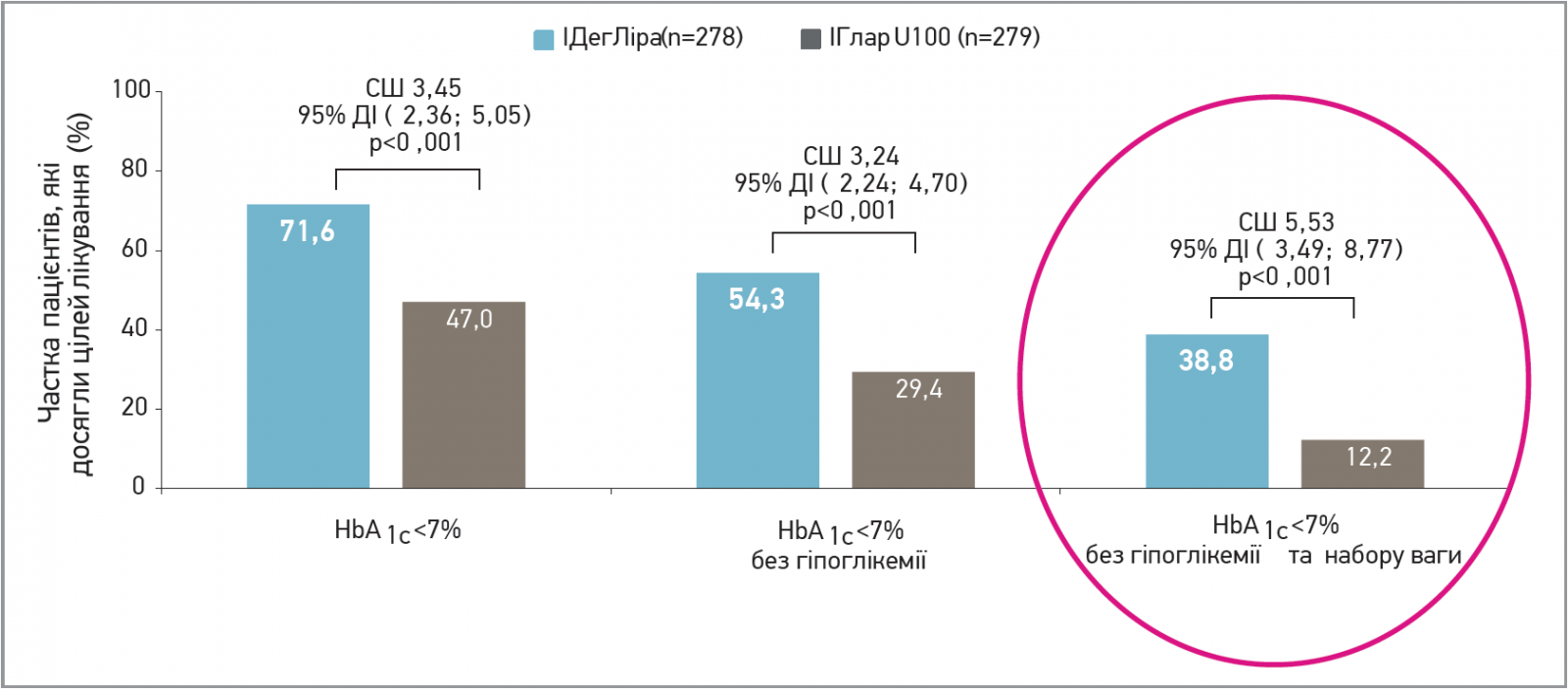
Серед учасників дослідження, що отримували Ксалтофай, більша частка пацієнтів досягли цільового рівня HbA1c з меншим ризиком гіпоглікемії та набору ваги (рис. 2).
Рис. 2. Дослідження DUAL V: пацієнти, які досягли цілей лікування
Примітки. Дані базуються на розрахованих даних повної вибірки пацієнтів і переносі останнього вимірювання вперед. Співвідношення шансів (СШ) ІДегЛіра/ІГлар U100 отримані з регресійної логістичної моделі.
ІДегЛіра – інсулін деглюдек/ліраглутид; ІГлар U100 – інсулін гларгін 100 Од/мл.
Багатоцентрове відкрите 26-тижневе дослідження DUAL VII було присвячене порівнянню ефективності та безпеки препарату Ксалтофай і базально-болюсної інсулінотерапії. У дослідження включили 506 пацієнтів із ЦД 2 типу з незадовільним контролем захворювання за допомогою метформіну й базального інсуліну (HbA1c – від 7 до 10%). Учасники були рандомізовані на дві групи, в одній з яких до інсуліну гларгін додавали до 4 ін’єкцій інсуліну аспарт перед їдою, а в другій – замінювали інсулін гларгін на Ксалтофай. Пацієнти обох груп продовжували приймати метформін.
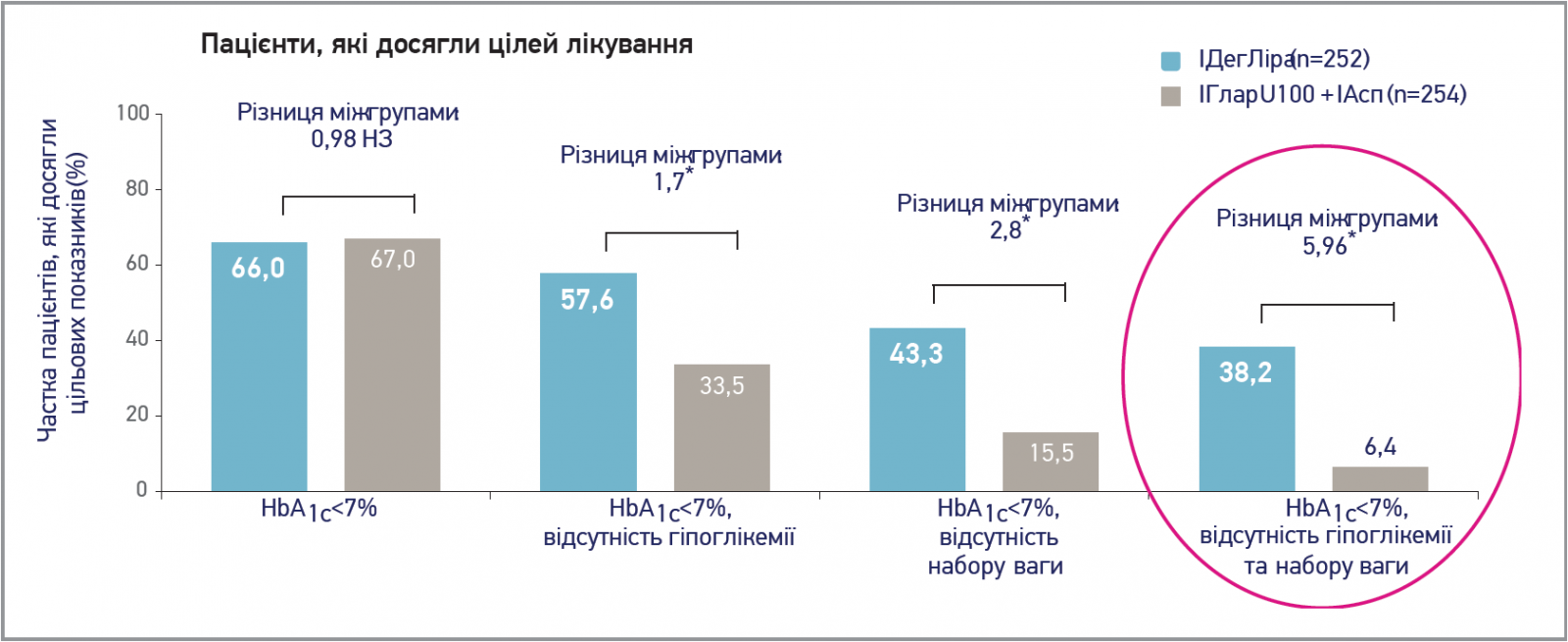
Терапія із застосуванням препарату Ксалтофай забезпечила майже аналогічне зниження рівня HbA1c, як і базально-болюсна інсулінотерапія (1,48 проти 1,46% відповідно) на тлі значно меншого ризику гіпоглікемії (19,8 проти 52,6%; р<0,0001) (рис. 3). Пацієнти, які отримували Ксалтофай, втратили в середньому 0,93 кг за 26 тиж, тоді як учасники групи порівняння додали 2,64 кг (р<0,0001).
Рис. 3. DUAL VII: інсулін деглюдек/ліраглутид vs базально-болюсний режим
Примітки. * Статистично значуща різниця (на користь препарату ІДегЛіра). Частота позитивного відгуку на лікування розрахована на основі повної вибірки пацієнтів. СШ (ІДегЛіра/ІГлар U100 + ІАсп) отримано з регресійної логістичної моделі з використанням зв’язку з методом лікування й регіоном як факторами та вихідним рівнем HbA1c (і маси тіла) як незалежними змінними. Для логістичної регресії пропущені дані на тижні 26 розраховано на основі моделі змішаних ефектів для багаторазових вимірювань. a Тяжка чи підтверджена симптомна гіпоглікемія – це епізоди гіпоглікемії впродовж останніх 12 тиж лікування. ІАсп – інсулін аспарт;
ІГлар U100 – інсулін гларгін 100 Од/мл; НЗ – не значущо.
Добова доза інсуліну в обох групах істотно відрізнялася. Середня доза інсуліну в групі препарату Ксалтофай становила 40 Од, тоді як у групі базис-болюсної терапії – 84 Од.
Ще однією перевагою була зручність терапії. Ксалтофай уводився лише 1 р/добу за допомогою 1 шприц-ручки, тоді як у групі порівняння пацієнти отримували по 2-4 ін’єкції (на час завершення дослідження 66,5% пацієнтів отримували ≥3 ін’єкцій інсуліну на добу), застосовуючи 2 шприц-ручки. Кожна ін’єкція болюсного інсуліну потребує моніторингу рівня глюкози крові, що істотно збільшує витрати на тест-смужки.
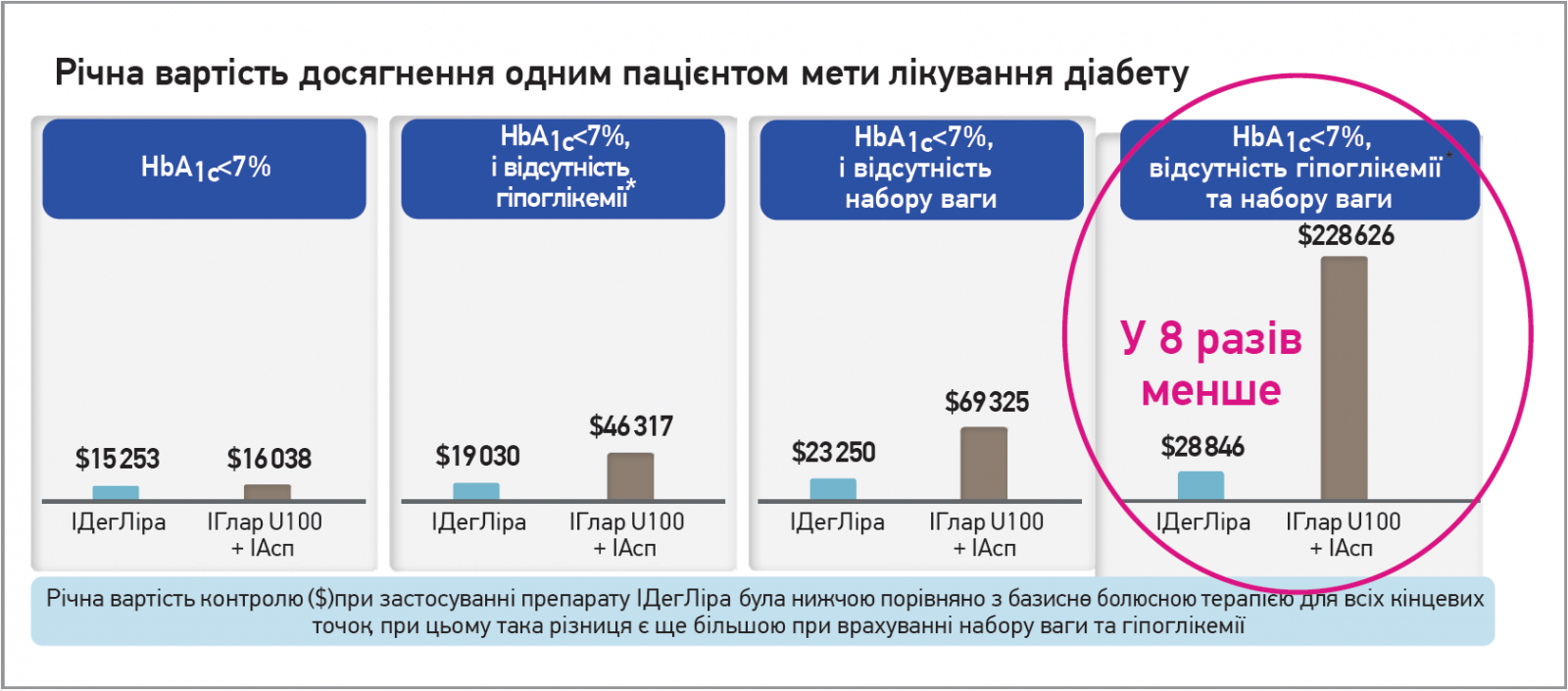
Було також проаналізовано вартість лікування з урахуванням лише витрат на лікарські препарати та засоби самоконтролю. Виявилося, що терапія на основі препарату Ксалтофай була в 6 разів дешевшою порівняно з базально-болюсною інсулінотерапією. При цьому різниця у вартості лікування серед пацієнтів обох груп, які досягли цільового рівня HbA1c за відсутності гіпоглікемій і збільшення маси тіла, виявилася 8-кратною (рис. 4).
Рис. 4. Економічна цінність інсуліну деглюдек/ліраглутид порівняно з базально-болюсною терапією (DUAL VII)
Примітки. * Тяжка чи підтверджена глюкозою крові симптомна гіпоглікемія: епізод, який вважається тяжким (потребує сторонньої допомоги) або підтверджений вмістом глюкози в плазмі крові <3,1 ммоль/л (<56 мг/дл) із симптомами, які свідчать про гіпоглікемію. ІАсп – інсулін аспарт; ІГлар U100 – інсулін гларгін 100 Од/мл.
Підготував В’ячеслав Килимчук
Медична газета «Здоров’я України 21 сторіччя» № 19 (512), 2021 р.