21 січня, 2022
Ішемічна хвороба серця і синдром обструктивного апное сну
 Синдром обструктивного апное сну (СОАС) є частим і недостатньо діагностованим розладом дихання під час сну, поширеність якого зросла від 10 до 30‑50% у загальній популяції та до 66% у пацієнтів із гострим інфарктом міокарда (ІМ) з елевацією сегмента ST. Захворюваність на СОАС збільшується з віком, в осіб з ожирінням та серед чоловіків. Враховуючи старіння населення та пандемію ожиріння в усьому світі, тягар СОАС, імовірно, посилюватиметься. Ішемічна хвороба серця (ІХС) є основною причиною захворюваності та смертності в розвинених країнах. СОАС частіше спостерігається у пацієнтів з ІХС (26‑69%) порівняно із загальною популяцією. Цей огляд літератури присвячений аналізу даних щодо зв’язку ІХС і СОАС, а також впливу цього синдрому на ІХС із метою поліпшення поінформованості лікарів щодо потенційних ризиків, покращення діагностики СОАС, своєчасного призначення відповідного лікування і поліпшення прогнозу для таких хворих.
Синдром обструктивного апное сну (СОАС) є частим і недостатньо діагностованим розладом дихання під час сну, поширеність якого зросла від 10 до 30‑50% у загальній популяції та до 66% у пацієнтів із гострим інфарктом міокарда (ІМ) з елевацією сегмента ST. Захворюваність на СОАС збільшується з віком, в осіб з ожирінням та серед чоловіків. Враховуючи старіння населення та пандемію ожиріння в усьому світі, тягар СОАС, імовірно, посилюватиметься. Ішемічна хвороба серця (ІХС) є основною причиною захворюваності та смертності в розвинених країнах. СОАС частіше спостерігається у пацієнтів з ІХС (26‑69%) порівняно із загальною популяцією. Цей огляд літератури присвячений аналізу даних щодо зв’язку ІХС і СОАС, а також впливу цього синдрому на ІХС із метою поліпшення поінформованості лікарів щодо потенційних ризиків, покращення діагностики СОАС, своєчасного призначення відповідного лікування і поліпшення прогнозу для таких хворих.
Згідно зі звітом Американської академії медицини сну (AASM), СОАС вражає 12% дорослого населення США, що становить загалом 29,4 млн осіб, з яких у 80% випадків він не діагностований. У 2015 р. економічний тягар через недіагностований СОАС складав приблизно 150 млрд доларів США [113]. Своєю чергою ІХС вражає >15 млн американців і є причиною до 17% смертей серед дорослого населення [32].
СОАС пов’язаний зі зростанням захворюваності та смертності й асоційований із такими клінічними станами й чинниками, як [18, 21, 33, 35, 48, 68, 96]:
- цукровий діабет (ЦД);
- інсульт;
- когнітивні порушення;
- депресія;
- зниження якості життя;
- дорожньо-транспортні пригоди.
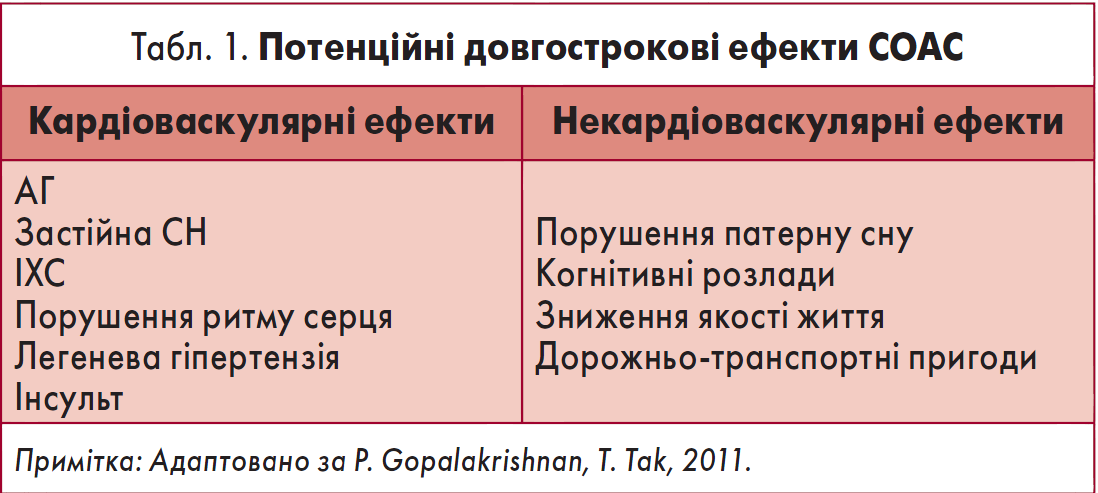
Потенційні довгострокові ефекти СОАС наведені у таблиці 1 [33]. СОАС визнано фактором ризику (ФР) серцево-судинних захворювань (ССЗ) [12, 36, 43]. Цей синдром пов’язаний із підвищеною імовірністю таких ССЗ, як ІХС, атеросклероз, артеріальна гіпертензія (АГ), застійна серцева недостатність (СН), інсульт, легенева гіпертензія, порушення ритму (зокрема, фібриляція передсердь, ФП) та провідності серця [34, 53, 65, 68, 91, 122].
Дані клінічних, епідеміологічних досліджень і досліджень in vitro й на тваринах показують, що СОАС може чинити прямий неcприятливий вплив на серцево-судинні (СС) події, незалежно від наявності таких ФР, як ожиріння та ЦД 2-го типу [60]. Окрім того, є дані, що в осіб із СОАС та ІХС ризик повторного ІМ і необхідність реваскуляризації менші у пацієнтів із СОАС та високою прихильністю до терапії CPAP (постійний позитивний тиск у дихальних шляхах) [29].
Результати досліджень демонструють зв’язок між СОАС і раптовою серцевою смертю (РСС), однак не дозволяють зробити чіткі висновки щодо їх причинно-наслідкового зв’язку. Асоціація між СОАС і РСС складна і включає ішемію міокарда, дезадаптивні зміни вегетативної нервової системи, зміни експресії іонних каналів, підвищення аритмогенності й порушення гемодинаміки тощо [11]. Необхідно зазначити, що РСС у 75% випадків пов’язана з ІХС [22].
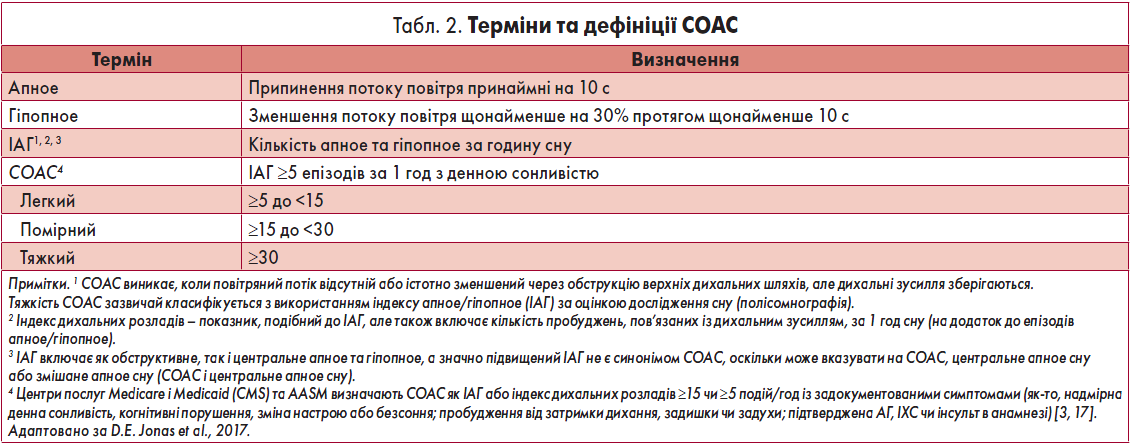
Визначення і дефініції СОАС
СОАС характеризується епізодами зупинки дихання, що пов’язані з повним або частковим колапсом верхніх дихальних шляхів під час сну й асоційований із наявністю хропіння, зниженням насичення крові киснем, короткочасними пробудженнями [35]. Епізоди апное/гіпопное вважають обструктивними, якщо під час них зберігаються дихальні зусилля [1, 93]. Терміни і дефініції СОАС наведені у таблиці 2 [46].
Фактори ризику СОАС
Розрізняють немодикофівані та модифіковані ФР СОАС. ФР, що не модифікуються, включають чоловічу стать, вік і расу. Генетична схильність або обтяжений сімейний анамнез щодо СОАС, а також черепно-лицьові анатомічні аномалії, що призводять до звуження верхніх дихальних шляхів, можуть спричиняти вищий ризик розвитку СОАС. До модифікованих ФР відносять: ожиріння, приймання речовин/медикаментів, що викликають розслаблення м’язів і звуження дихальних шляхів (опіатів, бензодіазепінів, алкоголю), ендокринні розлади (гіпотиреоз, синдром полікістозних яєчників), куріння та закладеність носа або його обструкцію тощо [6, 93]. Ожиріння є основним ФР СОАС, який виявляють у 70% випадків у осіб з ожирінням [90].
У чоловіків відзначено більшу ймовірність розвитку СОАС, ніж у жінок, однак у менопаузі останні мають подібний ризик. За даними дослідження T. Young et al., у жінок у постменопаузі, які отримували замісну гормональну терапію, виявлений нижчий ризик СОАС. Імовірно, це свідчить про те, що дефіцит гормонів може призводити до вищої імовірності виникнення цього синдрому [118].
Патофізіологія СОАС
Патогенез СОАС багатофакторний, складний і не до кінця вивчений [6, 80]. Зміна анатомії і нервово-м’язової функції верхніх дихальних шляхів відіграє основну роль у розвитку СОАС [6, 80]. Патогенез СОАС та зв’язок із його наслідками представлені на рисунку 1 [6].
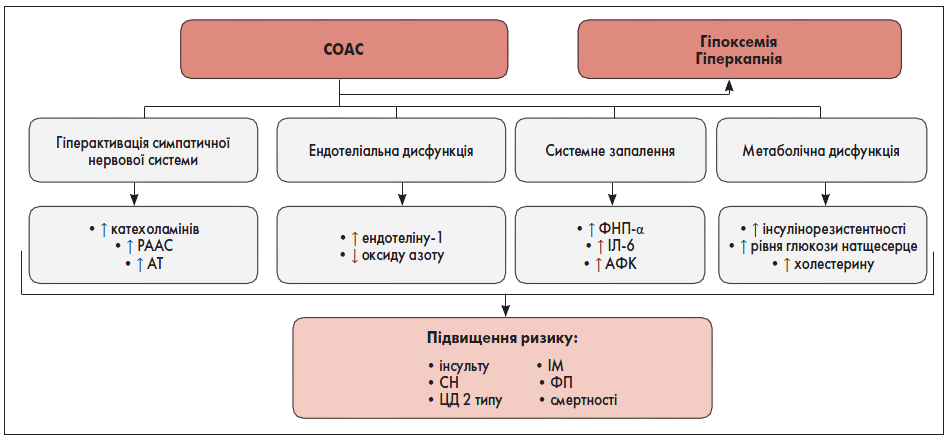 Рис. 1. Багатофакторний патогенез СОАС і підвищення ризику його наслідків через комбіновані ефекти
Рис. 1. Багатофакторний патогенез СОАС і підвищення ризику його наслідків через комбіновані ефекти
Примітки: РААС – ренін-ангіотензин-альдостеронова система, АТ – артеріальний тиск, ФНП-α – фактор некрозу пухлин альфа, ІЛ – інтерлейкін, АФК – активні форми кисню.
Адаптовано за E. Arredondo et al., 2021.
Рецидивувальні епізоди апное призводять до періодичної гіпоксії, що викликає різноманітні вегетативні, гемодинамічні, біохімічні зміни і спричиняє розвиток АГ та інших ССЗ [95]. При СОАС розвиваються, зокрема [6, 41, 87]:
- ендотеліальна дисфункція;
- системне запалення;
- оксидантний стрес;
- порушення метаболізму;
- схильність до підвищення згортання крові;
- інсулінорезистентність.
За даними дослідження C.L. Phillips et al. показано, що лікування СОАС за допомогою CPAP зменшує виразність цих процесів [87].
Симпатична нервова система
У фізіологічних умовах під час сну домінує парасимпатична система [95]. При СОАС декілька патофізіологічних механізмів призводять до стійкої активації симпатичної нервової системи. Негативний внутрішньогрудний тиск і повторювані епізоди гіпоксії, гіперкапнія викликають активацію центральних і периферичних хеморецепторів, що спричиняє активацію симпатичної нервової, ренін-ангіотензин-альдостеронової систем та підвищення рівня катехоламінів, реніну, ангіотензину II, альдостерону, що зумовлює затримку води й периферичну вазоконстрикцію, підвищення артеріального тиску (АТ) [14, 27, 45, 95].
Ендотеліальна дисфункція
Для СОАС характерний розвиток дисфункції ендотелію [6]. В осіб із СОАС виявлений вищий рівень ендотеліну‑1 у плазмі крові, а середній нічний його вміст корелював з індексом апное/гіпопоное (ІАГ) як мірою тяжкості СОАС [30]. Окрім того, встановлене зниження концентрації циркулювального оксиду азоту в сироватці крові, який нормалізується після лікування CPAP [40].
Системне запалення
При СОАС спостерігають хронічне запалення низької активності, що викликане підвищенням рівня у сироватці крові таких маркерів запалення, як фактор некрозу пухлин α (ФНП-α) та інтерлейкіну 6 (IЛ‑6) [6, 50, 94]. Окрім того, гіпоксія, що розвивається внаслідок періодичного колапсу верхніх дихальних шляхів, призводить до надмірної продукції активних форм кисню [120].
Метаболічна дисфункція
У більшості пацієнтів із СОАС спостерігають вищу поширеність ЦД 2-го типу, інсулінорезистентність [41, 48]. За даними the Sleep Heart Health Study, продемонстрований зв’язок між СОАС та підвищенням рівня глюкози натщесерце, порушенням толерантності до глюкози і предіабетом [97]. На додачу, результати регресійного метааналізу R. Nadeem et al. показали, що в осіб із СОАС визначали зібльшення вмісту загального холестерину, ліпопротеїнів низької щільності та тригліцеридів [81].
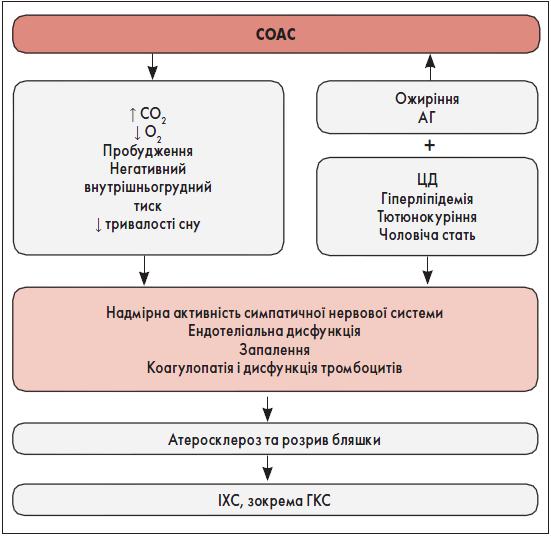
Механізми впливу СОАС на СС-систему та розвиток ІХС
Механізми зв’язку між СОАС і ССЗ досі до кінця не ясні, а ефект СОАС на розвиток ССЗ, зокрема, ІХС і прогноз багатофакторний [125]. Механізми впливу СОАС на коронарні артерії наведені на рисунку 2 [36].
Рис. 2. Механізми впливу СОАС на коронарні артерії
Примітка: ГКС – гострий коронарний синдром.
Адаптовано за T. Hein et al., 2012.
Як було зазначено вище, для СОАС характерний періодичний кардіометаболічний стрес під час повторних спроб дихальних зусиль при обструкції дихальних шляхів уві сні, яка призводить до інтермітуючої гіпоксемії, фрагментації сну та перепадів внутрішньогрудного тиску, що спричиняють зміни гемодинаміки й посилення симпатичної активності [12, 43, 49, 125]. Окрім того, накопичені дані показали, що СОАС впливає на СС-систему, зокрема внаслідок розвитку оксидантного стресу, ендотеліальної дисфункції та запалення – взаємодіючі процеси, що спричиняють виникнення і прогресування ІХС. Ці порушення часто призводять до підвищення АТ, частоти серцевих скорочень і розвитку атеросклерозу [28, 55, 68, 94, 98, 125].
Є дані, що у хворих на СОАС та ІМ з елевацією сегмента ST порушується коронарна мікроциркуляція [82]. За даними дослідження C.H. Lee et al., у пацієнтів із ІМ з елевацією сегмента ST і тяжким СОАС виявлено більшу поширеність мікросудинної обструкції [57]. Окрім того, СОАС асоційований із прокоагулянтним станом через підвищення рівня факторів згортання, активацію та посилення агрегації тромбоцитів, а також ендотеліальну дисфункцію, спричинену періодичною гіпоксією та запаленням. Однак взаємозв’язок між СОАС і деякими окремими факторами згортання крові чи регуляторними молекулами є суперечливим, а вплив терапії СОАС на гемостаз – непереконливим. Кілька досліджень продемонстрували, що коротко- та довготривала терапія CPAP чинила сприятливий вплив на систему згортання крові й функцію тромбоцитів при СОАС; в інших же роботах такого ефекту не виявлено [10].
Однак необхідно відзначити, що є деякі докази про можливу захисну дію інтермітуючої гіпоксії на серце через ішемічне прекондиціонування [5]. Але варто підкреслити потенційно шкідливі ефекти інтермітуючої гіпоксії при СОАС та підвищений ризик ССЗ [68].
СОАС і атеросклероз
СОАС асоційований із прискореним розвитком атеросклерозу коронарних артерій [105]. Зв’язок атеросклерозу і СОАС надзвичайно складний, а результати досліджень in vitro та in vivo іноді суперечливі [18]. Основними патофізіологічними механізмами СОАС, які можуть призводити до виникнення атеросклерозу та тромбозу, є [18, 36, 68]:
- інтермітуюча гіпоксемія;
- активація симпатичної нервової системи;
- дисфункція ендотелію;
- запалення;
- оксидантний стрес;
- коагулопатія;
- активація тромбоцитів;
- порушення метаболізму та ін.
Інтермітуюча гіпоксія відіграє основну роль, адже призводить до низки дезадаптивних реакцій, які можуть у кінцевому підсумку спричинити розвиток атеросклерозу [55, 68]. Відомо, що оксидантний стрес, ендотеліальна дисфункція та запалення посилюють процеси виникнення атеросклерозу [62].
За результатами дослідження L.F. Drager et al., у пацієнтів середнього віку із СОАС без явних ССЗ були виявлені ранні ознаки атеросклерозу. Функціональні та структурні зміни артерій великого калібру суттєво корелювали з тяжкістю СОАС (величина ІАГ). Це підтверджує гіпотезу про те, що СОАС відіграє роль у прогресуванні атеросклерозу. Зокрема, спостерігалися значущі відмінності у групі контролю порівняно з особами із легким/помірним та тяжким СОАС (ІАГ 3,1±0,3; 16,2±1,7 та 55,7±5,9 епізодів за 1 год відповідно) у швидкості поширення пульсової хвилі (8,7±0,2; 9,2±0,2 і 10,3±0,2 м/с; p<0,0001), товщині комплексу інтима-медіа (604,4±25,2; 580,2±29,0 і 722,2±35,2 мкм; p=0,004) та діаметрі сонної артерії (6607,8±126,7; 7152,3±114,4 та 7539,9±161,2 мкм; p<0,0001). Багатоваріантний аналіз показав, що ІАГ незалежно корелює зі швидкістю поширення пульсової хвилі та товщиною комплексу інтима-медіа (r=0,61; p<0,0001 і r=0,44, p=0,004 відповідно) [24].
Згідно із даними систематичного огляду та метааналізу 20 досліджень M. Lu et al., встановлено вищу частоту атеросклерозу коронарних артерій. Було проведено оцінку кальцифікації коронарних артерій, об’єму атеросклеротичної бляшки, ремоделювання та дисфункції серця [66]. Також автори виявили, що СОАС незалежно пов’язаний із більшим об’ємом атеросклеротичної бляшки за результатами внутрішньосудинного ультразвукового дослідження [105].
При вивченні зв’язку між СОАС та наявністю субклінічного атеросклерозу в жінок віком від 45 до 65 років, який оцінювали за допомогою томографічної оцінки вмісту коронарного кальцію (>100 одиниць Агатстона), останній був поширенішим у пацієнток із помірним/тяжким СОАС (ІАГ ≥15 епізодів за 1 год), ніж без нього або із легким СОАС (19; 4,5 та 1,6% відповідно; p<0,01). Помірний і тяжкий СОАС корелював зі збільшенням коронарного кальцію у некорегованому (відношення шансів [ВШ] 6,25; 95% довірчий інтервал [ДІ] 1,66‑23,52; p<0,01) та скорегованому логістичному регресійному аналізі [75].
В осіб із СОАС за допомогою комп’ютерної томографії виявлено, що значна частка з них мала більшу кількість некальцифікованих/змішаних атеросклеротичних бляшок (63 vs 16% у групі без СОАС; р<0,0001), кореговане ВШ 7,0 (95% ДІ 1,9‑26,5; р<0,05), багатосудинний стеноз та виразніший стеноз коронарних артерій порівняно з пацієнтами без СОАС [102].
Зв’язок СОАС та ІХС
Вивчення впливу СОАС на ІХС викликає все більший інтерес серед науковців [12, 125]. Як відомо, СОАС поширений у пацієнтів із ССЗ, частота якого у хворих на ІХС становить 26‑69% випадків [21, 43]. За даними дослідження O. Ludka et al., в осіб із гострим ІМ СОАС діагностований у 65,7% випадків. Легкий СОАС (ІАГ 5‑15 епізодів за 1 год) виявлений у 32,6%, помірний (15‑30 епізодів на 1 год) – у 20,4% і тяжкий СОАС (≥30 епізодів на 1 год) – у 12,7% хворих [67].
Це підтверджують результати іншого дослідження, за якими у пацієнтів із гострим ІМ поширеність СОАС складала 66% [58]. Також подібні дані отримали R. Mehra et al., згідно з якими у 66,4% хворих на гострий коронарний синдром (ГКС) були діагностовані порушення дихання під час сну (ІАГ >10 епізодів за 1 год), причому в 72,1% із них встановлений СОАС [76]. Своєю чергою в іншому випробуванні показано, що близько третини осіб зі стабільною ІХС мали СОАС [54].
Як зазначено вище, СОАС часто не діагностується, що підтверджують дані роботи C.H. Lee et al. [57]. Автори виявили, що 42% пацієнтів, госпіталізованих із приводу ІМ з елевацією сегмента ST (STEMI), мали недіагностований тяжкий СОАС (ІАГ ≥30 епізодів за 1 год).
Результати випробувань дозволили встановити кореляцію між СОАС і ССЗ, зокрема ІХС [23, 69, 77, 85, 117]. Обсерваційні дослідження показали, що СОАС асоційований із підвищеним ризиком подальших СС-ускладнень у різних підгрупах пацієнтів з ІХС [57, 59, 72, 117, 121]. Хворі на ГКС та СОАС мали вищу частоту як коротко-, так і довгострокових несприятливих СС-подій, ніж без СОАС [9, 57, 64, 72]. У двох когортних дослідженнях вчені виявили збільшення ймовірності ІХС у пацієнтів із СОАС [34, 37]. Так, K.M. Hla et al. встановили, що в осіб із розладами дихання під час сну при ІАГ >30 епізодів за 1 год у 2,6 раза підвищений ризик ІХС чи СН порівняно з такими без порушень дихання [37]. Дані інших випробувань продемонстрували підвищений ризик СС-подій лише серед хворих на ІХС, що не отримували лікування СОАС [23, 77].
Згідно з результатами випробування A. Zapater et al. за участю осіб із СОАС (ІАГ ≥15 епізодів за 1 год), упродовж 2,67 року спостереження було встановлено два фенотипи:
- Пацієнти без попереднього захворювання серця та ГКС (81%).
- Пацієнти із попереднім захворюванням серця та ГКС (19%).
У хворих на СОАС першого фенотипу скорегований відносний ризик (ВР) ГКС становив 1,54 (95% ДІ 1,06‑2,24; р=0,02), тоді як для другого фенотипу – 0,69 (95% ДІ 0,46‑1,04; р=0,08). Таким чином, СОАС асоційований із підвищеним ризиком повторних СС-подій у пацієнтів в анамнезі без ССЗ і ГКС [122].
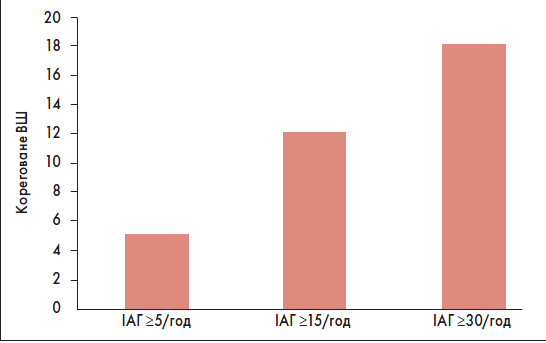
За даними дослідження F. Garcia-Rio et al., показане зростання ймовірності ІМ при різних значеннях ІАГ (рис. 3). Метаболічний синдром, ІАГ та індекс атерогенності були незалежними ФР ІМ. Окрім того, автори виявили відмінності у часі виникнення симптомів ІМ у пацієнтів з/без СОАС. Розвиток симптомів ІМ з опівночі до 8 год ранку частіше спостерігали в осіб із СОАС (ІАГ ≥5 епізодів за 1 год), ніж без цього синдрому (44,2 vs 17,9%, p=0,004).
Рис. 3. Корегований ризик ІМ у пацієнтів із СОАС залежно від ІАГ
Примітка: Адаптовано за F. Garcia-Rio et al., 2013.
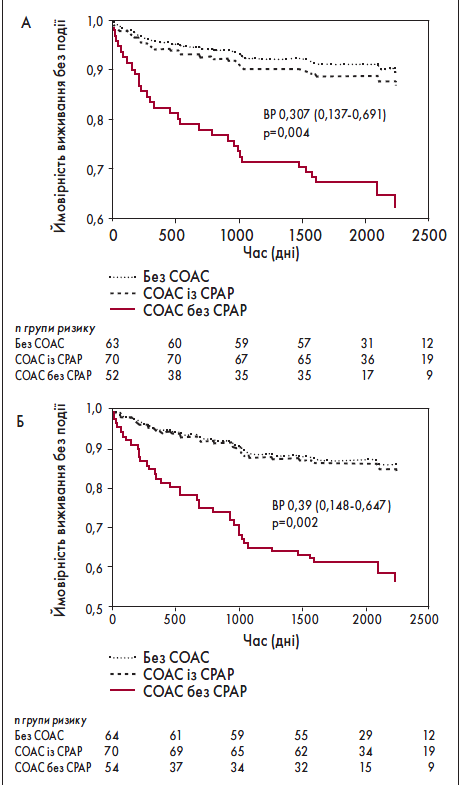
На початку дослідження у 65,6% хворих на ІМ було діагностовано СОАС. Після середнього періоду спостереження (6,5±1 років) пацієнти із СОАС, які не отримували лікування CPAP, мали вищий ризик повторних подій, ніж такі без СОАС (рис. 4).
Рис.4. Час до розвитку повторного ІМ (А) або реваскуляризації (Б) у трьох групах пацієнтів з ІМ
Примітка: Адаптовано за F. Garcia-Rio et al., 2013.
Після корегування коефіцієнт частоти захворюваності був 3,24, (95% ДІ 1,53‑6,87; p=0,0018). Крім того, початок симптомів повторного ІМ з опівночі до 8 ранку виявився значно частішим у пацієнтів із СОАС без CPAP-терапії, ніж у двох інших групах (56,3 vs 14,3 vs 0%; p=0,030). Було встановлено, що СОАС – незалежний предиктор ІМ (ВШ 4,9; 95% ДІ 2,9‑8,3; p=0,017).
Після корегування особи із СОАС, які отримували CPAP-терапію (>3,5 год/добу), мали нижчий ризик повторного ІМ (скорегований ВР 0,16; 95% ДІ 0,03‑0,76; p=0,021) та реваскуляризації (скорегований ВР 0,15; 95% ДІ 0,03‑0,79; p=0,025), ніж такі без лікування, який був подібним до показника у пацієнтів без СОАС. Таким чином, СОАС – незалежний ФР ІМ. Імовірність повторного ІМ та реваскуляризації є меншою в осіб із СОАС із високою прихильністю до CPAP-терапії [29].
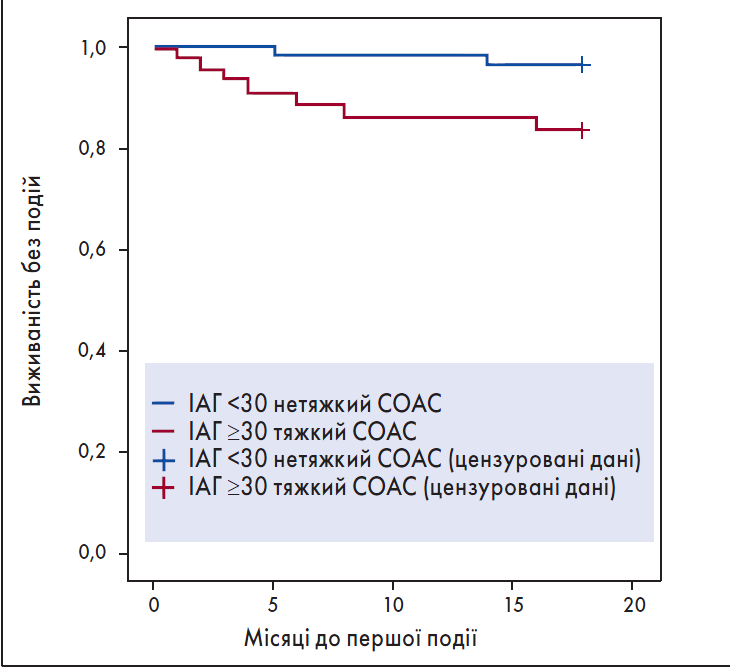
CH. Lee et al. встановлено, що СОАС є предиктором фатальних і нефатальних СС-ускладнень у хворих на ГКС [44]. За даними роботи J. Xie et al., у багатоваріантній моделі виразна гіпоксемія (≤85%) була незалежним фактором основних несприятливих серцевих подій (ВР 6,05; р=0,004) за 15 місяців спостереження [117]. Тяжкий СОАС чинив негативний прогностичний вплив при ІМ з елевацією сегмента ST. Показники виживаності без СС-подій через 18 місяців (рис. 5) у групі з тяжким СОАС (ІАГ ≥30 епізодів за 1 год) були значно гіршими, ніж в осіб із нетяжким СОАС (p=0,021; log-rank-тест). До того ж мала місце вища частота непланових реваскуляризацій порівняно з пацієнтами із нетяжким СОАС [57].
Рис. 5. Крива Каплана – Мейєра виживаності без подій пацієнтів із тяжким СОАС (ІАГ ≥30 епізодів за 1 год)
Примітка: Адаптовано за C.H. Lee et al., 2011.
Однак дані деяких невеликих випробувань ставлять під сумнів надійність досліджень сну, проведених під час гострих СС-подій [13, 103]. Серед 18 пацієнтів, госпіталізованих із нестабільною стенокардією, ІМ чи лівошлуночковою недостатністю, поширеність розладів дихання під час сну становила 56% при поступленні до стаціонара, а через шість тижнів зменшилася до 28%. Автори вважають, що порушення дихання під час сну в осіб із гострими СС-подіями можуть бути тимчасовими, а дослідження сну для підтвердження/виключення СОАС як потенційного ФР СС-захворюваності слід проводити, коли хворий клінічно стабільний [103].
У невеликому дослідженні, яке включало 40 хворих на гострий ІМ, поширеність СОАС (ІАГ ≥15 епізодів за 1 год) протягом ≤5 днів після розвитку ІМ становила 55%. Протягом 12 тижнів після події кількість епізодів апное та гіпопное зменшилася серед пацієнтів, у яких спостерігали підвищення фракції викиду (ФВ) лівого шлуночка (ЛШ) порівняно із групою без її змін. Автори дійшли висновку, що поліпшення скоротливої функції ЛШ в осіб з ІМ пов’язане зі зменшенням обструктивних подій під час сну [13]. Однак слід зазначити, що розглянуті дослідження включали малі вибірки хворих.
Подібні результати були отримані також в інших роботах [65, 106]. У хворих на ІМ з елевацією сегмента ST та із вперше діагностованим СОАС при надходженні хворого до стаціонара частота останнього була 46%. Тяжкість СОАС у пацієнтів з ІМ із часом зменшилася, а зниження ІАГ корелювало із підвищенням ФВ ЛШ та зворотним ремоделюванням ЛШ [106]. У 36,9% осіб з ІМ та стабільною ІХС, які частіше мали ЦД, АГ, гіперліпідемію, хронічну хворобу нирок та більший індекс маси тіла (ІМТ), був діагностований СОАС (р<0,05 для всіх). Автори зазначають, що на частоту діагностики СОАС впливає час дослідження: СОАС частіше виявляли впродовж перебування хворих у стаціонарі, ніж при амбулаторному обстеженні (р=0,037) [65].
Як відомо, при ІМ з елевацією сегмента ST відбувається зниження скоротливості ЛШ, яка може покращитися через 3‑6 місяців [4]. До того ж транзиторний стан дисфункції міокарда під час гострої фази ІМ часто призводить до затримки рідини, яка перерозподіляється рострально до шиї під час сну, що викликає набряк верхніх дихальних шляхів і зворотний СОАС [15]. Слід також зазначити, що, на відміну від центрального апное сну та за відсутності порушень дихання під час нього, СОАС асоційований зі сферичним ремоделюванням серця протягом перших 12 тижнів після гострого ІМ, що пов’язано з негативними перепадами внутрішньогрудного тиску [26].
Систематичний огляд та метааналіз H. Wang et al. показав, що основні несприятливі серцеві події, як-то смерть, повторний ІМ, реваскуляризація, MACE (ВШ 2,28; 95% ДІ 1,24‑4,18; р=0,008) та смертність від усіх причин (ВШ 1,95; 95% ДІ 1,08‑3,54; р=0,03), були достовірно вищими у групі СОАС. Однак тяжкі ускладнення – серйозні несприятливі серцеві й цереброваскулярні явища (MACCE), повторний ІМ, реваскуляризація, інсульт, летальні випадки (ВШ 1,38; 95% ДІ 0,97‑1,98; р=0,07) і серцева смерть (ВШ 1,79; 95% ДІ 0,77‑4,16; р=0,18), істотно не відрізнялися [110].
Інші дані отримані у дослідженні в Йорданії за участю 398 хворих на ІХС, яким проводили коронарну ангіографію (≥50% стенозу принаймні однієї коронарної артерії). Відмінностей щодо поширеності симптомів та ймовірності СОАС між пацієнтами з/без ІХС не спостерігалося (р>0,05). Крім того, за допомогою логістичної регресії не було встановлено значущого зв’язку між ризиком СОАС та ІХС (скореговане ВШ 0,93; 95% ДІ 0,60‑1,44; р=0,752) [42].
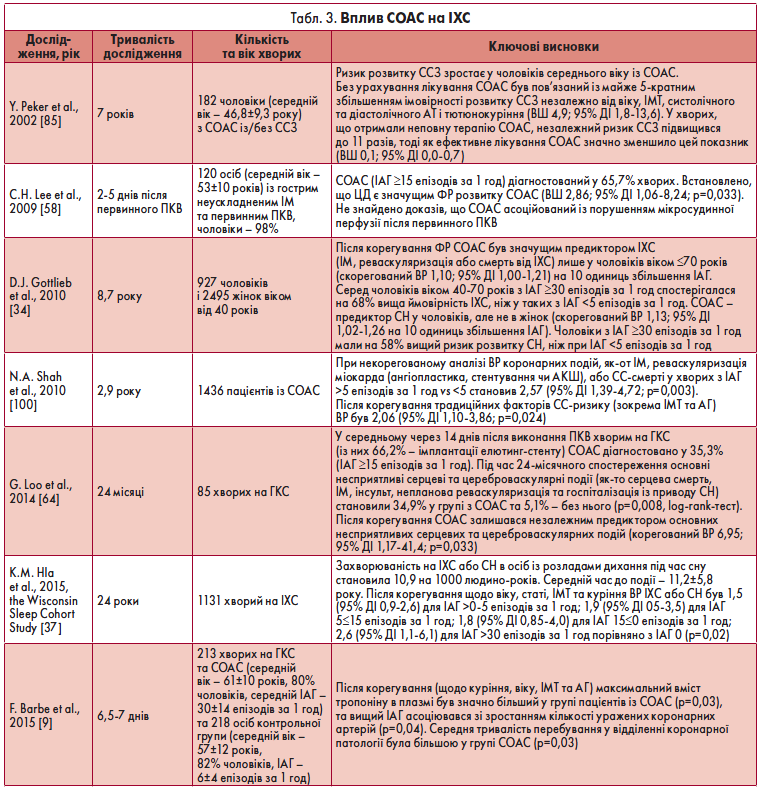
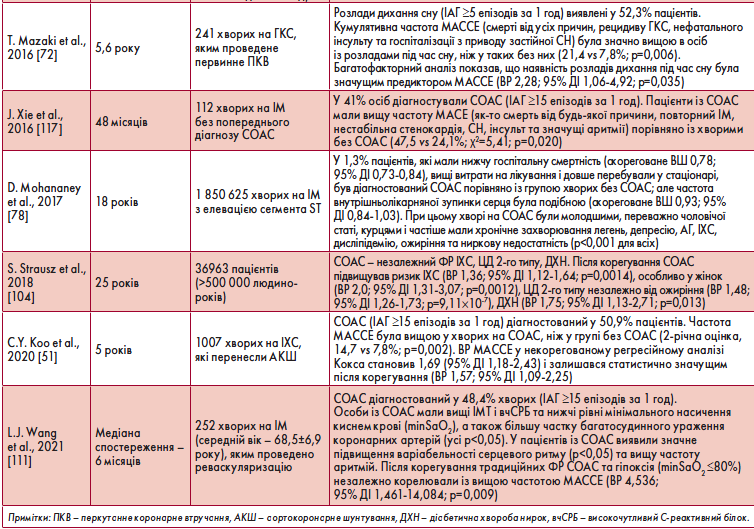
У таблиці 3 наведені дослідження, проведені з метою з’ясування зв’язку чи впливу СОАС на ІХС.
Продовження >>
Список літератури знаходиться в редакції.
Продовження читайте у наступному номері.
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 6 (79) 2021 р.