21 серпня, 2022
Лікування нейропатичного болю в осіб старшого віку
 При складанні плану ведення пацієнта з хронічним болем старшої вікової групи слід розглянути можливість комбінованого застосування фармакологічного та нефармакологічного втручань.
При складанні плану ведення пацієнта з хронічним болем старшої вікової групи слід розглянути можливість комбінованого застосування фармакологічного та нефармакологічного втручань.
Вибір лікарських засобів для фармакологічного контролю болю в осіб старших вікових груп потребує суворого персоніфікованого підходу.
Нефармакологічні методи
Продемонстровано високу ефективність мультимодального підходу у веденні пацієнтів із хронічним болем старших вікових груп. Фізична та професійна реабілітація в поєднанні з когнітивно-поведінковою терапією (КПТ) і руховою активністю чинять позитивний вплив у цій когорті пацієнтів, але відповідно до клінічних даних застосовуються недостатньо. Водночас стратегія мультимодального підходу забезпечує посилення терапевтичного альянсу між пацієнтом і медичним персоналом, оскільки сприяє підвищенню ефективності лікування хворих старших вікових груп із хронічним болем.
До нефармакологічних методів, які застосовують у пацієнтів із хронічним болем, належать [1] КПТ, акупунктура, адаптивні техніки медитації (mindfulness), масаж, фізична активність, тай-чи, йога.
КПТ являє собою неінвазивні й безпечні методики, спрямовані на зменшення болю, відновлення функціональної активності, а також поліпшення загального фізичного та психічного здоров’я. КПТ допомагає пацієнтам керувати стресом, самостійно знижувати сприйняття больових відчуттів і зменшувати больовий поріг. Для пацієнтів, які не мають доступу до психолога, навченого КПТ, рекомендуються методи зниження стресу, що допомагають покращити фізичне та психічне здоров’я. До методів зниження стресу належать медитація, йога, дихальні вправи. Такий підхід дає пацієнтам змогу долати неприємні емоції та фізичний дискомфорт і загалом покращує якість життя осіб із хронічним болем.
У нашій країні застосовують такі методики, як лазерна терапія, електромагнітні стимуляції, бальнео- й термотерапія тощо. Для пацієнтів із хронічним м’язово-скелетним болем, зокрема при остеоартриті або міофасціальному синдромі, фізіотерапія є неінвазивним методом лікування, спрямованим на підвищення рухливості, полегшення болю та в підсумку зниження інвалідності й поліпшення функціональної активності пацієнта. За неможливості проведення фізіотерапії в домашніх умовах застосовується лікувальна фізкультура (вправи на розтяжку), також зменшенню болю може сприяти термотерапія тощо. Можна розглянути застосування й таких методик, як йога, тай-чи, ходьба. Слід наголосити, що аеробні фізичні вправи підбираються індивідуально. Наприклад, пацієнтам старших вікових груп із хронічним болем і скутістю можуть бути рекомендовані вправи у воді для підтримки рухливості суглобів і зменшення болю.
Серед додаткових методів лікування, що зменшують вираженість болю, – акупунктура, масаж та ін. Треба зауважити, що немає переконливих даних стосовно ефективності зазначених методик. Водночас включення їх у план лікування позитивно впливає на функціональний, фізичний і ментальний стани геронтологічних пацієнтів, сприяє найефективнішому знеболюванню.
Медикаментозна терапія
Незважаючи на важливість проблеми знеболювання в геріатричних пацієнтів із хронічним больовим синдромом, є нечисленними дослідження, присвячені застосуванню в цій популяції аналгетиків [2-4]. Залишається нез’ясованим, яка частка людей похилого віку приймає аналгетики та яким із них віддається перевага. У фінському популяційному дослідженні [5], що включало 1420 пацієнтів віком 62-86 років, вивчали ефективність аналгетиків із застосуванням опитувальника якості життя SF‑36. Серед усіх учасників дослідження 84% купували рецептурні аналгетики протягом 1 року. Встановлено, що 77% припадало на нестероїдні протизапальні препарати (НПЗП), 41% – на парацетамол, 32% – на опіоїди, 17% – на габапентиноїди, 7% – на трициклічні антидепресанти. Вік хворих не мав істотного впливу на вибір препарату. Автори звернули увагу на необхідність правильної оцінки болю та важливість персоніфікованого підходу для вибору аналгетика з огляду на наявність у пацієнтів протипоказань до препаратів та уточнення характеристик болю, а також немедикаментозне знеболювання з метою оптимізації лікування болю в людей похилого віку.
Одним з основних принципів лікувальної тактики в геріатрії є вибір простішого способу введення препарату (переважно пероральний або трансдермальний) із невеликою кратністю. Для контролю хронічного болю не рекомендується парентеральне введення аналгетиків, оскільки знеболювальний ефект препарату хоч і настає швидко, проте є короткочасним. Для пацієнтів із легким хронічним болем рекомендовано неопіоїдні аналгетики, як-от НПЗП або ацетамінофен.
Ацетамінофен (парацетамол)
Ацетамінофен, також відомий як парацетамол, є широко доступним аналгетиком і жарознижувальним засобом, що рекомендується більшістю світових геріатричних асоціацій як початкова терапія в пацієнтів віком понад 60 років із хронічним болем легкої або помірної інтенсивності для усунення больового синдрому будь-якої етіології [6].
Механізм дії парацетамолу остаточно не вивчений, але показано, що він активує низхідні серотонінергічні інгібувальні шляхи в центральній нервовій системі, завдяки чому знижується сприйняття болю [7].
Ацетамінофен приймають у дозі 325-650 мг перорально що 6 год (рекомендований максимум – 3 г на день, а в пацієнтів зі старечою астенією чи віком понад 80 років – 2 г на день) [8]. Потрібно попереджати пацієнтів про наявність парацетамолу в більшості жарознижувальних препаратів і комбінованих засобів з аналгетичним ефектом, щоб мати змогу точніше моніторувати добову дозу.
За аналгетичним ефектом парацетамол значно поступається НПЗП, але він, як і раніше, залишається препаратом першого вибору в пацієнтів старших вікових груп із хронічним больовим синдромом, адже вважається відносно безпечним щодо профілю побічних ефектів порівняно з НПЗП. Основним побічним ефектом ацетамінофену є гепатотоксичність через передозування препарату.
Ацетамінофен варто призначати з обережністю в пацієнтів із печінковою недостатністю або хронічним зловживанням алкоголем в анамнезі. Препарат може зумовлювати статистично (й, можливо, клінічно) значне підвищення міжнародного нормалізованого відношення (МНВ) у пацієнтів, які приймають варфарин. Попри те що це не є прямим протипоказанням, якщо після виписки зі стаціонара рекомендується продовження прийому ацетамінофену в людей похилого віку, мабуть, потрібне ретельне спостереження за рівнем МНВ.
Слід зазначити, що в одному систематичному огляді при болю в спині й остеоартриті парацетамол не підтвердив свою ефективність [10], але пізніші систематичні огляди довели аналгетичний потенціал препарату при цих патологіях [11].
Нестероїдні протизапальні засоби
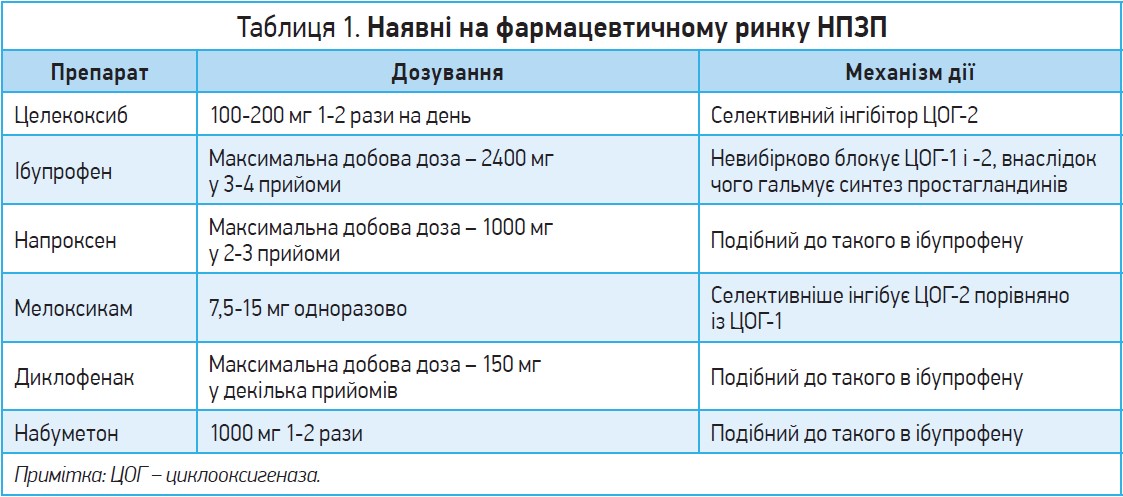
Якщо біль адекватно не контролюється парацетамолом, можна розглянути призначення іншого класу широкодоступних лікарських засобів – НПЗП, які мають протизапальну, жарознижувальну та знеболювальну дії. Ці засоби зменшують біль від легкої до помірної інтенсивності запального генезу, зокрема при остеоартриті або ревматоїдному артриті. НПЗП широко представлені на фармацевтичному ринку, відрізняються режимом дозування та профілем безпеки (табл. 1). За неефективності в конкретного пацієнта одного препарату з класу НПЗП може бути доцільним спробувати призначити інший препарат із цього класу.
НПЗП зменшують біль, зворотно інгібуючи активність ферментів ЦОГ‑1 і -2, й таким чином запобігають синтезу простагландинів, які опосередковують запалення, а також передачу болю. НПЗП, що діють неселективно, не рекомендуються для тривалого застосування через побічні ефекти, пов’язані з інгібуванням ЦОГ‑1. Останній присутній у всьому організмі й окрім інших ефектів відіграє роль у захисті слизової оболонки шлунка, підтримці ниркової та печінкової функцій. Пацієнти, котрі приймають НПЗП протягом будь-якого періоду часу, мають перебувати під наглядом щодо симптомів шлунково-кишкового болю або кровотечі. Слід бути обережними, призначаючи НПЗП або ацетилсаліцилову кислоту літнім людям, які отримують антикоагулянтну терапію, через підвищений ризик виникнення кровотечі. Серед інших ускладнень тривалого прийому НПЗП – підвищений ризик розвитку серцево-судинних захворювань і хвороб нирок.
ЦОГ‑2 присутній в організмі в нижчих концентраціях і експресується у відповідь на запалення або пошкодження. Застосування НПЗП, які вибірково блокують ЦОГ‑2 (наприклад, целекоксиб), ефективно зменшує запалення та біль. Однак селективні ЦОГ‑2 НПЗП не позбавлені ризику й подібно до неселективних засобів цієї групи асоціюються з підвищеним ризиком настання серцево-судинних подій.
Більшість НПЗП переконливо довели свою ефективність у терапії гострого та хронічного болю, в тому числі в осіб віком понад 60 років. Такі НПЗП, як ібупрофен, напроксен, кетопрофен і диклофенак, можуть застосовуватися з обережністю в людей похилого віку (кеторолак також може використовуватися, хоча є менш бажаним з огляду на критерії Бірса) [12].
При легкому гострому болю ібупрофен призначають по 400 мг що 4-6 год у міру потреби, максимальна доза становить 3200 мг на день [13]. Систематичний огляд показав, що 400 мг ібупрофену є кращими, ніж 1000 мг парацетамолу для полегшення гострого болю, але було зазначено, що комбінація ібупрофену та парацетамолу ефективніша за будь-який аналгетик у вигляді монотерапії [14].
Рекомендується призначення НПЗП пацієнтам віком понад 60 років із сильним ноцицептивним хронічним болем у спині та/або суглобах або як компонент мультимодальної терапії при онкологічному болю [15]:
- у мінімально ефективних дозах, достатніх для настання знеболювального ефекту;
- короткими курсами (не більш як 14 днів);
- з урахуванням ризику небажаних ефектів із боку шлунково-кишкового тракту та серцево-судинної системи.
Особливу увагу варто звертати на небажані ефекти НПЗП (гастротоксичність, нефротоксичність, тромбоемболічні ускладнення, підвищення артеріального тиску), а також ураховувати зміни фармакокінетики в осіб старших вікових груп. Це потребує дуже серйозного аналізу клінічної ситуації та зважування ризику розвитку небажаних ефектів.
Тому пацієнта, якому рекомендовано прийом НПЗП, слід попередити про необхідність здійснення 3-4 рази на день контролю рівня артеріального тиску з консультацією лікаря при його підвищенні [16]. Обов’язковим є моніторинг скарг із боку шлунково-кишкового тракту. Це зумовлено тим, що ризик гострого ерозивно-виразкового ураження гастродуоденальної слизової оболонки на тлі прийому НПЗП різко збільшується в літніх пацієнтів з атеросклерозом аорти та серцевою недостатністю, що призводять до хронічної ішемії гастродуоденальної слизової оболонки.
За появи небажаних ефектів у разі прийому НПЗП найперше слід переглянути показання до їх використання, а за неможливості скасування ліків – зменшити дозу або призначити препарат із найменшою кількістю побічних ефектів.
При виборі інгібіторів протонного насоса для лікування пацієнта з поєднаною (ревматичною, кардіологічною та неврологічною) патологією велику роль відіграють особливості лікарської взаємодії. Важливе значення надається впливу на ізофермент печінки CYP2C19, оскільки він бере участь у метаболізмі значної кількості лікарських засобів. Показано, що омепразол і частково лансопразол уповільнюють метаболізм варфарину, клопідогрелу, дигоксину, ніфедипіну, фенітоїну, теофіліну, карбамазепіну, циклоспорину, діазепаму [17]. Крім того, важливою є pH‑селективність інгібіторів протонного насоса, низьке значення котрої розглядають як патогенетичний механізм потенційних побічних ефектів за тривалої терапії цими препаратами, оскільки протонні насоси (H+/K+- або H+/Na+-АТФази) крім парієтальних клітин виявлено в клітинах інших органів і тканин: в епітелії кишечнику та жовчного міхура, рогівки, ниркових канальцях, м’язах, клітинах імунної системи (нейтрофілах, макрофагах і лімфоцитах), остеокластах та ін.
Не рекомендується призначення НПЗП пацієнтам віком понад 60 років із хронічним болем і старечою астенією, перенесеними серцево-судинними та цереброваскулярними катастрофами (або іншими станами, пов’язаними з високим і дуже високим серцево-судинним ризиком), перенесеними операціями на судинах (у тому числі судинах серця, шиї, голови, нижніх кінцівок), хронічною хворобою нирок у разі швидкості клубочкової фільтрації <30 мл/хв, оскільки ризик розвитку небажаних ефектів перевищує користь від їх застосування [18-21].
За наявності абсолютних протипоказань для призначення НПЗП рекомендується вибрати інші способи знеболювання чи направити пацієнта до клініки болю та/або до профільного фахівця (невропатолога, ревматолога, ортопеда, онколога, фахівця з паліативної медичної допомоги).
Трансдермальні аналгетики
НПЗП для місцевого застосування переважно накопичуються в цільових зонах із концентраціями, що в 7 разів вищі в хрящах і менісках і до 100 разів у сухожиллях, аніж у сироватці крові [22]. Місцеві аналгетики ідеальні для людей похилого віку з численними супутніми захворюваннями, як-от виразкова хвороба та серцево-судинні патології, за яких пероральні НПЗП відносно протипоказані.
Із метою усунення больового синдрому рекомендується призначення місцевих форм НПЗП (креми, мазі, гелі, пластирі) пацієнтам віком понад 60 років із болем у спині та/або суглобах з урахуванням сумарної добової дози зазначених засобів [23].
Наприклад, у літніх пацієнтів із ризиком розвитку побічних ефектів, пов’язаних із системними НПЗП, можливе місцеве застосування 1% гелю диклофенаку, що втирається в неушкоджену хворобливу ділянку, наприклад суглоб, уражений остеоартритом, або при інших запальних станах. Дані високої якості з дослідження за участю значної кількості пацієнтів виявили невеликі переваги курсу тривалістю понад 12 тиж. При цьому слід ретельно контролювати кількість суглобів, на які наноситься місцевий НПЗП, а також ураховувати, чи приймає пацієнт додатково будь-який пероральний НПЗП, через потенційний ризик перевищення загальних рекомендованих доз.
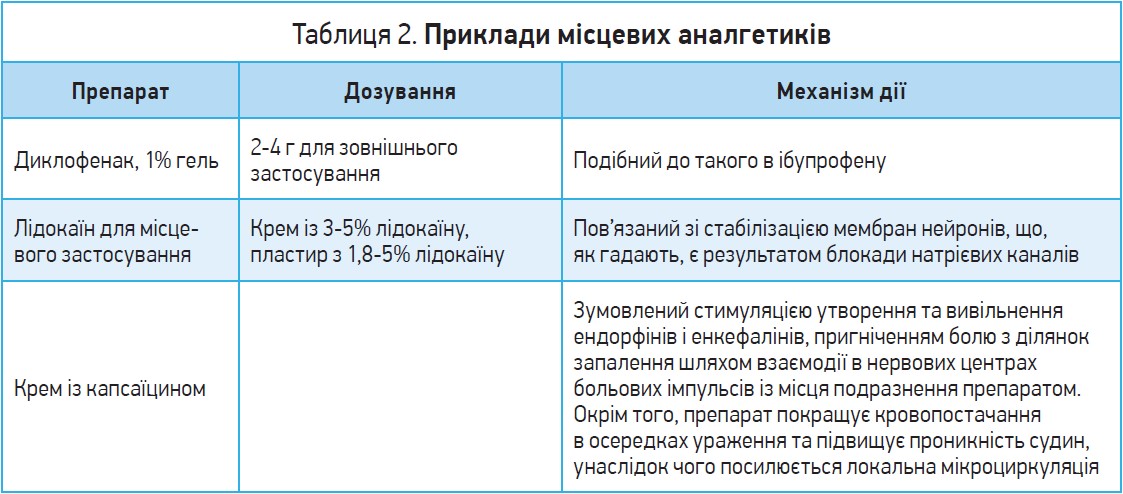
До місцевих аналгетиків належать такі засоби, як диклофенак, кетопрофен, ібупрофен, пластир із 4-5% лідокаїном, крем із капсаїцином (табл. 2).
Призначення лідокаїну (пластир, гель, крем) рекомендується пацієнтам віком понад 60 років із хронічним нейропатичним болем, включаючи постгерпетичну невралгію, з метою зниження інтенсивності болю [24-27]. Топічні форми лідокаїну в концентрації не менш як 5% здатні знижувати інтенсивність нейропатичного болю, включаючи випадки постгерпетичної невралгії. Рекомендовано креми та пластирі. Можливим є розвиток слабких шкірних реакцій, які зникають після припинення використання.
Перевагами такої терапії є легкість застосування, відсутність токсичності та лікарських взаємодій. У клінічному дослідженні в пацієнтів із діабетичною полінейропатією порівнювали ефективність застосування 5% лідокаїну у вигляді пластиру та прегабаліну. Відзначено зіставний ефект в обох групах терапії. Проте в групі місцевого застосування лідокаїну зареєстровано менше побічних ефектів і випадків скасування терапії. Це дає змогу рекомендувати аплікацію 5% лідокаїну при нейропатичному болю в пацієнтів, які не можуть приймати ліки per os.
Крем із капсаїцином рекомендовано при остеоартриті, нейропатичному болю, постгерпетичній невралгії. Тривалість терапії – до 13 тиж.
Показаннями для призначення місцевих аналгетиків є нейропатії, артралгії, міалгії, больовий синдром у разі захворювань навколосуглобових тканин, люмбоішіалгія, забиті місця, гострий герпетичний оперізувальний лишай та ін. [28].
Наркотичні аналгетики
Цікаві дані метааналізу, що включав 41 рандомізоване клінічне дослідження [29], в яких оцінювали ефективність опіоїдів у лікуванні різних форм хронічного неонкологічного болю, в тому числі болю в спині, за остеоартриту, ревматоїдного артриту, діабетичної нейропатії. Встановлено, що в середньому опіоїди можуть забезпечити незначне зниження інтенсивності болю та функціональне поліпшення порівняно з плацебо й аналогічне зменшення болю, але менш виражене поліпшення функціонального стану порівняно з іншими аналгетиками.
Отже, наркотичні аналгетики пацієнтам віком понад 60 років із хронічним болем неонкологічного походження не рекомендовано через відсутність надійних доказів ефективності при хронічному скелетно-м’язовому та нейропатичному болю [30-34].
Інші препарати для лікування хронічного болю
Ці лікарські засоби часто відносять до ад’ювантних, оскільки вони спочатку призначалися при станах, відмінних від болю, як-от депресія або судоми, проте багато із цих препаратів можна використовувати як терапію першої лінії при певних хронічних больових станах.
Протиепілептичні препарати
У 1993 р. у клінічну практику впроваджено протисудомний препарат другого покоління габапентин. Надалі було встановлено, що засіб також є ефективним у лікуванні низки хронічних нейрогенних больових синдромів, зокрема при діабетичній нейропатії, постгерпетичній невралгії та невралгії трійчастого нерва. Ефективність і безпека прегабаліну та габапентину в усуненні больового синдрому надійно досліджені в пацієнтів старших вікових груп із нейропатичним болем [35].
Терапію слід розпочинати з мінімальної дози (прегабалін – 75 мг, габапентин – 200 мг), поступово титруючи її до настання знеболювального ефекту (максимальна доза в клінічних дослідженнях для прегабаліну – 600 мг, габапентину – 1800 мг). У перші дні прийому можливий розвиток психотропного ефекту, загальмованості. Така дезорієнтація може спровокувати падіння або призвести до того, що пацієнти прийматимуть неправильні дози. Не рекомендується керування автотранспортом під час прийому цих препаратів.
Екскреція прегабаліну та габапентину здійснюється нирками, що потребує оцінювання функції нирок перед призначенням такої терапії та титрування дози. Лікування починається з найменшої дози з подальшим збільшенням до терапевтичної на підставі даних щодо відповіді на терапію та переносимості препарату.
Не рекомендується призначати похідні бензодіазепіну пацієнтам віком понад 60 років із хронічним болем через високий ризик виникнення небажаних ефектів, серед яких седація, сплутаність свідомості та падіння [8]. На тлі терапії карбамазепіном підвищується ризик розвитку гіпонатріємії та блокади синтезу антидіуретичного гормону [36]. Крім того, карбамазепін є потужним індуктором цитохрому Р450, який може впливати на метаболізм інших препаратів, особливо з вузьким терапевтичним індексом, як-от варфарин або літій.
Антидепресанти
Трициклічні антидепресанти й інгібітори зворотного захоплення серотоніну та норадреналіну можуть використовуватися для лікування хронічного болю. Підвищуючи активність серотоніну й норадреналіну, ці препарати модулюють больовий шлях, пригнічуючи висхідні больові шляхи та стимулюючи низхідні гальмівні шляхи.
У ранніх дослідженнях було відзначено позитивний вплив трициклічних антидепресантів (амітриптилін та іміпрамін) як допоміжної терапії при лікуванні невропатичного болю, діабетичної нейропатії та скелетно-м’язового болю. Незважаючи на ефективність у низьких дозах, трициклічні антидепресанти мають потужну антихолінергічну активність, що призводить до розвитку побічних ефектів, особливо в геронтологічній популяції. Ці побічні ефекти включають ортостатичну гіпотензію, седацію (обидва препарати збільшують ризик падіння), нудоту, нечіткість зору, затримку сечі, запори, аритмії тощо. У зв’язку із цим зазначені препарати в більшості випадків протипоказані пацієнтам старших вікових груп.
Селективні інгібітори зворотного захоплення серотоніну та норадреналіну (дулоксетин) теж варто призначати з обережністю через їхню серотонінергічну активність і збільшення ризику падінь. Рекомендується призначення дулоксетину пацієнтам віком понад 60 років із хронічним болем за наявності симптомів депресії з метою найефективнішого усунення больового синдрому [37]. Крім того, дулоксетин може розглядатися для призначення в пацієнтів віком понад 60 років із хронічним нейропатичним болем і протипоказаннями та/або непереносимістю антиконвульсантів [37]. Рішення про необхідність такої терапії потрібно приймати колегіально з невропатологом. Варто звертати увагу й на наявність у пацієнта в анамнезі падінь і переломів, оскільки експерти Американського геріатричного товариства (AGS, 2019) радять уникати призначення селективних інгібіторів зворотного захоплення серотоніну та норадреналіну таким пацієнтам [38]. Також слід ретельно моніторувати пацієнтів на комбінованій терапії, що включає антиконвульсанти та дулоксетин, уживати надійніших заходів щодо зниження ризику падінь і профілактики когнітивних порушень.
Не рекомендується використовувати венлафаксин через ризик виникнення гіпонатріємії, запаморочення та болю в животі [7]. У дослідженнях відзначено прогіпертензивний ефект венлафаксину в пацієнтів старших вікових груп.
Міорелаксанти
Пацієнтам із хронічним м’язово-скелетним болем від помірного до тяжкого можуть бути показані міорелаксанти. Проте з урахуванням змін м’язово-скелетної системи в процесі старіння ефективність цих препаратів у геронтологічній популяції значно знижується. Разом із тим усі міорелаксанти мають потенційні побічні ефекти седативної й антихолінергічної дій, що збільшують ризик падінь [38]. Отже, цей клас препаратів рекомендовано молодшим пацієнтам для лікування м’язового спазму, пацієнтам із хронічними скелетно-м’язовими болями та ін.
Лікування хронічного болю в геронтологічній популяції є складним завданням. Урахування фізіологічних основ старіння, знання механізмів нейропатичного болю, фармакологічних властивостей застосовуваних лікарських засобів дають змогу скласти індивідуальний план лікування больового синдрому, що ґрунтується на мультимодальному підході. Він передбачає терапію не лише основного захворювання, внаслідок якого в пацієнта розвинувся больовий синдром, а й коморбідних станів геріатричних синдромів, і спрямований на збільшення мобільності та покращення якості життя пацієнта.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 5-6 (522-523), 2022 р.