20 січня, 2023
Вірусний гепатит С
Клінічна настанова, заснована на доказах
Вірусні гепатити (ВГ) В і С становлять загрозу громадському здоров’ю, оскільки 96% цирозу печінки (ЦП) та гепатоцелюлярної карциноми (ГЦК) викликані саме цими двома типами ВГ. За даними Всесвітньої організації охорони здоров’я (ВООЗ), у світі тільки 9% осіб із хронічним вірусним гепатитом В (ВГВ) знають про свій діагноз і 20% – про вірусний гепатит С (ВГС). В Україні, за оціночними даними, 1 342 418 осіб інфіковані ВГС, під медичним наглядом перебуває 87 269 осіб, що становить 6,5% від оціночної кількості. ВГВ інфіковані 559 341 осіб, під медичним наглядом перебуває 23 631 особа (4,2%). В останні роки лікування таких пацієнтів значно покращилося завдяки поглибленому розумінню патофізіології захворювання, розвитку діагностичних процедур та поліпшенню лікування і профілактики. Рекомендації Європейської асоціації з дослідження печінки (EASL) щодо лікування ВГС описують оптимальну тактику ведення пацієнтів із гострим та хронічним ВГС, починаючи з 2018 р.
У листопаді 2019 року Україна приєдналася до Глобальної стратегії з елімінації вірусних гепатитів B та C, ухваливши Державну стратегію протидії ВІЛ-інфекції/СНІДу, туберкульозу та ВГ до 2030 року, цілями реалізації якої є:
- попередження 90% нових випадків ВГ;
- 90% осіб, що хворіють на ВГ, будуть продіагностовані та знатимуть про свою хворобу;
- до 90% хворих отримають ефективне лікування, яке призведе до повного одужання (для ВГ C) або ефективного контролю хвороби (для ВГ B).
Завдяки низці адвокаційних заходів Міністерства охорони здоров’я України, міжнародних організацій та неурядових організацій в Україні забезпечено доступ до генеричних форм лікарських засобів. Наразі зареєстровано 11 таких препаратів для лікування ВГС, які закуповуються за кошти державного бюджету, що допомогло збільшити обсяги лікування.
Вступ
Інфікування ВГС є однією з основних причин хронічного захворювання печінки в усьому світі [1]. Ураження печінки при ВГС може варіюватися від мінімальних гістологічних змін до вираженого фіброзу та ЦП із ГЦК або без неї. Приблизно 71 млн людей мають хронічний ВГС [1, 2]. Багато з них не знають про свій статус, їх кількість відрізняється залежно від географічної зони.
Основною метою лікування ВГС є повне виліковування інфекції, тобто досягнення стійкої вірусологічної відповіді (СВВ), яка визначається як невиявлення РНК ВГС на 12-ий (СВВ12) або 24-ий тиждень (СВВ24) після закінчення лікування. Досягнення СВВ означає виліковування ВГС, з дуже низькою ймовірністю рецидиву. СВВ зазвичай асоціюється з нормалізацією рівня печінкових ферментів та поліпшенням або зникненням некрозапалення печінки і фіброзу у пацієнтів без ЦП. Пацієнти з вираженим фіброзом (F3 за шкалою METAVIR) або ЦП (F4) мають ризик розвитку небезпечних для життя ускладнень. Однак фіброз може регресувати, і ризик розвитку ускладнень, таких як печінкова недостатність та портальна гіпертензія, зменшується після досягнення СВВ. Останні дані показують, що ризик виникнення ГЦК та пов’язаний із захворюваннями печінки рівень смертності значно знижуються, але не зникають у пацієнтів із ЦП, які вилікували ВГС, порівняно з пацієнтами, які не отримували лікування, та респондентами, які не досягли СВВ, особливо за наявності кофакторів захворюваності, таких як метаболічний синдром, зловживання алкоголем та/або одночасне інфікування ВГВ [3-9]. ВГС також асоціюється з низкою позапечінкових проявів захворювання, й елімінація вірусу викликає пригнічення більшості з них, що зменшує загальну смертність [10-16].
Ці рекомендації EASL щодо лікування ВГС призначені для допомоги лікарям та іншим медичним працівникам, а також пацієнтам у прийнятті клінічних рішень шляхом опису поточної оптимальної тактики лікування пацієнтів із гострим та хронічним ВГС. Рекомендації включають схеми лікування, схвалені Європейським агентством з контролю лікарських засобів та іншими національними європейськими агенціями на момент публікації.
Діагностика гострого та хронічного ВГС
Антитіла ВГС виявляються у сироватці або плазмі крові за допомогою імунологічного ферментного аналізу (ІФА) у переважної більшості пацієнтів із ВГС, однак результати ІФА можуть бути негативними на ранній гострій фазі ВГС і у пацієнтів, які пройшли курс імуносупресивної терапії. Після спонтанного кліренсу вірусу або кліренсу вірусу, який настав після проходження лікування, антитіла до ВГС все ще визначаються при відсутності РНК ВГС, але їх рівень може знижуватися й остаточно зникнути у деяких осіб [18-20].
Діагноз гострий та хронічний ВГС ґрунтується на виявленні РНК ВГС у сироватці або плазмі крові чутливим, якісним або якісним та кількісним молекулярним методом. Рекомендовані обстеження з нижчою межею виявлення ≤15 міжнародних одиниць (МО)/мл. Однак переважна більшість пацієнтів із показанням до лікування ВГС мають рівень РНК ВГС вище 50 000 МО/мл [21]. Існує потреба у доступних (дешевше 5-10 доларів США) діагностичних системах, які можна застосовувати для широкомасштабної діагностики в регіонах із низьким і середнім рівнем доходу, а також у певних умовах у країнах із високим рівнем доходу. Такі обстеження на виявлення РНК ВГС повинні мати нижчу межу виявлення ≤1000 МО/мл (3,0 Log10 МО/мл). За таких умов ризик отримання хибнонегативного результату вкрай низький. У середовищі, де кількість інфікованих незначна, застосування зазначених методів має значні переваги з точки зору збільшення доступу до діагностики більшої кількості населення. Дослідження пацієнтів із хронічним ВГС (генотип 1) виявило лише 4 із 2472 пацієнтів (0,16%) із рівнем РНК ВГС нижче 1000 МО/ мл [22].
Ядерний антиген (core Ag) ВГС у сироватці або плазмі крові є маркером реплікації ВГС. Метод його виявлення можна використовувати замість методу виявлення РНК ВГС для діагностики гострого або хронічного ВГС. Обстеження на виявлення core Ag ВГС менш чутливі, ніж обстеження на виявлення РНК ВГС (нижня межа виявлення еквівалентна приблизно 500-3 000 РНК ВГС МО/мл залежно від генотипу) [23-25]. У результаті core Ag ВГС виявляється в сироватці або плазмі крові через кілька днів після РНК ВГС у пацієнтів із гострим ВГС. У рідких випадках core Ag ВГС не визначається за наявності РНК ВГС [26]. Діагноз гострого ВГС може бути встановлений з упевненістю, якщо нещодавно була задокументована сероконверсія до антитіл ВГС, оскільки не існує серологічного маркера, який свідчить, що ВГС вперше діагностований у гострій фазі. Не всі пацієнти із гострим ВГС будуть мати позитивний результат при виявленні антитіл до ВГС. У цих випадках гострий ВГС можна припустити, якщо клінічні ознаки та симптоми є схожими із гострим гепатитом (рівень аланінамінотрансферази (AЛT) >10 разів перевершує норму та/або наявна жовтяниця), за відсутності анамнезу хронічного захворювання печінки або інших причин розвитку гострого гепатиту та/або, якщо відомо про нещодавній контакт із джерелом інфекції/або шлях передачі інфекції. В усіх випадках РНК ВГС (або core Ag ВГС) може бути виявлений протягом гострої фази, хоча їх рівні можуть дуже варіювати, і можуть бути проміжки часу (до декількох тижнів), коли РНК ВГС (або core Ag ВГС) не є визначальним. Таким чином, РНК-негативні пацієнти повинні бути повторно протестовані через 12 та 24 тижні для підтвердження остаточного кліренсу.
Реінфекція ВГС може настати після спонтанного кліренсу або кліренсу внаслідок лікування, особливо якщо пацієнти з високим рівнем ризику інфікування повторно піддаються ризику. Реінфекція визначається повторним виявленням РНК ВГС (або core Ag ВГС) після СВВ та демонстрації того, що інфекція зумовлена іншим штамом ВГС (інший генотип або пов’язаний штам за результатом філогенетичного аналізу, у випадку такого ж генотипу).
Реінфекцію треба припустити у випадках рецидиву ВГС після СВВ12 або СВВ24, якщо ризикована поведінка продовжується.
Діагноз хронічного ВГС базується на виявленні як ВГС-антитіл, так і РНК ВГС (або core Ag ВГС). Спонтанний вірусний кліренс рідко виникає через 4-6 місяців після набутої інфекції [27], тому діагноз хронічний ВГС можна встановити після цього періоду часу.
Рекомендації
- Усі пацієнти з підозрою на ВГС повинні пройти тестування на визначення антитіл до ВГС у сироватці або плазмі крові як перший діагностичний тест першого ряду (A1).
- При підозрі на гострий ВГС у пацієнтів із порушеною імунологічною реакцією та у пацієнтів на гемодіалізі треба провести аналіз на визначення РНК ВГС у сироватці або плазмі крові, що є частиною первинної оцінки (А1).
- Якщо ВГС-антитіла виявляються, РНК ВГС слід визначати за допомогою чутливого молекулярного методу з нижньою межею виявлення ≤15 МО/мл (А1).
- У країнах із низьким і середнім рівнем доходу та в окремих регіонах у країнах із високим рівнем доходу може бути використаний якісний аналіз РНК ВГС із нижньою межею виявлення ≤1000 МО/мл (3,0 Log10 МО/мл) для забезпечення можливості широкого доступу до діагностики та лікування ВГС (B2).
- Пацієнти з позитивним результатом на антитіла та негативним результатом на РНК ВГС повинні бути повторно протестовані на РНК ВГС через 12 та 24 тижні для підтвердження кліренсу (А1).
- Визначення антигену ВГС у сироватці або плазмі крові як маркеру реплікації ВГС може використовуватися замість визначення РНК ВГС для діагностики гострого або хронічного ВГС, коли обстеження на виявлення РНК ВГС не доступні (А1).
Скринінг хронічного ВГС
Основним бар’єром для елімінації ВГС все ще є той факт, що значна частина хворих із хронічним ВГС не знають про свій статус; при цьому існує велика різниця у відповідній статистиці між регіонами, країнами та групами ризику. Точні дані про поширеність і захворюваність на ВГС необхідні для аналізу масштабів пандемії в різних регіонах та розробки заходів охорони громадського здоров’я. Таким чином, скринінг ВГС необхідний для виявлення інфікованих осіб та залучення їх до програм догляду і лікування.
З огляду на місцеву епідеміологію, в різних регіонах були впроваджені різноманітні стратегії скринінгу. Групи з підвищеним ризиком інфікування ВГС можуть і повинні бути ідентифіковані та перевірені. У регіонах, де більшість пацієнтів належать до чітко визначеної вікової групи, тестування вікової когорти показало себе ефективним, хоча й з деякими обмеженнями [28-29]. Масове одноразове тестування було рекомендовано в країнах із високою ендемічністю та/або з метою повної ліквідації ВГС. Необхідно визначити оптимальні регіональні або національні підходи до скринінгу.
Скринінг ВГС ґрунтується на виявленні ВГС-антитіл. На додаток до скринінгу типу ІФА для перевірки рівня антитіл ВГС можна застосовувати швидкі діагностичні тести (ШТ). Для ШТ може використовуватися сироватка та плазма крові, цільна капілярна кров з пальця або слина, що полегшує процедуру скринінгу без необхідності венепункції, центрифугування, заморожування, а також кваліфікованих фахівців для забору зразків. ШТ дуже прості у виконанні та використовуються при кімнатній температурі без спеціальних приладів або попереднього навчання [30-32].
Якщо виявлені антитіла до ВГС, слід визначити наявність РНК ВГС (або як альтернатива – core Ag ВГС, якщо аналіз на РНК ВГС недоступний та/або занадто дорогий) для виявлення пацієнтів із хронічною інфекцією. Сьогодні більшість лабораторій використовують двоетапний підхід: крок 1 – обстеження на антитіла, крок 2 – визначення рівня РНК ВГС. У результаті значній частині пацієнтів, у яких виявлено антитіла до ВГС, не проводять обстеження на РНК ВГС для підтвердження інфекції. Тому, коли виявляють антитіла до ВГС, слід виконувати аналіз на РНК ВГС, якщо це можливо [33].
Сухі плями крові можуть використовуватися як зразки цільної крові для виявлення ВГС- антитіл методом ІФА у центральній лабораторії [34-36]. Додаткове вільне місце на картці можна використовувати для аналізу на РНК ВГС, що дозволяє провести аналіз у випадку виявлення антитіл.
ВООЗ ухвалила використання тест-систем на основі картриджу в закладах надання медичної допомоги [37]. Це потенційно спрощує алгоритми обстеження, збільшує рівень діагностування захворювання та розширює доступ до лікування, особливо в районах із низьким і середнім рівнем доходу, а також для неблагополучних верств населення, зокрема осіб, що вживають ін’єкційно наркотичні речовини. Залежно від витрат, прямий аналіз на РНК ВГС, а також експрес-тести можна вважати заміною скринінговим методам, заснованим на виявленні антитіл до ВГС, шляхом безпосередньої ідентифікації інфікованих осіб.
Рекомендації
- Необхідно розробити стратегії скринінгу на ВГС відповідно до епідеміологічної ситуації в регіоні, в ідеалі – в рамках національних планів (A1).
- Стратегія скринінгу на ВГС може включати скринінг осіб, що належать до груп ризику, тестування новонароджених, а також обстеження усієї популяції в районах із середнім та високим рівнем поширеності серологічних маркерів ВГС (≥2-5%) (B2).
- Скринінг на ВГС повинен ґрунтуватися на виявленні антитіл до ВГС у сироватці або плазмі крові методом ІФА (А1).
- Скринінг шляхом виявлення антитіл до ВГС має бути запропонований разом із профілактичними заходами, доглядом і лікуванням (A1).
- Цільну кров у вигляді сухих плям можна використовувати для виявлення антитіл до ВГС як альтернативу сироватці або плазмі крові, отриманій шляхом венепункції. У центральній лабораторії цільну кров буде використано для ІФА (А2).
- ШТ із використанням сироватки, плазми, цільної крові, отриманої з пальця, або кревікулярної рідини (слини) можна виконувати замість класичного ІФА, що проводиться безпосередньо в медичному закладі, для розширення доступу до скринінгу та збільшення доступності медичної допомоги (A2).
- Якщо було виявлено антитіла до ВГС, слід визначити наявність РНК ВГС (або як альтернативу core Ag ВГС, якщо аналіз на РНК ВГС недоступний та/або занадто дорогий) у сироватці або плазмі крові для виявлення пацієнтів із хронічною інфекцією (A1).
- Зразки цільної крові для сухих плям можуть бути використані як альтернатива сироватці чи плазмі, отриманій шляхом венепункції, для тестування на РНК ВГС після відправки у центральну лабораторію, де буде проводитися молекулярний аналіз (А2).
- У пацієнтів, у яких було виявлено ВГС-антитіла, слід проводити аналіз для виявлення РНК ВГС та сприяти скороченню часу між встановленням діагнозу та початком лікування (B1).
- Скринінговий аналіз на ВГС-антитіла може бути замінений аналізом на РНК ВГС із нижньою межею виявлення ≤1000 МО/мл (3,0 Log10 МО/мл) або аналізом на core Ag ВГС, якщо такі аналізи доступні і скринінгова стратегія з їх використанням виявиться економічно ефективною (C2).
Коментар робочої групи: у настанові EASL 2018 відсутній алгоритм скринінгу, діаностики та лікування, тому було вирішено додати фрагмент
Рекомендації WHO 2018
Короткий огляд поточних рекомендацій ВООЗ
Кого необхідно тестувати на інфекцію ВГС?
Настанова з тестування 2017 р. [3]
1. Цілеспрямоване тестування найбільш вразливих груп населення.
За будь-яких умов (незалежно від того, проводиться тестування у медичному закладі чи на рівні громади) рекомендовано пропонувати серологічне тестування на антитіла до ВГС1 із прив’язкою до послуг з профілактики, лікування та догляду наступним особам.
- Дорослим та підліткам із популяцій, найбільш уражених інфекцією ВГС2 (тобто представникам популяції з високим рівнем серопревалентності ВГС, мають в анамнезі контакти з інфекцією ВГС та/або дотримуються поведінки з високим ризиком інфікування).
Дорослим, підліткам та дітям із клінічною підозрою на хронічний ВГ3 (тобто особам із симптомами, ознаками, лабораторними маркерами ВГ) (наполеглива рекомендація, низька якість доказів).
Примітка. Періодичне повторне проведення тесту на визначення нуклеїнових кислот (ТНК) ВГС методом ПЛР слід розглядати в осіб, що мають постійний ризик інфікування або повторного інфікування.
2. Тестування загального населення.
За умов, коли серопревалентність антитіл до ВГС у загальній популяції становить ≥2% або ≥5%4, рекомендовано забезпечити проведення серологічного аналізу на ВГС в усіх дорослих із перенаправленням їх до отримання послуг із профілактики, лікування та догляду.
Підходи до загального тестування населення повинні передбачати використання наявних можливостей тестування на рівні громад, у медичних закладах, клініках з лікування ВІЛ або ТБ, закладах, що надають послуги з лікування наркотичної залежності, та жіночих консультаціях5 (умовна рекомендація, низька якість доказів).
3. Тестування вікових когорт.
Такий підхід можна застосовувати до певних вікових когорт, що мають більш високий ризик інфікування6 порівняно із загальною популяцією, де спостерігаються нижчі показники загальної поширеності захворювання (умовна рекомендація, низька якість доказів).
Як проводити тестування на хронічний ВГС та здійснювати моніторинг відповіді на лікування?
Настанова з тестування 2017 р. [3]
1. Яке серологічне тестування використовувати?
Для визначення серологічних даних щодо перенесеної у минулому або виявлення поточної інфекції у дорослих, підлітків та дітей (віком >18 міс)7 рекомендовано проводити серологічне дослідження на ВГС (антитіла чи антитіла/антиген) із використанням ШТ або лабораторного імунологічного дослідження8, що відповідатиме мінімальним стандартам безпеки, якості та продуктивності9 (з урахуванням як аналітичної, так і клінічної чутливості і специфічності).
В умовах обмеженого доступу до лабораторної інфраструктури і тестування та/або у групах населення, де доступ до швидкого тестування полегшить перехід до лікування та догляду, рекомендовано проводити ШТ (наполеглива рекомендація, якість доказів від низької до помірної).
2. Стратегії проведення серологічного тестування.
У дорослих та дітей віком старше 18 міс перед проведенням додаткового ТНК рекомендовано провести одне серологічне дослідження на первинне виявлення серологічних ознак перенесеної у минулому або виявлення поточної інфекції для підтвердження наявності вірусної інфекції (умовна рекомендація, низька якість доказів).
3. Виявлення вірусної інфекції.
Безпосередньо після отримання результату серологічного дослідження на реактивні антитіла до ВГС як краща стратегія діагностики вірусної інфекції рекомендовано використовувати кількісний або якісний ТНК для виявлення РНК ВГС (наполеглива рекомендація, помірна/низька якість доказів).
Дослідження для виявлення ядерного антигену ВГС (p22), що має клінічну чутливість, співставну з ТНК, є альтернативою проведення ТНК для діагностики на наявність вірусної інфекції (умовна рекомендація, помірна якість доказових даних).10
4. Оцінювання відповіді на лікування ВГС.
Для визначення результатів після завершення противірусного лікування, що тривало 12 або 24 тижні (тобто СВВ12 або СВВ24), слід використовувати ТНК для якісного або кількісного виявлення РНК ВГС (умовна рекомендація, помірна/низька якість доказів).
Скринінг на вживання алкоголю та консультування для зниження середнього і високого рівнів споживання алкоголю
Настанова з лікування ВГС 2016 р. [2]
В осіб із ВГС рекомендовано проводити оцінювання споживання алкоголю, після чого особам із середнім та високим рівнем споживання слід пропонувати поведінкові втручання для зниження рівня споживання алкоголю (наполеглива рекомендація, помірна якість доказів).
Визначення ступеня фіброзу та ЦП
Настанова з лікування ВГС 2016 р. [2]
В умовах обмежених ресурсів для виявлення фіброзу печінки рекомендовано використовувати APRI або FIB-4, уникаючи використання інших неінвазивних тестів, що потребують більшого обсягу ресурсів, зокрема еластографії або FibroTest (умовна рекомендація, низька якість доказів).
1 Це може включати комбіновані дослідження на антитіла/антигени IV покоління.
2 Сюди входять особи з популяції з вищою серопревалентністю (наприклад, деякі мобільні/мігруючі групи населення з країн із високою/проміжною ендемічністю та певні популяції корінного населення) або особи, що мають в анамнезі контакт із вірусом чи дотримуються поведінки з високим ризиком інфікування (наприклад, люди, які вживають ін’єкційно наркотичні речовини, ув’язнені, гомосексуальні чоловіки та секс-працівники, а також діти матерів із хронічним ВГС, особливо коінфікованих ВІЛ).
3 Ознаки, які можуть вказувати на основну хронічну інфекцію ВГС, включають клінічні ознаки наявного захворювання печінки, а саме: ЦП, ГЦК або захворювання печінки, причини якого не з’ясовані, включаючи патологічні результати функціональних проб печінки або УЗД печінки поза межами норми.
4 Поріг серопревалентності ≥2 або ≥5% було визначено на підставі декількох опублікованих порогових значень середнього та високого рівнів серопревалентності. Поточне визначення порогу залежатиме від інших міркувань на рівні країни й епідеміологічного контексту.
5 Планове дослідження на наявність ВГС у вагітних жінок проводити не рекомендовано.
6 Через наявність в анамнезі контактів із неперевіреними або неналежним чином перевіреними продуктами крові та/або низького рівня безпеки ін’єкцій.
7 У дітей віком до 18 міс наявність ВГС може бути підтверджена лише шляхом проведення вірусологічних аналізів на виявлення РНК ВГС, оскільки трансплацентарні материнські антитіла залишаються у крові дитини до 18 міс, що робить результати серологічних аналізів недостовірними.
8 Лабораторні імунологічні дослідження включають імуноферментний аналіз (ІФА), хемілюмінесцентний імуноаналіз (CLIA) та електрохемілюмінесцентний аналіз (ECL).
9 Дослідження повинні відповідати мінімальним критеріям прийнятності за прекваліфікацією ВООЗ або органу державного контролю лікарських засобів щодо засобів для проведення діагностики in vitro. Всі засоби для проведення діагностики in vitro повинні використовуватися відповідно до інструкцій виробників і, за можливості, у місцях тестування, зареєстрованих у національній або міжнародній системі зовнішнього оцінювання якості.
10 Нижчий рівень аналітичної чутливості можна розглядати, якщо дослідження може підвищити доступ (тобто дослідження, яке можна провести у медичному закладі, або для якого підходить зразок сухої краплі крові та/або доступність.
Виходячи з наявних даних, дослідження із порогом виявлення 3000 МО/мл або нижче може бути прийнятним та виявлятиме 95% осіб із вірусною інфекцією.
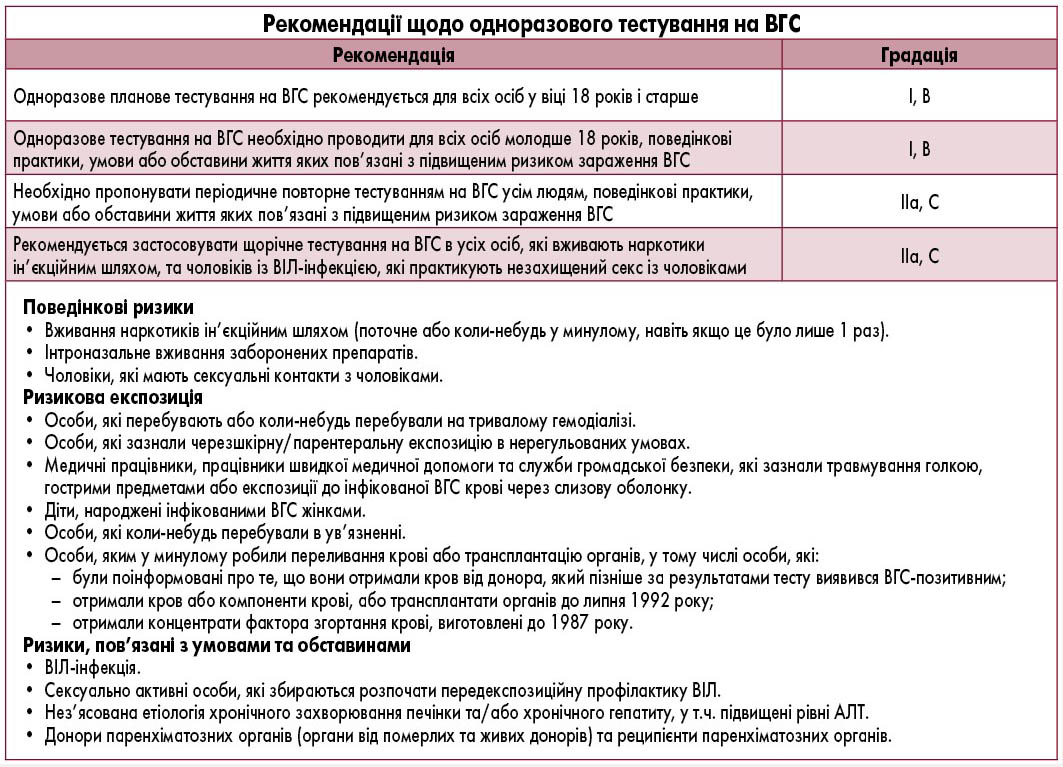
Коментар робочої групи: робоча група вважає, що одноразове тестування на хронічний ВГС в Україні має відповідати рекомендаціям настанови AASLD/IDSA, 2019.
Рекомендації щодо одноразового тестування на ВГС (AASLD/IDSA, 2019)
Цілі лікування ВГС
Метою терапії є ліквідація ВГС задля:
- запобігання ускладненням захворювань печінки та позапечінковим розладам, пов’язаним із ВГС, у тому числі некротичному запаленню печінки, фіброзу, ЦП, декомпенсованому ЦП, ГЦК, тяжким позапечінковим проявам і смерті;
- поліпшення якості життя пацієнтів і ліквідація стигми;
- запобігання наступній передачі вірусу.
Кінцевою точкою терапії є досягнення СВВ, що визначається як відсутність РНК ВГС у сироватці або плазмі крові через 12 (СВВ12) або 24 тижні (СВВ24) після закінчення лікування. Оцінка відбувається за допомогою чутливого молекулярного методу з нижньою межею виявлення ≤15 МО/мл. Як СВВ12, так і СВВ24 були прийняті регуляторними органами в Європі та США як кінцеві точки терапії, враховуючи те, що їх узгодженість становить >99% [38]. У регіонах, де чутливі тест-системи для виявлення РНК ВГС недоступні та/або занадто дорогі, для оцінки вірусологічної відповіді можна використовувати якісні аналітичні системи з нижньою межею виявлення ≤1000 МО/мл (3,0 Log10 МО/мл); у цьому випадку відповідь на лікування слід оцінювати через 24 тижні після завершення лікування (СВВ24).
Довгострокові спостереження за пацієнтами продемонстрували, що СВВ відповідає остаточному подоланню ВГС у переважній більшості випадків [39]. Визначення сore Ag ВГС через 24 тижні після завершення лікування може бути використано як альтернатива аналізу на РНК ВГС, для того щоб визначити СВВ24, відповідно, у пацієнтів, у яких було виявлено core Ag до початку лікування [23, 24, 26, 40].
У пацієнтів із вираженим фіброзом (за шкалою METAVIR відповідає стадії F3) і ЦП (F4) СВВ асоціюється зі зменшенням частоти декомпенсації захворювання, а також зменшенням, однак не повною ліквідацією, ризику розвитку ГЦК [8]. Таким чином, необхідно продовжити стеження за цими пацієнтами на випадок виникнення ГЦК.
Коментар робочої групи: для оцінки відповіді на противірусне лікування та прогнозування досягнення СВВ+ робоча група вважає за доцільне оцінювати також вірусне навантаження на 4-му та 12-му тижнях лікування.
Рекомендації
- Метою терапії є елімінація ВГС для:
- запобігання ускладненням захворювань печінки та позапечінковим розладам, пов’язаним із ВГС, зокрема некротичному запаленню печінки, фіброзу, ЦП, декомпенсації ЦП, ГЦК, тяжким позапечінковим проявам і смерті;
- поліпшення якості життя пацієнтів і ліквідації стигми;
- запобігання наступній передачі вірусу (A1).
- Кінцевою точкою терапії є відсутність РНК ВГС у сироватці або плазмі крові через 12 (СВВ12) або 24 тижні (СВВ24) після закінчення лікування, визначена за допомогою чутливої тест-системи (нижня межа для виявлення ≤15 МО/мл) (A1).
- Відсутність сore Ag ВГС через 24 тижні після завершення лікування (СВВ24) може бути використана як альтернативна кінцева точка терапії у пацієнтів, у яких було виявлено core Ag до початку лікування, якщо аналізи на РНК ВГС недоступні та/або занадто дорогі (A1).
- Відповідь на лікування слід оцінювати через 24 тижні після завершення лікування у регіонах, де чутливі тест-системи для виявлення РНК ВГС недоступні та/або занадто дорогі, для оцінки вірусологічної відповіді можна використовувати якісні аналітичні системи з нижньою межею виявлення ≤1000 МО/мл (3,0 Log10 МО/мл) (B1).
- У пацієнтів із вираженим фіброзом і ЦП слід продовжити спостереження після досягнення СВВ, оскільки ризик розвитку ГЦК зменшується, однак не зникає повністю (A1).
Попередня терапевтична оцінка
Необхідно оцінити тяжкість захворювання печінки, а також визначити базові вірусологічні параметри, що будуть корисними при виборі терапії.
Пошук інших причин захворювання печінки
Слід систематично досліджувати інші можливі причини хронічного захворювання печінки або фактори, які можуть впливати на перебіг або прогресування захворювання. Усіх пацієнтів слід обстежити на наявність інших вірусів, що передаються через кров, зокрема ВГВ і ВІЛ. Невакцинованим пацієнтам слід запропонувати вакцинацію проти ВГВ та ВГ А. Необхідно оцінити рівень споживання алкоголю та рекомендувати пацієнту скоротити вживання алкоголю, якщо є така проблема. Окрім того, ВГС може спричиняти розвиток різноманітних позапечінкових проявів, які необхідно враховувати під час лікування. Необхідно провести оцінку супутніх захворювань, зокрема серцево-судинних, алкоголізму, порушень функції нирок, аутоімунних розладів, генетичних або метаболічних захворювань печінки (наприклад, генетично зумовлений гемохроматоз, цукровий діабет або ожиріння) і можливість медикаментозно-індукованої гепатотоксичності.
Оцінка тяжкості захворювання печінки
До початку лікування необхідно провести оцінку тяжкості захворювання печінки. Особливо важливим є виявлення пацієнтів із ЦП (за шкалою METAVIR F4) або розвиненим (септальним) фіброзом (за шкалою METAVIR F3), оскільки вибір схеми лікування, а також прогноз після нього залежить від стадії фіброзу. Не потрібно оцінювати стадію фіброзу у пацієнтів із клінічними ознаками ЦП. У пацієнтів із ЦП слід оцінити прояви портальної гіпертензії, у тому числі варикозного розширення вен стравоходу. Кожні 6 місяців після завершення лікування потрібно обстежувати пацієнтів із вираженим фіброзом і ЦП на відсутність/наявність ГЦК. Оскільки у пацієнтів із вираженим фіброзом рівень АЛТ може бути в межах норми при кількаразовому визначенні рівня трансфераз, необхідно проводити оцінку тяжкості захворювання незалежно від рівня AЛТ.
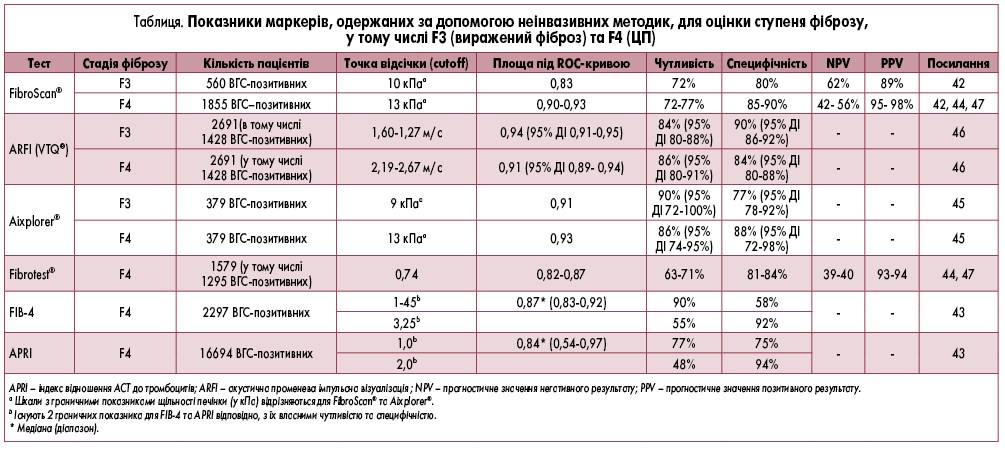
При хронічному ВГС для оцінки тяжкості захворювання печінки до початку лікування слід застосовувати неінвазивні методи діагностики замість біопсії. У пацієнтів із хронічним ВГС для оцінки фіброзу та наявності портальної гіпертензії можна використовувати визначення щільності печінки. Слід враховувати фактори, які можуть негативно впливати на проведення обстеження, такі як, наприклад, ожиріння, високий рівень АЛТ тощо. Також можна використовувати добре вивчені біомаркери фіброзу. Як визначення щільності печінки, так і біомаркери успішно використовують для встановлення наявності ЦП або відсутності фіброзу, але вони менш точні при визначенні проміжних стадій фіброзу [41]. Показники неінвазивних маркерів, на основі яких встановлюють стадії фіброзу у пацієнтів із хронічним ВГС до початку лікування, продемонстровано в таблиці [42-47]. У країнах із низьким і середнім рівнем доходу, а також у місцях, де лікування проводиться поза межами спеціалізованих клінік, тести для визначення індексу співвідношення рівня аспартатамінотрансферази (АСТ) до тромбоцитів (APRI) та фіброзу (FIB-4), як правило, доступні, прості у виконанні та дешеві, а отримані за їх допомогою дані достатньо достовірні. Неінвазивні методики не слід використовувати для визначення стадії фіброзу після проведення лікування, оскільки вони недостовірні на цьому етапі.
Комбінація біомаркерів крові або комбінація вимірювання щільності печінки та аналізів крові підвищують точність обстеження [48, 49]. Біопсія печінки може знадобитися у випадках, коли відомо або існує підозра, що захворювання має змішану етіологію (наприклад, метаболічний синдром, алкоголізм або аутоімунна патологія).
Коментар робочої групи: гістологічне дослідження пунктатів печінки за шкалою оцінок METAVIR є найбільш інформативним та об’єктивним, що дозволяє окремо враховувати як ступінь запалення, так і ступінь розвитку фіброзу печінки. В Україні проводиться, проте через інвазивність, високу вартість (більше 2000 грн) і для спрощення підходів до діагностики пацієнтів із ВГ цей метод рекомендований не на перших етапах обстеження.
Останніми роками виявлено недоліки біопсії, результатом цього стала поява неінвазивних методів оцінки фіброзу у пацієнтів із хронічним ВГС, що включають всебічний аналіз: біохімічні маркери, визначення індексу APRI та FIB-4, за наявності ресурсів проводиться еластографія чи FibroTest. Еластографія чи FibroTest призначаються також у випадках, коли результати APRI та FIB-4 потрапляють у «сіру зону» (для APRI це значення в межах 0,3-1,5, для FIB-4 – значення в межах 1,3-2,67).
Рекомендації
- Необхідно оцінити вплив коморбідних станів на перебіг захворювання печінки, а також запровадити відповідні коригувальні заходи (А1).
- Тяжкість захворювання печінки необхідно оцінити до початку лікування (A1).
- Слід виявляти пацієнтів із ЦП, оскільки необхідно коригувати їх схему лікування і обов’язково продовжувати спостереження за ними щодо ГЦК після завершення лікування (A1).
- Після завершення лікування також потрібно проводити спостереження за пацієнтами з вираженим фіброзом (за шкалою METAVIR F3) щодо ГЦК (B1).
- Попередньо необхідно оцінити ступінь фіброзу печінки за допомогою неінвазивних методів, біопсія печінки проводиться в окремих випадках або тоді, коли можливі додаткові етіологічні фактори (A1).
- Необхідно оцінити функцію нирок (креатинін/швидкість клубочкової фільтрації (ШКФ) (A1).
- Якщо виявлено відповідні симптоми, слід ідентифікувати позапечінкові прояви ВГС (А1).
- Невакцинованим пацієнтам необхідно запропонувати вакцинацію проти ВГВ та ВГ А (A1).
Якісні/кількісні аналізи на РНК ВГС та core Ag ВГС
Якісне/кількісне визначення РНК ВГС у сироватці або плазмі крові призначене для пацієнтів, які отримують противірусне лікування. Визначення РНК ВГС повинно проводитися за допомогою достовірного чутливого аналізу, рівні РНК ВГС повинні бути виражені в МО/мл. Якісний та кількісний аналіз на виявлення core Ag ВГС за допомогою ІФА може бути виконаний, коли тести на РНК ВГС недоступні і/або занадто дорогі. Визначення рівня core Ag ВГС повинно виконуватися за допомогою достовірного аналізу і відображати рівні антигену в моль/л.
Визначення генотипу ВГС
Зважаючи на попередній досвід лікування та наявність ЦП, для того щоб підібрати лікування та визначити його тривалість, необхідне визначення генотипу ВГС, у тому числі субтипу 1 генотипу (1а або 1b). Генотипування/субтипування слід виконувати за допомогою аналізу, який дає змогу точно розрізнити субтипи 1a та 1b, тобто аналізу, в якому використовується 5’ нетрансльована ділянка плюс частина іншої ділянки геному, як правило, та, що кодує core Ag, або ділянки, що кодують NS5B (не структурний білок 5В) [50]. Найбільш широко використовується метод, що ґрунтується на зворотній гібридизації за допомогою аналізу з використанням олігонуклеотидних зондів. Незабаром також буде доступним аналіз на основі глибокого секвенування [51].
У зв’язку з наявністю пангенотипних схем лікування ВГС можливо проводити лікування пацієнтів без ідентифікації генотипу та субтипу ВГС. Така можливість буде особливо корисною у регіонах, де вірусологічні тести недоступні або їх вартість перевищує вартість противірусного лікування, або для спрощення терапії в інших регіонах, для того щоб збільшити доступність медичної допомоги.
Аналізи для визначення резистентності ВГС
Немає стандартизованих обстежень для визначення стійкості ВГС до лікарських засобів (ЛЗ) у вигляді спеціальних наборів, які можна було б придбати. Перевірка резистентності переважно полягає у внутрішньолабораторних методиках, що ґрунтуються на популяційному секвенуванні (секвенування за методом Sanger) або глибокому секвенуванні [52]. Такі тести доступні лише в обмеженій кількості лабораторій в Європі та ще кількох місцях у світі. Аналіз на резистентність ВГС може бути технічно складним завданням, зокрема, для інших генотипів, окрім 1 та 4, параметри наявних внутрішньолабораторних аналізів значно відрізняються. Комплект для виконання аналізу на основі вивчення глибокого секвенування сьогодні перебуває на етапі розробки.
Доступність достовірного тесту на резистентність ВГС обмежена, немає єдиної думки щодо техніки виконання, інтерпретації та звітності про результати цих тестів. Крім того, існують високоефективні методи лікування пацієнтів зі встановленою до лікування резистентністю вірусу. Таким чином, не рекомендовано виконувати систематичне тестування на резистентність ВГС до початку лікування противірусними ЛЗ прямої дії у пацієнтів, які раніше не отримували жодних ЛЗ для лікування ВГС [53].
Поточні рекомендації EASL пропонують використовувати схеми лікування, які не потребують проведення будь-яких аналізів на резистентність вірусу до початку лікування ЛЗ 1-ої лінії. Відповідно до рекомендацій EASL щодо лікування ВГС (2016), у тих регіонах, де такі схеми лікування недоступні або не відшкодовуються, а лікарі мають доступ до достовірних тестів на резистентність, для прийняття рішень щодо лікування можна керуватися результатами цих аналізів [54].
Рекомендації
- Якісне/кількісне визначення РНК ВГС у сироватці або плазмі крові повинно проводитися за допомогою чутливого аналізу з нижньою межею виявлення ≤15 МО/мл (А1).
- У країнах із низьким і середнім рівнем доходу, а також за певних умов у країнах із високим рівнем доходу можна використовувати якісний аналіз на РНК ВГС із нижньою межею виявлення ≤1000 МО/мл, якщо більш чутливі кількісні аналізи недоступні і/або занадто дорогі (B1).
- Якщо аналіз на РНК ВГС недоступний та/або занадто дорогий, може бути використано якісне/кількісне виявлення core Ag ВГС як сурогатного маркера реплікації вірусу методом ІФА (A1).
- Для того щоб підібрати лікування та його тривалість, окрім інших параметрів, до початку терапії слід визначити генотип ВГС, у тому числі субтип 1 генотипу (1а або 1b) (A1).
- Може бути призначено пангенотипну схему лікування ВГС у пацієнтів без ідентифікації генотипу та субтипу ВГС у тих регіонах, де генотипування є недоступним або занадто дорогим, а також для того, щоб полегшити доступність лікування (B1).
- Виконання аналізів на резистентність ВГС до початку лікування не рекомендується (B1).
- Відповідно до рекомендацій EASL щодо лікування ВГС (2016), у тих регіонах, де доступні лише схеми лікування, що потребують попереднього визначення резистентності вірусу, а лікарі мають доступ до достовірних тестів, які визначають резистентність вірусу до інгібіторів NS5A (охоплюючи амінокислоти з 24 до 93), для прийняття рішень щодо лікування можна керуватися результатами цих аналізів (В2).
Продовження у наступному номері.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 3(65)-4(66) 2022 р.