30 січня, 2023
Мікробіом як мішень для впливу на стан здоров’я
Серед усіх гастроентерологічних порушень одні з найпоширеніших – кишкові захворювання, пов’язані з нездоровим способом життя, неправильним харчуванням, психоемоційними факторами й іншими причинами, тому проблема діагностики та лікування кишкових захворювань на сьогодні є актуальною і важливою. В листопаді відбувся науково-практичний онлайн-семінар із міжнародною участю «Запальні та функціональні захворювання кишечнику». Один зі спікерів – професор мікробіології Університетського коледжу Корка, доктор Колін Хілл (Ірландія) мав слово з доповіддю «Ви маєте мікробіом, на який ви (і ваш спосіб харчування) заслуговуєте!».
 Очевидним є те, що людина живе в мікробному світі. Мікроорганізми існують на планеті мільярди років. Два мільйони з них – у сусідстві та симбіозі з людиною, існування якої цілком залежить від життєдіяльності мікроорганізмів. Навіть кисень, який потрібен для дихання людини, продукується мікробами (ціанобактеріями).
Очевидним є те, що людина живе в мікробному світі. Мікроорганізми існують на планеті мільярди років. Два мільйони з них – у сусідстві та симбіозі з людиною, існування якої цілком залежить від життєдіяльності мікроорганізмів. Навіть кисень, який потрібен для дихання людини, продукується мікробами (ціанобактеріями).
Відомо, що до молока усіх ссавців, у т. ч. людей, входить комплекс олігосахаридів грудного молока, котрий являє собою сукупність цукрів, які немовля не здатне перетравлювати. Функція цих олігосахаридів полягає у тому, щоб підтримувати бактерії у кишечнику новонародженого. Еволюція створила людей так, що одна з найважливіших функцій матері – вигодовування немовля і одночасно його мікробіому, оскільки олігосахариди грудного молока не перетравлюються.
Також очевидним є те, що організм людини не виробляє власні хімічні сполуки для таких речовин, як нейротрансмітери та сигнальні молекули. Замість цього він пристосовує хімічні сполуки та сигнали мікробів.
Бактерії, як і людський організм, продукують серотонін, ацетилхолін, γ-аміномасляну кислоту (ГАМК), бутирати тощо. Отже, людський організм можна вважати значною мірою схожим на організм мікробів. Завдяки цьому людина має тісний зв’язок з його мікробіомом.
Якщо говорити простими словами, мікробіом (інша назва – мікробіота) людини – це сукупність усіх мікробів, які живуть на поверхні та всередині людини. Більша частина мікробіому знаходиться в кишковому тракті. Також велика кількість мікробів є на шкірі та в легенях. Мікроби живуть на кожній відкритій та порожнинній поверхні тіла людини.
Мікробіом складається не лише з бактерій, але вони є найпоширенішою популяцією з усіх представників. До інших складових мікробіому належать археї, гриби, протозої, бактеріофаги та віруси.
Діти народжуються із практично стерильним кишечником; одразу після народження починає формуватися мікробіом, що відбувається завдяки впливу мікробіому матері та навколишньому середовищу.
Існують певні речі, які впливають на стан мікробіому кишечнику в період новонародженості. Вони залежать від того, як була народжена дитина (фізіологічно чи за допомогою кесаревого розтину), а також від способу її годування (грудним молоком або спеціальною сумішшю). Все це зумовлює розвиток мікробіому, склад і стан якого майже упродовж усього життя є відносно стабільним та постійним й може зазнавати лише незначних змін. Водночас він може зазнавати впливу певних факторів. Найсильніше на стан мікробіому впливає дієта. З віком раціон людини зазнає значних змін. Це призводить до порушень складу та стану мікробіому або його руйнування. Менше (але також значно) на стан мікробіому впливають антибіотики. Крім того, вплив на нього можуть чинити різні захворювання.
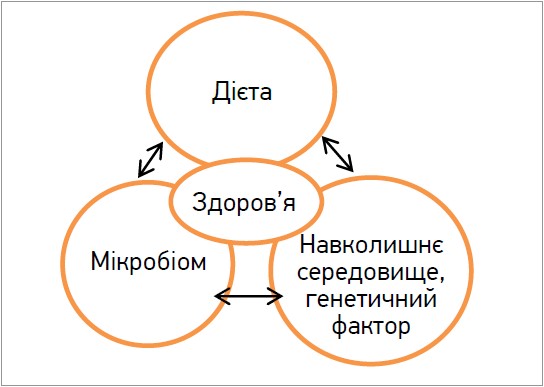
Процес порушення стану мікробіому і його вплив на стан організму можна представити у вигляді тріади (рис.).
Рис. Вплив дієти на стан здоров’я та мікробіом
Очевидно, що це три різні аспекти, на які можна впливати з метою покращити стан здоров’я людини.
Існують декілька різних основних мікробіомів (кишковий, шкірний, урогенітальний, легеневий), типи яких відрізняються за складом мікрофлори. Навіть уздовж кишечнику залежно від локалізації, починаючи від дванадцятипалої і закінчуючи прямою кишкою, визначаються помітні зміни структури мікробіому. Те ж саме стосується шкіри. Завдяки такому розмаїттю мікрофлори можна казати про наявність сотень різних мікробіомів.
Особистий мікробіом кожної людини є унікальним і формується протягом усього життя. Він цілком залежить від генетики, способу життя, харчових звичок, стану навколишнього середовища тощо. Наприклад, було доведено, що мікробіом людей, які мають домашніх тварин, відрізняється від такого тих, котрі з тваринами не контактують.
У клінічній практиці доцільним є розглядати мікробіом як ще один орган людського організму, адже він має метаболічну здатність, значний об’єм та генетичний матеріал, причому останнього в ньому міститься більше, ніж у будь якому іншому органі людини. Однак треба розуміти, що мікробіом – набутий орган, якого немає до народження. Порівняно з іншими органами мікробіом досить сильно піддається впливу. Водночас сам він здатен суттєво впливати на стан інших органів (нирок, печінки, головного мозку тощо), а також змінювати нервову, імунну, метаболічну та інші важливі функції організму. Тому патологічні зміни мікробіому можуть призводити до розвитку багатьох хронічних захворювань.
До основних способів впливу на стан мікробіому належать корегування дієти, обережність у використанні антибіотиків, призначення пробіотиків та мікробного консорціуму, повторне насичення мікробіому за допомогою фекальної трансплантації (ця процедура полягає у транспортуванні фекалій здорового донора до кишечнику реципієнта).
Але важливо пам’ятати цитату відомого голландського вченого Лоуренса Бааса Бекінга: «Все є всюди, але середовище вибирає» (Everything is everywhere, but the environment selects). Відповідно до цього правила мікробіом є результатом власного вибору кожної людини, а саме її способу життя.
Під час відносно нещодавнього дослідження був проаналізований фекальний мікробіом 160 здорових учасників похилого віку. Виявилося, що в деяких людей більшість складали бактероїди (від 14 до 91%), а в інших – фірмікути (від 10 до 81%) (Claesson et al., PNAS, 2011; Claesson et al., Nature, 2012). Оскільки всі учасники були здоровими, можна дійти висновку, що немає суттєвої різниці в тому, якими саме мікробами насичений мікробіом. Це змушує задуматися над тим, яку роль він відіграє для стану здоров’я людини.
Інше дослідження показало, що в людей з різноманітним складом кишкової мікрофлори функція мікробіому може бути однаковою. Це свідчить про те, що у здорових людей більшість різних мікробів виконує однакові функції (Huttenhower et al., Nature, 2012).
Якщо відбувається певне ушкодження мікробіому, що зумовлює порушення його функції, це може негативно впливати на стан здоров’я людини. Між порушенням мікробіому і певними патологічними станами організму існує багато асоціацій. Деякі докази наявності цих асоціацій можна відобразити за допомогою фекальної трансформації мікробіому на тваринах. Якщо здоровій тварині ввести в кишечник зразки фекалій від людини, що має один із таких патологічних станів, можна спостерігати поступовий розвиток симптомів ідентичного захворювання, тобто має місце факт передачі певних фенотипів за допомогою трансплантації мікробіому. Можливо, в багатьох випадках, коли використовується термін «дисбактеріоз», зміна мікробіому відображає зміну навколишнього середовища в результаті захворювання, а не є тригером захворювання (Shanahan F., Hill C., Nature Reviews Gastroenterology & Hepatology, 2012).
При визначенні зв’язку між станом мікробіому і захворюванням важливо приділяти достатньо уваги комплексному усуненню потенційних спотворювальних факторів, щоб правильно розуміти патогенез. Наприклад, вважається, що одним із патологічних станів, асоційованих зі станом мікробіому, є аутизм. Проте нещодавнє велике дослідження метагеноміки випорожнень при аутизмі показало, що більшість змін у людей із цим захворюванням пов’язані з особливостями харчування, а не з мікробіомом, який не є безпосередньою причиною аутизму. Водночас люди з аутизмом дотримуються специфічної дієти, тому мають і дещо специфічний склад мікробіому. Саме харчові звички, пов’язані з аутизмом, опосередковують певні асоціації аутизму та кишкового мікробіому (Chloe X. et al., Cell, 2021).
Мікробіом також може відігравати значну роль у реакції організму на різні терапевтичні засоби. Так, наприклад, відомо, що деякі люди не реагують на імунотерапію препаратами, які зумовлюють програмовану смерть клітин для лікування раку. Проте дослідження показали таке: якщо взяти зразки мікробіому людини, яка не реагує на імунотерапію, і помістити їх у кишечник миші або щура, то тварини також припинять реагувати на терапію інгібіторами контрольної точки. Отже, реакція на препарат, призначений рятувати життя, може залежати від специфічної структури мікробіому.
Мікробіом можна використовувати як терапевтичний засіб для лікування певних захворювань. Наприклад, діарея, зумовлена C. difficile, дуже складно піддається лікуванню і має високий рівень смертності. Натомість дійсно ефективним є метод фекальної трансплантації від здорового донора до кишечнику хворого на діарею. Ефективність такого лікування досягає 90%, при цьому цей метод запобігає рецидиву захворювання.
Нещодавнє дослідження ефективності методу фекальної трансплантації, проведене на мишах, продемонструвало цікаві та навіть дещо вражаючі результати. З’ясувалося, що при трансплантації фекального мікробіому від молодого щура до старого можна зменшити ступінь деяких проявів старіння (Boehme M. et al., Nature Aging, 2021).
Багато досліджень доводять, що стан мікрофлори кишечнику має зв’язок із функціональним станом головного мозку. Виявилося, що мікробіом має здатність контролювати реакцію на стрес, рівень тривоги і навіть запалення мозку. Отже, наразі вісь «кишечник – мозок» є доволі захопливою ділянкою наукових досліджень.
Багато людей мають певну непереносимість лактози. Це пов’язано з порушенням вироблення ферменту лактази, що пояснюється еволюційними змінами (в далекому минулому дорослій людині не було притаманним вживання великої кількості молока). Але деякі люди мають генетичну непереносимість лактози, тому вони не здатні експресувати лактазу в ентероцитах кишечнику. Нещодавнє голландське дослідження показало, що люди, в яких немає симптомів непереносимості лактози, навіть якщо вони генетично не можуть перетравлювати лактозу, мають у мікробіомі високий рівень біфідобактерій, котрі, своєю чергою, містять високий рівень ферменту лактази. В цьому випадку мікробіом компенсує генетичний дефект.
Порівняльний аналіз мікробіомів здорових літніх людей та осіб такого самого віку, котрі перебувають у стаціонарі, продемонстрував, що здорові особи дотримуються більш схожих дієт і мають більш схожі мікробіоми, тоді як мікробіоми хворих змінені у зв’язку з характером їхнього раціону. Цілком імовірно, що можна розробити кращі дієти для літніх людей (забезпечення організму оптимальною кількістю енергії, вітамінів, мікро- та мікроелементів тощо), які допомогли б їм підтримувати свій мікробіом (Claesson et al., Nature, 2012).
Отже, якщо вважати, що стан здоров’я залежить від поєднання генетичних факторів, навколишнього середовища і стану мікробіому, то останній стає дуже цікавим аспектом, у який можна втрутитися з метою поліпшення здоров’я. Тому його доцільно використовувати як інтервенційну мішень для впливу на перебіг низки інших захворювань. Суттєво впливати на мікробіом можуть такі чинники, як дієта, спосіб життя, контроль антибіотикотерапії, використання пробіотиків, бактеріофагів, фекальна трансплантація тощо, причому першочергову роль у цьому, як показують останні дослідження, може відігравати спеціально розроблена дієта.
Підготував Олександр Соловйов