26 лютого, 2023
Еторикоксиб: ефективність і безпека використання при остеоартриті
Остеоартрит (ОА) є найпоширенішим прогресуючим захворюванням опорно-рухового апарату, на яке страждають понад 250 млн осіб у світі. Розповсюдженість ОА демонструє тенденцію зростати. Захворювання має складну, гетерогенну та лише частково вивчену етіологію. Нині ОА розуміють як комплексну патологію, за якої спостерігаються руйнування хряща між кістками, ремоделювання кісток і запалення суглобів. Це спричиняє зниження рухливості, розвиток больового синдрому, втрату функції суглоба та значне погіршення якості життя пацієнта.
Є багато варіантів симптоматичної терапії ОА, як-от аналгетики (опіоїдні та неопіоїдні), традиційні нестероїдні протизапальні препарати (НПЗП), симптом-модифікувальні засоби повільної дії та ліки для місцевого застосування.
Спеціалісти міжнародних профільних організацій рекомендують НПЗП як препарати першої лінії для короткочасної терапії стійкого болю в пацієнтів з ОА, котрі не мають високого ризику серцево-судинних розладів. Зокрема:
- в настановах Американської академії хірургів-ортопедів, опублікованій у 2013 р., позитивну рекомендацію до використання отримали 3 групи препаратів – пероральні та топічні форми НПЗП, а також опіоїдні знеболювальні засоби. Експерти рекомендували використання НПЗП у симптоматичному лікуванні ОА колінного суглоба як терапії першої лінії (Jevsevar D.S., 2013);
- в настановах Американської колегії ревматологів (2020) НПЗП (пероральні та топічні) рекомендовано для початкового фармакологічного лікування ОА (Kolasinski S.L., 2019);
- в документі, присвяченому рекомендованому плану лікування ОА, що був оприлюднений спеціалістами Міжнародного товариства дослідження остеоартриту (2019), пероральні форми НПЗП рекомендовані для лікування стійкого болю (Bannuru R.R., 2019);
- в рекомендаціях щодо короткочасної терапії, наведених у настановах Європейського товариства з вивчення клінічних та економічних аспектів остеопорозу, остеоартриту та захворювань опорно-рухового апарату (2019), НПЗП також рекомендовані як препарати першого ряду. Для довготривалого лікування у цьому документі, на відміну від попередніх, вказані симптом-модифікувальні лікарські засоби повільної дії (Bruyère O., 2019; Arden N.K., 2019).
Еторикоксиб – ефективний селективний НПЗП
НПЗП, котрі широко використовуються для купірування болю, асоціюються з підвищеним ризиком негативного впливу на шлунково-кишковий тракт (ШКТ) через пригнічення ними ферменту ЦОГ-1, тому сьогодні перевагу віддають застосуванню високоселективних інгібіторів ЦОГ-2 із незначним ризиком серцево-судинних ускладнень.
Добре відомим представником останніх є еторикоксиб, ефективність і безпека якого були підтверджені чималою кількість рандомізованих плацебо-контрольованих досліджень. Слід зазначити, що еторикоксиб здатний долати гематоенцефалічний бар’єр, проникати в спинномозкову рідину та пригнічувати синтез PGE2, забезпечуючи аналгезію за центральним механізмом (Renner B. et al., 2010). Відтак, еторикоксиб чинить подвійну аналгетичну дію за рахунок пригнічення як центрального, так і периферичного механізмів формування болю.
За даними Кокранівського огляду 350 досліджень за участю загалом 45 тис. пацієнтів (Moore R. A. et al., 2011), еторикоксиб у дозі 120 мг за своєю аналгетичною дією поступався лише комбінації наркотичного аналгетика оксикодону (10 мг) із парацетамолом (500 мг).
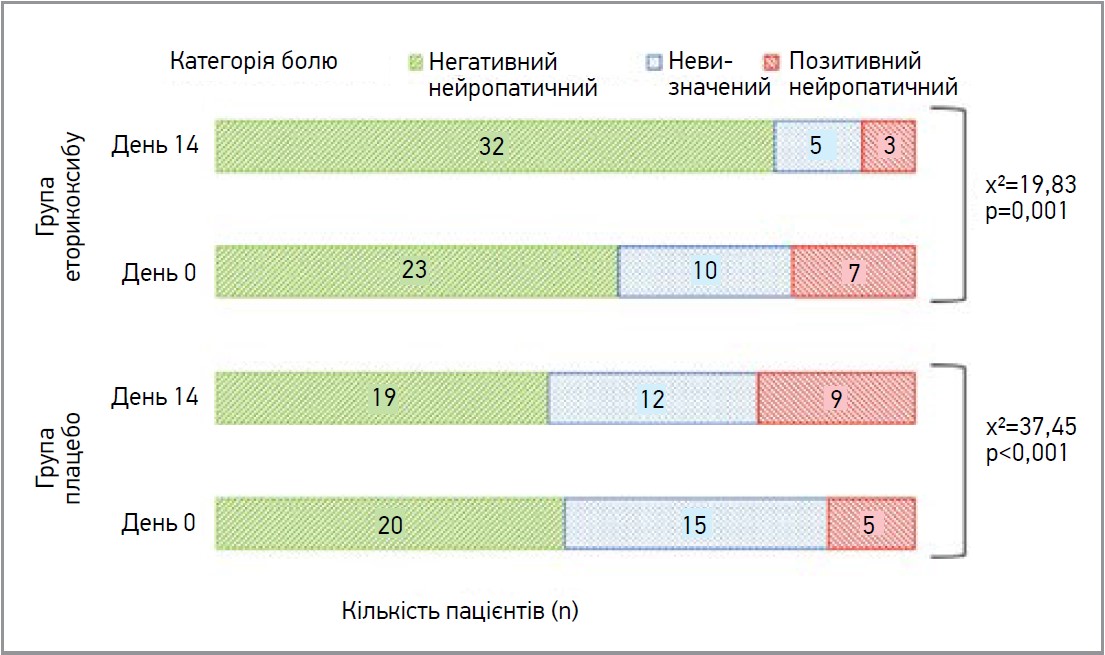
Дослідники з Австалії під керівництвом P. Moss (2017) вивчали ефективність прийому еторикоксибу (60 мг/день упродовж 14 діб) у пацієнтів з ОА. Автори констатували, що така терапія забезпечила суттєве покращення низки функціональних показників опорно-рухового апарату та рівня самооцінки болю. Показник болю, оцінений за допомогою індекса вираженості ОА WOMAC, покращився на 30,7% за 14 днів, індекс механічної гіпералгезії – на 32,6%; біль під час рухових завдань зменшився на 32,6% (p<0,001) (рис. 1).
Рис. 1. Зміни за опитувальником PainDETECT з дня 0 на день 14 в учасників, які отримували плацебо, порівняно з учасниками групи активного лікування (n=40 у кожній групі)
(Moss P. et al., 2017)
Схоже дослідження було проведено (Huang W.- N., Tsa T. K., 2018) за участю пацієнтів старечого віку (79-96 років) з ОА та недостатньою відповіддю на попереднє застосування традиційних НПЗП або опіатів протягом 4 тижнів. Після 4-тижневого курсу прийому еторикоксибу в дозі 60 мг/добу пацієнти відзначили значне зменшення суглобового болю (в 4,5 рази, оцінка за WOMAC; р<0,001), покращення функції суглобів (у 2 рази, оцінка за WOMAC; р=0,020), зменшення скутості в суглобах (у 2 рази, оцінка за WOMAC; р=0,068), а також значуще поліпшення якості життя (за TSQM). Водночас лікування еторикоксибом характеризувалося хорошою переносимістю та високим профілем безпеки.
Ці висновки підтверджуються результатами роботи Arendt-Nielsen і співавт. (2016), які досліджували еторикоксиб протягом тривалішого періоду та виявили зменшення нейропатичного болю (на 22%) і модулювання порогів болю від тиску (р=0,012 для локалізованої сенсибілізації; р=0,025 для поширеної сенсибілізації) в пацієнтів з ОА. Вчені констатували, що еторикоксиб позитивно впливав на центральні механізми модуляції болю, зменшував його вираженість і покращував функцію суглобів при ОА. На думку авторів цього дослідження, на центральний механізм дії препарату вказує той факт, що зменшення тимчасової сумації болю було асоційоване з вищою ефективністю еторикоксибу.
Хондропротекторна дія
Останнім часом увагу вчених привернула роль трансформуючого фактора росту-β (TGF-β) та фактора росту нервів (NGF) у патогенезі ОА. TGF-β можна назвати хондропротекторним цитокіном, оскільки він знижує експресію та секрецію колагеназ (Hui Т. et al., 2001). Своєю чергою, NGF – це білок, який сприяє зростанню аксонів, активації периферичних нейронів і бере участь у виникненні больової сенсибілізації (McKelvey О. et al., 2013). Підвищений рівень NGF спостерігається в синовіальній рідині пацієнтів із запальними або дегенеративними ревматичними захворюваннями, в тому числі ОА (Seidel et al., 2010). У ході нещодавнього дослідження (Wen Z.-H., 2019) шляхом імуногістохімічного вимірювання експресії TGF-β1 та NGF у суглобовому хрящі оцінювався вплив еторикоксибу на розвиток ОА та ноцицепцію в щурів. Дослідники виявили, що у тварин, котрі отримували препарат, спостеріглися значно нижчий ступінь дегенерації хряща, послаблення експресії NGF і збільшення експресії TGF-β у хрящі (р<0,05), ураженому ОА; це проявлялося послабленням проявів ноцицептивної поведінки. Висновки зазначеного дослідження свідчать про те, що еторикоксиб може чинити не лише знеболювальний, а й хондропротекторний вплив.
Безепека
Добре відомо, що прийом НПЗП асоціюється з підвищенням ризику розвитку шлунково-кишкових порушень, а селективність до ЦОГ-2 підвищує ризик серцево-судинних уражень. Досліджуючи механізми дії еторикоксибу, вчені довели, що в здорових осіб інгібування синтезу простагландинів у слизовій оболонці шлунка суттєво не відрізняється від такого для плацебо (Dallob et al., 2003); це свідчить про низький ризик розвитку шлунково-кишкових ускладнень. Декілька досліджень були присвячені порівнянню безпеки й ефективності еторикоксибу та інших інших НПЗП. Так, S.P. Curtis і співавт. (2005) встановили, що в пацієнтів з ОА прийом еторикоксибу (30 мг, 60 мг та 120 мг) 1 раз на добу забезпечував клінічний ефект, подібний до такого диклофенаку, і зберігався до 52 тижнів. Водночас пацієнти в групі еторикоксибу відчували менше симптомів розладу ШКТ під час дослідження. Більша частка пацієнтів у групі диклофенаку припинила лікування через порушення з боку ШКТ.
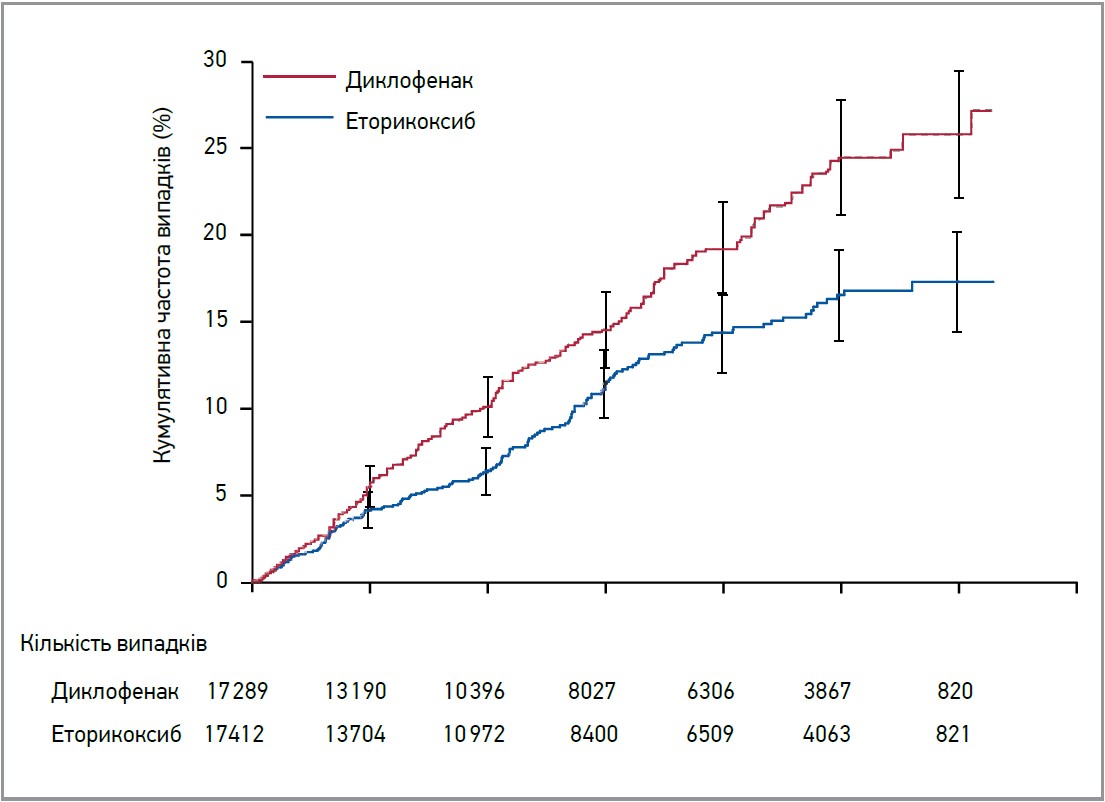
L. Laine та співавт. (2007) провели об’єднаний аналіз подвійних сліпих рандомізованих досліджень, у яких порівнювали гастроінтестинальну та кардіоваскулярну безпеку тривалого лікування еторикоксибом (60 або 90 мг/день) і диклофенаком (150 мг/день) у 34 701 пацієнта з ОА або ревматоїдним артритом на тлі застосування інгібіторів протонної помпи. Загалом побічні ефекти з боку верхніх відділів ШКТ спостерігалися значно рідше при застосуванні еторикоксибу, ніж при прийомі диклофенаку (ВР 0,69; 95% ДІ 0,57-0,83; р=0,0001) (рис. 2). При цьому ризик неускладнених шлунково-кишкових подій при застосуванні еторикоксибу виявився майже удвічі нижчим порівняно з таким диклофенаку (ВР 0,57; 0,45-0,74; p<0,0001). Частота кардіоваскулярних ускладнень майже не відрізнялася між групами. Отже, ризик виникнення серцево-судинних подій, пов’язаних із застосуванням еторикоксибу, не перевищує відповідний показник при прийомі таких неселективних НПЗП, як диклофенак.
Рис. 2. Кумулятивна частота клінічних побічних ефектів із боку верхніх відділів ШКТ на тлі лікування еторикоксибом і диклофенаком (Laine L. et al., 2007)
Висновки
Наведені вище дані свідчать про те, що еторикоксиб може бути оптимальним варіантом знеболення в пацієнтів з ОА, оскільки на тлі високої аналгетичної ефективності є порівняно безпечним і має доведені хондропротекторні властивості. Втім, висока вартість оригінального еторикоксбу може обмежувати його широке застосування. В такому випадку слід звернути увагу на високоякісні генерики еторикоксибу. Наразі єдиним генериком еторикоксибу з доведеною біоеквівалентністю оригінальному препарату на вітчизняному фармацевтичному ринку є препарат Форсанек компанії Kusum Healthcare Pvt Ltd. Форсанек випускається у вигляді таблеток по 60, 90 та 120 мг. У пацієнтів з ОА прийом еторикоксибу в дозі 60 мг 1 раз на добу забезпечує значне полегшення болю. Позитивний ефект спостерігається вже на другий день лікування і зберігається протягом періоду лікування (до 52 тижнів). Форсанек здатен значно посилювати знеболювальний ефект за неефективності традиційних НПЗП. Препарат не пригнічує синтез простагландинів шлунка і тому має високий профіль безпеки щодо ШКТ при зіставних з іншими НПЗП серцево-судинних ризиках. За рахунок збільшення рівня експресії TGF-β у хондроцитах еторикоксиб запобігає руйнуванню суглобового хряща. Препарат переважно добре переноситься пацієнтами, в тому числі особами похилого віку, що має важливе значення при виборі терапії ОА.
Підготувала Юлія Котикович