12 квітня, 2023
Ефекти β-блокаторів на вуглеводний та ліпідний метаболізм
 Одним із найвагоміших винайдень із часу відкриття дигіталісу Нобелівський комітет назвав синтез і дослідження β-блокаторів (ББ) під керівництвом Джеймса Блека (James Whyte Black), який отримав за нього Нобелівську премію в 1988 р. Приблизно 60 років тому створено пропранолол, який поклав початок ері клінічного використання ББ із властивостями, яких перший препарат не мав: селективність, внутрішня симпатоміметична активність, гідрофільність, додаткові вазодилатувальні характеристики.
Одним із найвагоміших винайдень із часу відкриття дигіталісу Нобелівський комітет назвав синтез і дослідження β-блокаторів (ББ) під керівництвом Джеймса Блека (James Whyte Black), який отримав за нього Нобелівську премію в 1988 р. Приблизно 60 років тому створено пропранолол, який поклав початок ері клінічного використання ББ із властивостями, яких перший препарат не мав: селективність, внутрішня симпатоміметична активність, гідрофільність, додаткові вазодилатувальні характеристики.
 На сьогодні абсолютно доведено здатність ББ знижувати смертність і частоту серцево-судинних подій у пацієнтів з артеріальною гіпертензією, гострим та перенесеним раніше інфарктом міокарда, хронічною серцевою недостатністю (рівень доказів 1А), стенокардією напруги (1В), тахіаритміями (1С). З огляду на рекомендації щодо тривалого (а подеколи й пожиттєвого) застосування ББ украй важливого значення набувають їхні ефекти на вуглеводний та ліпідний обміни, що не перестає бути предметом наукових дискусій. Вирішення питання використання ББ за порушення вуглеводного обміну порівнюють із рухом маятника, оскільки тривалий час вважалося, що ББ через свої несприятливі метаболічні впливи протипоказані пацієнтам із цукровим діабетом (ЦД) [20, 21].
На сьогодні абсолютно доведено здатність ББ знижувати смертність і частоту серцево-судинних подій у пацієнтів з артеріальною гіпертензією, гострим та перенесеним раніше інфарктом міокарда, хронічною серцевою недостатністю (рівень доказів 1А), стенокардією напруги (1В), тахіаритміями (1С). З огляду на рекомендації щодо тривалого (а подеколи й пожиттєвого) застосування ББ украй важливого значення набувають їхні ефекти на вуглеводний та ліпідний обміни, що не перестає бути предметом наукових дискусій. Вирішення питання використання ББ за порушення вуглеводного обміну порівнюють із рухом маятника, оскільки тривалий час вважалося, що ББ через свої несприятливі метаболічні впливи протипоказані пацієнтам із цукровим діабетом (ЦД) [20, 21].
Вплив β-адреноблокаторів на вуглеводний метаболізм
Вуглеводний обмін – складний процес, основними регуляторними органами якого є печінка та підшлункова залоза [1, 16], яка виробляє інсулін. У його регуляції беруть участь контрінсулярні гормони: глюкагон, гормони щитоподібної залози та надниркових залоз (глюкокортикоїди), гормон росту. Контрінсулярні ефекти чинять також катехоламіни, які стимулюють глікогеноліз у печінці та м’язах унаслідок збільшення синтезу цАМФ усередині клітини. Як і всі інші органи та системи організму, відповідальні за обмін вуглеводів, клітини містять на поверхні масу рецепторів, у т. ч. адренорецептори. На жаль, на відміну від кардіоміоцитів, адренорецептори клітин підшлункової залози та печінки менш вивчені, тому дані літератури щодо підтипів наявних рецепторів є неоднозначними, проте немає сумніву, що на клітинах існують рецептори із протилежною дією [4, 29, 30] (табл. 1). Вважають, що клітини острівців підшлункової залози мають β3-рецептори, блокада яких спричиняє зменшення секреції інсуліну та глюкагону, тоді як загалом протилежну дію має блокада α2-рецепторів на тих самих клітинах. Натомість блокада β2-адренорецепторів (за іншими даними, β1 чи β3) на гепатоцитах зумовлює сповільнення глікогенолізу та глюконеогенезу в печінці, що, своєю чергою, також викликає зменшення вивільнення інсуліну. Блокада β3-рецепторів на адипоцитах послаблює ліполіз [30] і спричиняє зміну чутливості до інсуліну, що дотепер остаточно не вивчено.
Саме тому вплив ББ на 2-й та 3-й підтипи адренорецепторів може зумовити зміни вуглеводного метаболізму: зменшення продукції інсуліну, сповільнення (послаблення) ліполізу та гіпоглікемії, а також зниження продукції контрінсулярних гормонів, що ще більше порушує внутрішню регуляцію вивільнення інсуліну. Це разом із блокадою β3-рецепторів у панкреатичних острівцях може супроводжуватися підвищенням глікемії та появою інсулінорезистентності, що запускає хибне коло метаболічного синдрому, складові частини якого ще більше обтяжують одна одну. Однак усі відомі сучасні ББ, які широко застосовуються в кардіології, – це насамперед блокатори β1-рецепторів (кардіоселективні), які не є основними рецепторами клітин підшлункової залози, печінки, жирової тканини, щитоподібної залози, що опосередковують вуглеводний обмін, тому сучасні ББ не мають таких ефектів на параметри вуглеводного метаболізму, хоча за умов їх використання у високих дозах вони діють як неселективні, тому можуть викликати певні метаболічні ефекти.
Негативна дія ББ на вуглеводний обмін була описана одночасно з обґрунтуванням доцільності їхнього медичного застосування. Відомо, що в хворих на ЦД 1 типу неселективні ББ підвищують небезпеку прихованої гіпоглікемії, а після парентерального введення інсуліну вони стримують повернення рівня глікемії до нормального [30]. Небезпека прихованої гіпоглікемії зумовлена тим, що ББ можуть маскувати клінічні її прояви, зокрема тремор і тахікардію. Однак інші ознаки гіпоглікемії (пітливість) залишаються, а їхня діагностична цінність зростає [9, 30]. Крім того, описано, що неселективні та кардіоселективні β-адреноблокатори підвищують резистентність тканин до інсуліну і рівень глікозильованого гемоглобіну [30, 37]. Негативну дію на вуглеводний обмін доповнює описаний судинозвужувальний вплив перших неселективних ББ, що має особливе значення для хворих на ЦД, який часто ускладнюється периферійними ангіопатіями.
Доказова медицина щодо впливу ББ на вуглеводний обмін
У деяких дослідженнях (CFPP, LIFE, INVEST) за використання ББ було виявлено більшу частоту виявлення ЦД, однак цей факт потребує пояснення. Так, за однією тезою, в дослідженні LIFE частота розвитку ЦД при застосуванні атенололу була на 25% більшою, ніж у разі лікування лозартаном. Однак таке порівняння виявилося методично неправильним, оскільки абсолютні значення були також визначені у відсотках і становили 8 та 6%, тому різниця складала не 25%, а лише 2%. У цих пацієнтів не проводили рандомізацію за факторами ризику розвитку ЦД [5]. Загалом більшість клінічних досліджень не демонструє негативних впливів ББ на вуглеводний обмін. У дослідженні UKPDS (2723 хворих на ЦД та ішемічну хворобу серця, ІХС) виявлено нижчий рівень глюкози натще в пацієнтів, які приймали ББ, що супроводжувалося зменшенням смертності. Навіть через 9 років застосування препаратів (у т. ч. ББ) не виявлено різниці в рівнях глікованого гемоглобіну між пацієнтами, які приймали інгібітори ангіотензинперетворювального ферменту і ББ, тоді як смертність у групі ББ була нижчою.
Із часів використання перших неселективних препаратів залишилася думка, що ББ збільшують ризик розвитку гіпоглікемії, однак у жодному сучасному дослідженні не виявлено ані порушення сприйняття початку епізоду гіпоглікемії пацієнтами, ані зростання ризику таких епізодів загалом [2, 33]. Випробування ефективності лікування 13 000 хворих літнього віку не виявило збільшення частоти розвитку гіпоглікемії на тлі застосування ББ. Крім того, ризик розвитку тяжкої гіпоглікемії серед хворих, які приймали ББ, виявився нижчим, ніж за умов застосування інших груп антигіпертензивних препаратів [11, 31], тобто селективні ББ не спричиняли збільшення частоти епізодів гіпоглікемії та не впливали на швидкість повернення зниженого рівня глюкози до норми.
Виявилося, що вплив ББ на параметри вуглеводного метаболізму не був однаковим у межах групи, а залежав від основних властивостей препарату, що дозволяє прицільно обрати найдоцільніший засіб для лікування пацієнта в конкретній ситуації.
• Атенолол (кардіоселективний гідрофільний препарат) широко представлений на українському ринку; в метаболічному сенсі вважається найнебезпечнішим. Його перевагою є низька вартість, що робить цей препарат доступним для малозабезпечених верств населення [15]. Найбільш метаболічно несприятливою виявилася комбінація атенололу з діуретиком, що підтверджується даними доказової медицини: в дослідженні ASCOT за лікування атенололом і діуретиком ЦД розвинувся у 8,3%, а в групі амлодипін + периндопріл – в 5,9% [5]. Отже, атенолол можна розглядати як основу лікування лише за монотерапії, яка досить рідко є достатньо ефективною.
• Бетаксолол (селективний ББ із >24-годинною дією без власної симпатоміметичної дії та мембраностабілізувального ефекту) вважають одним із найкращих препаратів вибору за ЦД і метаболічного синдрому [13]. Продемонстровано відсутність його впливу на рівень глюкози натще [24]. Через 3 міс застосування бісопрололу в хворих на гіпертонічну хворобу та стабільну стенокардію на тлі ЦД чи порушення толерантності до глюкози спостерігалася нормалізація глюкози крові (з 6,4 до 5,4 ммоль/л), інсуліну натще (із 22,3 до 16,9 МОд/мл), а потреби в підвищенні дози пероральних протидіабетичних засобів не виникало. В аналогічних хворих без порушення вуглеводного обміну цукор у крові, інсулін натще та індекс НОМА через 3 міс також не змінилися [13]. До переваг бетаксололу належить і можливість застосування його 1 р/добу, що збільшує комплаєнс.
• Бісопролол (один із найселективніших ББ без внутрішньої симпатоміметичної активності) також вважають метаболічно нейтральним. Результати вітчизняного дослідження КОНТУР (КОНкор: Тактика Уменьшения Риска) із залученням 4199 пацієнтів довели, що застосування оригінального бісопрололу не супроводжувалося суттєвими змінами рівнів глюкози, в т. ч. у хворих із ЦД 2 типу [3]. Метаболічно нейтральними та аналогічними за дією виявилися генеричні препарати бісопрололу, місяць застосування яких у групах у складі 30 пацієнтів не показав змін глюкози через 1, 2, 3 і 6 міс терапії [8, 10, 19, 23].
• Карведилол (неселективний ББ і селективний блокатор постсинаптичних α1-адренорецепторів із додатковими вазодилатувальними та антиоксидантними властивостями) також не має несприятливих метаболічних ефектів на метаболізм глюкози. В рандомізованому клінічному дослідженні GEMINI (Glycemic Effects in Diabetes Mellitus Carvedilol-Metoprolol Comparison in Hypertensives) застосування карведилолу в дозі 35 мг/добу не супроводжувалося зростанням плазмової концентрації глікованого гемоглобіну та маси тіла [6]. Вважається, що карведилол, на відміну від інших ББ, не лише не зменшує, а підвищує чутливість тканин до інсуліну [12], тобто знижує інсулінорезистентність [36]. Блокада α1-адренорецепторів, притаманна цьому препарату, сприяє покращенню кровотоку в скелетних м’язах, що збільшує інсулінопосередковане надходження глюкози до міоцитів. Суттєвого впливу карведилолу на рівень глюкози не спостерігали й інші лікарі [8, 22].
• Метопролол (кардіоселективний ББ без внутрішньої симпатоміметичної та мембраностабілізувальної дії, із частковим вазодилатувальним ефектом) належить до найчастіше вживаних ББ. Пролонговані форми застосовуються 1 р/добу, звичайні – 2 р/добу. В рандомізованому клінічному дослідженні GEMINI метопролол у великій дозі (метопрололу тартрат 254 мг/добу) сприяв збільшенню плазмової концентрації глікозильованого гемоглобіну та маси тіла [6, 28], хоча, за іншими даними, тривале застосування метопрололу (тартрат) не спричиняло негативних змін рівня глюкози в 30 хворих із серцевою недостатністю через 6 міс лікування (4,4 та 4,5 ммоль/л) [8]. Застосування метопрололу в постінфарктних пацієнтів із супутнім ЦД не виявило погіршення ЦД у жодному випадку [18].
• Небіволол (високоселективний ББ ІІІ покоління, який модулює синтез азоту ендотелієм судин і викликає ендотелійзалежну вазодилатацію) також не має негативного впливу на вуглеводний метаболізм [35]. Детально метаболічний профіль небівололу описаний E. Agabiti, D. Rizzoni (Metabolic Profile of Nebivolol, a β-adrenoreceptor Antagonist with Unique Characteristics; Drug, 2007). За їхніми даними, за використання небівололу глюкоза плазми не змінилася, а рівень інсуліну зменшився на 10% [26]. Терапія небівололом сприяла покращенню чутливості тканин до інсуліну (значно зменшилася частка пацієнтів з інсулінорезистентністю) та оптимізації ліпідного обміну [1, 7]. За терапії небівололом знижувалися рівень глікованого гемоглобіну та мікроальбумінурія (нефропротекторна дія) [27].
Принципи застосування ББ у хворих із порушеннями вуглеводного обміну
Загроза негативної дії ББ на параметри вуглеводного метаболізму перебільшена, оскільки клінічні дослідження їх не виявили. Здебільшого вона стосується неселективних препаратів і комбінацій атенололу з тіазидами. Однак призначення ББ хворим на ЦД, метаболічний синдром має не тільки доцільність, а й пряме патогенетичне обґрунтування, оскільки описано прямий зв’язок між інсулінорезистентністю і підвищеною симпатоадреналовою активністю [11, 25]. Призначення ББ у таких випадках може розірвати хибне коло, зменшуючи симпатоадреналову активність й інсулінорезистентність, яка є основою всіх патофізіологічних змін.
Ще у 2003 р. до рекомендацій Об’єднаного національного комітету США було внесено ББ як препарати І ряду антигіпертензивної терапії у хворих на ЦД [38]. Крім того, застосування ББ у хворих із метаболічним синдромом є доцільним для профілактики раптової серцевої смерті, запобігання розвитку ішемії міокарда, зменшення ризику розвитку гострого інфаркту міокарда та мозкового інсульту. Особливо ББ показані за поєднання ЦД або метаболічного синдрому з ІХС (стенокардія, перенесений інфаркт міокарда), аритміями (екстрасистолія). Встановлено, що серед 2723 хворих на ЦД та ІХС, які отримували ББ, виявлено нижчі рівні глюкози і смертності, а частота серцево-судинних ускладнень не перевищувала аналогічну за використання інших серцевих препаратів.
За рекомендаціями Європейського товариства кардіологів (ESC) і Європейської асоціації з вивчення цукрового діабету (EASD), з метою досягнення задовільного контролю артеріального тиску хворий на ЦД зазвичай потребує комбінації декількох антигіпертензивних препаратів, одним з яких може бути ББ; ББ метопрололу сукцинат, бісопролол, карведилол рекомендуються як терапія першої лінії у хворих на ЦД із серцевою недостатністю; ББ мають найвищий рейтинг доказовості щодо кращого прогнозу після гострого інфаркту міокарда [32].
З огляду на те що в хворих на ЦД, які лікувалися неселективними ББ, описано парадоксальне підвищення артеріального тиску з рефлекторною брадикардією внаслідок підвищення рівня адреналіну на тлі гіпоглікемії, препаратами вибору є лише селективні засоби. Слід з обережністю призначати ББ пацієнтам із початковими стадіями порушення вуглеводного обміну та дотримуватися певних застережень (табл. 2).
β-Адреноблокатори та ліпідний метаболізм
Вуглеводний метаболізм патогенетично неможливо повністю відокремити від ліпідного метаболізму, оскільки як глюкоза, так і жири є основними джерелами енергії в організмі, а кінцевий продукт гліколітичного циклу ацетилкоензим А бере також участь у синтезі тригліцеридів (ТГ), жирних кислот, холестерину (ХС), стероїдів. Не менш дискутабельним сьогодні є вплив ББ на стан ліпідного метаболізму, оскільки частота таких порушень у популяції невпинно зростає. Дані, отримані під час епідеміологічного обстеження в Україні, свідчать про те, що лише 51% чоловіків і 42% жінок мають нормальну масу тіла, а ожиріння діагностовано в 12% чоловіків та 20% жінок, причому частота надмірної маси тіла й ожиріння стрімко зростає з віком хворих. Особливо яскраво цей процес фіксується в осіб, що мешкають у сільській місцевості [7]. Однак застарілі уявлення про негативний вплив ББ на ліпідний метаболізм часто стають перешкодою для раціонального застосування цих препаратів у кардіології та інших галузях медицини.
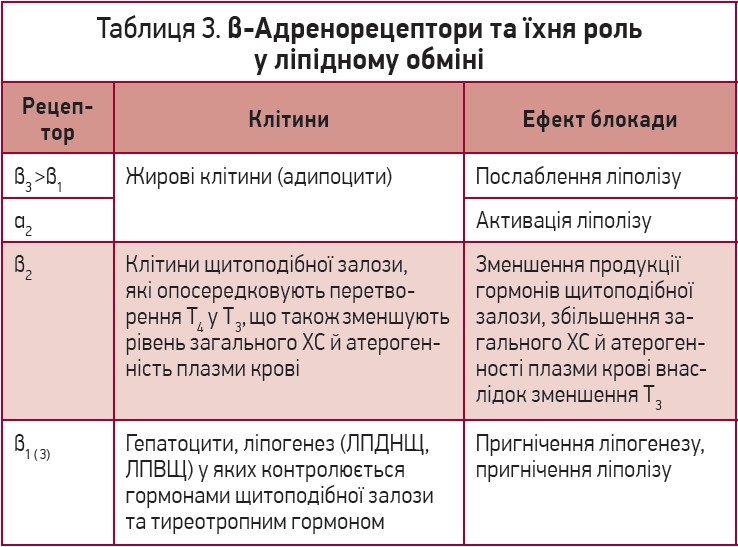
Як й інші органи та системи організму, клітини, що відповідають за ліпідний метаболізм, серед величезної кількості рецепторів містять на своїй мембрані адренорецептори. На відміну від рецепторів кардіоміоцитів, адренорецептори клітин печінки та жирової тканини є менш вивченими, тому дані літератури щодо їх підтипів виявилися неоднозначними (табл. 3). Труднощі ідентифікації також зумовлені тим, що одночасно на клітинах існують рецептори із протилежною дією [3, 23, 24].
Жировий обмін передбачає два процеси – ліпогенез (синтез жовчних кислот, ЛПДНЩ і ЛПВЩ, який найінтенсивніше перебігає у печінці та жировій тканині) й ліполіз (гідроліз ліпідів під дією ліпази з утворенням неестерифікованих жирних кислот). Провідним фактором активації ліполізу в адипоцитах є β-адренергічна система та натрійуретичний пептид, які активуються в умовах фізичної активності чи стресу: збільшення адренергічного тонусу разом із підвищенням кортизолу спричиняє збільшення рівня вільних жирних кислот у крові; >40 років тому J.L. Day, J. Metcalf, C.N. Simpson висловили гіпотезу про те, що саме зміна концентрацій ліпідів плазми зв’язує стрес і кардіоваскулярні події [25].
Гормональна регуляція жирового обміну є доволі складною. Ліполітичну дію мають гормони гіпофіза (насамперед соматотропний гормон, адренокортикотропний гормон, тиреотропний гормон). Активують ліполіз також гормони щитоподібної залози. Різке збільшення ліполізу відбувається також у разі запалення в жировій тканині, що описано в осіб з ожирінням чи ЦД 2 типу [6]. Інсулін, навпаки, пригнічує ліполіз, що призводить до збільшення утворення вільних жирних кислот крові при ЦД. Слід пам’ятати, що активація симпатичної нервової системи за ожиріння, що відбувається внаслідок збільшення продукції лептину, гіперінсулінемії та надлишкового вмісту вільних жирних кислот, зумовлює також підвищення артеріального тиску [6].
Читати продовження >>
Медична газета «Здоров’я України 21 сторіччя» № 4-5 (540-541), 2023 р.