12 квітня, 2023
Інгібітори пропротеїнової конвертази субтилізин-кексинового типу 9: нові можливості ліпідомодифікувальної терапії при цукровому діабеті
 Зростає кількість доказів того, що ліпідознижувальна терапія, а саме використання статинів, пов’язана з довгостроковими патофізіологічними змінами гомеостазу глюкози та розвитком цукрового діабету (ЦД) 2 типу. Зокрема, результати метааналізу 17 рандомізованих контрольованих досліджень (РКД) свідчать, що розувастатин (20 мг/добу), аторвастатин (80 мг/добу) і правастатин (40 мг/добу) підвищують ризик ЦД 2 типу на 25, 15 і 7% відповідно. Ці ефекти частково пояснюються статинозалежною блокадою Ca2+-каналів L-типу в β-клітинах підшлункової залози, що зумовлює порушення секреції інсуліну.
Зростає кількість доказів того, що ліпідознижувальна терапія, а саме використання статинів, пов’язана з довгостроковими патофізіологічними змінами гомеостазу глюкози та розвитком цукрового діабету (ЦД) 2 типу. Зокрема, результати метааналізу 17 рандомізованих контрольованих досліджень (РКД) свідчать, що розувастатин (20 мг/добу), аторвастатин (80 мг/добу) і правастатин (40 мг/добу) підвищують ризик ЦД 2 типу на 25, 15 і 7% відповідно. Ці ефекти частково пояснюються статинозалежною блокадою Ca2+-каналів L-типу в β-клітинах підшлункової залози, що зумовлює порушення секреції інсуліну.
В жировій тканині внаслідок дисбалансу регуляції транспортера глюкози типу 4 змінюється чутливість до інсуліну. Крім того, варіанти порушень функції 3-гідрокси-3-метилглутарил-коензим А-редуктази (ГМГ-КоА-редуктаза), пов’язані з пригніченням біосинтезу холестерину (ХС), зумовлені посиленням його поглинання через рецептор ліпопротеїнів низької щільності (ЛПНЩ), що зрештою може сприяти розвитку ЦД.
З огляду на важливість проведення гіполіпідемічної терапії для хворих з діабетичною (атерогенною) дисліпопротеїнемією (ДЛП) інтенсивно досліджуються нові лікарські засоби (ЛЗ). Актуальні випробування на цьому тлі зосереджені на пошуку нестатинових ліпідомодифікувальних ЛЗ. Зокрема, результати дослідження IMPROVE-IT (The Improved Reduction of Outcomes: Vytorin Efficacy International Trial) дозволяють дійти висновку про те, що одночасне застосування езетимібу зі статинами надає змогу ефективніше знизити рівні ХС ЛПНЩ і частоту кардіоваскулярних подій порівняно з монотерапією статинами. Отримані дані свідчать, що інші ліпідознижувальні засоби, які не впливають на активність ГМГ-КоА‑редуктази, також можуть покращити кардіоваскулярний прогноз.
Діабетична ДЛП, що характеризується кількісними, якісними, кінетичними змінами всіх основних циркулювальних ліпідів, сприяє підвищенню серцево-судинного (СС) ризику в пацієнтів із ЦД 2 типу. Багатообіцяльним терапевтичним напрямом лікування діабетичних ДЛП є пригнічення пропротеїнової конвертази субтилізин-кексинового типу 9 (PCSK9) людськими моноклональними антитілами (mAb), які на додаток до статинів потужно зменшують рівень ХС ЛПНЩ у плазмі крові та знижують ризик розвитку СС захворювань (ССЗ). АнтиPCSK9 mAb зазвичай не є найефективнішими ЛЗ при лікуванні пацієнтів із ЦД 2 типу порівняно із загальною популяцією хворих із високим ризиком атеросклеротичних ССЗ (АССЗ). Однак абсолютне зниження ризику основних СС подій є значимішим для хворих на ЦД 2 типу. Це свідчить про те, що лікування пацієнтів із ЦД 2 типу антиPCSK9 mAb, крім інших позитивних чинників, може бути привабливим із погляду рентабельності.
Отже, останніми роками активно обговорюються механізми дії, ефективність, безпека використання в клінічній практиці інгібіторів PCSK9. Продемонстровано, що активність PCSK9 у плазмі крові в пацієнтів із ЦД 2 типу позитивно корелює з показниками Homeostasis Model Assessment of Insulin Resistance (HOMA-IR). Кореляцію між рівнями PCSK9 і HOMA-IR можна пояснити тим, що експресія PCSK9 регулюється інсуліном через білок, що зв’язує регулювальний елемент стеролу-1 (SREBP‑1). Дійсно, гіперінсулінемія здатна індукувати транскрипцію гена PCSK9 з подальшою деградацією ЛПНЩ‑рецепторів і підвищенням рівня циркулювального ХС.
Існує низка препаратів, які відрізняються за механізмами пригнічення активності PCSK9. Умовно виокремлюють такі групи: mAb проти PCSK9 (антиPCSK9 mAb) – еволокумаб, алірокумаб, бокоцизумаб (ін’єкційні лікарські форми); інші ін’єкційні ЛЗ із різними механізмами дії – інклісиран, SPC4061, SPC5001, adnectin BMS‑962476, LIB003, антиPCSK9-вакцина; антиPCSK9-вакцина (на основі наночастинок); пероральні ЛЗ – PF‑06446846, DS‑9001a, SRT3025; інгібітори білка-переносника ефіру ХС (CETP)/PCSK9 – анацетрапіб, евацетрапіб, торцетрапіб, K‑312.
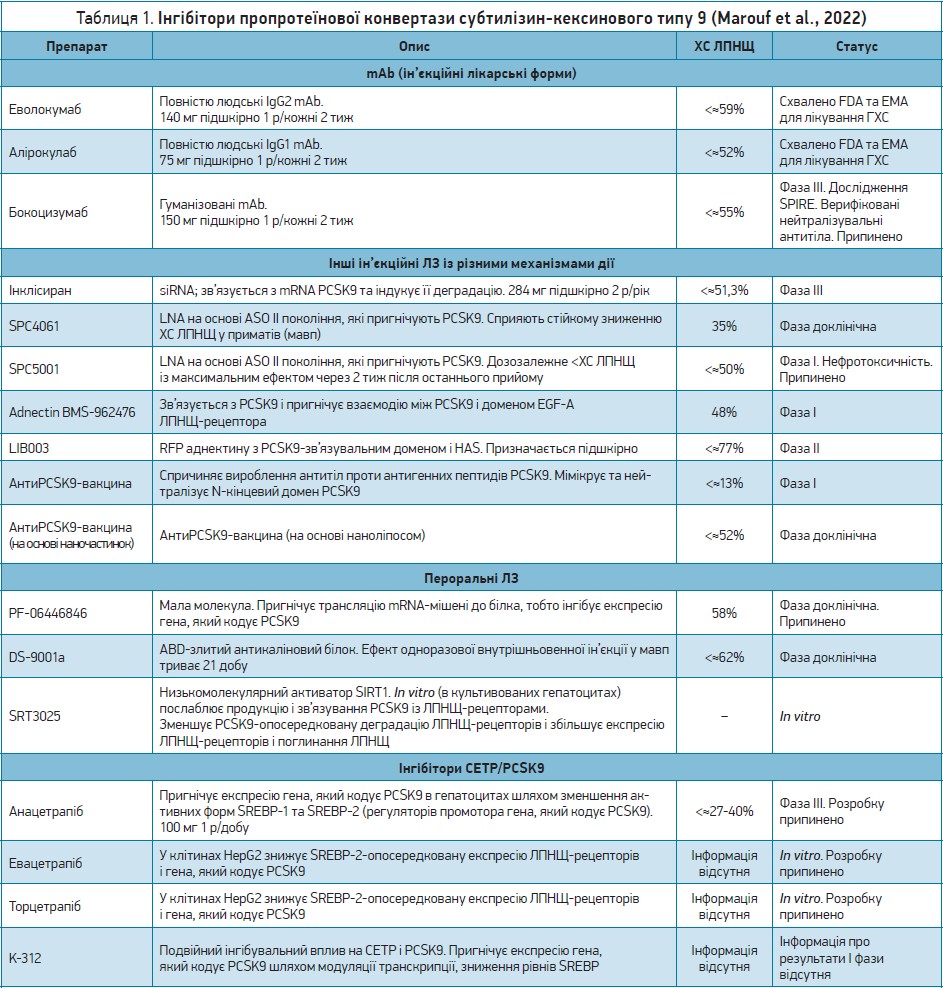
У таблиці 1 наведено характеристику основних інгібіторів PCSK9 (Marouf et al., 2022).
Примітки: ГХС – гіперхолестеринемія; ABD – альбумінозв’язувальний домен; ASO – антисмислові (антисенсові) олігонуклеотиди; CETP – білок-переносник ефіру ХС; EGF-A – епідермальний фактор росту-А; EMA – European Medicines Agency (Європейське агентство з лікарських засобів); FDA – US Food and Drug Administration (Управління з контролю за якістю продуктів харчування та лікарських засобів США); HAS – сироватковий альбумін людини; HepG2 – клітинна лінія раку печінки людини; IgG – імуноглобулін G; LNA – заблокована нуклеїнова кислота; mRNA – матрична РНК; PCSK9 – пропротеїнова конвертаза субтилізин-кексинового типу 9; RFP – рекомбінантний злитий білок; siRNA – мала інтерферувальна РНК; SIRT1 – сиртуїн-1; SPIRE – Studies of PCSK9 Inhibition and the Reduction of Vascular Events; SREBP‑2 – білок, що зв’язує регуляторний елемент стеролу-2.
FDA/EMA наразі схвалили 2 повністю гуманізовані mAb – інгібітори PCSK9: алірокумаб та еволокумаб. FDA й EMA дозволили використання алірокумабу для лікування дорослих із встановленим або високим ризиком АССЗ і дорослих хворих із сімейною ГХС (СГХС). Мета: зниження рівня ХС ЛПНЩ.
Показання:
- зниження ризику гострого коронарного синдрому (ГКС), інсульту та нестабільної стенокардії (НС) у дорослих пацієнтів із діагностованими ССЗ, які потребують госпіталізації;
- доповнення до дієти – окремо чи в поєднанні з іншою холестеринознижувальною терапією для лікування дорослих із первинною гіперліпопротеїнемією (ГЛП), у т. ч. із гетерозиготною формою СГХС;
- доповнення до дієти та іншої холестеринознижувальної терапії у дорослих із гомозиготною формою СГХС.
FDA й EMA дозволили використання еволокумабу для лікування дорослих пацієнтів із встановленим або високим ризиком ССЗ, а також для дорослих і дітей віком від 10 років із СГХС. Мета: зниження рівня ХС ЛПНЩ.
Показання:
- зниження ризику ГКС, інсульту та проведення реваскуляризації коронарних судин у дорослих із діагностованими ССЗ;
- лікування дорослих із первинною ГЛП, у т. ч. із гетерозиготною формою СГХС, як доповнення до дієти – окремо чи в поєднанні з іншою холестеринознижувальною терапією;
- лікування дітей віком від 10 років із гетерозиготною формою СГХС як доповнення до дієти та холестеринознижувальної терапії;
- доповнення до іншої холестеринознижувальної терапії для лікування дорослих і дітей віком від 10 років із гомозиготною формою СГХС.
АнтиPCSK9 mAb
Еволокумаб і алірокумаб – mAb імуноглобулінів (Ig)G2 і IgG2 людини цілеспрямовано інактивують PCSK9, серинову протеазу, яка зв’язує домен позаклітинного EGF-A печінкових ЛПНЩ‑рецепторів, що забезпечує їхні інтерналізацію та деградацію в лізосомах. PCSK9-опосередкована деградація ЛПНЩ‑рецептора відбувається внутрішньоклітинним і позаклітинним шляхом. У разі внутрішньоклітинного шляху PCSK9 сприяє деградації ЛПНЩ‑рецептора зв’язуванням та переміщенням новоутворених ЛПНЩ‑рецепторів від трансмережі комплексу Гольджі до лізосом. У позаклітинному шляху циркулювальний PCSK9 безпосередньо зв’язує домен EGF-A ЛПНЩ‑рецепторів на поверхні гепатоцитів, отже, через клатринозалежний ендоцитоз зумовлює лізосомальну деградацію. Більшість PCSK9 синтезується в печінці, але фермент також виробляється в нирках, тонкому кишечнику, центральній нервовій системі, епітелії товстої кишки, непосмугованих клітинах судин і підшлунковій залозі. У β-клітинах підшлункової залози накопичення ХС відбувається здебільшого через ЛПНЩ‑рецептор, експресія якого значною мірою здійснюється в острівцях Лангерганса. Отже, будь-яке генетичне чи фармакологічне втручання, яке збільшує експресію ЛПНЩ‑рецепторів, сприяє перевантаженню β-клітин ХС, порушенню секреції інсуліну та приєднанню згодом гіперглікемії.
Клінічні й експериментальні дані свідчать про те, що генетично зумовлена інактивація PCSK9 пов’язана з підвищеним ризиком розвитку ЦД 2 типу. Результати досліджень менделівської рандомізації майже одностайно показали, що пацієнти з генетичними варіантами втрати функції PCSK9 демонструють нижчий рівень ХС ЛПНЩ, але вищий уміст глюкози в крові, а також мають підвищений ризик розвитку ЦД 2 типу. Аналогічно, делеція генів у PCSK9-дефіцитних мишей пов’язана з порушеннями секреції інсуліну та толерантності до глюкози. Ці ефекти можна пояснити тим, що системна втрата PCSK9 сприяє підвищенню регуляції ЛПНЩ‑рецепторів у β-клітинах підшлункової залози з подальшим накопиченням ХС, клітинною дисфункцією та порушенням секреції інсуліну.
Da Dalt і співавт. (2019) повідомляють, що в мишей з делецією гена PCSK9 порівняно із тваринами дикого типу, котрі мають типову форму гена (стандарт гено- та фенотипу, WT), спостерігається порушення толерантності до глюкози (ПТГ). Виявилося, що дефекти в гомеостазі глюкози в мишей PCSK9-/- є результатом порушення секреції інсуліну, а не периферичної резистентності до гормона. Дійсно, рівні інсуліну та C‑пептиду в плазмі крові істотно зменшені в тварин PCSK9-/- порівняно з WT‑мишами. Введення інсуліну однаково знизило концентрацію глюкози та зумовило аналогічну інсулінозалежну активацію протеїнкінази В у печінці й посмугованих м’язах. Продемонстровано, що β-клітини мишей PCSK9-/- (порівняно з аналогічними WT‑тварин) зазвичай неправильної форми, більшого розміру, хаотично розподілені та характеризуються порушенням секреції інсуліну. Da Dalt і співавт. (2019) вважають, що морфологічні та функціональні зміни β-клітин зумовлені посиленням експресії ЛПНЩ‑рецепторів, що зрештою спричинило накопичення ХС і апоптозу. Дійсно, дисфункція β-клітин не спостерігалася в мишей з подвійною мутацією гена, а також з генетичними змінами як PCSK9, так і ЛПНЩ‑рецепторів.
Потенційний вплив PCSK9 на секрецію інсуліну підтверджено в біобанку людини. Зокрема, виявилося, що PCSK9 46L асоціювався з дисфункцією β-клітин, оціненою за допомогою гомеостатичної моделі оцінки функції β-клітин, але не з використанням HOMA-IR. Продемонстровано, що вміст PCSK9 не виходить визначити в плазмі крові мишей зі специфічною для печінки делецією алельних генів PCSK9 (AlbCreþ/Pcsk9LoxP/LoxP). Окрім того, в мишей AlbCreþ/Pcsk9LoxP/LoxP показники тесту на толерантність до глюкози, а також рівні глюкози в крові й інсуліну знаходилися в межах фізіологічної норми. Отже, експресія ЛПНЩ‑рецепторів у β-клітинах не змінена та свідчить, що вибіркове пригнічення циркулювального PCSK9 не впливає на гомеостаз глюкози. Саме тому з високою імовірністю можна стверджувати, що фармакологічні підходи, спрямовані на пригнічення специфічних рецепторів PCSK9 у печінці, не сприятимуть підвищенню ризику розвитку ЦД 2 типу.
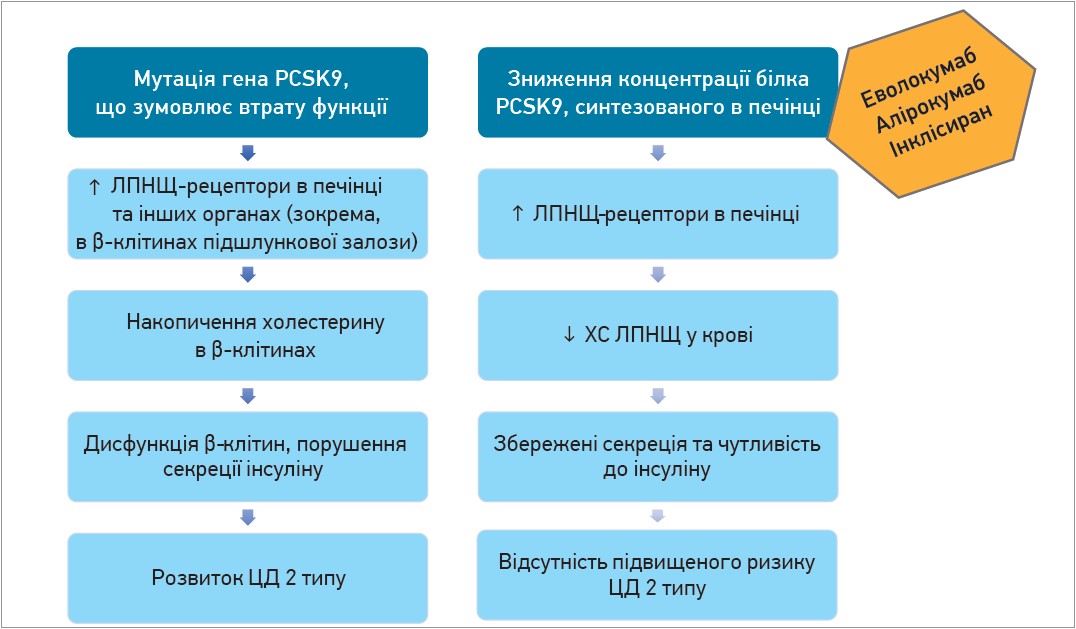
На рисунку наведено відомості про значення мутації гена PCSK9, що спричиняє втрату функції, а також зниження концентрації білка PCSK9, синтезованого в печінці, на ризик розвитку ЦД 2 типу (Paneni F., Costantino S., 2019).
Рис. Вплив мутації гена PCSK9 на пригнічення синтезу білка PCSK9, синтезованого в печінці, та на ризик розвитку ЦД 2 типу
(Paneni F., Costantino S., 2019)
Примітки: PCSK9 – пропротеїнова конвертаза субтилізин-кексинового типу 9.
PCSK9 і ЦД 2 типу
Підвищення ризику ЦД 2 типу спостерігається в осіб із генетично зумовленим або набутим зниженням ХС ЛПНЩ. Однак відомо, що СГХС, яка вважається автосомно-домінантним захворюванням, забезпечує захист від розвитку ЦД 2 типу. Водночас результати досліджень щодо ролі PCSK9 досить суперечливі. Зокрема, мутація гена PCSK9 у PCSK9-дефіцитних мишей супроводжується ПТГ і відсутністю жодного впливу. Bonnefond і співавт. (2015) не виявили змін у гомеостазі глюкози серед 4630 обстежених з генотипом PCSK9 p.R46L, тоді як метааналіз, проведений Lotta та співавт. (2016), показав, що цей генотип асоціюється з вищим рівнем пре- і постпрандіальної глюкози. Schmidt і співавт. (2017) досліджували чотири генетичні варіації PCSK9 і виявили їхній зв’язок із підвищеною концентрацією глюкози, масою тіла та ризиком ЦД. Однак, незважаючи на суперечливі результати, масштабніші дослідження підтверджують припущення, що поліморфізм генів PCSK9, який зумовлює низький рівень ХС ЛПНЩ, підвищує ризик ЦД 2 типу.
На відміну від генетичних, клінічні дослідження з використанням антиPCSK9 mAb продемонстрували нейтралітет щодо стану гомеостазу глюкози. Зокрема, Sattar і співавт. (2016) провели метааналіз трьох 12-тижневих РКД з оцінки ефективності еволокумабу порівняно із плацебо й еволокумабу порівняно з езетимібом на параметри вмісту ліпідів у пацієнтів із ЦД 2 типу / відсутністю верифікованого діагнозу ЦД 2 типу.
Продемонстровано, що еволокумаб порівняно із плацебо:
- в пацієнтів із ЦД 2 типу сприяє зниженню середнього рівня ХС ЛПНЩ на 60% (95% довірчий інтервал (ДІ) 51-69); ХС ліпопротеїнів невисокої щільності (ХС неЛПНЩ) на 55% (95% ДI 47-63); загального ХС (ЗХС) на 38% (95% ДI 32-44), тригліцеридів (ТГ) на 23% (95% ДI 12-34); аполіпопротеїну А (АпоА) на 31% (95% ДІ 25-37) і підвищенню середнього рівня ХС ліпопротеїнів високої щільності (ЛПВЩ) на 7% (95% ДI 4-11; р<0,0001 для всіх порівнянь);
- за відсутності верифікованого діагнозу ЦД 2 типу сприяє зниженню середнього рівня ХС ЛПНЩ на 66% (95% ДI 62-70); ХС неЛПНЩ на 58% (95% ДI 55-61); ЗХС на 40% (95% ДI 37-42), ТГ 17% (95% ДI 14-21); АпоА на 29% (95% ДІ 26-31) і підвищенню середнього рівня ХС ЛПВЩ на 7% (95% ДI 5-9; р<0,0001 для всіх порівнянь).
Установлено, що еволокумаб порівняно з езетимібом:
- у пацієнтів із ЦД 2 типу сприяє зниженню середнього рівня ХС ЛПНЩ на 39% (95% ДI 32-47); ХС неЛПНЩ на 34% (95% ДI 26-41); ЗХС на 24% (95% ДI 16-31); ТГ на 9% (95% ДI 5-23); АпоА на 26% (95% ДІ 16-35) і підвищенню середнього рівня ХС ЛПВЩ на 8% (95% ДI 4-13; p=0,20 для ТГ; р<0,0001 для всіх інших порівнянь);
- за відсутності верифікованого діагнозу ЦД 2 типу сприяє зниженню середнього рівня ХС ЛПНЩ на 40% (95% ДI 36-45); ХС неЛПНЩ на 35% (95% ДI 31-40); ЗХС на 25% (95% ДI 23-27); ТГ на 3% (95% ДI 3-8); АпоА на 30% (95% ДI 24-36) і підвищенню середнього рівня ХС ЛПВЩ на 6% (95% ДI 3-9; p=0,31 для ТГ; р<0,0001 для всіх інших порівнянь);
- для всіх ліпідних параметрів не спостерігалося взаємодії щодо ефектів лікування незалежно від верифікованого діагнозу ЦД 2 типу / відсутності ЦД 2 типу.
Отже, в хворих на ЦД 2 типу еволокумаб (порівняно із плацебо й езетимібом) сприяє зниженню ХС ЛПНЩ, ХС неЛПВЩ, апоА та ЗХС, а також значному підвищенню вмісту ХС ЛПВЩ. Отримані результати відповідають аналогічним, що спостерігаються в пацієнтів за відсутності верифікованого діагнозу ЦД 2 типу. Описані ефекти спостерігалися в хворих, які вже знаходилися на статинотерапії. Рекомендується бути обережним щодо узагальнення результатів цього метааналізу, адже короткотривалість проаналізованих РКД обмежує об’єктивну оцінку побічних ефектів; незрозуміло, чи інгібітори PCSK9 здатні негативно впливати на гомеостаз глюкози. Крім того, висока вартість ЛЗ (інгібіторів PCSK9) обмежує їхнє придбання пацієнтами з дуже високим ризиком АССЗ, які не досягли цільового рівня ХС ЛПНЩ за використання альтернативних гіполіпідемічних засобів.
Систематичний огляд і результати метааналізу 35 РКД, до якого залучили 45 539 пацієнтів (середній термін спостереження складає 85,5 тиж), не продемонстрували впливу інгібіторів PCSK9 на маніфестацію та/або декомпенсацію ЦД 2 типу (відношення шансів 1,05; 95% ДI 0,95-1,17). Крім того, у зведеному аналізі ODYSSEY (Evaluation of Cardiovascular Outcomes After an Acute Coronary Syndrome During Treatment with Alirocumab) (фаза III, 10 РКД, n=4974, тривалість становила 24-104 тиж) продемонстровано, що алірокумаб порівняно із плацебо не впливав на жодну кінцеву точку (КТ), пов’язану із ЦД (коефіцієнт ризиків (КР) 0,64, 95% ДI 0,36-1,14). Відносний ризик (ВР) для алірокумабу, пов’язаний з переходом від предіабету до маніфестного ЦД, становив 0,90 (95% ДI 0,63-1,29). На відміну від цих результатів, метааналіз 20 РКД (фази II, III), що передбачав участь 68 123 осіб (медіана спостереження становила 78 тиж), довів, що інгібітори PCSK9 порівняно із плацебо підвищують рівень глікованого гемоглобіну A1c (HbA1c) і препрандіальної глюкози в крові. Однак цей ефект був недостатнім для підтвердження статистично значущого збільшення захворюваності на ЦД (ВР 1,04; 0,96-1,13); тест неоднорідності (І2)=0%; р=0,427).
Sattar і співавт. (2017) вивчали особливості впливу еволокумабу на динаміку рівня глюкози в плазмі натще, HbA1c, маси тіла хворих і ймовірність приєднання вперше діагностованого ЦД. Автори перед початком проведення відкритого розширеного клінічного випробування (OLE) об’єднали результати обстежень пацієнтів протягом 1 року (48 тиж), у яких завершилося дослідження особливостей впливу еволокумабу. Проведений аналіз ефективності лікування в двох дослідженнях OLE серед 4802 учасників (1602 знаходилися на стандартному лікуванні, SOC; 3200 – еволокумаб + SOC). Повідомляється, що еволокумаб порівняно із SOC сприяв зниженню рівня ХС ЛПНЩ ≈на 60%. Установлено, що протягом 1 року проведення OLE не виявлено різниці в змінах вмісту HbA1c (0,1% (-0,1, 0,2) в медіані Q1, Q3 як для SOC, так і для еволокумабу + SOC) і рівня препрандіальної глюкози (0,06 ммоль/л) (-0,28, 0,38 ммоль/л) для SOC і 0,06 ммоль/л (-0,28, 0,44 ммоль/л для еволокумабу + SOC). Середня зміна показників маси тіла через 1 рік спостереження становила для SOC – -0,1 кг (0,2), еволокумабу + SOC – -0,3 кг (0,1). Рівень захворюваності (95% ДI) для вперше діагностованого ЦД на 100 пацієнто-років дорівнював 3,7 (2,9-4,7) у контрольній групі / SOC і 3,9 (3,2-4,6) при лікуванні еволокумабом / еволокумабом + SOC. Отже, терапія еволокумабом протягом однорічного періоду проведення OLE статистично значуще не впливала на стан гомеостазу глюкози.
Y.X. Cao і співавт. (2018) на вебсайтах PubMed, MEDLINE, Embase, Cochrane та ClinicalTrials.gov провели систематичний пошук РКД, в яких повідомлялося про особливості впливу алірокумабу й еволокумабу на рівень глюкози в плазмі крові натще, HbA1c або захворюваності на вперше виявлений ЦД. З метою проведення метааналізу відібрано 18 РКД, які включали 26 123 пацієнтів за відсутності верифікованого діагнозу ЦД 2 типу. Встановлено, що в хворих, котрі отримували антиPCSK9 mAb, порівняно з контрольними групами не спостерігалося істотної різниці щодо виявлення нових випадків ЦД (ВР 1,05; 95% ДI 0,95-1,16), рівня глюкози в плазмі крові натще (середня різниця (СР) 0,00 ммоль/л, 95% ДI -0,02 до 0,02) або HbA1c (СР 0,00%, 0 ммоль/л, 95% ДI від -0,01 до 0,01). Повідомляється, що алірокумаб і еволокумаб незалежно від типу антиPCSK9 mAb, характеристик учасників, тривалості та методів лікування статистично значуще не впливали на виявлення нових випадків ЦД, а також на гомеостаз глюкози.
De Carvalho та співавт. (2018), використовуючи бази даних MEDLINE (PubMed), Cochrane Library і ClinicalTrials.gov, провели метааналіз 20 РКД (68 123 учасники із середнім періодом спостереження 78 тиж).
Оригінальні дослідження включали до метааналізу, якщо вони відповідали таким критеріям:
1) фаза ІІ або ІІІ РКД;
2) пацієнти із СГХС або несімейною ГХС;
3) хворі з групи лікування знаходилися на терапії препаратами інгібіторів PCSK9 порівняно із групою контролю, яка отримувала плацебо з іншою гіполіпідемічною терапією або без неї;
4) тривалість лікування – ≥12 тиж.
Автори з використанням моделей випадкових величин і фіксованих ефектів, провели розрахунок ВР, 95% ДI. Повідомляється, що інгібітори PCSK9 порівняно із плацебо сприяли збільшенню рівня препрандіальної глюкози в крові (зважена СР 1,88 мг/дл; 95% ДI 0,91-2,68; I2=0%; р<0,001 та HbA1c (0,032%, 0,011-0,050); I2=15,5%; р<0,001). Однак такий ефект виявився недостатнім для ствердження про статистично значуще збільшення частоти розвитку ЦД (ВР 1,04, 0,96-1,13; I2=0%; р=0,427). Результати метарегресійного аналізу свідчать про зв’язок між підвищеним ризиком ЦД та ефективністю (р=0,029) і тривалістю лікування інгібіторами PCSK9 (р=0,026). Отже, лікування пацієнтів із СГХС або несімейною ГХС лікарськими препаратами із групи інгібіторів PCSK9 протягом ≥12 тиж сприяє незначному, однак статистично значущому підвищенню рівня препрандіальної глікемії в плазмі та HbA1c.
Guedeney та співавт. (2019) провели огляд РКД, під час яких порівнювали лікування алірокумабом або еволокумабом із плацебо чи іншими гіполіпідемічними препаратами. Автори мали на меті оцінити ефективність і безпеку алірокумабу та еволокумабу в пацієнтів із ДЛП/АССЗ. Проведено метааналіз 39 РКД із залученням 66 478 хворих, з котрих 35 896 учасників отримували інгібітори PCSK9 (14 639 – алірокумаб, 21 257 – еволокумаб), а 30 582 представляли контрольну групу. Основні первинні КТ – смерть від усіх причин, від ССЗ, а також ГКС та інсульт. Оцінювали ВР і 95% ДI за допомогою моделей випадкового ефекту; проводили І2. Встановлено, що вплив інгібіторів PCSK9 на показники смерті від усіх причин, у т. ч. СС, загалом не був статистично значущим (р=0,15 і р=0,34 відповідно). Використання інгібіторів PCSK9 поєднувалося з нижчим ризиком ГКС (1,49 проти 1,93 на 100 пацієнто-років; ВР 0,80, 95% ДI 0,74-0,86; І2=0%; р<0,0001), ішемічного інсульту (0,44 порівняно з 0,58 на 100 пацієнто-років; ВР 0,78, 95% ДI 0,67-0,89; І2=0%; р=0,0005) і коронарною реваскуляризацією (2,16 проти 2,64 на 100 пацієнто-років; ВР 0,83, 95% ДI 0,78-0,89; І2=0%; р<0,0001) порівняно з контрольною групою. Застосування інгібіторів PCSK9 не було пов’язане з підвищеним ризиком розвитку нейрокогнітивних побічних ефектів (р=0,91), зростання рівня печінкових ферментів (р=0,34), рабдоміолізу (р=0,58) або вперше зареєстрованих випадків ЦД (NOD) (p=0,97). Отже, пригнічення PCSK9 алірокумабом або еволокумабом було пов’язане з меншим ризиком ГКС, інсульту та коронарної реваскуляризації зі сприятливим профілем безпеки, зокрема NOD діагностованого ЦД.
Khan і співавт. (2019) за допомогою баз даних Medline, Embase, Cochrane Central Register відібрали та провели метааналіз 33 РКД (21 – з дослідження ефективності статинів, 12 – із впливу інгібіторів PCSK9). Загалом 163 688 пацієнтів без ЦД випадково розподілялися на групи з більш інтенсивною (83 123 хворих) або менш інтенсивною (80 565 пацієнтів) ліпідознижувальною терапією. Більш інтенсивна гіполіпідемічна терапія визначалася як фармакологічна стратегія, що передбачала використання інгібіторів PCSK9, високоінтенсивної статинотерапії, тоді як менш інтенсивна відповідала групі активного контролю або плацебо. Метарегресію та метааналіз проводили з використанням моделі випадкових ефектів. Повідомляється, що при використанні більш інтенсивної ліпідознижувальної терапії не спостерігалося жодного суттєвого зв’язку між зниженням рівня ХС ЛПНЩ на 1 ммоль/л і випадком розвитку ЦД (ВР 0,95; 95% ДI 0,87-1,04; р=0,30; І2=4%). Однак виявилося, що більш інтенсивна гіполіпідемічна терапія пов’язана з вищим ризиком розвитку ЦД порівняно з менш інтенсивною (ВР 1,07; 95% ДI 1,03-1,11; р<0,001; І2=0%). Отримані результати зумовлювалися вищим ризиком розвитку ЦД при застосуванні статинів (ВР 1,10; 95% ДI 1,05-1,15; р<0,001; І2=0%), тоді як використання інгібіторів PCSK9 не мало зв’язку з ризиком випадків уперше діагностованого ЦД (ВР 1,00; 95% ДI 0,93-1,07; р=0,96; І2=0%).
Мета пошуку в Medline, ClinicalTrials.gov, а також метааналізу РКД, проведеного Monami та співавт. (2019), – оцінка впливу інгібіторів PCSK9 на метаболізм глюкози, рівень ХС ЛПНЩ, стан СС захворюваності й смертності в пацієнтів із ЦД 2 типу / відсутністю верифікованого діагнозу ЦД 2 типу. Проведений метааналіз 38 РКД, у яких порівнювали інгібітори PCSK9 із плацебо чи активними лікарськими препаратами. Первинні КТ включали випадки ЦД, рівні препрандіальної глікемії та HbA1c; уміст ХС ЛПНЩ у КТ у пацієнтів із ЦД і в загальній вибірці, серйозні СС події (MACE), смертність в осіб із ЦД 2 типу / відсутністю верифікованого діагнозу ЦД 2 типу. Повідомляється, що інгібітори PCSK9 порівняно із плацебо чи будь-яким ЛЗ порівняння не сприяли підвищенню ризику розвитку ЦД. Зниження вмісту ХС ЛПНЩ порівняно із плацебо в пацієнтів із ЦД становило 52,6 (41,3; 63,8) мг/дл; відповідний показник для всіх хворих дорівнював 66,9 (62,4; 71,3) мг/дл. Метарегресійний аналіз показав обернену кореляцію між часткою пацієнтів із ЦД і впливом інгібіторів PCSK9 на вміст ХС ЛПНЩ у дослідженнях проти езетимібу, але не порівняно із плацебо. Крім того, аналіз результатів РКД дозволив стверджувати, що інгібітори PCSK9 не впливають на метаболізм глюкози; ймовірно, не впливають на показники MACE та смертності окремо для осіб із ЦД / відсутністю верифікованого діагнозу ЦД 2 типу.
Chen і співавт. (2020) проаналізували питання безпеки використання антиPCSK9 mAb щодо ризику вперше верифікованого діагнозу ЦД. Автори провели метааналіз результатів 23 РКД (65 957 учасників), в яких надавалася інформація про випадки вперше верифікованого діагнозу ЦД або декомпенсацію клінічного ЦД. Із метою порівняння КТ розраховувалися ВР і 95% ДІ. Встановлено, що порівняно з контрольною групою лікування антиPCSK9 mAb не супроводжувалося ризиком розвитку ЦД (ВР 0,97; 95% ДI 0,91-1,02; р=0,22), причому вигіднішим із цього погляду здавався алірокумаб, ніж еволокумаб або бокоцизумаб (ВР 0,91; 95% ДI 0,85-0,98; р=0,01).
Chiu та співавт. (2020) у базах PubMed, Cochrane Central Register і ClinicalTrials.gov переглянуто результати та проведено систематичний метааналіз 11 подвійно сліпих РКД. Мета – оцінити вплив інгібіторів PCSK9 і езетимібу на ризик NOD ЦД. Для проведення метааналізу ефективності інгібіторів PCSK9 загалом було залучено 52 214 учасників і 20 084 особи для езетимібу. Встановлено, що результати, отримані в пацієнтів, рандомізованих на інгібітори PCSK9, а також езетимібу, не відрізнялися за частотою ризику вперше верифікованого діагнозу ЦД від контрольної групи (ВР 0,99; 95% ДI 0,92-1,07; р=0,87 і ВР 1,05; 95% ДI 0,95-1,15; р=0,37). На підставі отриманих результатів автори вважають, що використання інгібіторів PCSK9 та езетимібу, ймовірно, не впливає на ризик розвитку ЦД.
На сьогодні проведено декілька провідних РКД щодо вивчення особливостей і можливостей впливу антиPCSK9 mAb на стан несприятливих наслідків ССЗ, одне з яких внаслідок імуноопосередкованого ослаблення ефективності бокоцизумабу дотерміново припинено. Це такі клінічні випробування: FOURIER (Further Cardiovascular Outcomes Research with PCSK9 Inhibition in Subjects with Elevated Risk) – ефективність еволокумабу; SPIRE – бокоцизумабу; ODYSSEY – алірокумабу і DESCARTES – Durable Effect of PCSK9 Antibody Compared with Placebo Study.
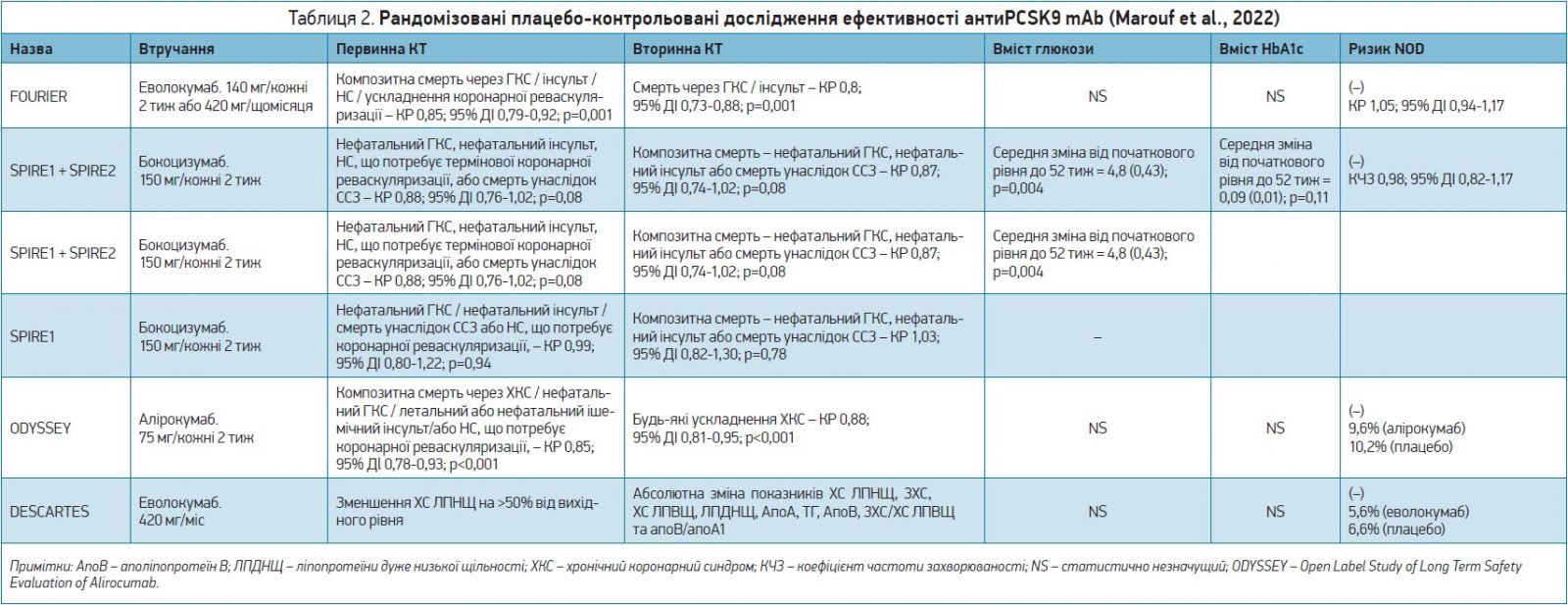
Результати основних рандомізованих плацебо-контрольованих досліджень ефективності антиPCSK9 mAb наведено в таблиці 2 (Marouf et al., 2022).
У випробуванні FOURIER 27 564 пацієнтів із діагностованими AССЗ, котрі знаходилися на статинотерапії, було рандомізовано з метою призначення еволокумабу (140 мг 2 р/тиж або 420 мг/міс підшкірно) чи плацебо. Продемонстровано, що еволокумаб порівняно із плацебо стійко знижував рівень ХС ЛПНЩ у середньому на 59%, що відповідало 0,78 ммоль/л. Повідомляється, що 48-тижневе лікування еволокумабом сприяло 15% зниженню первинної комбінованої КТ (КР 0,85; ДІ 0,79-0,92; р<0,001). Пригнічення PCSK9 еволокумабом не супроводжувалося збільшенням частоти ризику вперше верифікованого діагнозу ЦД або погіршенням стану глікемії у пацієнтів із ЦД.
SPIRE. У дослідженні, розподіленому на два субдослідження (SPIRE‑1, SPIRE‑2), 27 438 учасників з AССЗ або СГХС в анамнезі чи високим ризиком АССЗ рандомізовані з метою призначення 150 мг бокоцизумабу кожні 2 тиж підшкірно або вживання плацебо. Тривалість SPIRE‑1 становила 7 міс, SPIRE‑2 – 12 міс. Результати SPIRE‑2 свідчать про зниження рівня несприятливих наслідків ССЗ на 21%. Водночас аналіз результатів SPIRE‑1 не виявив аналогічного зниження. Можливі причини: недовготривалість спостереження і нижчий базовий рівень ХС ЛПНЩ. Висновки SPIRE‑2 і SPIRE‑1 свідчать, що призначення 150 мг бокоцизумабу статистично значуще не впливає на рівні HbA1c.
Дослідження ODYSSEY тривало 2,8 року. Обстежено 18 924 пацієнтів із ГКС від 1 до 12 міс в анамнезі, рівнем ХС ЛПНЩ щонайменше 1,8 ммоль/л, ХС неЛПВЩ не <2,6 ммоль/л, апоB не <80 мг/дл. Хворі знаходилися на високоінтенсивній статинотерапії чи отримували максимально переносимі дози інгібіторів ГМГ-КоА‑редуктази. Алірокумаб зменшив частоту СС подій на 15% після середнього періоду спостереження тривалістю 2,8 року. В пацієнтів, що отримували алірокумаб, спостерігалося незначне зниження частоти ризику вперше верифікованого діагнозу ЦД порівняно із плацебо (9,6 проти 10,1%).
DESCARTES. Тривалість РКД становила 52 тиж. Аналізувалася ефективність еволокумабу (420 мг кожні 4 тиж) у відсотковому та абсолютному зниженні вмісту ХС ЛПНЩ. Обстежено 901 пацієнта з ГХС, з них було 120 хворих на ЦД 2 типу, 293 мали порушення глікемії натще (ПГН), 289 – метаболічний синдром (у 194 з них діагностовано ПГН, а у 393 не спостерігалося жодного із цих станів. Аналітичний аналіз результатів DESCARTES свідчить про таке: незважаючи на досягнення значного зниження рівня ХС ЛПНЩ >50% від вихідного, не спостерігалося статистично значущих змін параметрів глікемії в жодній з підгруп із базовою еуглікемією, ПГН або ЦД 2 типу.
Отже, глікемічна безпека антиPCSK9 mAb, що спостерігалася під час клінічних випробувань, може бути частково пояснена відносно короткотривалим впливом цих препаратів порівняно із природним поліморфізмом PCSK9, який забезпечує нижчий рівень ЛПНЩ. Окрім того, можливо, mAb, націлені на білок PCSK9, не впливають на внутрішньоклітинну продукцію PCSK9 і фізіологічні особливості метаболізму ХС. Хоча генетичні дослідження свідчать про потенційний зв’язок між пригніченням гена PCSK9 і гомеостазом глюкози, антиPCSK9 mAb не погіршують глікемічного контролю в пацієнтів із ЦД 2 типу, але їхню безпеку слід підтвердити довготривалим спостереженням.
На сьогодні інгібітори PCSK9 варто розглядати як додаткові фармакологічні агенти за неефективності статинів у максимально переносимих дозах. Найменш суперечлива популяція пацієнтів із високим ризиком ССЗ для використання інгібіторів PCSK9 включає хворих із СГХС; тяжким перебігом та/або дуже високим ризиком АССЗ, зі стійким підвищеним рівнем ХС ЛПНЩ, незважаючи на використання високоінтенсивної терапії інгібіторами ГМГ-КоА‑редуктази. Пацієнти із ЦД, які додатково мають будь-який із цих станів, становлять підгрупу особливо високого ризику, для якої інгібітори PCSK9 заслуговують на серйозну увагу.
Хворим із нещодавно діагностованим ЦД 2 типу поточний алгоритм контролю ліпідів для зниження ризику ССЗ рекомендується розпочинати зі статинів. Езетиміб є наступним ЛЗ, який слід додати, якщо рівень ХС ЛПНЩ у пацієнтів є вищим за прийнятний. Обґрунтування: задовільна переносимість і низька вартість, простота введення та сприйняття пацієнтами, докази користі для СС системи, особливо в пацієнтів із ЦД. У випадках неефективності комбінації статинів з езетимібом інгібітор PCSK9 є доцільним і раціональним вибором.
Майже всі клінічні випробування інгібіторів PCSK9 проводилися з фоновою терапією статинами, тому з погляду доказової медицини ці препарати необхідно використовувати разом з інгібіторами ГМК-КоА‑редуктази як базову терапію. Гіполіпідемічний ефект лікування потрібно оцінювати протягом 3 міс після початку лікування. Хоча наднизькі рівні ХС ЛПНЩ як результат пригнічення PCSK9 добре переносяться пацієнтами, дозу статинів доцільно знизити, якщо рівень ХС ЛПНЩ настільки низький, що його практично неможливо визначити, наприклад, <0,4 ммоль/л.
Загалом клінічні дані свідчать про те, що інгібітори PCSK9 добре переносяться та забезпечують (на додаток до високоінтенсивної терапії статинами) значне зниження рівня ХС ЛПНЩ у хворих на ЦД 2 типу і діабетичну ДЛП. Використання інгібіторів PCSK9 не супроводжується втратою глікемічного контролю або підвищенням ризику розвитку ЦД в осіб без попереднього діагностованого ЦД, а також може запобігти чи зменшити подальші СС події.
Отже, припускають, що антиPCSK9-терапія, спрямована на циркулювальний білок PCSK9 печінкового походження, може достатньо обмежено впливати на експресію ЛПНЩ‑рецепторів у β-клітинах підшлункової залози, отже, і не підвищувати ризику розвитку ЦД. Довгострокове спостереження за результатами рандомізованих клінічних випробувань інгібіторів PCSK9 має надати чітку відповідь на це важливе запитання.
Медична газета «Здоров’я України 21 сторіччя» № 4-5 (540-541), 2023 р.