30 травня, 2023
Роль таргетних препаратів у лікуванні пацієнтів із недрібноклітинним раком легені та вторинним метастазуванням у ЦНС
 25 березня відбулася конференція «Cучасне лікування метастатичного недрібноклітинного раку легені в Україні». Провідні вітчизняні науковці висвітлили ключові проблеми, з якими стикаються клініцисти при веденні пацієнтів з недрібноклітинним раком легені (НДРЛ). Зокрема, фокус доповідей було зміщено саме на аспекти діагностики та сучасні можливості лікування вторинних метастазів у центральній нервовій системі (ЦНС) при НДРЛ.
25 березня відбулася конференція «Cучасне лікування метастатичного недрібноклітинного раку легені в Україні». Провідні вітчизняні науковці висвітлили ключові проблеми, з якими стикаються клініцисти при веденні пацієнтів з недрібноклітинним раком легені (НДРЛ). Зокрема, фокус доповідей було зміщено саме на аспекти діагностики та сучасні можливості лікування вторинних метастазів у центральній нервовій системі (ЦНС) при НДРЛ.
https://qr.short.az/r/b8ob8hykbbfnm1l
 Методи виявлення метастазів НДРЛ у ЦНС охарактеризувала лікар-радіолог КЛ «Феофанія» ДУС (м. Київ) Ірина Олегівна Буріна.
Методи виявлення метастазів НДРЛ у ЦНС охарактеризувала лікар-радіолог КЛ «Феофанія» ДУС (м. Київ) Ірина Олегівна Буріна.
– Відповідно до сучасних рекомендацій, золотим стандартом діагностики НДРЛ є позитронно-емісійна комп’ютерна томографія (ПЕТ-КТ) з внутрішньовенним (в/в) контрастуванням. При неможливості її проведення рекомендована комп’ютерна томографія (КТ) грудної, черевної порожнин та малого таза з в/в контрастуванням (D.S. Ettinger, 2022). Треба зазначити, що ні КТ, ні ПЕТ-КТ не підходять для сканування головного мозку з метою виявлення метастазів у ЦНС. Однак загальновідомо, що понад 20% пацієнтів з НДРЛ на момент встановлення діагнозу мають метастази в головному мозку, і непроведення візуалізаційного обстеження ЦНС призводить до заздалегідь некоректного вибору подальшої терапії, швидкого прогресування захворювання саме в ЦНС і вкрай негативно впливає на прогноз пацієнта. Стандартом візуалізаційної діагностики новоутворень у ЦНС є магнітно-резонансна томографія (МРТ) із в/в контрастуванням, яку необхідно проводити в рамках стандартного комплексу базового первинного обстеження пацієнтів з НДРЛ перед початком лікування. Особливо це важливо для пацієнтів з наявністю мутацій EGFR та ALK, оскільки статистичні дані свідчать, що від 25 до 40% пацієнтів з EGFR-позитивним НДРЛ мають метастази в головному мозку на початку хвороби, а впродовж усього захворювання – понад 50% (L.J. Schouten, 2002; M. Nishino, 2019; F. Petrelli, 2018).
Відомими факторами ризику розвитку метастазів у ЦНС при НДРЛ є молодий вік пацієнта на момент встановлення діагнозу, неплоскоклітинна гістологічна форма НДРЛ, тобто аденокарцинома легені, ступінь диференціювання GII і GIII, лімфоваскулярна інвазія, ураження хілярних лімфатичних вузлів і наявність драйверних мутацій, особливо EGFR (C.H. Han, 2017; H.J. Kang, 2014). У рекомендаціях Національної онкологічної мережі США (2023) з ведення хворих на НДРЛ зазначено, що проведення МРТ головного мозку з в/в контрастуванням рекомендовано починати з ІІ стадії, при ІB стадії виконувати опціонально, як і за наявності центральних пухлин ≥1 см при І стадії НДРЛ (D.S. Ettinger, 2022). Важливо також зазначити, що відсутність неврологічної симптоматики у хворих на НДРЛ зовсім не виключає наявність метастазів у головному мозку. Сучасні дані свідчать, що метастази в головному мозку у 35-40% пацієнтів є безсимптомними, тому важливість проведення МРТ із в/в контрастуванням на початку захворювання з подальшим моніторингом не викликає сумнівів.
Метастатичне ураження ЦНС не лише змінює прогноз у пацієнтів, а й вимагає зміни терапевтичної стратегії. Так, симптомні ураження з вираженим компресійно-дислокаційним синдромом частіше підлягають хірургічному видаленню. При асимптомних вогнищах невеликих розмірів можна застосовувати радіохірургію. Наявність у хворого множинного ураження потребує призначення препаратів, які мають здатність проникати через гематоенцефалічний бар’єр (ГЕБ; N. Lamba, 2021; M.A. Vogelbaum, 2022).
Сам по собі факт можливості безсимптомного метастазування пухлини у комбінації з супутніми факторами ризику у пацієнта, а також наявність драйверних мутацій вимагає більш частого радіологічного контролю. Сучасні стратегії діагностики метастатичного НДРЛ мають свої особливості. Так, проведення КТ без контрастування пацієнтам цього профілю не рекомендоване, оскільки може використовуватися лише з метою швидкого виключення небезпечних для життя станів, таких як крововилив, гідроцефалія, вклинення головного мозку та ін. КТ з контрастуванням не є методом вибору, оскільки показана лише при неможливості проведення МРТ. Це пов’язано з тим фактом, що КТ має певні обмеження: обмежену візуалізацію вогнищ <2 см та прилеглих до кісткових структур, а також недостатнє диференціювання дуральних метастазів від менінгіом, внутрішньомозкових гематом від крововиливу в метастаз, неможливість розрізнити рецидив від постпроменевого некрозу (N. Chakrabarty, 2023). Враховуючи всі обмеження КТ, золотим стандартом діагностики при метастазах у ЦНС є саме МРТ із в/в контрастуванням, яку рекомендовано проводити пацієнтам починаючи з ІІ стадії НДРЛ, а також у разі центральної пухлини ≥1 см при І стадії НДРЛ. Важливо також зазначити, що візуалізація пухлин має свої особливості. Так, при більшості мутацій EGFR та ALK новоутворення є кістозними, мають геморагічні включення та нечіткі контури, периферичний або кільцеподібний тип накопичення контрастної речовини (G.N. Marta, 2018; F. Facchinetti, 2019).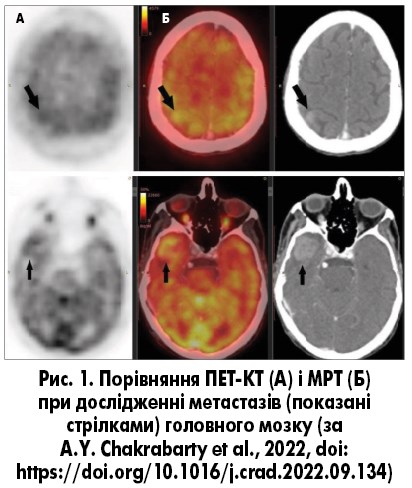
Наявність/відсутність первинних метастазів у ЦНС принципово впливає на подальшу стратегію лікування, в тому числі на призначення препаратів, що проникають через ГЕБ і створюють високу концентрацію у лікворі. З метою спостереження за відповіддю на призначену терапію та контролю ефективності лікування при метастатичному ураженні проводиться оцінка за критеріями Response Assessment in Neuro-Oncology Brain Metastases (RANO BM), особливо при наявності мутацій EGFR та ALK. Критерії RANO BM включають різні параметри, такі як розмір пухлин, кількість метастазів, симптоми тощо, дозволяють оцінити ефективність лікування і приймати рішення про його подальшу тактику у пацієнтів з метастатичним ураженням головного мозку (F. Deng, 2021; D.S. Ettinger, 2022).
Клінічний випадок 1
Пацієнт Ч., 60 років, НДРЛ, безсимптомний.
Немуцинозна аденокарцинома G3 нижньої частки лівої легені T1N0M0, I стадія.
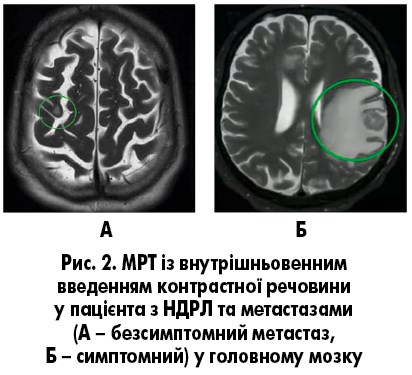 Клінічно неврологічна симптоматика відсутня, проте результати МРТ з контрастуванням вказують на наявність метастазів у головному мозку (рис. 2А).
Клінічно неврологічна симптоматика відсутня, проте результати МРТ з контрастуванням вказують на наявність метастазів у головному мозку (рис. 2А).
Клінічний випадок 2
Пацієнт Ч., 73 роки, НДРЛ, метастази в головному мозку.
Плоскоклітинна карцинома нижньої частки правої легені cT3N3M1c (головний мозок – рис. 2Б, права надниркова залоза, хребець L3), PDL+, EGDR-.
Неврологічна симптоматика: згладження правої пригубної складки, легка девіація язика праворуч, зниження сили в правій кінцівці до 4 балів, легке похитування при ходьбі.
Результати сучасних досліджень свідчать, що чим довший час минув після встановлення діагнозу, тим вищий ризик розвитку метастазів наявний у пацієнта. M. Kim та співавт. (2021) продемонстрували, що метастазування в ЦНС має пряму кореляцією з часом після встановлення діагнозу, стадією захворювання (зокрема ІІІ-IV стадія характеризується найвищим ризиком розвитку метастазів), наявністю аденокарциноми легені порівняно з плоскоклітинною карциномою, а також драйверних мутацій EGFR та ALK.
Отже, золотим стандартом виявлення метастазів у ЦНС при НДРЛ є МРТ із в/в контрастуванням. При цьому важливо враховувати, що відсутність неврологічної симптоматики у хворого не виключає наявності у нього метастазів у головному мозку. Саме тому проведення МРТ рекомендовано починати при ІІ стадії захворювання, а також у пацієнтів з центральною пухлиною ≥1 см та І стадією захворювання. Це особливо стосується хворих із наявними драйверними мутаціями, при яких значно підвищується ризик метастазування в ЦНС. Правильне використання методів візуалізації та дотримання термінів контрольних обстежень допомагає уникнути хибнопозитивних результатів, а у разі променевої та імунотерапії – виключити псевдопрогресування.
 Про роль нейрохірурга у прийнятті рішення щодо ведення пацієнтів з метастатичним ураженням головного мозку розповів лікар-нейрохірург вищої категорії, головний науковий співробітник відділу нейроонкології та нейрохірургії дитячого віку Інституту нейрохірургії ім. академіка А.П. Ромоданова НАМН України (м. Київ), доктор медичних наук Микола Олександрович Гук.
Про роль нейрохірурга у прийнятті рішення щодо ведення пацієнтів з метастатичним ураженням головного мозку розповів лікар-нейрохірург вищої категорії, головний науковий співробітник відділу нейроонкології та нейрохірургії дитячого віку Інституту нейрохірургії ім. академіка А.П. Ромоданова НАМН України (м. Київ), доктор медичних наук Микола Олександрович Гук.
– Метастази в головному мозку є найпоширенішою формою внутрішньочерепних пухлин у дорослих, частота яких у популяції хворих на рак становить близько 25%. За популяційними даними, лише 8-10% пацієнтів з раком мають симптомні метастатичні новоутворення в головному мозку. При цьому, завдяки досягненням у діагностиці та лікуванні, значна частка хворих не помирає безпосередньо від прогресування цих метастатичних уражень. Тому актуальним питанням є стратегії ведення таких пацієнтів, зокрема вибір найефективнішої стратегії терапії. Основні варіанти вторинного ураження наведені в таблиці.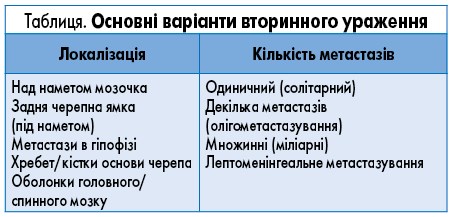
Важливо зазначити, що незважаючи на успіхи сучасної медицини, одного лише хірургічного видалення метастазів у мозку недостатньо для досягнення місцевого контролю захворювання. Мета оперативного лікування при метастазах полягає в тому, щоб отримати тканини для діагностики (за запитом онколога), зменшити вираженість неврологічних симптомів, мас-ефекту та набряку. Рішення про необхідність проведення хірургічного втручання є дискутабельним і розглядається мультидисциплінарною командою фахівців для кожного пацієнта індивідуально. І хоча сучасні рекомендації регламентують проведення оперативного лікування метастазів у ЦНС, які підлягають безпечному та повному видаленню, на практиці ж ці рекомендації не виконуються через суб’єктивність прийняття рішення, а градації радикальності хірургічного втручання відсутні. За даними Інституту нейрохірургії ім. акад. А.П. Ромоданова НАМН України, лише 3-5% хворих з метастазами в ЦНС оперовані в ургентному порядку, у решті випадків є час, щоб визначити обґрунтовану тактику ведення, в тому числі застосування стереотаксичної променевої хірургії (stereotactic radiosurgery – SRS), променевої терапії на всю ділянку головного мозку (Whole Brain Radiation Therapy – WBRT) або таргетної терапії. Остання зараз є найефективнішим варіантом лікування метастазів за умови наявності відповідних мутацій.
Клінічний випадок 3
Пацієнт Н., 55 років, НДРЛ, метастази в головному мозку.
Отримував хіміотерапію (ХТ) з приводу НДРЛ. Протягом 2021-2022 рр. декілька разів переніс хірургічне лікування: березень 2021 – лобектомія правої легені (плоскоклітинна карцинома) та медіастинальна лімфодисекція; травень 2021 – ХТ карбоплатином і неоад’ювантна променева терапія (сумарна вогнищева доза 50 Гр); лютий 2022 – поява неврологічної симптоматики: геміплегія та гемігіпестезія.
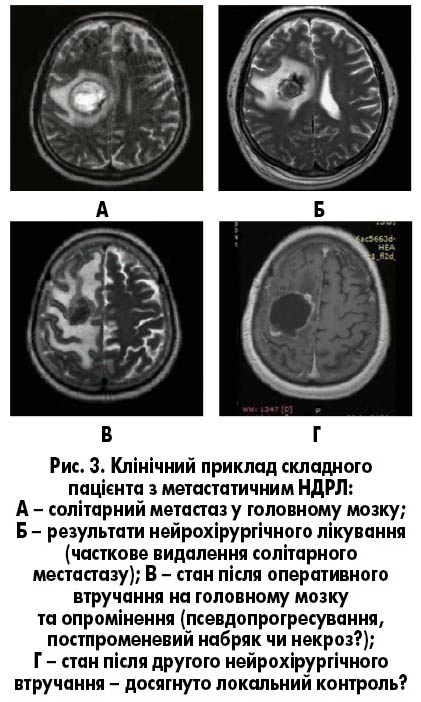 У 2022 р. на МРТ із в/в контрастуванням виявлено солітарний метастаз зі значним набряком, що потребувало ургентного нейрохірургічного лікування (рис. 3А). Результатом оперативного втручання стало неповне видалення солітарного метастазу, проте на момент контрольного обстеження після операції – 17.03.2022 – спостерігалося полегшення клінічної симптоматики у хворого: регресування рухових розладів (рис. 3Б).
У 2022 р. на МРТ із в/в контрастуванням виявлено солітарний метастаз зі значним набряком, що потребувало ургентного нейрохірургічного лікування (рис. 3А). Результатом оперативного втручання стало неповне видалення солітарного метастазу, проте на момент контрольного обстеження після операції – 17.03.2022 – спостерігалося полегшення клінічної симптоматики у хворого: регресування рухових розладів (рис. 3Б).
Пацієнту була призначена радіохірургія (на ділянку частково видаленого метастазу), після якої його загальний стан погіршився – наростав геміпарез, епілептичні напади. Під час МРТ була виявлена незрозуміла рентгенологічна картина, яку можна було трактувати у трьох варіантах: постпроменевий набряк, некроз чи продовження прогресування метастазу (рис. 3В). Важливо зазначити, що протягом двох років терапії пацієнту так і не виконано молекулярно-генетичне дослідження, хоча направлення були і після лобектомії правої легені, і після нейрохірургічної операції.
Через погіршення загального стану, появу неврологічної симптоматики та погіршення якості життя вирішено провести другу нейрохірургічну операцію. Після хірургічного втручання було досягнуто локального контролю захворювання за даними МРТ (рис. 3Г), але якість життя лишалася невисокою (50-60 за шкалою Карновського). Пацієнт постійно отримує протинабрякову та протисудомну терапію, але він все одно має пройти другий курс променевої терапії.
Отже, хірургічне лікування метастазів у головному мозку є обмеженим, а його ефективність вкрай низька. Саме тому відповідь на питання щодо доцільності проведення нейрохірургічної резекції метастазів у ЦНС має давати мультидисциплінарна команда фахівців у кожному випадку окремо.
 Завідувачка відділення променевої терапії Національного інституту хірургії та трансплантології ім. О.О. Шалімова (м. Київ), кандидат медичних наук Олена Валеріївна Сафронова представила доповідь «Стратегії лікування метастазів в ЦНС при наявності драйверних мутацій: WBRT/SRS чи інгібітори тирозинкінази – що обрати лікарю?».
Завідувачка відділення променевої терапії Національного інституту хірургії та трансплантології ім. О.О. Шалімова (м. Київ), кандидат медичних наук Олена Валеріївна Сафронова представила доповідь «Стратегії лікування метастазів в ЦНС при наявності драйверних мутацій: WBRT/SRS чи інгібітори тирозинкінази – що обрати лікарю?».
– Сьогодні у розпорядженні клініцистів чимало результатів досліджень щодо різних підходів до ведення пацієнтів з метастазами в ЦНС при НДРЛ. Вони включають як застосування інгібіторів тирозинкінази (ІТК), так і стандартні схеми лікування, зокрема WBRT та SRS. Кожен з варіантів такої терапії має свої переваги й обмеження. Так, за сучасними даними, застосування ІТК І покоління, які не проникають через ГЕБ, та WBRT з ХТ не покращують виживаності без прогресування (ВБП) і загальної виживаності (ЗВ) хворих із метастазами в головному мозку (J.J. Yang, 2017). T. Jiang та співавт. (2016) продемонстрували, що у пацієнтів з EGFR+ НДРЛ та метастазами в ЦНС поєднане використання ІТК та WBRT забезпечувало зіставну інтракраніальну і системну ВБП, але гіршу ЗВ порівняно з монотерапією ІТК І покоління.
C.L. Pechoux та співавт. (2016) визначили, що у пацієнтів після WBRT наявний високий ризик розвитку неврологічних ускладнень, які включають гостру енцефалопатію, сомноленцію, різноманітні нейрокогнітивні порушення, деменцію та ін. Так, отримання променевої терапії перед початком прийому осимертинібу (ІТК ІІІ покоління) не лише не сприяло подовженню ЗВ і ВБП, а й мало токсичний вплив на ЦНС (L. Xie, 2018; A.E. Dohm, 2022). Враховуючи вищезазначені дані, а також рекомендації різних міжнародних профільних медичних товариств, можна констатувати, що єдиним ефективним варіантом лікування метастазів у ЦНС при НДРЛ у пацієнтів з мутаціями EGFR та ALK є застосування таргетних препаратів, зокрема ІТК ІІІ покоління осимертинібу, який характеризується високою проникністю в ЦНС (M.A. Vogelbaum, 2022).
Відповідно до сучасних рекомендацій, варіантом лікування безсимптомних метастазів у головному мозку при НДРЛ є застосування ІТК І-ІІ поколінь. При наявності неврологічної симптоматики можна розглянути можливість додавання локальної терапії, зокрема SRS показана при розмірі ураження <20 см3, WBRT рекомендована при ураженні >20 см3 та мультифокальному ураженні (A. Bulbul, 2018). Схожі рекомендації і для ведення пацієнтів з ALK+ НДРЛ: за відсутності симптомів доцільно розпочинати лікування специфічними ALK-інгібіторами ІІ і ІІІ поколінь, тоді як променеву терапію використовувати під час прогресування пухлини або при появі неврологічних симптомів. Саме така стратегія лікування забезпечує найкращу якість життя хворих (S. Ceddia, 2021).
Таким чином, згідно з останніми даними, додавання WBRT не впливає на ЗВ пацієнтів з безсимптомними метастазами в ЦНС, асоціюється з затримкою початку системної терапії, а також чинить токсичний вплив на когнітивне здоров’я.
.jpg) Завідувачка відділення хіміотерапії № 1 КНП КОР «Київський міський клінічний онкологічний центр», доцент кафедри онкології Національного університету охорони здоров’я України імені П.Л. Шупика, кандидат медичних наук Ольга Володимирівна Пономарьова розповіла про основні переваги застосування ІТК ІІІ покоління при терапії метастатичного НДРЛ, фокусуючи увагу на здатності препаратів цієї групи проникати через ГЕБ.
Завідувачка відділення хіміотерапії № 1 КНП КОР «Київський міський клінічний онкологічний центр», доцент кафедри онкології Національного університету охорони здоров’я України імені П.Л. Шупика, кандидат медичних наук Ольга Володимирівна Пономарьова розповіла про основні переваги застосування ІТК ІІІ покоління при терапії метастатичного НДРЛ, фокусуючи увагу на здатності препаратів цієї групи проникати через ГЕБ.
– Сучасні стратегії лікування НДРЛ з метастазами в ЦНС значною мірою визначаються статусом мутації та безпосередньою кількістю цих метастазів (G. Tsakonas, 2017). Так, за наявності 1-3 метастазів, мутацій EGFR або ALK та відсутності позачерепних уражень рекомендованою стратегією лікування при НДРЛ є застосування ІТК та, за можливості, проведення хірургічного втручання. При наявності понад 3 метастазів у ЦНС крім мутацій EGFR або ALK показане використання лише ІТК, а також затримка/пропуск WBRT. У разі наявності 1-3 метастазів у ЦНС та відсутності у пацієнта клінічно значущих мутацій рекомендоване застосування ХТ або локальне лікування ЦНС за показаннями. При наявності більше 3 метастазів у ЦНС або екстракраніальних уражень рекомендована імунотерапія, затримка/пропуск WBRT.
Загальновідомо, що проникність ІТК через ГЕБ є важливим аспектом їх фармакокінетики й ефективності лікування метастазів у ЦНС. ГЕБ є комплексною системою захисту, що представлена клітинами ендотелію, базальної мембрани й астроцитів, які «співпрацюють» для забезпечення високої селективності проникності різних речовин до мозку. Проникність ГЕБ безпосередньо залежить від ліпофільності речовини та щільних міжклітинних контактів (W.K. Oldendorf, 1974; R. Kaliszan, 1996); молекулярної маси речовини та розмірів молекул, а також ефлюкс-системи, яка забезпечує зменшення концентрації лікарських препаратів у ЦНС (W.K. Oldendorf, 1974; R. Kaliszan, 1996).
Одним із важливих механізмів, які регулюють проникність ГЕБ, є ефлюкс-система, яка включає спеціальні насоси, що забезпечують активний транспорт різних речовин через клітинні мембрани. Основні ефлюкс-системи в ГЕБ мають здатність виводити різні речовини з мозку у кров, зменшуючи їх концентрацію в мозковій тканині. Це також стосується і лікарських засобів. Сучасні дані демонструють, що такі препарати, як ерлотиніб і гефітиніб, хоча і мають здатність проникати через ГЕБ, але одразу виштовхуються з клітин ЦНС, що забезпечується ефлюкс-системою.
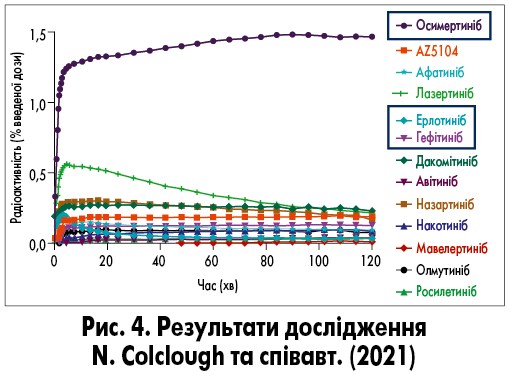 Перевагою препарату осимертиніб є його здатність блокувати ефлюкс-системи в ГЕБ шляхом пригнічення Р-глікопротеїну. Це забезпечує терапевтичну концентрацію лікарського засобу в ЦНС – так званий ефект губки – ЦНС, немов губка, насичується речовинами крові, які згодом не виштовхуються назад у кров, а залишаються в головному мозку. При цьому осимертиніб швидко досягає максимальної концентрації в ЦНС та рівномірно розподіляється між усіма відділами головного мозку (N. Colclough, 2021; K. Vishwanathan, 2018; рис. 4). Що це дає пацієнту? У 2019 р. S. Ekman та співавт. показали, що на тлі високої концентрації осимертинібу в ЦНС відбувалося значне зменшення кількості первинних метастатичних вогнищ у різних відділах головного мозку (рис. 5).
Перевагою препарату осимертиніб є його здатність блокувати ефлюкс-системи в ГЕБ шляхом пригнічення Р-глікопротеїну. Це забезпечує терапевтичну концентрацію лікарського засобу в ЦНС – так званий ефект губки – ЦНС, немов губка, насичується речовинами крові, які згодом не виштовхуються назад у кров, а залишаються в головному мозку. При цьому осимертиніб швидко досягає максимальної концентрації в ЦНС та рівномірно розподіляється між усіма відділами головного мозку (N. Colclough, 2021; K. Vishwanathan, 2018; рис. 4). Що це дає пацієнту? У 2019 р. S. Ekman та співавт. показали, що на тлі високої концентрації осимертинібу в ЦНС відбувалося значне зменшення кількості первинних метастатичних вогнищ у різних відділах головного мозку (рис. 5).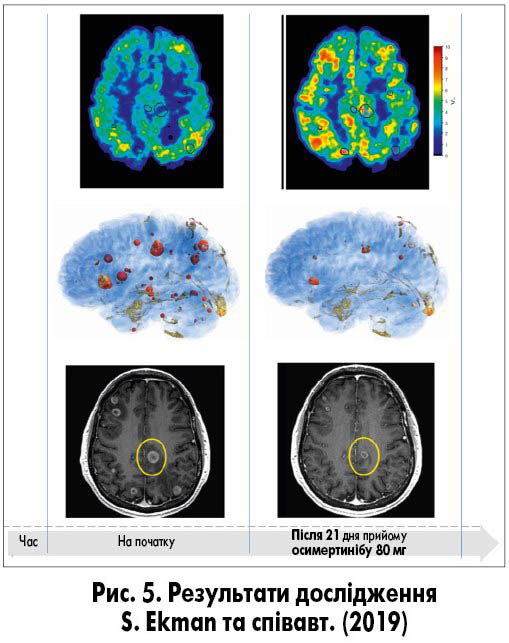
Висока концентрація осимертинібу в ЦНС відображається на клінічних результатах лікування більш широкої популяції пацієнтів з метастатичним НДРЛ. Так, у дослідженні FLAURA частота загальної (в тому числі і повної) відповіді у ЦНС у групі осимертинібу була вищою та склала 64%, тоді як у групі ІТК І покоління – лише 45% без випадків повної відповіді на терапію (рис. 6). Одночасно треба зазначити, що в ході дослідження кількість пацієнтів з ураженням ЦНС зменшувалася при застосуванні осимертинібу та зросла при використанні ІТК І покоління порівняно з початковим рівнем (T. Reungwetwattana, 2018). Це також підтверджувалося зниженням відносного ризику прогресування у ЦНС в групі осимертинібу на 52% порівняно з терапією ІТК І покоління (95% довірчий інтервал 0,26-0,86; р=0,014; рис. 7).
Якщо розглядати дані клінічної практики, то у дослідженні FLOURISH також було продемонстровано ефективність осимертинібу щодо ВБП у пацієнтів з метастатичним НДРЛ на рівні 77-78% протягом 12 міс незалежно від наявності чи відсутності метастазів у ЦНС на початку лікування. Крім вищезазначеного треба відмітити, що в клінічному дослідженні ADAURA, де вивчали ефективність застосування осимертинібу в ад’ювантному режимі у пацієнтів з EGFR+ НДРЛ на більш ранніх стадіях (ІІ-ІІІА стадії), 97% хворих не мали рецидиву у ЦНС протягом 3 років після радикального втручання.
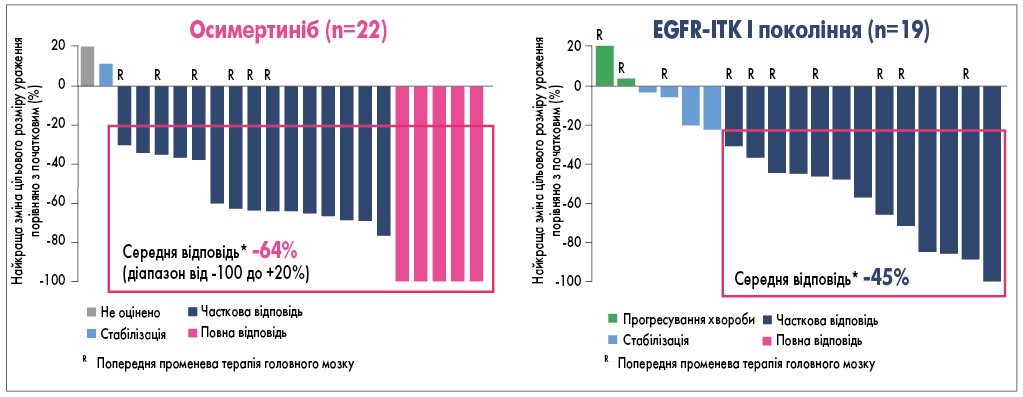 Рис. 6. Результати дослідження FLAURA: оцінка відповіді в ЦНС
Рис. 6. Результати дослідження FLAURA: оцінка відповіді в ЦНС
FLAURA data cut-off: June 12, 2017.
*Найкращою зміною цільового розміру ураження у відсотках було максимальне зменшення порівняно з початковим або мінімальне збільшення порівняно з початковим розміром за відсутності зменшення. Уся попередня променева терапія проведена менш ніж за 6 міс до рандомізації. Reungwetwattana T. et al. J Clin Oncol. 2018; 36: 3290-3297.
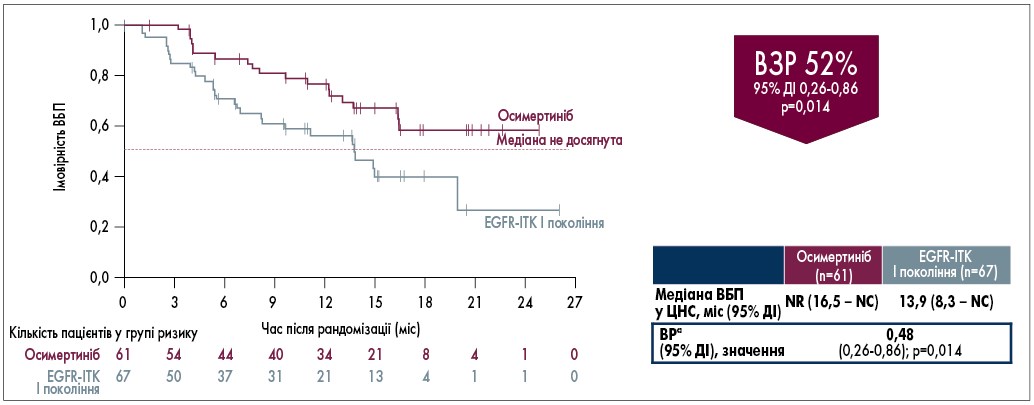 Рис. 7. Результати дослідження FLAURA: зниження ризику прогресування у ЦНС у пацієнтів з EGFR+ НДРЛ
Рис. 7. Результати дослідження FLAURA: зниження ризику прогресування у ЦНС у пацієнтів з EGFR+ НДРЛ
ВЗР – відносне зниження ризику; ДI – довірчий інтервал; ВР – відносний ризик; NC – не обчислюється; NR – не досягнуто.
a ВР було розраховано за моделлю пропорційних ризиків Кокса з фактором лікування; ДІ розраховували з використанням правдоподібності профілю. ВР <1 засвідчує перевагу осимертинібу.
1. Reungwetwattana T. et al. J Clin Oncol. 2018; 36: 3290-3297; 2.Vansteenkiste J. et al. Presented at: European Society for Medical Oncology (ESMO) Asia Conference; November 17-19, 2017; Singapore. Ann Oncol. 2017; 28 (suppl). Abs LBA5.
Клінічний випадок 4
Пацієнтка А., НДРЛ, метастази в ЦНС.
У лютому 2020 р. хворій проведена операція – передня лобектомія лівої легені, лімфодисекція з подальшим призначенням 4 циклів ад’ювантної поліхіміотерапії (вінрелбін + цисплатин) з березня по червень 2020 р.
У грудні 2019 р. під час профілактичного огляду виявлено новоутворення в лівій легені, після чого вперше звернулася на консультацію до онкоторакального хірурга. Рекомендовано КТ органів грудної порожнини, на якій виявлена пухлина лівої легені з ураженням лімфатичних вузлів середостіння. На підставі отриманих даних пацієнтці встановлено діагноз аденокарцинома лівої легені pT1bN2M0, ІІІА стадія з метастазуванням в лімфатичні вузли середостіння.
У вересні 2020 р. зафіксовано прогресування захворювання, на КТ виявлені нові метастатичні вузли 0,6-1,2 см у нижніх частках обох легень. Відповідно до даних МРТ метастази в ЦНС не виявлені. Хворій призначено 6 циклів поліхіміотерапії (цисплатин + пеметрексед) із вересня по січень 2021 р. Після проведення КТ-контролю виявлено, що діаметр уражень збільшився на +15, нових вогнищ не зафіксовано (стабілізація захворювання).
Після стабілізації захворювання з січня по квітень 2021 р. хворій призначена таргетна терапія ІТК І покоління ерлотинібом. У квітні 2021 р. хвора почала скаржитися на головний біль і нудоту. Проведено МРТ, виявлені численні внутрішньочерепні метастази. Відповідно до даних КТ діаметр уражень у легенях зменшився на 35% (часткова відповідь), нових вогнищ не виявлено.
Після прогресування захворювання у червні 2021 р. хворій було призначено таргетний препарат осимертиніб (Тагріссо) у дозі 80 мг. За даними контрольної КТ діаметр уражень у легенях зменшився на 42% (часткова відповідь); МРТ з контрастуванням виявила зменшення внутрішньочерепних метастазів на 75% (часткова відповідь).
У вересні 2022 р. під час контрольної МРТ ознаки внутрішньочерепних метастазів були відсутні – повна відповідь; на КТ білатеральні метастатичні вузли у легені зменшені.
Таким чином, ЦНС є поширеною локалізацією метастазів при НДРЛ. Осимертиніб – лікарський засіб, який демонструє високу ефективність у лікуванні пацієнтів з EGFR+ НДРЛ. Результати сучасних досліджень, таких як FLAURA та FLOURISH, підтвердили його високу ефективність як для лікування, так і профілактики метастазів у ЦНС у пацієнтів без початкового метастатичного ураження.
Підготувала Анна Сочнєва
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 2 (81) 2023 р.




