30 листопада, 2023
Неденатурований колаген II типу (UC-II®, Меркана®): вплив на здоров’я та рухливість суглобів
Повсякденна життєдіяльність потребує різноманітної фізичної активності, що створює змінне навантаження на суглоби. Механічні перевантаження, анатомічні недоліки або нестабільність суглоба призводять до появи локального болю та скутості, які обмежують гнучкість і рухливість суглобів у здорових людей, навіть без діагностованих ревматичних захворювань [1]. Дослідження показали, що навіть незначна втрата діапазону рухів коліна (ДРК) може зумовлювати зміну моделей ходи, що призводить до труднощів під час бігу та стрибків [2, 3]. ДРК є важливим показником як для спортсменів, так і для звичайних активних людей. Втручання, спрямовані на покращення ДРК, як було показано, полегшують стан суглобів, збільшують рухливість і зберігають функцію.
Остеоартрит (ОА) є найпоширенішою формою артриту, що характеризується поступовим руйнуванням суглобового хряща аж до підлеглої кістки. Профілактичні дії, до яких входять захист суглобів шляхом фізичної активності, дієти, прийому дієтичних добавок, є важливим чинником стримування прогресування ОА. Неденатурований колаген є однією з таких дієтичних добавок, яку можна споживати людям із дискомфортом у суглобах, щоб запобігти прогресуванню обмеження рухливості та розвитку ОА.
Попередні дослідження показали, що додавання неденатурованого колагену до раціону харчування може покращити рухливість суглобів як у пацієнтів з ОА, так і в здорових осіб зі скаргами на суглобовий дискомфорт, пов’язаний із навантаженнями [4, 5]. Зокрема, в плацебо-контрольованому дослідженні Lugo та співавт. [5] спостерігали покращення розгинання колінного суглоба при споживанні неденатурованого колагену в здорових людей, які мали досвід болю в суглобах під час тредміл-ходьби. Дослідницька група Schon і співавт. підтвердила тест «крок униз однією ногою» (SLSD) як надійну модель для відбору здорових суб’єктів із досвідом суглобового дискомфорту, пов’язаного з навантаженням [6]. Метою нового дослідження Schon і співавт. було оцінити вплив добавки неденатурованого колагену на гнучкість суглобів у здорових осіб, які відчували біль під час тесту SLSD [7].
Матеріали та методи
Проспективне багатоцентрове рандомізоване подвійне сліпе плацебо-контрольоване дослідження проводилося в BioTeSys GmbH та в Інституті спорту й руху Штутгартського університету з вересня 2019 року по січень 2021 року [7]. У дослідженні брали участь здорові чоловіки та жінки віком 20-55 років з індексом маси тіла від 19 до 29,9 кг/м2, які займалися спортом не менш як 2 рази на тиждень і повідомляли про оборотний дискомфорт у колінних суглобах під час або відразу після фізичної активності протягом принаймні 3 міс. Для подальшого відбору учасників під час скринінгового візиту проводили тест SLSD [11, 12].
Під час тесту SLSD суб’єкти мали зробити крок уперед і вниз із платформи з регульованою висотою. Після торкання підлоги п’ятою ногу слід повернути назад на платформу до повного розгинання коліна. Частота повторень задавалася метрономом. Якщо принаймні через 10 хв біль у суглобах не виникав, стрес-тест припиняли. Лише особи, які відчували біль рівня 5 балів за 11-бальною шкалою Лайкерта під час виконання тесту SLSD (від 30 до 150 кроків), відбиралися для рандомізації.
Учасників розподіляли в групи для споживання дієтичної добавки (40 мг неденатурованого колагену II типу (UC-II®) на день) або плацебо (препарат, що містить лише допоміжну речовину – мікрокристалічну целюлозу) в ідентичних капсулах по 1 капсулі щодня ввечері перед сном. Тривалість дослідження становила 24 тиж (6 міс) із загальною кількістю 7 візитів із 4-тижневими інтервалами. Під час кожного візиту вимірювали ДРК за допомогою цифрового гоніометра. Оцінку згинання та розгинання здійснювали на нозі, в якій учасники зазвичай відчували інтенсивніший біль після фізичної активності (цільове коліно).
Для аналізу статистичних відмінностей між групами використовували коваріаційний аналіз (ANCOVA). Зміни протягом часу в досліджуваній групі оцінювали за допомогою дисперсійного аналізу (ANOVA) чи тесту Фрідмана. Різницю вважали статистично значущою при p<0,05.
Результати
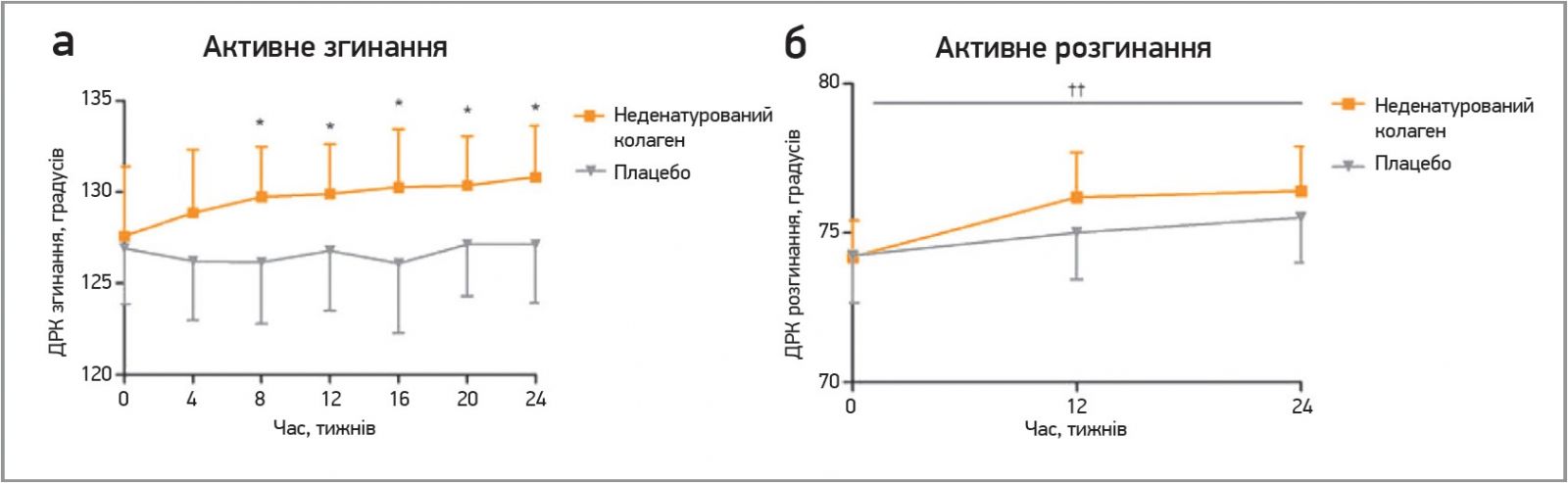
96 осіб, які пройшли скринінг, відповідали критеріям включення та були рандомізовані до групи плацебо (n=48) або неденатурованого колагену (n=48). Між групами не спостерігалося суттєвих відмінностей за вихідними характеристиками. За таким параметром ДРК, як активне згинання, суттєвих відмінностей між досліджуваними групами на початку дослідження не спостерігалося (p>0,05). Наприкінці дослідження група, яка отримувала неденатурований колаген, показала статистично значуще середнє збільшення кута згинання коліна 3,23° порівняно із середнім збільшенням на 0,21° у групі плацебо (95% довірчий інтервал (ДІ) 0,44-6,02 у дослідній групі; 95% ДІ від -1,67 до 2,08 у групі плацебо; p=0,0250). Значна різниця між групами неденатурованого колагену та плацебо в активному згинанні спостерігалася вже на 8-му тижні прийому добавки та продовжувала значно покращуватися протягом дослідження (рис. 1, а).
Рис. 1. Розподіл результатів вимірювань діапазону рухів колінного суглоба: a) активного згинання; б) активного розгинання в групі неденатурованого колагену порівняно з групою плацебо протягом дослідження
Примітки: * p<0,05; значуща різниця між втручаннями; †† p<0,01; значуща різниця з часом у групі вживання неденатурованого колагену.
У жінок спостерігалося статистично значуще збільшення кута згинання коліна на 4,79° у групі неденатурованого колагену проти незначного зниження на -0,32° у групі плацебо. У чоловіків спостерігалося невелике статистично незначуще збільшення згинання в обох групах наприкінці дослідження. Аналіз за віком показав, що в підгрупі віком понад 35 років учасники в групі неденатурованого колагену продемонстрували значне збільшення згинання колінного суглоба порівняно з групою плацебо (неденатурований колаген, n=19: +6,79°, 95% ДІ 2,38-11,20; плацебо, n=27, +0,30°, 95% ДІ від -2,60 до 3,19; p=0,0092). У підгрупі 20-35 років спостерігалося незначне та статистично незначуще збільшення ДРК наприкінці дослідження в обох групах.
Такий параметр ДРК, як розгинання, оцінювали під час першого (вихідний рівень), четвертого (12 тиж) і сьомого (24 тиж) візитів. Вихідні значення були порівнянними в обох досліджуваних групах (p>0,05). Після 24 тиж прийому добавок спостерігалося невелике збільшення розгинання на 2,21° у групі неденатурованого колагену та незначне збільшення на 1,27° у групі плацебо. Аналіз змін порівняно з початковим рівнем (p<0,01) і з часом (p=0,0061) показав значуще збільшення в групі неденатурованого колагену. У групі плацебо такої зміни не спостерігалося (p>0,05; рис. 1, б).
Обговорення та висновки
Гнучкість суглобів має велике значення в повсякденному житті спортсменів, а також активних людей. Навантаження на колінні суглоби під час фізичної активності може призвести до імунологічних реакцій, які віддзеркалюють ті, котрі спостерігаються при артритних захворюваннях, що в підсумку може спричинити зменшення гнучкості колінного суглоба [8]. Подібним чином було показано, що старіння обмежує ДРК через зношування суглобів від щоденної активності. Згідно з даними Центрів із контролю та профілактики захворювань США (CDC) середня доросла людина втрачає 1° згинання та розгинання колінного суглоба за кожні 10 років життя. Цю втрату гнучкості з віком пояснюють зниженням активності та зменшенням рухливості суглобів [9]. Тому відновлення та підтримка ДРК є критично важливими для підтримки здоров’я суглобів.
ДРК зазвичай використовують як критерій ефективності втручань у клінічних дослідженнях у людей з ОА колінного суглоба, ревматоїдним артритом і в спортсменів. У дослідженні Schon і співавт. [7] спостерігалося значне покращення згинання колінного суглоба в активних здорових людей, які вживали добавку неденатурованого колагену. Збільшення діапазону згинання колінного суглоба спостерігалося вже через 8 тиж прийому добавки, і воно продовжувало покращуватися, досягнувши наприкінці дослідження показника 3,23°. Цей результат свідчить про те, що добавка неденатурованого колагену може покращити згинання колінних суглобів у здорових осіб, які мають ризик розвитку захворювань суглобів.
У жінок спостерігалося більше покращення згинання у відповідь на додавання неденатурованого колагену, ніж у чоловіків. Цю гендерну різницю в ефективності можна пояснити тим фактом, що жінки із захворюваннями суглобів демонструють нижчий ДРК [10], через що зростає шанс побачити кращі результати від уживання добавки неденатурованого колагену в жіночій популяції. Особи віком 35 років і старше зазнали більшого покращення активного згинання коліна у відповідь на добавку неденатурованого колагену, ніж це спостерігалося в осіб віком від 20 до 35 років. Одне з можливих пояснень полягає в тому, що літні люди мають очікувано нижчий ДРК на початку порівняно з молодшими особами. Отже, літні дорослі можуть отримати більшу користь від добавки неденатурованого колагену [7].
У попередніх дослідженнях було показано, що суб’єкти з ОА, а також із дискомфортом у суглобах, пов’язаним із фізичною активністю, можуть отримати користь від прийому UC-II® шляхом підвищення рухливості суглобів [4, 5], але точний механізм дії досі не повністю з’ясований. Згідно з дослідженнями на тваринах та in vitro передбачається, що під час фізичних вправ активуються деякі процеси, які також відбуваються при ОА, наприклад розподіл прозапальних цитокінів. UC-II® зменшує запалення суглобів, діючи через пов’язану з кишечником лімфоїдну тканину. Було показано, що він стимулює імунні клітини (Т-клітини) виробляти протизапальні цитокіни в суглобах [11]. Цей механізм допомагає зменшити запальні процеси та стимулювати відновлення хряща, що є можливим способом дії досліджуваного продукту.
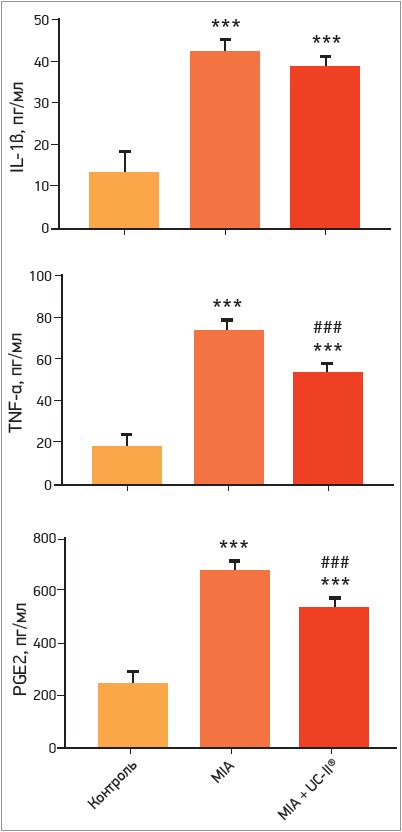
Зокрема, дослідження Orhan і співавт. [12] було проведено для перевірки впливу UC-II® на маркери запалення суглобів у тваринній моделі ОА, спричиненого монойодацетатом (MIA). Запалення хряща та синовіальної оболонки ініціює розвиток ОА, а в міру прогресування захворювання багато факторів запалення посилюються ще більше. У цьому дослідженні UC-II® ефективно зменшувала симптоми артриту, мікроструктурні деформації колінного суглоба та пригнічувала деякі катаболічні сигнальні шляхи в щурів із MIA-індукованим ОА. Зокрема, UC-II® пригнічувала фактори запалення, пов’язані з сигнальним шляхом NF-κB, та інші медіатори запалення. Сироваткові рівні прозапальних інтерлейкінів (IL-1β та IL-6), фактора некрозу пухлини-α (TNF-α), хрящового олігомерного матриксного білка COMP, С-реактивного білка були істотно знижені в групі, учасники якої отримували UC-II® (рис. 2). Крім того, після додавання UC-II® були ефективно пригнічені сигнальні шляхи деградації суглобового хряща: продукція PGE2, експресія IL-1β, IL-6, TNF-a, COX-2, MCP-1, NF-κB, MMP-3, RANKL достовірно знизилися в хрящовій тканині (р<0,001) [12].
Рис. 2. Вплив прийому неденатурованого колагену типу II (UC-II®) на сироваткові рівні IL-1β, простагландину Е2 та TNF-α у тваринній моделі ОА, спричиненого МІА
Примітки: *** p<0,001 порівняно з контрольною групою; ††† p<0,001 порівняно з групою MIA; PGE2 – простагландин Е2.
У підсумку дані клінічних досліджень [4, 5, 7] підтверджують те, що неденатурований колаген є харчовим інгредієнтом, який позитивно впливає на функцію колінного суглоба, зокрема покращує діапазон згинання коліна, що може мати профілактичне значення для людей групи ризику розвитку захворювань суглобів.
Експертна думка українських фахівців
 Олег Борисович Яременко, доктор медичних наук, професор, віцепрезидент Асоціації ревматологів України, завідувач кафедри внутрішньої медицини № 3 Національного медичного університету ім. О.О. Богомольця (м. Київ):
Олег Борисович Яременко, доктор медичних наук, професор, віцепрезидент Асоціації ревматологів України, завідувач кафедри внутрішньої медицини № 3 Національного медичного університету ім. О.О. Богомольця (м. Київ):
– До перспективних напрямів менеджменту ОА відносять методи тканинної інженерії, препарати рослинного походження, а також препарати колагену та його похідних.
Колаген становить 50-70% сухого залишку суглобового хряща й відповідає за його міцність і витривалість до навантажень. Наразі для лікування ОА використовують повністю чи частково денатуровані форми колагену (гідролізати) та UC-II®. Гідролізати колагену являють собою лише «будівельний матеріал», тобто джерело амінокислот і пептидів для синтезу колагену. Натомість неденатурований колаген реалізує свою дію через каскад імуноопосередкованих реакцій, активуючи процес відновлення хрящової тканини суглобів, що було продемонстровано в низці контрольованих експериментальних і клінічних досліджень.
На цьому механізмі заснована дія нативного колагену, який представлений на фармацевтичному ринку України хондропротектором Меркана®, що має у своєму складі запатентований UC-II®. За перорального прийому UC-ІІ® із порожнини кишечнику захоплюється дендритними клітинами, розташованими в пеєрових бляшках тонкого кишечнику, оскільки нативний колаген не всмоктується в кров. Дендритна клітина встановлює, що цей антиген є безпечним для організму (оральна толерантність), і перетворює неспеціалізовані лімфоцити на «навчені», або специфічні, Т-регулятори. Ці клітини дозрівають у лімфатичних вузлах кишечнику, потрапляють у системний кровоток і мають здатність продукувати синтез двох типів медіаторів: інтерлейкіну-10 як головного протизапального цитокіна та трансформувального фактора росту-β, який є стимулятором регенеративних процесів у суглобовому хрящі.
Відповідно, Меркана® виявляє одразу два ефекти – протизапальну дію та відновлення хряща, що забезпечує сповільнення прогресування захворювання й покращення функції суглобів.
Метою нашого дослідження (Яременко О.Б., Федьков Д.Л., 2021) було оцінити ефективність і переносимість UC-II® (Меркана®), а також визначити його вплив на метаболізм хрящової тканини при монотерапії у хворих з ОА колінних суглобів. У дослідження були включені 30 хворих на ОА із залученням колінних суглобів, які мали на момент початку дослідження ІІ чи ІІІ рентгенологічну стадію за Kellgren-Lawrence. Крім колінних суглобів, залучалися дрібні суглоби кистей, суглоби стопи, кульшові суглоби, переважала поліартритична форма. Третина хворих мала вузликову форму ОА. Вираженість клінічної симптоматики ОА була значною, про що, зокрема, свідчать середні величини оцінки болю за візуальною аналоговою шкалою лікарем і хворим – більш ніж 50 мм.
Усі включені хворі приймали UC-II® (Меркана®) по 1 капсулі (40 мг) 1 раз на добу протягом 6 міс. За потреби дозволялося продовження прийому НПЗП у звичних для пацієнта дозах протягом усього періоду проведення дослідження. У результаті було встановлено поліпшення всіх клінічних показників уже на 4-му тижні лікування – індекси Лекена та WOMAC (опитувальник вираженості ОА університетів Західного Онтаріо та Мак-Мастер) знизилися на 5,3 та 9,1% відповідно. На момент завершення дослідження поліпшення за індексом Лекена становило 25%, а за індексом WOMAC – 33,1% від вихідного значення. Позитивні клінічні зміни супроводжувалися вірогідним збільшенням сумарного значення товщини суглобового хряща за даними ультразвукового дослідження: за 6 міс потовщення хряща становило 5,6% для правого та 17,6% – для лівого колінного суглобів. Принципову можливість репарації, збільшення товщини суглобового хряща при лікуванні SYSADOA відзначали і в інших дослідженнях.
Отже, UC-II® (Меркана®) ефективний щодо поліпшення клінічних проявів і метаболічних розладів хряща при лікуванні хворих на ОА з ураженням колінних суглобів. Динаміка клінічних та інструментальних показників під впливом лікування свідчить на користь тривалого застосування UC-II® – строком не менш ніж 6 міс.
 Керівник Центру ревматології Клінічної лікарні «Феофанія» Державного управління справами (м. Київ), доктор медичних наук, професор Ірина Юріївна Головач:
Керівник Центру ревматології Клінічної лікарні «Феофанія» Державного управління справами (м. Київ), доктор медичних наук, професор Ірина Юріївна Головач:
– Перебіг ОА може мати вигляд багатьох фенотипів, які суттєво впливають на швидкість прогресування захворювання, тяжкість симптомів, відповідь на лікування, прогноз тощо. Наразі розрізняють 13 фенотипів ОА, кожен з яких тією чи іншою мірі пов’язаний із метаболічними порушеннями. Крім того, як окрему форму виділяють асоційований із метаболічним синдромом метаболічний фенотип. У його основі лежить концепція порушення системної регуляції суглобових тканин, переважно під впливом прозапальних цитокінів. Механізм формування метаболічного фенотипу ОА є багатокомпонентним та включає ожиріння, цукровий діабет 2 типу, дисліпідемію, артеріальну гіпертензію. Ожиріння призводить до механічного перевантаження суглобів, що супроводжується розвитком механозапалення з одного боку, а з іншого – зростанням концентрації низки прозапальних цитокінів, які сприяють розвитку хронічного системного запалення. За цукрового діабету 2 типу відбувається накопичення продуктів глікування, які порушують метаболізм суглобових клітин. Дисліпідемія та зростання концентрації окислених ліпопротеїнів низької щільності чинять негативний вплив на метаболічну активність хондроцитів. Артеріальна гіпертензія та атеросклероз зумовлюють розвиток субхондральної ішемії та порушення живлення хряща. Кожен із зазначених факторів збільшує ризик розвитку ОА, а також хронічного болю при ОА.
Таким чином, у лікуванні пацієнтів з метаболічним типом ОА велике значення має корекція обмінних порушень. Не менш важливим є застосування якісних хондропротекторів. Зазвичай із цією метою застосовують симптоматичні препарати сповільненої дії (SYSADOA): глюкозаміну сульфат, хондроїтинсульфат, неомилювані сполуки олії авокадо, неденатурований колаген ІІ типу (UC-ІІ®) та ін. За даними низки досліджень, у разі тривалого прийому UC-ІІ® продемонстрував кращі за глюкозамін із хондроїтином результати щодо зменшення болю при ОА, причому клінічний ефект суттєво покращувався із часом. Слід зазначити, що на початку застосування найвираженішою знеболювальною дією характеризувались екстракти босвелії та куркуми. Екстракт босвелії, який протягом тисячоліть широко використовувався в медицині Індії та Китаю, здатен пригнічувати активність 5-ліпооксигенази та зменшувати запалення за рахунок інгібування утворення лейкотрієнів. Куркумін знижує рівень прозапальних ферментів, а також пригнічує міоген-активовані протеїнкінази.
Широке застосування екстрактів куркуми та босвелії тривалий час обмежувалося їхньою хімічною нестабільністю в зовнішньому середовищі, низькою розчинністю у воді, незначною біодоступністю та швидкою елімінацією з організму людини. Створений за новітньою технологією NovaSOL® рідкий екстракт куркуми та босвелії має значно вищу (у 185 разів для куркуміну та у 56 для AKBA) біодоступність порівняно з нативними порошкоподібними екстрактами. Поєднання запатентованого рідкого екстракту куркуми та босвелії з UC-ІІ® та вітаміном D реалізоване в хондропротекторному комплексі Меркана Актив. Цей комплекс забезпечує швидке та тривале знеболення, ефективно усуває запалення, покращуючи рухливість суглобів.
Список літератури знаходиться в редакції.
Підготував Ігор Петренко
Медична газета «Здоров’я України 21 сторіччя» № 19/1 (556), 2023 р