17 липня, 2024
Міжнародний конгрес із серцевої недостатності – 2024: важливість упровадження результатів новітніх досліджень до клінічної практики
 Серцева недостатність (СН) – це загрозливий для життя синдром, на який страждають >64 млн людей у всьому світі (Savarese G. et al., 2023). 1 із 3 пацієнтів із СН помирає протягом 1-го року після госпіталізації, а 50-75% – упродовж 5 років після неї. Цьогоріч конгрес із СН – провідна світова подія, що охоплює увесь спектр цього патологічного стану (від профілактики до діагностики та лікування), – відбувався з 11 по 14 травня в Лісабонському конгрес-центрі в Португалії. Організатор щорічного заходу – Асоціація серцевої недостатності (HFA) Європейського товариства кардіологів (ESC), місія котрої полягає у поліпшенні якості та тривалості життя хворих із СН завдяки удосконаленню профілактичних, діагностичних, лікувальних стратегій.
Серцева недостатність (СН) – це загрозливий для життя синдром, на який страждають >64 млн людей у всьому світі (Savarese G. et al., 2023). 1 із 3 пацієнтів із СН помирає протягом 1-го року після госпіталізації, а 50-75% – упродовж 5 років після неї. Цьогоріч конгрес із СН – провідна світова подія, що охоплює увесь спектр цього патологічного стану (від профілактики до діагностики та лікування), – відбувався з 11 по 14 травня в Лісабонському конгрес-центрі в Португалії. Організатор щорічного заходу – Асоціація серцевої недостатності (HFA) Європейського товариства кардіологів (ESC), місія котрої полягає у поліпшенні якості та тривалості життя хворих із СН завдяки удосконаленню профілактичних, діагностичних, лікувальних стратегій.
До уваги читачів пропонуємо огляд декількох найцікавіших досліджень, результати яких уперше були представлені на цьому конгресі.
Вакцинація проти COVID‑19 може подовжити життя пацієнтів із СН
Зв’язок між вакцинацією проти COVID‑19 і клінічними наслідками в хворих із СН вивчали в своїй роботі науковці Університетського медичного коледжу та лікарні Ільсан (м. Сеул, Корея) Кьон Хьон Чун і співавт.
 Передумовою для проведення цього дослідження стало те, що вакцинація проти COVID‑19 доведено знижує частоту серцево-судинної патології, пов’язаної з цим захворюванням. Хоча ефективність вакцини широко вивчалася в загальній популяції, її переваги в пацієнтів із СН усе ще недостатньо вивчені. Науковці проаналізували дані когорти пацієнтів із COVID‑19 та базу даних Корейської національної служби медичного страхування. В дорослих хворих із СН вивчали такі клінічні результати, як госпіталізація щодо СН, серцево-судинні події (ССП) та критичні стани внаслідок COVID‑19: перебування у відділенні інтенсивної терапії або необхідність у проведенні штучної вентиляції легень. Вакциновані пацієнти були визначені як ті, хто отримав ≥2 дози вакцини проти COVID‑19, а невакциновані – як ті, хто взагалі не отримав жодної дози чи лише 1 дозу вакцини.
Передумовою для проведення цього дослідження стало те, що вакцинація проти COVID‑19 доведено знижує частоту серцево-судинної патології, пов’язаної з цим захворюванням. Хоча ефективність вакцини широко вивчалася в загальній популяції, її переваги в пацієнтів із СН усе ще недостатньо вивчені. Науковці проаналізували дані когорти пацієнтів із COVID‑19 та базу даних Корейської національної служби медичного страхування. В дорослих хворих із СН вивчали такі клінічні результати, як госпіталізація щодо СН, серцево-судинні події (ССП) та критичні стани внаслідок COVID‑19: перебування у відділенні інтенсивної терапії або необхідність у проведенні штучної вентиляції легень. Вакциновані пацієнти були визначені як ті, хто отримав ≥2 дози вакцини проти COVID‑19, а невакциновані – як ті, хто взагалі не отримав жодної дози чи лише 1 дозу вакцини.
Загалом до дослідження було включено 651 127 осіб із СН (середній вік становив 69,5 року; 50% складали чоловіки). Із загальної популяції 112 693 особи (17,3%) належали до групи невакцинованих осіб із СН, а 538 434 (82,7%) – до групи вакцинованих хворих із СН. Протягом середнього періоду спостереження (6 міс) у вакцинованих пацієнтів спостерігався значно нижчий ризик госпіталізації щодо СН порівняно з невакцинованими (відносний ризик (ВР) 0,68; 95% довірчий інтервал (ДІ) 0,66-0,7; p<0,0001). Також вакцинація знижувала ризик інфікування COVID‑19 (ВР 0,73; 95% ДІ 0,66-0,8) та критичного стану, обумовленого COVID‑19 (ВР 0,27; 95% ДІ 0,19-0,37). Що стосується інших ССП, то було встановлено, що вакцинація асоціювалася зі значно нижчим ризиком інсульту, інфаркту міокарда, міокардиту / перикардиту та венозної тромбоемболії (за всіма показниками p<0,0001).
Отже, цей ретроспективний аналіз свідчить про те, що вакцинація проти COVID‑19 у пацієнтів із СН не лише знижує ризик інфікування COVID‑19, а й зменшує ризик ССП, включаючи погіршення СН.
Затримка із проведенням ехокардіографії та встановленням діагнозу пов’язана з несприятливими наслідками за підозри СН
 Провідна фахівчиня Університетської лікарні Св. Георгія (м. Лондон, Сполучене Королівство Великої Британії та Північної Ірландії), керівниця напряму СН Товариства з питань інсульту та інфаркту Південно-Західного Лондону Ліза Андерсон представила доповідь «Підозра на СН de novo в амбулаторних умовах: високі показники смертності та захворюваності (REVOLUTION HF)».
Провідна фахівчиня Університетської лікарні Св. Георгія (м. Лондон, Сполучене Королівство Великої Британії та Північної Ірландії), керівниця напряму СН Товариства з питань інсульту та інфаркту Південно-Західного Лондону Ліза Андерсон представила доповідь «Підозра на СН de novo в амбулаторних умовах: високі показники смертності та захворюваності (REVOLUTION HF)».
Для зниження захворюваності та смертності в пацієнтів із СН de novo необхідними є швидке встановлення діагнозу і призначення відповідного лікування. Однак початок медикаментозної терапії, що базується на сучасних настановах, часто відтерміновується до проведення ехокардіографії та отримання фахового висновку за його результатами. В консенсусній заяві HFA ESC (2023) пропонується використовувати рівень NT‑proBNP (N‑кінцевий фрагмент попередника мозкового натрійуретичного пептиду) на додаток до клінічних ознак СН як підтверджувальний діагностичний тест.
Для визначення профілю ризику хворих із підозрою на СН de novo було проведено дослідження «випадок – контроль» з використанням шведської загальнонаціональної бази медичних даних і записів про причини смерті пацієнтів у період із 2015 по 2020 рік. До випробування залучили 5942 хворих, які звернулися по амбулаторну допомогу з ознаками СН (периферичні набряки) та/або симптомами СН (задишка), а також із рівнем NT‑proBNP ≥300 нг/л упродовж 30 днів із моменту звернення, а також залучили 2048 осіб контрольної групи, котрі звернулися з будь-якої іншої причини, крім ознак або симптомів СН. Для 1-ї групи індексною датою вважали день, коли зареєстрували ознаки та/або симптоми СН і визначений рівень NT‑proBNP.
Результати дослідження – зміни в застосуванні ліків і частоті подій, включаючи госпіталізацію щодо СН, смертність від усіх причин, час до першого встановлення діагнозу СН і час до проведення першої ехокардіограми впродовж 1-го року.
Основні результати:
• результат тесту на рівень NT‑proBNP був доступний протягом 1 дня для більшості хворих із підозрою на СН de novo, медіана часу до вперше проведеного ехокардіографічного дослідження становила 40 днів;
• через 1 рік 29% пацієнтів із підозрою на СН установлено діагноз СН;
• після індексної дати одразу збільшилося використання петльових діуретиків; натомість призначення інгібіторів ренін-ангіотензин-альдостеронової системи (РААС), антагоністів мінералокортикоїдних рецепторів, β-адреноблокаторів, інгібіторів натрій-глюкозного котранспортера (SGLT2) зростало значно повільніше;
• в перші тижні після індексної дати ризики госпіталізації щодо СН і смертності від усіх причин серед пацієнтів із підозрою на СН були високими; вони продовжували зростати протягом 1 року, особливо в хворих із NT‑proBNP >2000 нг/л;
• кумулятивна частота госпіталізацій щодо СН становила 16,1 випадку на 100 пацієнто-років у хворих із підозрою на СН порівняно із 2,2 випадку на 100 пацієнто-років у контрольній групі; кумулятивна частота смертності від усіх причин складала 10,3 і 6,5 випадку на 100 пацієнто-років відповідно.
Вчені зазначили, що як вік, так і рівень NT‑proBNP пов’язувалися з підвищеною частотою госпіталізації щодо СН, а також смертності від усіх причин.
Результати дослідження продемонстрували, що пацієнти, які звернулися по амбулаторну допомогу з підозрою на СН de novo, мали вищі ризики госпіталізації щодо СН і смертності від усіх причин, ніж хворі контрольної групи, що було очевидно вже в перші тижні після індексної дати. Хоча визначення рівня NT‑proBNP проводилося оперативно, ехокардіографічне дослідження виконувалося із затримкою; 29% пацієнтів із підозрою на СН діагноз СН був установлений лише через 1 рік. За винятком петльових діуретиків, дотримання рекомендацій стосовно медикаментозної терапії, зазначеної у настановах, протягом 1-го року було обмеженим.
Наостанок Ліза Андерсон зазначила, що отримані результати підкреслюють необхідність революції у діагностиці СН і впровадженні прагматичного підходу NT‑proBNP rule-in, який дозволяє уникнути потреби очікування на фенотипування СН за допомогою ехокардіографії. Крім того, для зниження захворюваності та смертності необхідно переглянути порогові величини відповідних показників для початку медикаментозної терапії у таких хворих.
Наявність СН не впливає на ефекти GLP‑1RA в пацієнтів із серцево-судинними захворюваннями (ССЗ) та надлишковою масою тіла чи ожирінням
 Провідний кардіолог, професор Університетського коледжу Лондона (Велика Британія) Джон Дінфілд представив результати дослідження «Семаглутид і серцево-судинні наслідки в пацієнтів із надлишковою масою тіла чи ожирінням та СН: попередньо визначений аналіз дослідження SELECT».
Провідний кардіолог, професор Університетського коледжу Лондона (Велика Британія) Джон Дінфілд представив результати дослідження «Семаглутид і серцево-судинні наслідки в пацієнтів із надлишковою масою тіла чи ожирінням та СН: попередньо визначений аналіз дослідження SELECT».
– Нещодавно у великому дослідженні SELECT (Semaglutide Effects on Heart Disease and Stroke in Patients With Overweight or Obesity) було продемонстровано, що семаглутид знижує ризик серйозних ССП (MACE) на 20% у пацієнтів із ССЗ і надлишковою масою тіла чи ожирінням порівняно із плацебо. В попередньо визначеному аналізі цього дослідження порівнювали ефективність і безпеку семаглутиду в хворих із СН і без неї. Семаглутид є аналогом глюкагоноподібного пептиду‑1 і належить до препаратів, що застосовуються в разі цукрового діабету. Він знижує рівень глюкози в крові, діючи в глюкозозалежний спосіб, стимулюючи секрецію інсуліну та пригнічуючи секрецію глюкагону за підвищеної концентрації глюкози в крові. Застосування семаглутиду спричиняє зменшення маси тіла та маси жирової тканини шляхом зменшення споживання калорій, а також зниження апетиту.
SELECT – багатоцентрове подвійне сліпе плацебо-контрольоване, орієнтоване на події, рандомізоване клінічне дослідження ІІІ фази, в якому 17 604 пацієнти віком ≥45 років із наявними ССЗ та індексом маси тіла (ІМТ) ≥27 кг/м², але без цукрового діабету були рандомізовані на підшкірне введення семаглутиду 2,4 мг 1 р/тиж або плацебо. Середній час спостереження становив 39,8±9,4 міс. Кінцеві точки поточного аналізу: час до настання першого MACE (сукупний результат смерті від ССЗ, нефатального інфаркту міокарда (ІМ) або нефатального інсульту), сукупний результат СН (госпіталізація щодо СН, ургентний візит щодо СН або смерть від СН), смерть від ССЗ і смертність від усіх причин.
Основні результати:
• вплив семаглутиду на частоту виникнення MACE порівняно із плацебо не відрізнявся між пацієнтами з наявною СН (ВР 0,72; 95% ДІ 0,60-0,87) та без СН (ВР 0,84; 95% ДІ 0,74-0,97);
• при стратифікації пацієнтів за підтипом СН також не було виявлено різниці у впливі семаглутиду на MACE порівняно із плацебо: ВР становив 0,65 (95% ДІ 0,49-0,87) для пацієнтів зі зниженою фракцією викиду (ФВ) (HFrEF) і 0,69 (95% ДІ 0,51-0,91) для хворих зі збереженою ФВ (HFpEF);
• наявність СН не позначалася на впливі семаглутиду на показник сукупного результату СН (ВР для СН 0,79; 95% ДІ 0,64-0,98 проти ВР за відсутності СН 0,85; 95% ДІ 0,68-1,06) як і підтип СН (ВР для HFrEF 0,79; 95% ДІ 0,58-1,08 проти ВР для HFpEF 0,75; 95% ДІ 0,52-1,07);
• рівень смертності від усіх причин також не залежав від наявності СН або її підтипу;
• профіль безпеки семаглутиду, включаючи частоту серйозних побічних явищ і побічних явищ, котрі зумовлювали остаточну відміну досліджуваного препарату, був схожим у пацієнтів із СН та без неї, а також між підтипами СН.
У цьому попередньо визначеному аналізі дослідження SELECT серед пацієнтів із ССЗ із надлишковою масою тіла чи ожирінням, але без цукрового діабету вплив семаглутиду (порівняно із плацебо) на показники MACE, подій, пов’язаних із СН, смертності від усіх причин не залежав від наявності СН або її підтипу. Професор Джон Дінфілд дійшов висновку, що дані про ефективність у поєднанні з переконливим профілем безпеки підтримують використання семаглутиду для покращення серцево-судинних наслідків у широкій популяції пацієнтів з атеросклеротичними ССЗ і надлишковою масою тіла чи ожирінням незалежно від наявності в анамнезі будь-якого типу СН.
Інгібітор кардіального міозину покращує функціональну здатність при обструктивній ГКМП
 Директор Центру гіпертрофічної кардіоміопатії (ГКМП) лікарні та медичного центру Лахі (м. Берлінгтон, США), провідний експерт у галузі ГКМП Мартін Марон презентував результати застосування нового преперату афікамтен для лікування симптомної обструктивної ГКМП.
Директор Центру гіпертрофічної кардіоміопатії (ГКМП) лікарні та медичного центру Лахі (м. Берлінгтон, США), провідний експерт у галузі ГКМП Мартін Марон презентував результати застосування нового преперату афікамтен для лікування симптомної обструктивної ГКМП.
– Обструкція вихідного тракту лівого шлуночка (ВТЛШ) при ГКМП є визначальним фактором обмежувальних симптомів, особливо задишки за фізичного навантаження та зниження функціональної здатності (толерантності до фізичного навантаження). Гіперскоротливість міокарда – важливий механізм, пов’язаний із захворюванням і відповідальний за обструкцію ВТЛШ.
Наразі зберігається потреба в терапевтичних опціях стосовно обструктивної ГКМП, оскільки сучасні препарати першої лінії мають обмежену ефективність та побічні ефекти. Афікамтен – це новий пероральний селективний інгібітор кардіального міозину, який зменшує надлишок міозинових поперечних містків на рівні саркомерів. У дослідженні REDWOOD-HCM (Randomized Evaluation of Dosing With CK‑274 in Obstructive Outflow Disease in HCM) ІІ фази було показано, що афікамтен зменшує градієнт ВТЛШ шляхом зменшення гіперскоротливості міокарда.
До дослідження ІІІ фази SEQUOIA-HCM (Safety, Efficacy, and Quantitative Understanding of Obstruction Impact of Aficamten in HCM) залучено пацієнтів із ГКМП, які отримували стандартну терапію і мали градієнт ВТЛШ ≥30 мм рт. ст., а також градієнт Вальсальви ≥50 мм рт. ст., функціональний клас (ФК) II-III за класифікацією Нью-Йоркської кардіологічної асоціації (NYHA), прогнозоване пікове споживання кисню (pVO₂) ≤90% для віку та статі. Учасники були рандомізовані на прийом афікамтену (n=142) або плацебо (n=140). Тривалість дослідження становила 24 тиж. Пацієнти в групі афікамтену отримували початкову дозу 5 мг 1 р/добу з можливістю збільшення на 5 мг до максимальної дози 20 мг/добу з урахуванням показників ехокардіограми. Первинна кінцева точка – зміна початкового рівня pVO₂ за даними кардіопульмонального тесту із фізичним навантаженням (CPET) у період до 24-го тиж.
Основні результати:
• спостерігалася значна різниця в зміні pVO₂ на 24-му тиж між групою афікамтену та плацебо зі сприятливою зміною в групі афікамтену (середня різниця в збільшенні pVO₂ порівняно із плацебо становила 1,74 мл/кг/хв; p=0,000002). Це клінічно значуща зміна, оскільки ризик смерті чи трансплантації при ГКМП знижується на ≈18% на кожне збільшення pVO₂ на 1 мл/кг/хв;
• у групі афікамтену зміни за всіма показниками вторинних кінцевих точок, включаючи збільшення середнього бала за Канзаським опитувальником для хворих на кардіоміопатію (KCCQ-CSS), зниження вираженості СН на один клас і більше за класифікацією NYHA, зниження градієнта Вальсальви, відповідність рекомендаціям щодо проведення септальної редукції та рівень NT‑proBNP на 24-му тиж, були статистично значущими порівняно із групою плацебо (p<0,0001);
• у пацієнтів із симптомною ГКМП лікування афікамтеном протягом 24 тиж зумовило клінічно значуще покращення функціональної здатності (pVO₂). Крім того, лікування афікамтеном спричинило зменшення вираженості обмежувальних симптомів, що характеризувалося покращенням показників KCCQ-CSS і NYHA FC.
Мартін Марон завершив свою презентацію такими словами: «SEQUOIA-HCM підкреслює клінічну ефективність афікамтену в лікуванні пацієнтів із симптомною обструктивною ГКМП».
Залізодефіцит (ЗД) і його корекція в пацієнтів із СН: результати міжнародного опитування IRON-HF
 Учений-кардіолог Католицького університету Святого Серця (м. Мілан, Італія) Федеріко Баллаччі від групи авторів представив результати міжнародного онлайн-опитування щодо скринінгу та лікування ЗД у хворих із СН.
Учений-кардіолог Католицького університету Святого Серця (м. Мілан, Італія) Федеріко Баллаччі від групи авторів представив результати міжнародного онлайн-опитування щодо скринінгу та лікування ЗД у хворих із СН.
– ЗД є поширеним супутнім станом у пацієнтів із СН; асоціюється з поганими наслідками незалежно від наявності анемії. Доведено, що застосування препаратів заліза покращує функціональну спроможність та якість життя хворих із СН із ФВ <50% і ЗД.
Із метою оцінки реальних даних із повсякденної клінічної практики щодо скринінгу та лікування ЗД у пацієнтів із СН було проведено онлайн-опитування IRON-HF, яке охоплювало 35 країн. У ньому взяли участь 256 кардіологів (59,8% – чоловіки, найпредставленіша вікова група – від 30 до 50 років). Більшість лікарів (98,4%) визначали ЗД відповідно до рекомендацій ESC і повідомили про проведення скринінгу на ЗД у понад половини (68,4%) своїх пацієнтів. Водночас періодичний скринінг (кожні 6 міс – 1 рік) проводили 54,3% респондентів. Більшість кардіологів (93,0%) призначали та/або вводили препарати заліза, надаючи перевагу внутрішньовенному застосуванню (86,3%). Оцінку стану хворих після курсу прийому препаратів заліза проводили 96,1% респондентів; найчастіше через 3-6 міс (67,6%). Більшість лікарів (93,8%) сприймали ЗД як недооцінену супутню патологію при СН. Вік кардіологів, рівень підготовки, вузька спеціалізація та місце роботи (академічна установа чи лікарня) пов’язувалися з неоднорідністю відповідей.
Автори зазначають, що результати цього дослідження підкреслюють необхідність послідовніших стратегій скринінгу та лікування пацієнтів із СН (рис.).
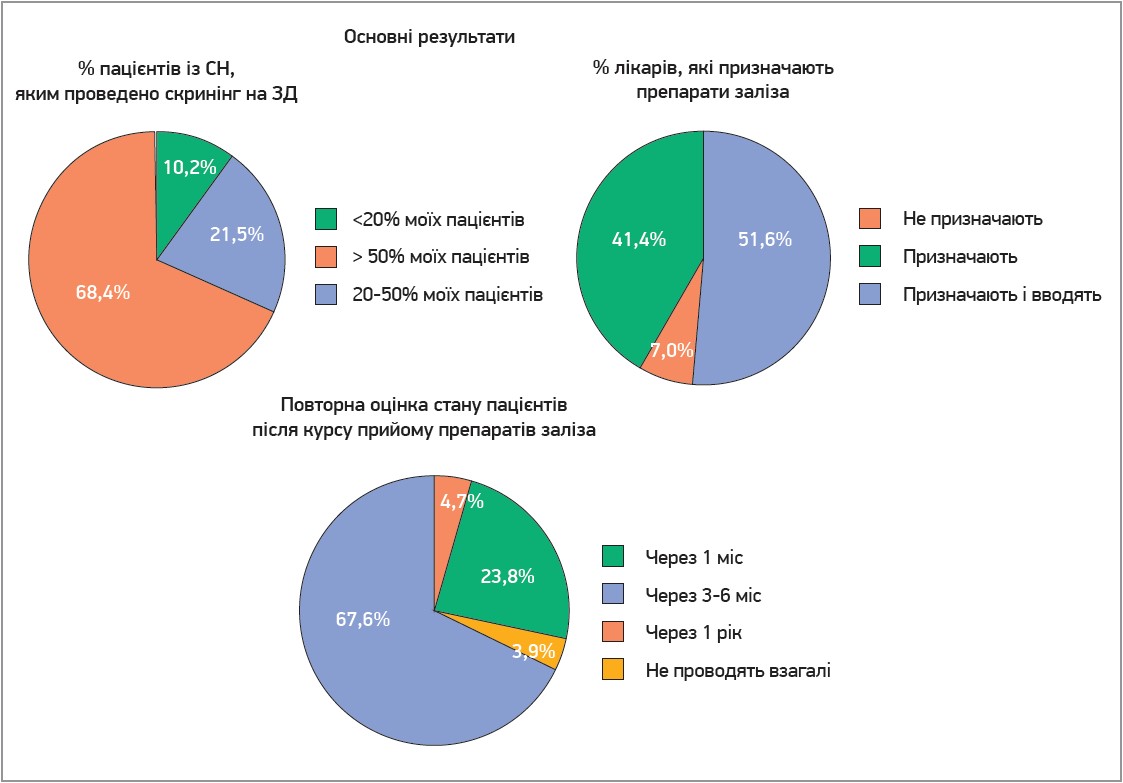
Рис. Результати міжнародного опитування IRON-HF
Отже, боротьба із ССЗ та їхніми ускладненнями є одним із найважливіших викликів для лікарів. Саме тому проведення таких важливих міжнародних науково-практичних заходів дозволяє клініцистам бути поінформованими стосовно останніх результатів та інновацій у сфері фундаментальних, діагностичних, терапевтичних й інтервенційних особливостей ведення хворих із СН.
За матеріалами:
1. https://esc365.escardio.org/Heart-Failure/programme?text=Association%20between%20vaccination%20against%20COVID-19%20&docType=Abstract&page=1
2. https://pace-cme.org/news/delays-echocardiography-and-diagnosis-are-related-adverse-outcomes-suspected-hf/2463032/
3. https://pace-cme.org/news/having-hf-does-not-alter-glp-1ras-effects-in-cvd-patients-with-overweight-or-obesity/2463124/
4. https://pace-cme.org/news/cardiac-myosin-inhibitor-improves-exercise-capacity-obstructive-hcm/2463054/
5. https://esc365.escardio.org/Heart-Failure/programme?text=IRON-HF&docType=Abstract&page=1
Підготувала Марія Ареф’єва



