20 вересня, 2024
Довгострокові ефективність та безпека едоксабану в пацієнтів із фібриляцією передсердь
Пероральні антикоагулянти є ключовим компонентом лікування пацієнтів із фібриляцією передсердь (ФП) та сприяють зниженню ризику інсульту. Упродовж останнього десятиліття застосування пероральних антикоагулянтів, які не є антагоністами вітаміну К (ПОАК), помітно змінило клінічну практику. Наразі ПОАК є стандартом лікування для профілактики інсульту в пацієнтів із ФП, головним чином завдяки вищій безпеці порівняно з антагоністами вітаміну К. Едоксабан є четвертим ПОАК, схваленим Європейським агентством із лікарських засобів (EMA) для профілактики інсульту / системної емболії в осіб із ФП. P. Kirchhof et al. виконали проспективне мультицентрове обсерваційне дослідження ETNA-AF-Europe, метою якого було оцінити довгострокові ефективність і безпеку едоксабану в пацієнтів із неклапанною ФП у повсякденній клінічній практиці. Пропонуємо до вашої уваги огляд отриманих результатів, розміщених в International Journal of Cardiology (2024; 408: 132118).
Матеріали й методи дослідження
Дизайн дослідження
ETNA-AF-Europe – проспективне багатонаціональне мультицентрове післяреєстраційне обсерваційне дослідження із залученням 13 164 пацієнтів, проведене у 776 медичних центрах 10 європейських країн (Австрія, Бельгія, Німеччина, Ірландія, Італія, Нідерланди, Португалія, Іспанія, Швейцарія та Велика Британія) (De Caterina et al., 2019). Дослідження тривало із 2016 по 2022 рр., стан пацієнтів оцінювали що 12±2 місяця протягом чотирьох років.
У дослідження були включені пацієнти із неклапанною ФП, які отримували лікування едоксабаном. Учасники, які припинили приймати едоксабан, перебували під наглядом протягом наступних двох років (або до кінця періоду спостереження). Чітких критеріїв виключення не було, щоб уникнути упередженості відбору та мати можливість документувати дані, отримані в рутинній клінічній практиці (De Caterina et al., 2019). Усі пацієнти надали письмову інформовану згоду на участь. Дизайн дослідження було узгоджено в тісній співпраці з EMA.
Оцінювані показники
Основними цілями ETNA-AF-Europe були збір та оцінка реальних даних про безпеку едоксабану шляхом визначення частоти:
- випадків кровотечі, зокрема внутрішньочерепних крововиливів (ВЧК);
- побічних ефектів, пов’язаних із прийманням препарату;
- смерті пацієнтів від серцево-судинних захворювань (ССЗ) та всіх причин.
Ключові вторинні результати включали частоту інсультів, системної емболії та транзиторних ішемічних атак (ТІА). Визначення частоти будь-яких інсультів та ВЧК включали події геморагічного інсульту.
Групи пацієнтів
У дослідженні порівнювали групи пацієнтів, які отримували едоксабан у дозі 60 або 30 мг на початку спостереження. Знижена доза едоксабану (30 мг) була показана особам із помірною або тяжкою нирковою недостатністю (кліренс креатиніну –15‑50 мл/хв), низькою вагою (≤60 кг) або при одночасному застосуванні певних інгібіторів Р-глікопротеїну. Учасників також оцінювали як таких, хто отримував дози едоксабану 60 і 30 мг відповідно до рекомендацій, зазначених у короткій характеристиці лікарського засобу (SmPC), і тих, у кого причину вибору дозування не було підтверджено. На додаток, пацієнтів порівнювали залежно від категорії ризику за шкалою оцінки ризику інсульту та системної емболії (CHA2DS2-VASc) на початковому етапі: низький (0‑1 бал), помірний (2‑4 бали) або високий (>4 балів).
Окрім того, базові характеристики та частоту подій в учасників ETNA-AF-Europe порівнювали із даними європейської когорти пацієнтів, включених до рандомізованого дослідження ENGAGE AF-TIMI 48.
Вихідні демографічні та клінічні характеристики учасників
Загальна популяція та пацієнти, які отримували дозування 60 або 30 мг на початку дослідження. До повного аналізу було включено 13 164 пацієнтів, з яких на початковому етапі приблизно три чверті отримували едоксабан у дозі 60 мг (n=9617), а решта – 30 мг (n=3042). Інформації про дозування бракувало для 505 осіб.
У загальній популяції хворих середній вік становив 75 (68‑80) років, маса тіла – 80 (70,0‑90,0) кг. Медіана тривалості спостереження була чотири роки. Середній показник за шкалою CHA2DS2-VASc і шкалою для оцінки ризику кровотеч (HAS-BLED) становив 3 (2‑4) і 2 (1‑2) бали відповідно. Середній бал за CHA2DS2-VASc був вищим у пацієнтів, які отримували едоксабан у дозі 30 мг порівняно із тими, хто приймав 60 мг (4 vs 3 бали). Учасники, які застосовували препарат у дозі 30 мг, були старшими (80 vs 73 роки), мали нижчу вагу (71 vs 81 кг) та з більшою імовірністю належали до категорії «слабких» пацієнтів (27 vs 6,6%) порівняно з тими, хто приймав едоксабан по 60 мг. Окрім того, хворі, які отримували едоксабан у дозі 30 мг, мали більше супутніх захворювань.
Із загальної кількості пацієнтів 72,4% завершили дослідження згідно із запланованим графіком, а 27,6% припинили передчасно. Під час дослідження померли 1883 хворих: 33,4% через серцево-судинну (СС) подію, 19,8% – злоякісні пухлини, 46,8% – з інших причин. Терапію едоксабаном припинили 23,8% учасників: 60,7% – із невідомих причин, 13,8% – через побічну реакцію на препарат або клінічну подію, 9,7% – власне бажання. Загалом 5,3% пацієнтів остаточно припинили лікування едоксабаном і перейшли на інший пероральний антикоагулянт.
Пацієнти, які отримували 60 або 30 мг едоксабану згідно з SmPC і без визначення причини вибору дозування. Група хворих, які отримували едоксабан у дозі 60 мг відповідно до SmPC, включала учасників популяції повного аналізу, яким було рекомендовано дозу 60 мг (n=7082) або не рекомендовано дозу 30 мг (n=819). Група пацієнтів, які отримували едоксабан у дозі 30 мг, включала учасників, яким було рекомендовано дозу 30 мг (n=2034) або не рекомендовано дозу 60 мг (n=1202). Правильність дозування не вдалося підтвердити для 1522 осіб (1333 приймали дозу 60 мг, 189 – 30 мг).
Аналіз демографічних і клінічних характеристик пацієнтів показав, що вони частіше отримували 60 мг без відповідних рекомендацій, ніж 30 мг. Найбільшу кількість «слабких» пацієнтів (32,7%) було зафіксовано у групі учасників, які отримували дозу 30 мг згідно з SmPC.
Базові характеристики за CHA2DS2-VASc. Пацієнти із високим показником за CHA2DS2-VASc (>4 балів) частіше належали до категорії «слабких» і страждали на більшу кількість ССЗ, ніж учасники із помірним показником (2‑4 бали). Подібна картина спостерігалася серед хворих із помірним значенням за CHA2DS2-VASc порівняно з низьким (0‑1 бал).
Пацієнти, включені до ETNA-AF-Europe та ENGAGE AF-TIMI 48. Середній вік учасників дослідження ETNA-AF-Europe був вищим порівняно з когортою включених у ENGAGE AF-TIMI 48, причому половина пацієнтів були ≥75 років. Незважаючи на це, медіана оцінки за CHA2DS2-VASc була нижчою, а ССЗ, як-от артеріальна гіпертензія, ішемічна хвороба серця та цукровий діабет, були менш поширеними в учасників ETNA-AF-Europe, ніж ENGAGE AF-TIMI 48.
Статистичний аналіз
Базові характеристики визначали як частоту (n,%) чи медіану та інтерквартильний діапазон (IQR), або як середнє ± стандартне відхилення (SD). Результати щодо безпеки та ефективності представляли як річну частоту подій (%/рік) для загальної популяції та вищезазначених груп. Дані щодо пацієнтів, стратифікованих за початковою дозою едоксабану на первинному етапі дослідження та потенційними причинами призначень різних доз, базувалися на вихідних характеристиках популяції.
Кумулятивну частоту подій розраховували для смерті від усіх причин, ССЗ, інсульту, кровотечі, зокрема великої, ВЧК, шлунково-кишкової кровотечі (ШКК), зокрема великої, для: загальної популяції; пацієнтів, розподілених для приймання початкової дози 60 або 30 мг на вихідному рівні; хворих, розподілених для приймання 60 і 30 мг згідно з SmPC і без такої відповідності. Дослідники використовували статистичне програмне забезпечення SAS версії 9.4 (SAS Institute, Cary, NC, USA).
Результати дослідження
За даними оцінки загальної популяції, річні показники смерті через ССЗ та від усіх причин становили 1 і 4,1% відповідно, причому були відносно стійкими протягом усього періоду спостереження. Більшу кількість летальних випадків було зафіксовано серед пацієнтів, які на початку дослідження отримували едоксабан у дозі 30 мг порівняно із 60 мг. Річна частота інсульту, ТІА та системної емболії становила <1%. Співвідношення випадків ТІА та системної емболії було подібним для хворих, які отримували по 60 або 30 мг едоксабану на початку дослідження, тоді як частота інсульту була дещо вищою у тих, хто приймав препарат по 30 мг (рисунок).
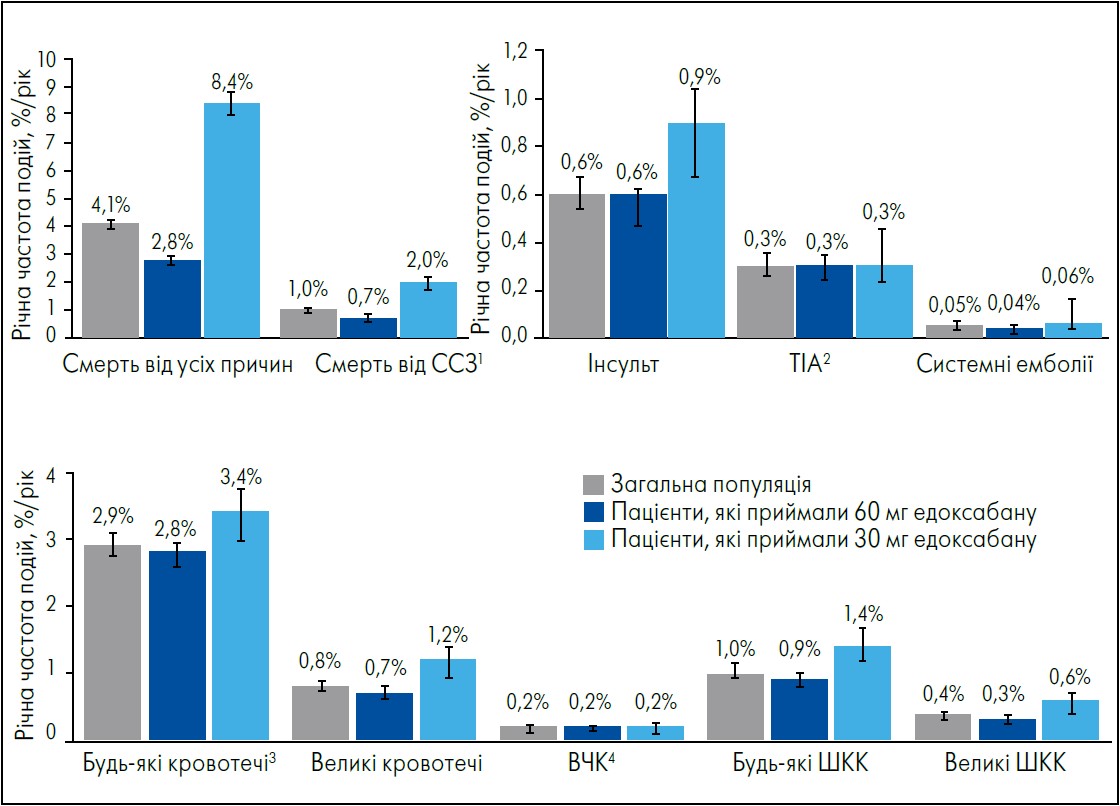 Рисунок. Річна частота клінічних подій протягом 4-річного спостереження у популяції повного аналізу та пацієнтів, які приймали едоксабан у дозах 60 і 30 мг на початку дослідження
Рисунок. Річна частота клінічних подій протягом 4-річного спостереження у популяції повного аналізу та пацієнтів, які приймали едоксабан у дозах 60 і 30 мг на початку дослідження
Примітки: 1 Зокрема смерть від тромбозу глибоких вен; 2 випадки ТІА не підтверджені оцінкою експертів; 3 випадки малих кровотеч не підтверджені оцінкою експертів; 4 геморагічний інсульт або епідуральна / субдуральна гематома.
Річна частота подій – будь-яких кровотеч, великих кровотеч, ВЧК, будь-яких ШКК та великих ШКК – у загальній когорті пацієнтів становила 2,9; 0,8; 0,2; 1 і 0,4% відповідно. Кількість будь-яких кровотеч, великих кровотеч, будь-яких ШКК та великих ШКК була дещо більшою у хворих, які отримували едоксабан по 30 мг, порівняно із 60 мг на початку дослідження, при цьому частота ВЧК була подібною.
У пацієнтів, які приймали едоксабан у дозі 30 мг без відповідності SmPC, було зареєстровано вищу річну частоту смерті від усіх причин і ССЗ порівняно з тими, хто отримував 60 мг. Своєю чергою річна частота інсульту, ТІА та системної емболії була зіставною в обох групах.
Частота кровотеч була здебільшого подібною у хворих, які отримували нерекомендовану дозу едоксабану 30 мг і рекомендовану – 60 мг, за винятком дещо вищої частоти ШКК у тих, хто приймав нерекомендоване дозування 30 мг. Серед пацієнтів, яким едоксабан був призначений у дозі 60 мг без відповідності SmPC, спостерігалася менша річна кількість летальних випадків від усіх причин і ССЗ порівняно з тими, хто отримував 30 мг згідно з SmPC. Проте річні показники частоти інсульту, ТІА та системної емболії були подібними в обох групах.
Частота кровотечі, зокрема великої, та ШКК була низькою та здебільшого зіставною у пацієнтів, які приймали едоксабан по 60 мг без відповідності SmPC, порівняно із тими, хто отримував 30 мг згідно з SmPC. Кількість ВЧК була малою і подібною в усіх чотирьох групах дозувань. Серед учасників, які на початку дослідження отримували дози відповідно до SmPC, у хворих на едоксабані по 30 мг було майже вдвічі більше великих кровотеч порівняно з тими, хто отримував 60 мг (1,3 vs 0,7%).
Згідно з оцінкою за шкалою CHA2DS2-VASc, серед пацієнтів із високим балом було відзначено більшу кількість летальних випадків від усіх причин, ССЗ, інсульту, ТІА, кровотечі (зокрема великої), ШКК (зокрема великої) порівняно з тими, хто мав помірні й низькі показники. Частота ВЧК була низькою й однаковою в усіх трьох групах.
Внаслідок порівняння результатів досліджень було показано, що смертність учасників з будь-якої причини в ETNA-AF-Europe була вищою, але через ССЗ – нижчою, ніж в ENGAGE AF-TIMI 48. Частота ішемічного інсульту, будь-якої кровотечі, великої кровотечі, будь-якої ШКК та великої ШКК була дещо вищою серед пацієнтів ENGAGE AF-TIMI 48 порівняно з ETNA-AF-Europe.
Дозування едоксабану згідно з SmPC та відповідні результати
Призначення дозування ПОАК, яке не відповідає зазначеним у SmPC рекомендаціям (особливо недостатня доза), часто спостерігається в рутинній практиці, що впливає на ефективність і безпеку терапії (Kong et al., 2021). Однак частота недостатнього дозування в ETNA-AF-Europe була нижчою (6,5%), ніж в інших дослідженнях: 9,4% в ORBIT-AF II та 23,2% у GARFIELD-AF (Steinberg et al., 2016; Camm et al., 2020).
Загалом пацієнти, які отримували дози едоксабану 30 і 60 мг без відповідності SmPC, мали проміжний профіль ризику, що схиляло лікарів призначати дози не за рекомендаціями. Крім того, існує висока ймовірність кровотечі на тлі антикоагулянтної терапії, особливо у літніх та «слабких» пацієнтів із підвищеним ризиком падінь (Sen, Dahlberg, 2014). Це може спонукати до призначення зниженої дози едоксабану (30 мг), оскільки кровотечі, пов’язані з ПОАК, можуть більше турбувати лікарів, ніж оптимальна профілактика інсульту (Beyer-Westendorf et al., 2021). У дослідженні ETNA-AF-Europe частота кровотечі була здебільшого зіставною серед пацієнтів, які отримували нерекомендовану дозу 30 мг і рекомендовану дозу 60 мг, що підкреслює доцільність дотримання SmPC.
Вищу частоту летальних випадків від усіх причин і ССЗ в учасників, які отримували нерекомендовану дозу едоксабану 30 мг, порівняно із тими, хто приймав рекомендовану дозу 60 мг, автори пояснюють більшою кількістю «слабких» хворих та осіб старшого віку. Подібні закономірності спостерігалися і в пацієнтів, які отримували інші ПОАК, причому нерекомендоване зниження дози асоціювалося з вищим ризиком смерті (Caso et al., 2023; van den Dries et al., 2023).
Менша кількість смертей від усіх причин і ССЗ спостерігалася серед хворих, яким призначали нерекомендовану дозу едоксабану 60 мг, порівняно із тими, хто приймав рекомендовану дозу 30 мг. Автори зазначають, що відмінності у результатах можуть бути зумовлені тим, що лікарі керуються причинами, пов’язаними із клінічними характеристиками, які не відображені в рекомендаціях стосовно дозування.
Показники пацієнтів за CHA2DS2-VASc
Дані 4-річного спостереження у дослідженні ETNA-AF-Europe показали, що несприятливі події частіше мали місце у пацієнтів із >4 балами за CHA2DS2-VASc (це можна пояснити значною часткою осіб старшого віку із підвищеним ризиком інсульту та кровотеч). Проте автори зазначають, що високий показник згідно з CHA2DS2-VASc не має бути протипоказанням до антикоагулянтної терапії. Адже хворі з 3‑5 балами за CHA2DS2-VASc раніше були виокремлені як популяція, яка може отримати найбільшу користь від антикоагулянтів (Xing et al., 2015). Також важливо зазначити, що у дослідженні ETNA-AF-Europe загальна річна частота несприятливих подій була низькою.
Порівняння даних ETNA-AF-Europe та ENGAGE AF-TIMI 48
Дані ETNA-AF-Europe демонструють низькі показники кровотеч та ішемічних подій і доповнюють результати ENGAGE AF-TIMI 48. Критерієм включення в ENGAGE AF-TIMI 48 була наявність щонайменше 2 балів за CHADS2 (Giugliano et al., 2013). Своєю чергою популяція ETNA-AF-Europe не обиралася на основі оцінки CHADS2 на початковому етапі. Це пояснює нижчі показники за CHA2DS2-VASc в учасників ETNA-AF-Europe порівняно з популяцією ENGAGE AF-TIMI 48. Відповідно, дещо вищу частоту СС-смерті, ішемічного інсульту і кровотеч в ENGAGE AF-TIMI 48 порівняно з ETNA-AF-Europe можна пояснити залученістю когорти хворих високого ризику і більшою поширеністю супутніх патологій на початку дослідження.
Обговорення
Дані, отримані протягом 4-річного періоду спостереження в межах дослідження ETNA-AF-Europe, демонструють довгострокову безпеку та ефективність едоксабану в пацієнтів із ФП. Також вони свідчать про належний комплаєнс хворих на тлі приймання цього антикоагулянту протягом довгострокової терапії. Показники смертності, частоти інсульту, великої кровотечі та ВЧК були відносно низькими у загальній популяції хворих. Окрім того, отримані результати підтверджують дані щодо ПОАК з інших проспективних досліджень, зокрема висновки щодо безпеки ПОАК на тлі ФП (Tittl et al., 2021; Fox et al., 2022).
Частота тромбоемболічних подій в межах ETNA-AF-Europe була набагато нижчою, ніж у пацієнтів, які не отримували і отримували варфарин (8,5 і 1,7‑2,7% відповідно) у попередніх дослідженнях (Bjorck et al., 2016; Sjogren et al., 2015). Показник ВЧК, зареєстрований в ETNA-AF-Europe, був значно нижчим порівняно з тим, що спостерігався в інших випробуваннях, учасники яких отримували антикоагулянти (Steiner et al., 2017; Morotti, Goldstein, 2020). За результатами ETNA-AF-Europe, частота інсульту, кровотечі та смерті також була нижчою, ніж у дослідженнях ефективності ПОАК ІІІ фази (Patel et al., 2011; Giugliano et al., 2013). Своєю чергою даний показник був зіставним із таким у групі учасників, які приймали рекомендовану дозу препарату, в ENGAGE AF-TIMI 48 (Giugliano et al., 2013).
Результати в осіб, які отримували едоксабан у дозі 60 або 30 мг на початку дослідження, дозволили дійти вагомих висновків. Загалом вища частота летальних випадків, інсульту та кровотечі у хворих, які приймали 30 мг едоксабану, потенційно була пов’язана зі старшим віком учасників, більшою кількістю «слабких» пацієнтів та вищою поширеністю супутніх захворювань. P. Kirchhof et al. також припускають, що хворі, які відповідали критеріями зниження дози едоксабану (ниркова недостатність при кліренсі креатиніну 15‑50 мл/хв, маса тіла ≤60 кг, супутнє застосування певних інгібіторів Р-глікопротеїну), були слабшими й більш схильними до тромбоемболії та кровотеч. Незважаючи на відмінності у вихідних характеристиках, у пацієнтів, які отримували 60 або 30 мг едоксабану на початку дослідження, спостерігалася подібна частота ВЧК.
Дані дослідження ETNA-AF-Europe із 4-річним періодом спостереження підтверджують результати 1- та 2-річного спостережень (Kirchhof et al., 2022; de Groot et al., 2021) і рандомізованого контрольованого випробування (Giugliano et al., 2013). Відповідно до них, частота інсульту та кровотеч у пацієнтів із ФП, які приймали едоксабан, була низькою.
Дані ETNA-AF-Europe щодо низької частоти інсульту, кровотеч та смерті додатково доповнюють результати мережевого метааналізу 55 досліджень, проведених в умовах реальної клінічної практики (Deitelzweig et al., 2022). Був продемонстрований подібний або нижчий ризик інсульту (зокрема ішемічного), системної емболії, великої кровотечі, ВЧК та смерті від усіх причин при застосуванні ПОАК порівняно з антагоністами вітаміну К, що підтверджує ефективність і безпеку ПОАК при застосуванні рутинної терапії.
Висновки
Згідно з даними дослідження ETNA-AF-Europe, протягом 4-річного періоду спостереження частота летальних випадків, інсульту, ВЧК, великої кровотечі та великої ШКК за тривалого лікування едоксабаном була низькою та відносно стійкою. На думку P. Kirchhof et al. (2024), на частоту кровотеч головним чином впливали вік учасників, належність до категорії «слабких» та супутні захворювання. Вища частота несприятливих подій серед хворих, які отримували едоксабан у дозі 30 мг, потенційно була зумовлена значною кількістю осіб старшого віку та тих, хто належав до категорії «слабких». Пацієнти, яким було призначено едоксабан без відповідності SmPC, переважно належали до проміжної категорії ризику, що відображалося у їхніх базових характеристиках. Автори припускають, що клініцисти могли обирати нерекомендовані дози на основі клінічних особливостей, що могло призвести до відмінностей у результатах порівняно з пацієнтами, які отримували рекомендовані дози відповідно до SmPC.
Таким чином, результати дослідження ETNA-AF-Europe засвідчують довгострокову ефективність та сприятливий профіль безпеки едоксабану в пацієнтів із ФП в умовах реальної клінічної практики та підтримують рекомендації щодо призначення едоксабану в дозах 60 і 30 мг.
Довідка «ЗУ»
Виробництво якісного генеричного едоксабану під назвою Едоксакорд налагоджено на АТ «Київський вітамінний завод». 1 таблетка Едоксакорду містить едоксабану (в формі тозилату моногідрату) 15, 30 або 60 мг.
Показання до застосування препарату Едоксакорд відповідають європейській інструкції для референтного лікарського засобу: для профілактики інсульту та системної емболії у дорослих пацієнтів із неклапанною ФП та одним або декількома факторами ризику, як-от застійна серцева недостатність, артеріальна гіпертензія, цукровий діабет, інсульт чи транзиторна ішемічна атака в анамнезі, вік >75 років; для лікування тромбозу глибоких вен і тромбоемболії легеневої артерії, а також для профілактики рецидивів цих станів у дорослих.
Рекомендована доза для профілактики інсульту в осіб із неклапанною ФП становить 60 мг едоксабану 1 р/добу. Терапія здійснюється впродовж тривалого часу.
Представлений спектр дозувань препарату Едоксакорд дає змогу підібрати оптимальну дозу хворим із різними факторами ризику, а також легко переходити з іншого антикоагулянту на едоксабан і навпаки, якщо виникає така потреба.
Підготувала Наталія Купко
Тематичний номер «Кардіологія. Ревматологія. Кардіохірургія» № 4 (95) 2024 р.


