8 травня, 2023
Дилема вибору в аритмології: бренд або генерик для лікування тахіаритмії?
Пошук відповіді крізь призму терапевтичного індексу
Закінчення терміну дії патенту на будь-який оригінальний лікарський засіб (ОЛЗ) супроводжується появою на фармацевтичному ринку його аналогів – генеричних ЛЗ (ГЛЗ). Головною метою переведення пацієнтів з ОЛЗ на ГЛЗ є економія коштів, оскільки вартість генерика може бути на 80-85% нижчою за бренд (Straka R. et al., 2017). Завдяки меншій вартості використання ГЛЗ здається дуже привабливим з економічного погляду як для самих пацієнтів, так і для державної системи охорони здоров’я, особливо в країнах зі слабко розвиненою економікою (Gozzo L. et al., 2022). Саме тому лікарі та пацієнти опиняються перед дилемою вибору між відносно дорогим ОЛЗ і дешевшим ГЛЗ.
Регуляторні органи підтримують застосування ГЛЗ за підтвердження біоеквівалентності (БЕ) ОЛЗ, вважаючи їхнє використання безпечним та ефективним. Утім, вибір між ОЛЗ і ГЛЗ в аритмології не є таким простим, як це може здаватися на перший погляд; він тісно пов’язаний з базовими питаннями БЕ – терапевтичною еквівалентністю (ТЕ) та терапевтичним індексом (ТІ).
Бренд vs генерик: ключові відмінності
Згідно із чинною дефініцією, ГЛЗ мають бути фармацевтично еквівалентними оригінальному чи референтному препарату, тобто мати однаковий якісний та кількісний склад за активною речовиною (речовинами), таку саму лікарську форму, а також спосіб застосування (Фармацевтична енциклопедія, 2023). Зазвичай ГЛЗ відрізняються від ОЛЗ допоміжними речовинами / додатковими компонентами, які потенційно здатні впливати на стабільність, абсорбцію та токсичність ЛЗ.
Відповідно до чинних міжнародних норм, ОЛЗ має довести свою ефективність/безпеку під час доклінічних, клінічних досліджень, тоді як схвалення ГЛЗ проводиться на підставі значно меншого обсягу доказової бази, ключовим компонентом якої є підтвердження БЕ (Seoane-Vazquez E. et al., 2016). Управлінням з контролю за якістю продуктів харчування та лікарських засобів США (FDA, 2003) визначено БЕ як відсутність суттєвої різниці між двома чи більше продуктами за швидкістю і ступенем абсорбції у місці дії препарату при введенні в однаковій молярній дозі в схожих умовах. Згідно з дефініцією Європейського агентства з ЛЗ (ЕМА, 2010), ГЛЗ являє собою медичний продукт, який відповідає критеріям однаково якісного та кількісного складу активних речовин, однакової лікарської форми і БЕ, за винятком випадків, коли наукові дані доводять його відмінність від ОЛЗ щодо безпеки й ефективності.
ГЛЗ вважають біоеквівалентним ОЛЗ у тому разі, якщо після прийому тієї самої дози генерик демонструє ступінь і швидкість абсорбції, схожі на такі брендового препарату (ЕМА, 2010). Такий підхід дозволяє гарантувати зіставність двох препаратів стосовно їхньої ефективності/безпеки in vivo, на підставі чого роблять висновок щодо їхньої взаємозамінності та взаємодоповнювання (Фармацевтична енциклопедія, 2023). Оскільки дослідження БЕ не є обов’язковими для ГЛЗ, деякі клініцисти висловлюють занепокоєння щодо ТЕ генериків.
Вузький та широкий ТІ: ключові поняття
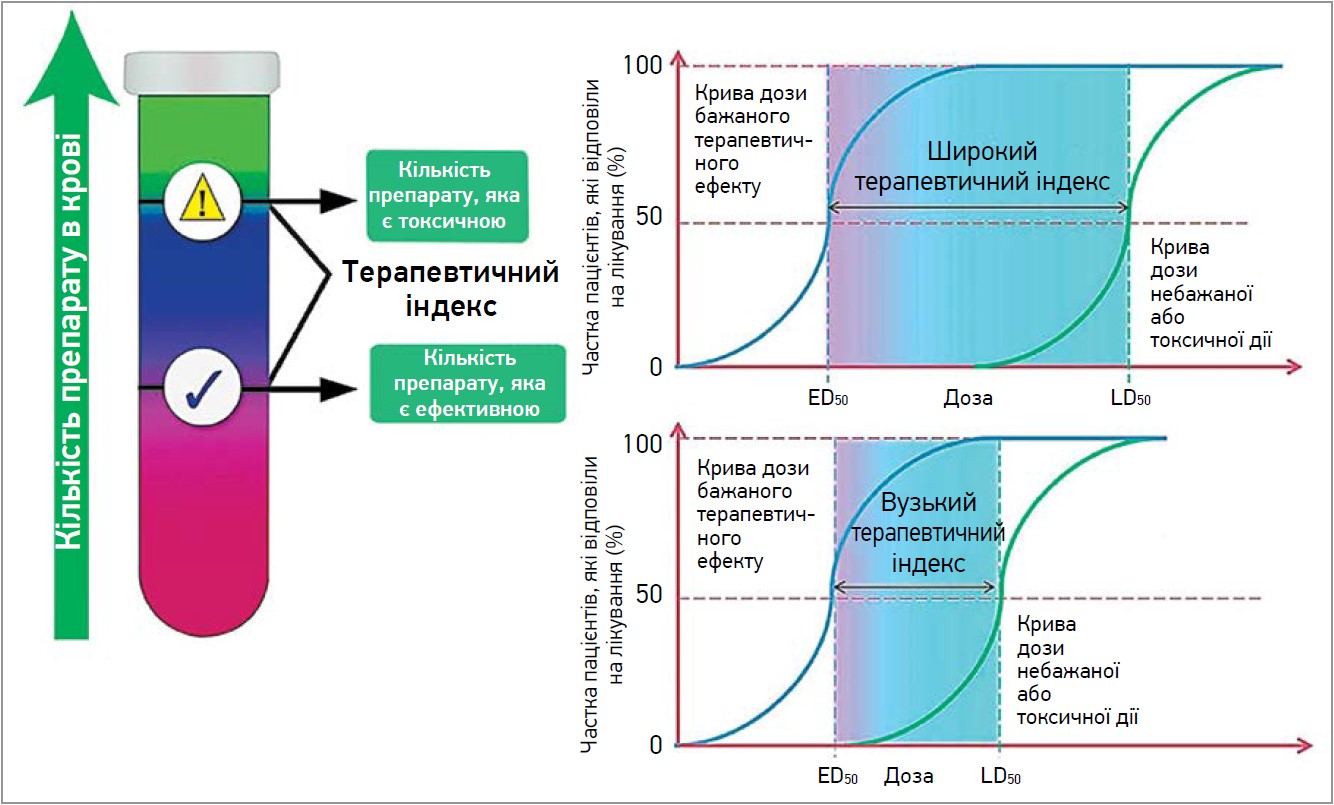
Підтвердження БЕ кожного ГЛЗ проводиться на підставі визначення декількох параметрів (максимальна концентрація ЛЗ у плазмі крові, площа під кривою (AUC) концентрації ЛЗ у плазмі після його прийому, швидкість і ступінь абсорбції ЛЗ), але найважливішим критерієм БЕ вважають терапевтичне вікно чи ТІ, який може бути широким або вузьким (рис. 1). Для більшості генериків значення ТІ складають 80,0-125,0%, тобто різниця між ОЛЗ і ГЛЗ може коливатися від –20 до +25% (Meyer M. et al., 2001). Ці критерії визнано такими поважними регуляторними органами, як FDA (2003), ЕМА (2010), Всесвітня організація охорони здоров’я (ВООЗ, 2017); вони вважають, що саме така різниця не зможе спричинити виникнення клінічно значущих відмінностей та є гарантією однакової ефективності, безпеки ГЛЗ порівняно з ОЛЗ (Tothfalusi, L. et al., 2012).
Рис. 1. Різниця між ЛЗ із широким і вузьким ТІ (за Hassanpour S. et al., 2021)
Примітки: TD50 – середня летальна доза; ED50 – середня терапевтична доза.
Деякі ОЛЗ, у т. ч. антиаритміки, належать до засобів із вузьким ТІ (ВТІ), тобто вони мають невелику різницю між токсичною та терапевтичною дозами. ВТІ також означає, що різноманітні фактори, які зазвичай не чинять суттєвого впливу на фармакологічні характеристики ЛЗ із широким ТІ (взаємодія ЛЗ з їжею, лікарські взаємодії, незначні помилки в дозуванні), можуть зумовити серйозні шкідливі наслідки: відносно невелика різниця в дозуванні/концентрації здатна обумовити зменшення ефективності лікування або спровокувати тяжкі побічні дії (Paixao P. et al., 2022). Саме тому вимоги для ГЛЗ із ВТІ є суворішими; допускається відмінність від ОЛЗ лише в межах ±10%, тобто ТІ для таких засобів складає 90,0-111,11%; схожої думки дотримуються такі організації, як FDA, ЕMA (2010), Канадський регулятор (2018) та ВООЗ (2017).
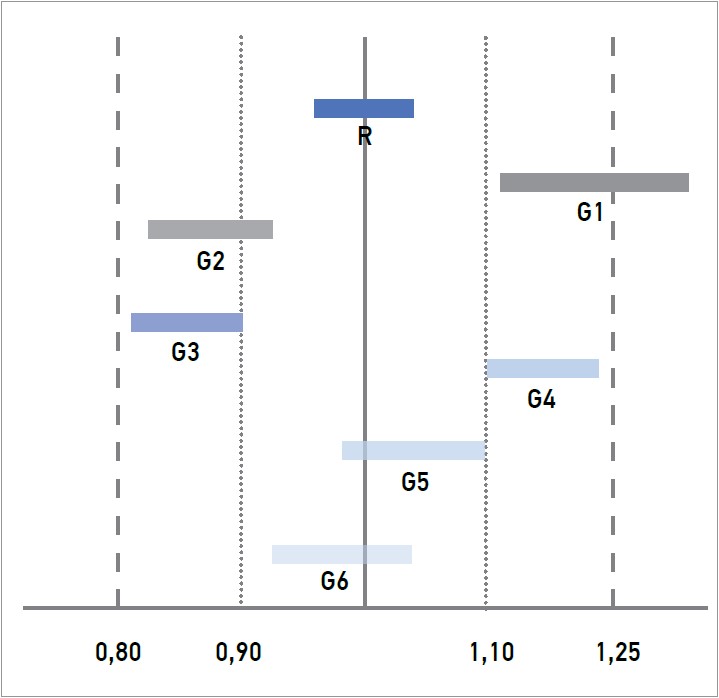
Оскільки дослідження БЕ не є обов’язковими, деякі клініцисти висловлюють занепокоєння щодо низької ТЕ ГЛЗ. Відсутність схваленої процедури переведення пацієнтів з ОЛЗ на ГЛЗ, а також з одного генерика на інший теж додає значущості побоюванням щодо ефективності/безпеки ГЛЗ із ВТІ. Такі побоювання стають ще серйознішими за наявності у фармацевтів можливості замінювати ОЛЗ на ГЛЗ і відпускати за рецептом не ЛЗ під зазначеною торговою назвою, а ЛЗ з аналогічною активною речовиною. Провізор здатен самостійно переводити пацієнта з одного ГЛЗ на інший, але така заміна може зовсім не відповідати ОЛЗ через феномен біовислизання (bio-creep) – це ситуація, коли два генерики біоеквівалентні референтному, але не є біоеквівалентними один одному (рис. 2).
Рис. 2. Феномен біовислизання ГЛЗ
(за Gozzo L. et al., 2022)
Примітки: R – референтний (оригінальний) ЛЗ; G – ГЛЗ.
Порівняння ОЛЗ і ГЛЗ свідчить про те, що генерик G1 не є біоеквівалентним оригіналу згідно зі стандартними критеріями (ТІ в межах –20/+25%), а G2 не може бути біоеквівалентним ОЛЗ відповідно до суворіших критеріїв для ЛЗ із ВТІ. Генерики G3 та G4 відповідають стандартним критеріям БЕ, але вони не є біоеквівалентними між собою; лише генерики G5 і G6 відповідають критеріям БЕ для ЛЗ із ВТІ (ТІ в межах ±10%). Перехід з ОЛЗ на генерик G3 або G4 без корекції дози може спричинити значне зниження рівня препарату в крові та потенційне падіння ТЕ; і навпаки, перехід із генерика G3 на G4 здатний обумовити підвищення рівня препарату в плазмі крові зі зниженням переносимості та появою побічних ефектів. І тільки застосування генериків G5, G6 відповідатиме ТЕ ОЛЗ; на жаль, кількість таких ГЛЗ із ВТІ та доведеною БЕ надзвичайно мала.
Лікування тахіаритмії: оригінальний аміодарон чи генеричний
Зазначені нюанси ускладнюють вибір між ОЛЗ і ГЛЗ при лікуванні тахіаритмій через необхідність застосування антиаритміків, які належать до ЛЗ із ВТІ (Gozzo L. et al., 2022). Саме тому висловлюються думки, що факт визначення ГЛЗ біоеквівалентним ОЛЗ не є достатнім для очікування повної ТЕ. В іншому випадку застосування ГЛЗ може вплинути на ефективність / безпеку лікування, результати терапії, взаємовідносини між лікарем і пацієнтом, юридичні права хворих (Holman A. et al., 2019).
Національний американський аналіз використання різноманітних антиаритмічних ЛЗ (55 ГЛЗ, 10 ОЛЗ) протягом 2014-2018 рр. продемонстрував, що найчастіше клініцисти призначають аміодарон, який є найдоступнішим антиаритміком з огляду на середні витрати на одного бенефіціара, тоді як найдорожчими антиартиміками визнано брендові пропафенон і дронедарон (Mirwais M. et al., 2021). Водночас останніми роками фіксується зростання кількості відкликаних ЛЗ і кількості попереджувальних листів, виданих FDA/ЕMA через порушення вимог належної виробничої практики, виведення на фармацевтичний ринок неякісних / забруднених ГЛЗ, які не відповідають стандартам GMP (Tamargo J. et al., 2020). Регуляторні органи висловлюють значне занепокоєння щодо низької якості ГЛЗ (Tamargo J. et al., 2020).
Аміодарон належить до препаратів із дуже вузьким ТІ; аритмологи під час призначення цього добре вивченого ЛЗ балансують між дозою, яка дозволить досягти ТЕ, та дозуванням, здатним зумовити побічні / токсичні дії. ВТІ аміодарону підкреслюють результати дослідження, під час проведення якого зафіксовано значне зниження біодоступності аміодарону за його одночасного прийому навіть зі звичайними морськими водоростями (Rodrigues M. et al., 2013). Генерики аміодарону можуть відрізнятися від ОЛЗ поширеністю побічних ефектів / токсичністю, а головне – ТЕ; цей факт пояснюють феноменом біовислизання та різними фізико-хімічними властивостями.
Встановлено, що генерики аміодарону скоріше/повільніше розчиняються у воді порівняно з оригіналом; при тривалому (≥3 міс) зберіганні за високої температури / відносної вологості генерики аміодарону мають вищий ступінь дисперсності, що суттєво впливає на профіль вивільнення ГЛЗ порівняно із брендовим аміодароном – Кордароном (Ngo S. et al., 2010). У ретроспективному когортному дослідженні, проведеному серед хворих на фібриляцію передсердь (n=60 220; 4,7% з яких отримували оригінальний аміодарон (Кордарон®), 10,4% – генеричний), констатовано тенденцію до скорішого розвитку клінічно значущої дисфункції щитоподібної залози при використанні генерика аміодарону порівняно з ОЛЗ (4,09 vs 4,32 відповідно), але під час подальшого аналізу зазначена відмінність виявилася статистично недостовірною (відношення ризиків 0,97; 95% довірчий інтервал 0,87-1,08) (Tsadok M. et al., 2011).
Доведено, що перехід з оригінального антиаритміка на ГЛЗ супроводжується частішим виникненням побічних ефектів, що може спричинити збільшення вартості лікування через додаткові звернення по медичну допомогу, часту госпіталізацію (Straka R. et al., 2017). Широке застосування ГЛЗ незадовільної якості з недоведеною БЕ в кардіологічній практиці являє собою серйозну проблему для системи охорони здоров’я зі значним впливом на клінічний та економічний національний тягар (Tamargo J. et al., 2020). Використання антиаритмічних ГЛЗ із ВТІ може виявитися небезпечним і супроводжуватися значними небажаними побічними ефектами: спостерігання за хворими з аритмією, які отримували антиаритмічні ГЛЗ, асоціювалося з появою аритмії (n=44), проаритмічних станів (n=7) та з летальними випадками (n=3) (Reiffel J. et al., 2001). Автори систематичного огляду і метааналізу, котрі досліджували клінічну еквівалентність різноманітних кардіологічних ГЛЗ та ОЛЗ, знайшли лише одне рандомізоване контрольоване дослідження, під час проведення якого доведено взаємозамінність антиартиміків лише І класу; схожих даних щодо антиаритміків ІІІ класу (аміодарон) не виявлено, тому експерти не змогли детально обґрунтувати доцільність використання ГЛЗ та підкреслили, що не підтримують застосування кардіологічних генериків із ВТІ (Kesselheim A. et al., 2008). Провідні вчені-аритмологи не вважають безпечним перехід з ОЛЗ із ВТІ на генерик (навіть з доведеною БЕ) та рекомендують моніторувати сироватковий рівень активної речовини за необхідності такої зміни ЛЗ (Al-Jazairi A. et al., 2008).
Потрібно зважати на психологічний компонент переведення з ОЛЗ на ГЛЗ. Деякі пацієнти негативно ставляться до призначення ГЛЗ, вважаючи, що низька вартість ЛЗ свідчить про незадовільну якість, погану переносимість; така переконаність зумовлює зниження прихильності до лікування. Хворі з хронічними захворюваннями, які тривалий час приймають один препарат і детально знають його зовнішні характеристики, психологічно менш готові до переходу на новий ЛЗ, очікуючи на меншу результативність (Straka R. et al., 2017). Своєю чергою, лікарі в разі отримання негативних відгуків від пацієнтів щодо ефективності генериків змушені не лише докладати зусиль стосовно стабілізування стану хворого, а й працювати над відновленням свого реноме та репутації системи охорони здоров’я.
Застосування ГЛЗ із доведеною БЕ приваблює своєю економічною доступністю, але спокуса призначення антиаритмічного ГЛЗ із ВТІ корелює з імовірністю зниження ефективності та безпеки лікування, розвитку рецидивів тахіаритмії (Habet S. et al., 2021), втрати довіри хворих і лікарів до фармацевтичних фірм-виробників, національної системи охорони здоров’я загалом (Tamargo J. et al., 2020). Доцільність призначення антиаритмічного ОЛЗ або ГЛЗ слід оцінювати в кожному конкретному випадку, знаходячи розумний баланс між вартістю терапії та її ефективністю, безпекою і переносимістю.
Список літератури знаходиться в редакції.