7 серпня, 2023
Сучасні стратегії відновлення і контролю ритму в пацієнтів із фібриляцією передсердь: практичні аспекти в роботі лікаря
За матеріалами ХІII Науково-практичної конференції Всеукраїнської асоціації аритмологів України
з міжнародною участю (18-19 травня 2023 року)
Фібриляція передсердь (ФП) є найпоширенішим порушенням ритму серця, що трапляється у лікарській практиці. Безпосередньо ФП не загрожує життю, але гострі порушення гемодинаміки внаслідок порушення серцевого ритму, зокрема інсульт та інші тромбоемболічні ускладнення, можуть стати причиною інвалідизації та смерті пацієнтів. Це обґрунтовує важливість активного контролю хвороби, на допомогу якому Європейське товариство кардіологів (ESC, 2020) розробило нові рекомендації з діагностики і лікування ФП.
 Власним досвідом і практичними рекомендаціями щодо основних підходів до відновлення та збереження синусового ритму у пацієнтів із ФП поділилась у своїй доповіді під час ХІII Науково-практичної конференції Всеукраїнської асоціації аритмологів України з міжнародною участю старша наукова співробітниця ДУ ННЦ «Інститут кардіології, клінічної та регенеративної медицини імені академіка М.Д. Стражеска НАМН України» (Київ), к.мед.н. Олена Миколаївна Романова.
Власним досвідом і практичними рекомендаціями щодо основних підходів до відновлення та збереження синусового ритму у пацієнтів із ФП поділилась у своїй доповіді під час ХІII Науково-практичної конференції Всеукраїнської асоціації аритмологів України з міжнародною участю старша наукова співробітниця ДУ ННЦ «Інститут кардіології, клінічної та регенеративної медицини імені академіка М.Д. Стражеска НАМН України» (Київ), к.мед.н. Олена Миколаївна Романова.
Як зазначила доповідачка, в останніх рекомендаціях щодо ведення пацієнтів із ФП автори настанови ESC (2020) сформулювали стратегію АВС (Atrial fibrillation Better Care – краща медична допомога в разі ФП), що передбачає такі основні кроки:
А (Anticoagulation / Avoid stroke) – антикоагулянтна терапія / запобігання інсульту.
В (Better symptom management) – кращий контроль симптомів.
С (Cardiovascular and Comorbidity optimization) – оптимізація перебігу серцево-судинних захворювань (ССЗ) і коморбідних станів.
Основна увага лікаря-практика завжди зосереджена на кращому контролюванні симптомів захворювання.
P. Kirchhof et al. (2020) у багатоцентровому рандомізованому дослідженні продемонстрували, що саме контроль ритму, порівняно зі стратегією контролювання частоти серцевих скорочень, у пацієнтів із ФП і супутніми ССЗ пов’язаний із меншим ризиком смерті від серцево-судинних причин, інсульту або госпіталізації через серцеву недостатність та гострий коронарний синдром.
Відповідно до рекомендацій ESC (2020), контролювання ритму рекомендоване для поліпшення симптомів і якості життя в пацієнтів із ФП (клас рекомендації І, рівень доказів А).
Стратегія контролю ритму спрямована на відновлення й утримання синусового ритму та може поєднувати різні підходи: кардіоверсію (фармакологічну чи електричну), приймання антиаритмічних препаратів (ААП) і катетерну абляцію, що комбінують з антикоагулянтною терапією та кардіоваскулярною профілактикою. Під час оцінювання стану пацієнта насамперед звертають увагу на наявність чи відсутність гемодинамічних порушень і час виникнення епізоду пароксизму.
Для гемодинамічно нестабільних пацієнтів перевагу віддають екстреній електричній кардіоверсії. Зокрема, для підвищення успіху електричної кардіоверсії в окремих пацієнтів із нещодавно виявленою ФП, а також без супутньої тяжкої структурної або ішемічної хвороби серця, необхідно брати до уваги можливість одноразового перорального застосування флекаїніду або пропафенону після оцінювання його ефективності й безпечності. В амбулаторних пацієнтів із виразною симптоматикою і нечастими пароксизмами ФП (від одного разу на місяць до одного разу на рік) та стабільною гемодинамікою можна застосовувати фармакологічну кардіоверсію, так званий підхід «таблетка в кишені».
Сьогодні одним із препаратів із найвищим класом рекомендацій та рівнем доказовості для кардіоверсії є пропафенон, який забезпечує швидке й безпечне відновлення синусового ритму.
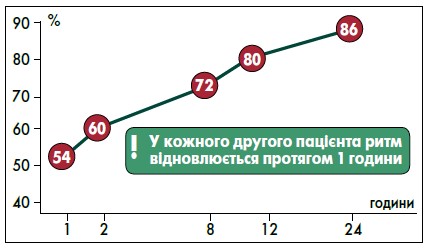
За даними дослідження, проведеного у відділенні аритмології ДУ ННЦ «Інститут кардіології, клінічної та регенеративної медицини імені академіка М.Д. Стражеска НАМН України» із застосуванням препарату Пропанорм®, у половини пацієнтів (54%) відбулося відновлення ритму через годину після приймання лікарського засобу.
Як продемонстровано на рисунку 1, через 24 год ефективність застосування препарату Пропанорм® для відновлення синусового ритму становила 86% (майже у 9 із 10 пацієнтів). За даними іншого дослідження, через 8 год після перорального приймання пропафенону частка успішної кардіоверсії є вищою, ніж у разі застосування флекаїніду (69-78% проти 72% відповідно).
Рис. 1. Ефективність застосування препарату Пропанорм® за даними власного дослідження
Адаптовано за О.С. Сичов, О.М. Романова, 2017.
У попередніх рекомендаціях ESC (2010) зазначалось, що пропафенон (450-600 мг) можна безпечно і ефективно застосовувати пацієнтам а амбулаторних умовах. Для цього необхідно виконати скринінг показань і протипоказань і перевірити безпеку стратегії в стаціонарних умовах.
Зокрема, застосовують такі схеми:
- схема 1 – початкова доза пропафенону становить 300 мг із наступною – 150 мг через годину після початкової та повторною 150 мг через 4-6 год після попередньої, або
- схема 2 – початкова доза пропафенону становить 150 мг із наступними другою і третьою – 150 мг через рівні проміжки часу по 8 год.
Співробітники ДУ ННЦ «Інститут кардіології імені акад. М.Д. Стражеска НАМН України» на підставі власного багаторічного досвіду розробили схему застосування пропафенону: початкова доза – 300 мг із наступним прийманням другої та третьої – 150 мг через годину після попередньої.
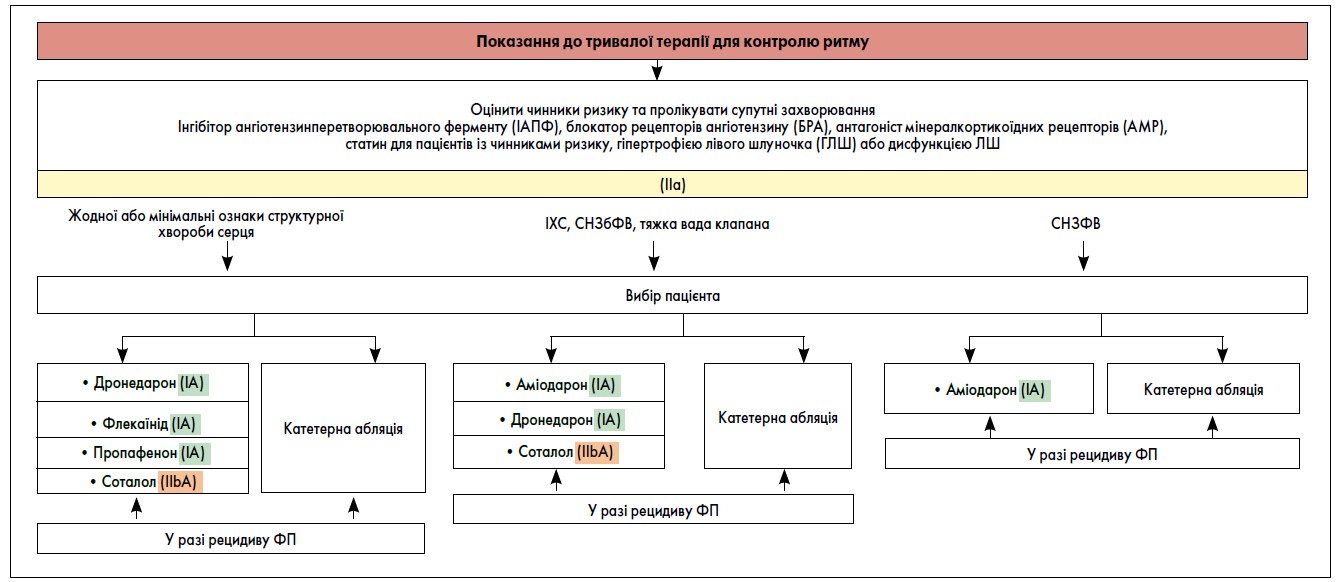
Як зазначила пані Романова, призначаючи довготривалу терапію пропафеноном, слід ретельно враховувати показання, протипоказання та можливі побічні ефекти ААП. На рисунку 2 представлено алгоритм вибору пацієнтів із ФП для довгострокового контролювання ритму. Олена Миколаївна навела основні правила призначення ААП для застосування у щоденній практиці лікаря, за схемою, що допомагає визначити, чи всі стандарти лікування основного захворювання, на тлі якого виникла ФП, були застосовані (таблиця).
Рис. 2. Тривала терапія для контролювання ритму
Порівняно з відсутністю лікування довготривала підтримувальна антиаритмічна терапія подвоює частоту утримання синусового ритму. Як препарат першої лінії пропафенон можна призначати в початкових дозах 150-300 мг тричі на добу.
|
Таблиця. Правила призначення ААП |
|
|
Міркування |
Критерії |
|
Показання для ААП |
Чи є у пацієнта симптоми? Чи симптоми ФП достатньо важкі (визначити клас ЄАСР), щоб виправдати використання ААП? Чи наявні асоційовані стани, що дають змогу прогнозувати низьку переносимість епізодів ФП? |
|
Коли починати застосовувати ААП? |
Зазвичай не при першому епізоді, але це може поліпшити ефект кардіоверсії |
|
Як вибрати препарат серед ААП? |
Мінімізувати проаритмогенний ризик і токсичність для органів Оцінити: відхилення від норми на базальній ЕКГ (тривалість інтервалів QRS, PR, відкоригованого QT) та можливого втручання з використанням ААП; вплив на функцію ЛШ; важливі фармакокінетичні та фармакодинамічні втручання (тобто антитромботичних препаратів); проаритмічні чинники ризику, які можуть бути динамічними та змінюватись із часом |
|
Як мінімізувати ризик проаритмії? |
Оцінка ЕКГ після лікування; періодичне оцінювання токсичної дії на органи (аміодарон); тривале холтерівське моніторування (ХМ) та за окремих випадків тест із фізичним навантаженням; уникати комбінацій ААП |
|
Як перевірити ефективність? |
Оцінювання ступеня тяжкості ФП під час терапії. Якщо пацієнт уже приймає ААП і вони були ефективними, але терапію припинили через непереносимість, вибір бажано робити з того самого класу препаратів |
|
Допоміжні втручання та змішана терапія |
У пацієнтів із порушеннями передсердно-шлуночкової провідності і/або дисфункцією синусового вузла слід розглянути можливість імплантації електрокардіостимулятора, якщо терапію ААП вважають необхідною. Короткострокова терапія може запобігти раннім рецидивам після абляції ФП |
У деяких випадках може знадобитися підвищення добової дози до максимальної – 900 мг на добу (по 300 мг тричі на добу). Збільшувати дозування препарату слід поступово, з інтервалом 3-4 дні.
Доповідачка наголосила, що пропафенон не варто застосовувати в пацієнтів із тяжкими захворюваннями печінки чи нирок, ішемічною хворобою серця, зниженою функцією викиду лівого шлуночка або астмою.
У разі розширення комплексу QRS >25% проти вихідного, блокади лівої ніжки пучка Гіса й інших блокад >120 мс лікування слід призупинити. Також обережно слід призначати цей препарат за хвороби синусового вузла, атріовентрикулярного вузла та порушення проведення.
Щоб знизити ризики планової антиаритмічної терапії необхідно строго враховувати показання і протипоказання та можливі побічні ефекти ААП, призначати малі пробні дози та підбирати мінімально ефективні лікувальні дози ААП. Якщо є така можливість, слід уникати тривалого безперервного застосування ААП (Forogos, 2009).
Втрата антиаритмічного ефекту, який супроводжуватиметься почастішанням пароксизмів ФП, подовженням їхньої тривалості та гіршою переносимістю, трансформацією пароксизму в тріпотіння передсердь, браком ефекту застосування тактики «таблетка в кишені», підштовхує лікаря звернути увагу на стан основного захворювання у пацієнта.
Отже, слід відповісти на такі запитання: чи достатньо ефективна антигіпертензивна терапія, чи наявні ішемічні ознаки, чи є загострення супутньої патології, прояви нових захворювань?
За рекомендацією Олени Миколаївни, необхідно повторно оцінити стан пацієнта, виконати лабораторні дослідження та за допомогою тестів визначити психоемоційний стан хворого.
Враховуючи численні докази ефективності пропафенону на противагу побічним ефектам лікування аміодароном у пацієнтів без структурної патології серця, Пропанорм® є препаратом першої лінії антиаритмічної терапії.
Якщо пацієнт уже отримував аміодарон як ААП, робоча група експертів із порушень ритму серця Всеукраїнської асоціації кардіологів України для переведення пацієнта з аміодарону на пропафенон пропонує:
- скасувати приймання аміодарону;
- призначити пропафенон (150 мг двічі на добу);
- протягом цього періоду до та через 1-2 тижні після призначення виконати ЕКГ або ХМ ЕКГ для оцінювання частоти серцевих скорочень, кількісних і якісних характеристик порушень ритму серця і стану провідної системи;
- через 7-14 днів можна збільшити дозування пропафенону до 150 мг тричі на добу за контролю комплексу QRST на ЕКГ.
Підготувала Ольга Загора