5 травня, 2023
Роль тромбоцитів у запаленні й інфекції
Продовження. Початок у № 3 (539), 2023 р.
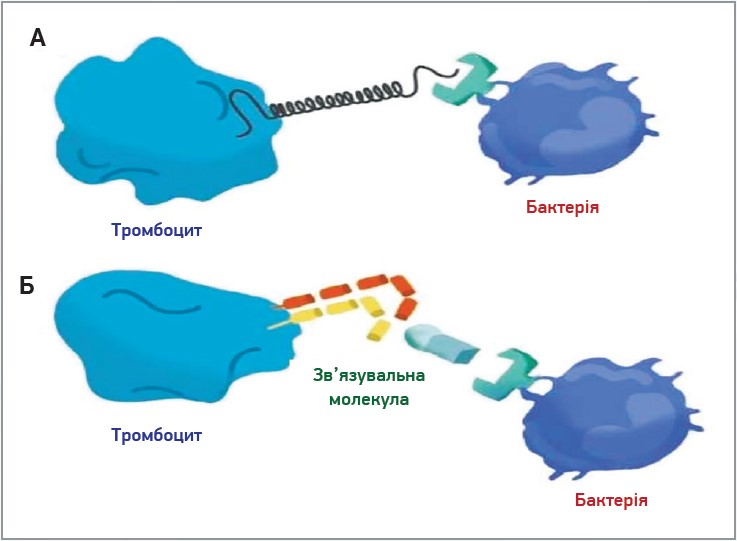
Рис. 4. Загальні механізми, які спостерігаються за взаємодії тромбоцитів із бактеріями: пряма (А) та непряма (Б) взаємодія
Причиною активації тромбоцитів може бути зв’язування секреторних бактеріальних продуктів, особливо токсинів. Такий механізм описаний S. aureus, S. pneumoniae, S. pyogenes, P. gingivalis тощо. Одна й та сама бактерія може використовувати всі зазначені шляхи активації тромбоцитів. У 2004 році на тромбоцитах уперше було виявлено Toll-подібні рецептори (TLR), що суттєво просунуло уявлення про них як про клітини, залучені до розпізнавання патогенів та пов’язаного з ними запалення. Показано наявність функціональних TLR2, TLR4, TLR7 та TLR9 [46, 47]. Активація тромбоцитів через усі перелічені TLR призводить до вивільнення імуномодулювальних агентів, активації інших клітин та представлення їм патогенів для фагоцитозу, при цьому стимуляція тромбоцитів через TLR2 і TLR9 викликає їхню агрегацію.
Токсини бактерій здатні до активації тромбоцитів різними механізмами. Наприклад, α-токсин деяких штамів S. aureus зв’язується з ліпідним бішаром мембрани тромбоцитів, формуючи пору, що зумовлює приплив іонів кальцію та активацію тромбоциту. Стрептолізин O, токсини S. pyogenes, S. pneumoniae формують пори в мембрані тромбоциту. Властивість ушкоджувати мембрани має також гемолізин, який продукується E. coli, що порушує мембранний потенціал мітохондрій. Це призводить до деградації антиапоптотичного білка BclxL у тромбоцитах, викликаючи їхній апоптоз [48]. Стафілококовий β-токсин має ферментативну активність сфінгомієліназ і розщеплює сфінгомієлін на церамід і фосфорилхолін, змінюючи склад ліпідів клітинної мембрани, що порушує функції тромбоцитів та ендотеліальних клітин. Коклюшний токсин, вироблений B. pertussis, містить субодиницю А, що має ферментативну активність АДФ‑рибозилтрансферази і субодиницю B, яка зв’язується з поверхнею клітин-мішеней, у т. ч. і тромбоцитів, спричиняючи їхню активацію.
Отже, існує декілька груп бактеріальних токсинів, які активують тромбоцити, руйнуючи електрохімічний градієнт плазматичної мембрани шляхом перфорації. Інші, які є секреторними молекулами на бактеріальній поверхні, зумовлюють взаємодію та активацію тромбоцитів і клітин імунної системи.
Оскільки бактерії зв’язуються з тромбоцитами через рецептори, залучені до гемостазу, вони можуть індукувати агрегацію тромбоцитів. Бактерії, які зв’язуються з GPIIb-IIIa через фібриноген або фібронектин, викликають агрегацію, схожу на інші об’єкти, покриті фібриногеном. Коли зв’язування бактерій не призводить до агрегації (наприклад, зв’язування S. sanguinis із GPIb), тромбоцити активуються і вивільнюють уміст своїх щільних гранул, де наявні вазоактивні речовини (АТФ та АДФ).
Тромбоцити та віруси
Тромбоцити активуються в разі контакту з вірусами [49]. Вірусне зараження клітин розпочинається зі зв’язування вірусу з поверхневим рецептором, який опосередковує його інтерналізацію, а тромбоцити експресують різні рецептори розпізнавання патерну (PRR або рецептори, що упізнають патоген), здатні опосередковувати зв’язування для проникнення різних вірусів [50].
Незалежно від прикріплення вірусу до поверхневих рецепторів або розпізнавання PRR у тромбоцитах активації тромбоцитів може сприяти імунна відповідь проти вірусів за допомогою різноманітних механізмів, у т. ч. вивільнення хемокінів, які сприяють ендотеліальній передачі сигналів і міграції лейкоцитів. Наприклад, тромбоцитарний фактор 4 (PF4/CXCL4), хемокін, секретований винятково тромбоцитами і мегакаріоцитами, був ідентифікований як есенціальний медіатор рекрутування нейтрофілів та елімінації вірусу за інфекції грипу А.
Імунна відповідь проти вірусів здійснюється послідовною активацією тромбоцитів і проявляється через різні механізми, як-от вивільнення хемокінів, що сприяють ендотеліальній передачі сигналів та міграції лейкоцитів, або фізично взаємодіючи з лейкоцитами. Крім того, тоді як традиційна активація тромбоцитів, пов’язана з G‑білком, зазвичай відбувається швидко, активація PRR тромбоцитів у відповідь на інфекції та імунні стимули може бути відтермінованою, зберігаючись через декілька годин після початкової агрегації, а також секреції.
Вірус-опосередкована тромбоцитопенія, що з’являється в результаті, зазвичай є багатофакторною. Віруси використовують різні стратегії зниження рівня циркулювальних тромбоцитів, продукування чи посилення руйнації тромбоцитів. Тромбоцити утворюються в кістковому мозку мегакаріоцитами. Віруси можуть порушувати продукцію тромбоцитів на різних етапах розвитку. Деякі віруси, як-от вірус імунодефіциту мавп (SIV) і вірус герпесу людини, можуть впливати на цитокіновий профіль господаря, що спричиняє зміну продукції тромбопоетину (ТПО) в печінці; деякі інші, в т. ч. вірус гепатиту С (HCV), безпосередньо перешкоджають виробленню ТПО руйнуванням тканини печінки. Крім того, вірус імунодефіциту людини (ВІЛ), цитомегаловірус (ЦМВ) і ВГС реплікуються в мегакаріоцитах, модулюючи їхню проліферацію та функцію [53-55]. Найшвидший шлях руйнування тромбоцитів відбувається за прямої їхньої взаємодії з вірусами через різні рецептори; здебільшого опосередковується поверхневими лектинами, інтегринами і TLR [56]. Ротавірус використовує рецептор колагену GPIa/IIa для зв’язування із тромбоцитами, тоді як хантавіруси та аденовіруси взаємодіють із тромбоцитами через рецептор фібриногену GPIIb/IIIa – найпоширеніший інтегрин тромбоцитів. Взаємодія вірусу Епштейна – Барр (ВЕБ) із тромбоцитами відбувається через рецептор комплементу 2 (CR2). ВІЛ та вірус денге активують тромбоцити, зв’язуючись з лектиновими рецепторами та клітинно-специфічною молекулою міжклітинної адгезії [57-60]. Ці прямі взаємодії часто спричиняють активацію тромбоцитів та адгезію активованих тромбоцитів до лейкоцитів.
Захисні механізми господаря у відповідь на вірусні інфекції можуть призводити до активації тромбоцитів і зменшують тривалість їхнього життя. Крім того, В‑лімфоцити виробляють антитіла проти деяких вірусів, що також перешкоджає виживанню тромбоцитів. Ці антитіла, зазвичай спрямовані на поверхневі глікопротеїни вірусів, виявляють перехресну реактивність з поверхневими інтегринами тромбоцитів, як-от GPIIb/IIIa. Це захворювання (імунна тромбоцитопенія), індуковане автоантитілами тромбоцитів, є характерним для ВГС, ВІЛ, ЦМВ, ВЕБ, хантавірусу, вірусу вітряної віспи, вірусів герпесу [61, 62]. Взаємодія між тромбоцитами та вірусами має вирішальне значення в патогенезі COVID‑19.
Клітинні зміни в структурі та функції тромбоцитів при інфекції
Взаємодія між тромбоцитами та бактеріями чи вірусами може вплинути на структуру і функцію тромбоцитів декількома способами. Найвідомішим наслідком інфекції є зниження кількості тромбоцитів, яке може мати різний ступінь тяжкості. Виникнення тромбоцитопенії давно відоме як незалежний фактор ризику найгірших результатів інфекції, а ступінь тромбоцитопенії використовується як маркер тяжкості сепсису. Дійсно, кількість тромбоцитів включено до динамічної оцінки органної недостатності (SOFA) [63], зміна якої має вирішальне значення в діагностиці сепсису. Крім прогностичної ознаки тромбоцитопенії, що добре зарекомендувала себе, існують й інші менш відомі характеристики тромбоцитів, які можна оцінити під час інфекції. Так, два індекси морфології тромбоцитів доступні в більшості лабораторій. Цими показниками є ширина розподілу тромбоцитів (PDW) та середній обсяг тромбоцитів (MPV). PDW – показник гетерогенності тромбоцитів, тоді як MPV характеризує середній розмір тромбоцитів. Розмір тромбоцитів зазвичай становить від 1,5 до 3 мкм, великі тромбоцити або макротромбоцити мають розмір 3-7 мкм, тоді як тромбоцити, що досягають розмірів еритроцитів або лімфоцитів (від 7 до 20 мкм), вважаються гігантськими. Здорові люди зазвичай мають <5% великих тромбоцитів, але за їхньої активації, зумовленій інфекцією, спостерігається значна зміна форми через порушення цитоскелету тромбоцитів. Показники MPV і PDW нещодавно були запропоновані як маркер активації тромбоцитів [64-66]. Наприклад, високі значення PDW та MPV були пов’язані з 90-денною смертністю в пацієнтів із септичним шоком, тому як PDW, так і MPV можуть використовуватися як маркер тяжкості інфекції і є незалежними предикторами смертності при інфекціях.
Висновки
Тромбоцити відомі як первинні медіатори гемостазу. Однак наукові дані підтверджують, що вони є ключовими гравцями при запаленні та імунних реакціях. На сьогодні опубліковано численні випробування, під час яких детально досліджено запальний та регуляторний потенціал тромбоцитів. Показано, що тромбоцити індукують секрецію біологічно активних речовин та експресують значну кількість рецепторів, розчинних молекул і сигнальних факторів, що дозволяють їм забезпечувати масштабну участь в імунній системі організму. Хоча першим повідомленням про агрегацію тромбоцитів навколо бактерій понад 100 років, лише нещодавно дослідники почали розуміти складну взаємодію між тромбоцитами та клітинами вродженого імунітету у відповідь на запалення та інфекції. Здебільшого тромбоцити поводяться як різноплановий актор. Вони можуть формувати комплекси з нейтрофілами і посилюють їхній фагоцитоз, продукують ROS та утворення NET тощо. В результаті взаємодії з клітинами крові з імунної системи видаляють бактерії та віруси різними способами (як безпосередньо, так і опосередковано).
Отже, тромбоцити беруть участь в імунній відповіді через різні механізми та відіграють важливу роль у боротьбі з інфекцією. Нині тромбоцити дедалі частіше визнаються імунними клітинами, оскільки встановлено їхню роль як чинника, що впливає на імунну систему.
Список літератури знаходиться в редакції.