23 грудня, 2023
Вакцина Гексаксим®: оновлення через 10 років після першого ліцензування
Вакцина Гексаксим® (DTaP-IPV-HB-Hib/Hexaxim) є комбінованою вакциною, яка забезпечує імунізацію проти шести педіатричних хвороб: дифтерії (D), правця (T), кашлюку, поліомієліту, гепатиту В (HB) та інвазивних захворювань, спричинених Haemophilus influenzae типу b (Hib). Дифтерія, правець, кашлюк і поліомієліт – це серйозні захворювання, які можуть призвести до тяжких ускладнень або навіть смерті у дітей раннього віку [1-4].
Вакцина Гексаксим® (Sanofi) була схвалена для використання в Європейському Союзі (ЄС) у квітні 2013 року [12] і дозволена у 120 країнах світу. Форма випуску препарату попередньо схвалена Всесвітньою організацією охорони здоров’я (ВООЗ) [13]. Склад вакцини наведено в таблиці. Широка клінічна оцінка показала стабільний і хороший профіль безпеки і продемонструвала здатність вакцини викликати сильну імунну відповідь проти кожного цільового патогену, з високим рівнем захисту, що спостерігається в широкому діапазоні клінічних ситуацій [14-16]. З моменту отримання ліцензії клінічні дослідження продовжують підтверджувати профіль безпеки та імуногенність у різних умовах, у тому числі в окремих популяціях. З моменту першого застосування у червні 2013 року і до теперішнього часу у світі було розподілено понад 180 млн доз вакцини. 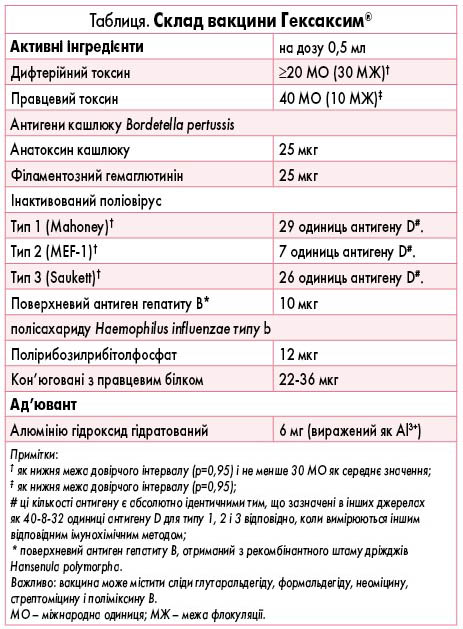
Клінічна розробка
Гексаксим® є результатом значного досвіду компанії Sanofi у розробці DTaP-IPV-вмісних вакцин і багаторічного досвіду роботи з 4-валентною (Тетраксим [DTaP-IPV]) і 5-валентною (Пентаксим [DTaP-IPV//Hib]) вакцинами [8, 9]. Гексаксим® містить добре відомі антигени, що використовуються у вакцині Пентаксим (DTaP-IPV//Hib), а також HBsAg, і представлений у вигляді повністю рідкої, готової до використання суспензії для ін’єкцій без консерванта і з додаванням гідроксиду алюмінію [12].
Імуногенність
6, 10, 14 тижнів – первинна серія і бустер у віці 15-18 місяців. 6, 10, 14 тижнів первинної серії і бустерної схеми у віці 15-18 місяців були оцінені в дослідженні у Південній Африці [17, 18]. Результати цього дослідження продемонстрували, що після закінчення первинного курсу показники серозахисту (анти-D, анти-T, анти-Polio1,2,3, анти-PRP, анти-HBs) становили ≥95,4% як у групі, яка отримувала Гексаксим® (без вакцини проти гепатиту В при народженні), так і в контрольній групі (DTwP/Hib, HB та оральна поліомієлітна вакцина (ОПВ). Після закінчення первинної вакцинації рівень серозахисту анти-HBs (≥10 МО/мл) був високим як за наявності дози вакцини проти гепатиту В при народженні (99,0%), так і за її відсутності (95,7%), проте середньогеометрична концентрація анти-HBs була вищою після дози вакцини проти гепатиту В при народженні (1913 МО/мл порівняно з 330 МО/мл). Ревакцинація викликала сильну відповідь у кожній групі на всі антигени (показники сероконверсії (PT, FHA) >83% і показники серозахисту (інші антигени) >90%) без помітних відмінностей між групами [17, 18].
В іншому дослідженні після отримання ліцензії в Індії була продемонстрована висока імуногенність для кожного антигену вакцини Гексаксим® після первинної вакцинації за схемою 6, 10, 14 тижнів з окремою вакцинацією проти гепатиту В при народженні, з >93% показниками вакцинної відповіді (PT, FHA)/показниками серозахисту (інші антигени) [19].
Таким чином, Гексаксим® у календарі розширеної програми імунізації (РПІ), з вакциною проти гепатиту В при народженні або без неї, є високоімуногенною вакциною порівняно з контрольними вакцинами.
2, 3, 4 місяці – первинна серія та бустер у віці 2, 3, 4 місяці, 11-17 місяців
Схема РПІ, що починається з 6-тижневого віку, і схема 2, 3, 4-місячного віку вважаються найбільш складними схемами первинних серій для досягнення захисних титрів антитіл, оскільки вони починаються в ранньому віці (у той час, коли імунна система ще не повністю дозріла) і мають лише 1-місячний інтервал між введеннями доз.
У дослідженні M. Ceyhan та співавт. (2017) було продемонстровано відсутність переваг вакцин Гексаксим® і Пентаксим проти гепатиту В за рівнем серопротекції анти-HBs постпервинної серії (94,0 проти 96,1%). Імуногенність інших антигенів була подібною в обох вакцин [20].
З трьох досліджень, проведених після отримання ліцензії, одне було рандомізованим клінічним дослідженням (РКД) проти іншої 6-валентної вакцини (DTPa-HBV-IPV/Hib) [21]. Первинні імунні відповіді були високими і подібними в обох групах. Була продемонстрована неповторність імунної відповіді після первинної серії для всіх досліджуваних антигенів. Описово, бустерна імуногенність вакцини Гексаксим® була подібною до DTPa-HBV-IPV/Hib. Інші 2 дослідження підтвердили гарну імуногенність Гексаксим® з/без дози вакцини проти гепатиту В при народженні.
2, 4, 6 місяці – основна серія та бустер у 12-24 місяці
У дослідженні, проведеному в Аргентині, було продемонстровано неперевершену імуногенність після первинних серій для кожного антигену порівняно з вакциною Пентаксим та окремою вакциною проти гепатиту В (рівень сероконверсії (анатоксин кашлюку, філаментозного гемаглютиніну (PT, FHA) ≥90% і рівень серозахисту (інші антигени) >94%). Аналогічним чином, не було продемонстровано переваг у постпервинних серіях для всіх антигенів порівняно з вакциною Пентаксим і окремою вакциною проти гепатиту В (Південна Корея, рівень сероконверсії (PT, FHA) >89% і рівень серопротекції (інші антигени) >96%).
Для усіх антигенів було продемонстровано неперевершеність постпервинної імунної відповіді порівняно з DTPa-HBV-IPV/Hib (Колумбія та Коста-Ріка: рівень відповіді на вакцину (PT, FHA) >97% і рівень серопротекції (інші антигени) >94%). У дослідженнях порівняння Гексаксим® і DTPa-HBV-IPV/Hib було продемонстровано не гіршу імуногенність Гексаксим® після первинної серії для всіх антигенів (Колумбія/Коста-Рика) чи окремих антигенів (Мексика, Таїланд, Перу).
Первинна серія у віці 3, 5 місяців і бустер у віці 11 місяців (схема 2+1). Схема первинної серії з 2 доз у віці 3 і 5 місяців із бустером у віці 11 місяців була оцінена в одному постліцензійному дослідженні у Фінляндії та Швеції [33], яке показало, що Гексаксим® не поступається DTPa-HBV-IPV/Hib за всіма антигенами після третьої дози за показниками серопротекції (≥85%) і реакції на вакцину (≥98%).
Сумісне застосування з іншими педіатричними вакцинами
Клінічні випробування показали подібну імуногенність вакцини Гексаксим® при сумісному застосуванні з іншими педіатричними вакцинами, що призвело до схвалення такого застосування з пневмококовими, вакциною проти кору-паротиту-краснухи, проти ротавірусу, менінгококовими вакцинами та ін. [18, 21, 23, 24, 29, 31, 33].
Змішана 6-5-6-валентна первинна серія у віці 2, 4, 6 місяців
У післяреєстраційному дослідженні в Іспанії оцінювали змішану схему первинної вакцинації 6-5-6-валентною первинною серією після введення вакцини проти гепатиту В при народженні [34]. Імунні відповіді і відповідь на бустер вакцини Пентаксим були сильними і порівнянними зі стандартними схемами (рівень сероконверсії/серопротекції >89-99%). Відповіді були подібними до схем 6-валентної первинної серії та 6-/5-валентної бустерної вакцинації [16, 31], що підтверджує можливість використання вакцини Гексаксим® у змішаній схемі після введення вакцини проти гепатиту В при народженні.
Стійкість імунітету. Стійкість антитіл оцінювали для всіх антигенів до шкільного віку (3,5 і 4,5 років) у Південній Африці і Колумбії [35], а також у більш тривалому періоді для HB у Таїланді (9-10 років) [36] і Фінляндії (6 років) [37]. У дослідженнях, проведених у Південній Африці і Колумбії [35], Гексаксим® індукував хорошу персистенцію антитіл до 4,5 років для кожного антигену, особливо після складного графіку первинної вакцинації у 6, 10, 14 тижнів у Південній Африці, де персистенція анти-HBs антитіл (≥10 мМО/мл) спостерігалася у 73% (без вакцини проти гепатиту В при народженні) до 96% (з вакциною проти гепатиту В при народженні) осіб, а персистенція серопротекторних рівнів анти-D, анти-Т, антиполіомієліту 1, 2, 3 і анти-PRP у ≥97% дітей.
Дослідження в Таїланді надало унікальну можливість оцінити рівень анти-HBs-антитіл за графіком 2, 4, 6 місяців після введення дози вакцини проти гепатиту В при народженні і без бустерної вакцини проти гепатиту В (згідно з національним календарем щеплень у Таїланді) [36]. Відповідно до отриманих даних, рівень антитіл знижувався подібно в групах вакцини Гексаксим® і DTPa-HBV-IPV/Hib до 9-10 років (49,3 і 42,9% відповідно). Після ревакцинації у 9-10 років рівень антитіл зріс в обох групах (92,8 і 98,7%), що вказує на збереження імунної пам’яті, а не персистенцію високих рівнів антитіл. Аналогічні дані отримані у фінському дослідженні, в якому рівень серопротекції проти гепатиту В після 3, 5 і 11 місяців вакцинації був нижчим для вакцини Гексаксим®, ніж для DTPa-HBV-IPV/Hib у віці 6 років (53,8 проти 73,5% ≥10 мМО/мл), але збільшився до аналогічного рівня після щеплення проти гепатиту В (96,7 і 95,9% відповідно), що підтверджує стійку імунну пам’ять [37].
Безпека і побічні реакції
Було проведено великомасштабне дослідження безпеки приблизно у 2000 учасників (з яких 1422 учасники отримали Гексаксим®) у Мексиці і Перу [25]. Як порівняльний засіб використовували реконституйовану 5-валентну вакцину з цілоклітинним кашлюковим компонентом (DTwP-HB/Hib) разом з ОПВ. Результати продемонстрували не вищу частоту тяжкої гарячки після застосування вакцини Гексаксим® порівняно з вакциною порівняння. Частота повідомлених реакцій була вищою для вакцини порівняння, що узгоджується з кращим профілем безпеки вакцин з ацелюлярним кашлюковим компонентом [38].
Інтегрований аналіз даних щодо безпеки вакцини Гексаксим® і DTPa-HBV-IPV/Hib [21, 28-31, 33] показав схожий профіль безпеки, за винятком болю в місці ін’єкції та дратівливості, про що трохи частіше повідомлялося для вакцини Гексаксим®.
Аналіз спонтанних даних з глобальної бази даних Sanofi з 1 червня 2013 р. по 17 квітня 2023 р. виявив 18320 спонтанних повідомлень про ПР в усьому світі після вакцинації вакциною Гексаксим®. Найчастіше повідомляли про: еритему, набряк, біль у місці ін’єкції, гарячку, плач, висип, дратівливість, діарею, блювання, зниження апетиту.
Висновок
Протягом приблизно 20 років масштабна програма клінічних випробувань у поєднанні з безперервним післяреєстраційним наглядом послідовно демонстрували сприятливий профіль безпеки і високу імуногенність вакцини Гексаксим® при широкому діапазоні графіків первинної і бустерної вакцинації. Повністю рідка 6-валентна вакцина Гексаксим® відіграє важливу роль у постійному і майбутньому контролі шести педіатричних інфекційних захворювань в усьому світі.
Реферативний огляд статті Boisnard F., Manson C., Serradell L. et al. (2023) DTaP-IPV-HB-Hib vaccine (Hexaxim): an update 10 years after first licensure. Expert Rev Vaccines. Jan-Dec; 22 (1): 1196-1213. doi: 10.1080/14760584.2023.2280236.
Підготувала Анна Хиць
Тематичний номер «Педіатрія» № 5 (71) 2023 р.


