30 березня, 2021
Системна терапія при метастатичному раку нирки
Аналіз сучасних рекомендацій
22 грудня 2020 р. відбувся захід, ініційований компанією «Іпсен», головною метою якого було привернення уваги онкологів до проблеми лікування метастатичного раку нирки. На ньому виступили провідний науковий співробітник відділення пластичної та реконструктивної онкоурології Національного інституту раку (м. Київ), кандидат медичних наук Олег Анатолійович Войленко, завідувачка відділення хіміотерапії № 1 Київського міського клінічного онкологічного центру, доцент кафедри онкології Національного університету охорони здоров’я України імені П.Л. Шупика, кандидат медичних наук Ольга Володимирівна Пономарьова та лікар-онколог, хіміотерапевт Медичного центру «Клініка Мануфактура» Ярослав Миколайович Куляба.
Варто зазначити, що доповіді О.А. Войленка та О.В. Пономарьової були також представлені на цьогорічній науково-практичній конференції «Рак нирки та сечовивідних шляхів – update», учасниками якої стали фахівці з усієї України.
 Олег Анатолійович Войленко розповів про оновлену стратегію системного лікування при метастатичному раку нирки в еру таргетної та імунної терапії.
Олег Анатолійович Войленко розповів про оновлену стратегію системного лікування при метастатичному раку нирки в еру таргетної та імунної терапії.
– Рак нирки посідає 10-те місце у світі за рівнем захворюваності на всі злоякісні новоутворення. Найпоширенішою формою раку нирки є нирковоклітинний рак (НКР). Згідно з даними GLOBOCAN за 2020 р., щорічно у світі реєструється понад 431 тис. нових випадків НКР та помирають від нього понад 179 тис. осіб. При цьому приблизно у 70% випадків діагностується неметастатичний НКР, а у 30% – первинно метастатичний НКР (мНКР). Проте у 30% осіб із первинно діагностованим неметастатичним НКР згодом відбувається прогресування хвороби із розвитком метастазів (GLOBOCAN, 2020).
Останнім часом спостерігається значний прогрес у лікуванні НКР, про що свідчить збільшення 5-річної виживаності пацієнтів із 50,1% у 1970-1977 рр. до 74,1% у 2007-2013 рр. Відомо, що до появи перших таргетних препаратів медіана загальної виживаності (ЗВ) становила 13-18 міс, а після їх впровадження зросла до 19-26 міс (R.J. Motzer et al., 2009). Наступним кроком стало застосування комбінованого лікування із подальшою таргетною терапією, що сприяло збільшеню ЗВ до 36 міс (D.Y. Heng et al., 2013). Варто зазначити, що 2020 р. вважається початком нового етапу лікування НКР – так званої ери імунної терапії, від якої очікують подальшого збільшення ЗВ (B.I. Rini et al., 2019).
Після створення критеріїв Memorial Sloan Kettering Cancer Center (MSKCC) Міжнародним консорціумом баз даних із мНКР (International Metastatic RCC Database Consortium, IMDC) розроблена модель ризиків, що сприяє точнішому визначенню прогнозу для пацієнтів з мНКР, які отримують лікування таргетними препаратами. Система IMDC базується на аналізі 190 публікацій із включенням понад 80 тис. пацієнтів та полягає у визначенні таких параметрів, як статус за шкалою Карновського <80%, час від встановлення діагнозу до початку терапії <1 року, рівень гемоглобіну нижчий за нижню межу норми, рівень коригованого кальцію сироватки крові ≥10 мг/дл (2,4 ммоль/л) та абсолютне число нейтрофілів і тромбоцитів, що перевищує верхню межу норми. Відсутність у пацієнтів зазначених вище факторів свідчить про їх належність до групи низького ризику із медіаною ЗВ 43,3 міс, наявність 1-2 факторів – до групи проміжного ризику із вдвічі меншою медіаною ЗВ – 22,5 міс, а 3 і більше факторів – до групи високого ризику із медіаною ЗВ лише 7,8 міс. При цьому 2-річна виживаність у групах низького, проміжного та високого ризику складає 75; 53 та 7% відповідно. Визначення групи ризику при мНКР необхідне для вибору подальшої тактики таргетної терапії.
Згідно з рекомендаціями Європейської асоціації урологів (EAU Guidelines) 2019 р., для пацієнтів з НКР, які належать до групи низького ризику, першою лінією лікування є сунітиніб і пазопаніб, а для груп проміжного та високого ризику – кабозантиніб (Кабометикс®, ІPSEN PHARMA), сунітиніб чи пазопаніб або комбінація іпілімумабу з ніволумабом (EAU Renal Cell Carcinoma (RCC) Guidelines, 2019). Проте у 2020 р. стандарти лікування змінилися. Сьогодні першою лінією лікування пацієнтів груп низького та високого ризику є імунотерапія та її поєднання із таргетною терапією. Таким чином, пембролізумаб з акситинібом рекомендовані для лікування пацієнтів групи низького ризику, а при проміжному та високому ризику рекомендується приєднання до них іпілімумабу з ніволумабом. Проте враховуючи, що така терапія є дорогою та може зумовлювати специфічні побічні явища, альтернативним лікуванням залишається призначення сунітинібу та пазопанібу незалежно від групи ризику та кабозантинібу (Кабометикс®) у групах проміжного та високого ризику (EAU RCC Guidelines, 2020).
Аналіз результатів міжнародного рандомізованого клінічного дослідження III фази, проведеного за участю 750 пацієнтів із мНКР, які отримували сунітиніб (n=375) або інтерферон (ІФН)‑α (n=375), продемонстрував достовірно вищу медіану ЗВ у групі сунітинібу порівняно з групою ІФН‑α (26,4 і 21,81 міс відповідно), а також виживаності без прогресування (ВБП) – 11 проти 5 міс відповідно (R.J. Motzer et al., 2009). Щодо пазопанібу, то варто зазначити, що його ефективність вивчали лише у порівнянні з плацебо. При цьому медіана ВБП була вищою у групі пазопанібу та сягала 9,2 міс порівняно з 4,2 міс у групі плацебо (95% довірчий інтервал – ДІ – 0,34-0,62; C.N. Sternberg et al., 2010).
Ефективність кабозантинібу (Кабометикс®) при мНКР вивчали у рандомізованому клінічному дослідженні ІІ фази CABOSUN, у якому її порівнювали з такою еталонного препарату сунітинібу. Особливістю цього дослідження стало включення пацієнтів із проміжним і високим ризиком. При оцінюванні результатів ВБП у середньому становила 8,2 міс у пацієнтів, які приймали кабозантиніб, та 5,6 міс у хворих, які застосовували сунітиніб. ЗВ також була вищою у групі кабозантинібу, проте статистичної достовірності не досягнуто. При оцінюванні частоти побічних явищ не відмічено значущої різниці між групами кабозантинібу та сунітинібу (T.K. Choueiri et al., 2017).
Наступним етапом лікування мНКР стало застосування імунної терапії. Сьогодні найдокладніше вивчені інгібітори рецепторів Т-клітин CTLA‑4 (cytotoxic T-lymphocyte associated protein 4) і PD‑1 (рrogrammed cell death pathway) та його ліганда PD-L1. PD‑1 є регуляторним рецептором, який експресується на поверхні активованих Т-лімфоцитів.
У дослідженні III фази CheckMate 214 із включенням 1096 хворих на мНКР порівнювали ефективність комбінації ніволумабу та іпілімумабу з сунітинібом. Пацієнти були рандомізовані на 2 групи у співвідношенні 1:1, у кожній 425 та 422 пацієнти відповідно належали до груп проміжного або високого ризику. Згідно з результатами дослідження, комбінація ніволумабу з іпілімумабом продемонструвала достовірну перевагу щодо ЗВ порівняно з сунітинібом у пацієнтів із проміжним або високим ризиком: 12-місячна ЗВ склала 80% (95% ДІ 76-84) та 72% (95% ДІ 67-76); 18-місячна ЗВ – 75% (95% ДІ 70-78) та 60% (95% ДІ 55-65) відповідно (відносний ризик – ВР – 0,63; 99,8% ДІ 0,44-0,89; p<0,001). Медіана ВБП сягала 11,6 міс (95% ДІ 8,7-15,5) у групі ніволумабу з іпілімумабом та 8,4 міс (95% ДІ 7,0-10,8) у групі сунітинібу, проте ця різниця була статистично недостовірна (ВР 0,82; 99,1% ДІ 0,64-1,05; p=0,03). Частота об’єктивної відповіді (ОВ) склала 42% (95% ДІ 37-47) при застосуванні комбінованої імунотерапії та 27% (95% ДІ 22-31) при використанні сунітинібу (р<0,001), при цьому частота повної відповіді дорівнювала 9 та 1% відповідно (R.J. Motzer et al., 2018).
Нещодавно були представлені результати багатоцентрового рандомізованого дослідження ІІІ фази KEYNOTE‑426, у якому порівнювали застосування інгібітора контрольних точок пембролізумабу у комбінації із таргетним препаратом акситинібом та сунітинібу. До групи комбінованого лікування включено 432 пацієнти, сунітинібу – 429 пацієнтів. Основна частина хворих, а саме 484 особи, належала до групи проміжного ризику, третина – до групи низького ризику та 108 осіб – до групи високого ризику за критеріями IMDC. При медіані спостереження 12,8 міс медіана ЗВ досягнута не була. Вісімнадцятимісячна ЗВ у групах комбінованого лікування та сунітинібу склала 82,3% (95% ДІ 77,2-86,3) та 72,1% (95% ДІ 66,3-77,0) відповідно. Медіана ВБП сягала 15,1 міс у групі пембролізумабу з акситинібом та 11,1 міс у групі сунітинібу (ВР 0,69; 95% ДІ 0,57-0,84; P<0,001).
Частота ОВ склала 59,3% для групи комбінованого лікування та 35,7% – сунітинібу, а повна відповідь була досягнута у 5,8 та 1,9% пацієнтів відповідно. Таким чином, сьогодні, згідно з рекомендаціями EAU (2020), стандартом першої лінії терапії вважається комбінація пембролізумабу з акситинібом для всіх груп ризику, а для груп проміжного та високого ризику – комбінація ніволумабу з іпілімумабом. Альтернативним варіантом залишається терапія сунітинібом з пазопанібом для хворих усіх груп, а для пацієнтів групи проміжного та високого ризику препаратом вибору, який продемонстрував вищу ефективність порівняно з сунітинібом у зазначених групах, є кабозантиніб (Кабометикс®).
Отже, ера таргетної та імунної терапії перевела боротьбу з мНКР на новий рівень. Подальші розробки, зосереджені на подоланні механізмів резистентності, дозволять покращити клінічні результати ЗВ пацієнтів, а вивчення нових агентів, спрямованих на ланку імунної відповіді, персоналізований підбір препаратів на основі дослідження антигенного статусу пухлини, груп ризику, комбінацій і послідовностей застосування різних препаратів, необхідні для покращення виживаності пацієнтів з мНКР.
.jpg) Ольга Володимирівна Пономарьова представила аналіз міжнародних рекомендацій щодо системного лікування поширеного раку нирки.
Ольга Володимирівна Пономарьова представила аналіз міжнародних рекомендацій щодо системного лікування поширеного раку нирки.
– Рак нирки становить 2-3% усіх випадків онкологічної патології у дорослих (B. Escudier et al., 2014; B. Ljungberg et al., 2015). При цьому 90% всіх первинних злоякісних новоутворень нирки представлені саме НКР (B. Ljungberg et al., 2015; NCCN Guidelines, 2016).
Варто зазначити, що у великої кількості пацієнтів відсутні будь-які прояви аж до пізніх стадій захворювання, при цьому класичну тріаду – біль у попереку, гематурію та абдомінальне утворення – виявляють лише у 6-10% пацієнтів (B. Ljungberg et al., 2015).
У пацієнтів з НКР визначають підвищення експресії ендотеліального фактора росту судин (VEGF) та її кореляцію із щільністю мікросудин, яка відображає інтенсивність ангіогенезу (G. Banumathy et al., 2010). Після активації індукованого гіпоксією фактора VEGF активується і зв’язується з рецептором (VEGFR) на поверхнях ендотеліальних клітин, що сприяє міграції та проліферації ендотеліальних клітин і є необхідним для розвитку нових пухлинних кровоносних судин (G. Banumathy et al., 2010; R. Pili et al., 2014; B.I. Rini et al., 2009). З огляду на ключову роль VEGF та VEGFR в ангіогенезі пухлин вони стали молекулярними мішенями для нових методів терапії при НКР (W.M. Linehan et al., 2011). Як блокатор VEGF упродовж багатьох років використовували бевацизумаб, а блокатором VEGFR став кабозантиніб (Кабометикс®).
Наявні декілька сигнальних шляхів, що активують рецептори тирозинкінази, такі як hepatocyte growth factor (MET) та growth arrest-specific protein 6 (AXL; T.K. Choueiri et al., 2015). Втрата експресії гена-супресора VHL, його мутація та гіпоксія спричиняють активацію МЕТ. Зрештою порушення регуляції МЕТ сприяє розвитку пухлини, інвазії та ангіогенезу (G.T. Gibney et al., 2013). Експресія AXL безпосередньо активується шляхами HIF‑1 і HIF‑2 та корелює з агресивною поведінкою пухлини й підвищеним ризиком смерті пацієнтів (E.B. Rankin et al., 2014). Відомо, що підвищена експресія МЕТ та AXL при НКР корелює з поганим прогнозом і резистентністю до інгібіторів VEGFR (T.K. Choueiri et al., 2015; E.B. Rankin et al., 2014).
Як вже було сказано, за клінічними рекомендаціями Національної онкологічної мережі США (NCCN, 2020) як перша лінія лікування пацієнтів із рецидивом чи IV стадією НКР, високим ризиком за IMDC показане застосування комбінації акситинібу з пембролізумабом або кабозантинібу (Кабометикс®).
Молекулярні мішені різних інгібіторів тирозинкінази, які використовуються для лікування НКР, є різноманітними. Найбільшу кількість точок прикладання має кабозантиніб. Відомо, що різні інгібітори тирозинкінази зв’язують 3 ізоформи рецептора VEGFR, проте афінність зв’язування відрізняється. Для кабозантинібу, акситинібу та ленватинібу характерне збереження активності після розвитку резистентності до сунітинібу й пазопанібу. Окрім VEGFR, спектр мішеней дії антиангіогенних інгібіторів тирозинкінази різниться (S. Weitzman, M. Cabanillas, 2015; E.M. Posadas et al., 2017; D.D. Hu-Lowe et al., 2008).
Кабозантиніб (Кабометикс®) є низькомолекулярним інгібітором різних рецепторів тирозинкінази, таких як MET, AXL та VEGFR‑1, ‑2, ‑3, та забезпечує багатоцільовий (multi-targeted) підхід при лікуванні НКР. Така властивість кабозантинібу може сприяти подоланню резистентності до інгібіторів VEGFR.
У рандомізованому багатоцентровому відкритому клінічному дослідженні ІІ фази CABOSUN оцінювали ефективність та безпеку застосування кабозантинібу у дозі 60 мг/добу перорально впродовж 6 тижнів порівняно з такими сунітинібу у дозі 50 мг/добу за схемою 4/2 (4 тижні з інтервалом між циклами 2 тижні) у пацієнтів з місцево-поширеним та/або метастатичним НКР, які раніше не отримували системну терапію. Згідно з дизайном, у дослідження включали хворих віком ≥18 років з наявністю вимірюваних пухлинних вогнищ за критеріями RECIST v.1.1, проміжного та високого ризику за IMDC (за відсутності активних метастазів у головному мозку) та оцінки загального стану 0-2 бали за шкалою Східної об’єднаної онкологічної групи (ECOG). Первинною кінцевою точкою була ВБП, вторинними – ЗВ, частота ОВ та безпека (T.K. Choueiri et al., 2017; 2018). Прийом кабозантинібу достовірно збільшував ВБП порівняно з сунітинібом (8,6 проти 5,3 міс відповідно), знижуючи при цьому ризик прогресування захворювання на 52% (ВР 0,48; 95% ДІ 0,31-0,74; рис. 1).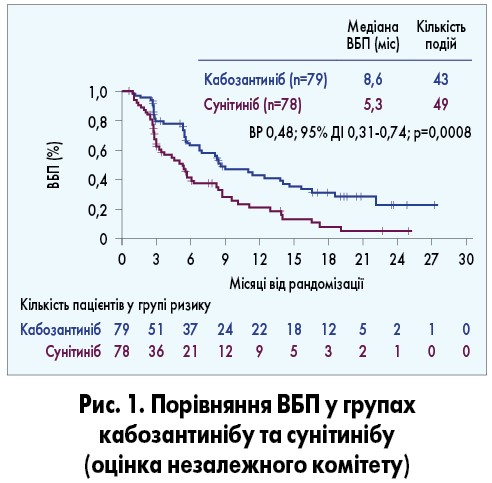
Частота ОВ сягала 20% (95% ДІ 12,0-30,8) у групі кабозантинібу та 9% (95% ДІ 3,7-17,6) – сунітинібу, а частота контролю захворювання (повна + часткова відповідь + стабілізація захворювання) – 75 та 47% відповідно. Згідно з оцінкою дослідника, будь-яке зменшення розміру пухлинних вогнищ частіше реєструвалось на фоні прийому кабозантинібу (87%), ніж сунітинібу (44%; рис. 2; T.K. Choueiri et al., 2018).
Медіана ЗВ у групі кабозантинібу сягала 26,6 міс (95% ДІ 14,6 – не досягнуто), а у групі сунітинібу – 21,2 міс (95% ДІ 16,3-27,4; T.K. Choueiri et al., 2018).
Частота побічних явищ 3-4 ступеня між групами кабозантинібу та сунітинібу була зіставна (68 та 65% відповідно). Варто зазначити, що перевага кабозантинібу зберігалась незалежно від групи ризику за IMDC. Так, зокрема, у групі проміжного ризику (n=127) медіана ВБП у пацієнтів, що приймали кабозантиніб, сягала 11,4 міс, що значно більше, ніж у хворих, які отримували сунітиніб, – 6,1 міс (ВР 0,52; 95% ДІ 0,32-0,82). У невеликій групі високого ризику (n=30) ці показники склали 6,8 та 2,7 міс відповідно (ВР 0,31; 95% ДІ 0,11-0,92).
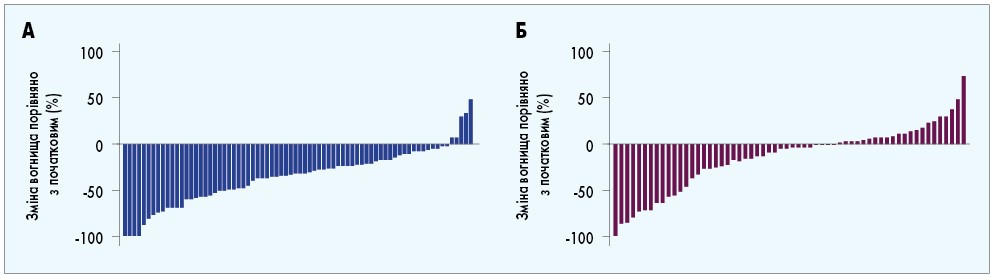 Рис. 2. Зменшення розміру таргетних вогнищ при терапії кабозантинібом (А) та сунітинібом (Б) за оцінкою дослідника
Рис. 2. Зменшення розміру таргетних вогнищ при терапії кабозантинібом (А) та сунітинібом (Б) за оцінкою дослідника
У рандомізованому клінічному дослідженні III фази METEOR проводилось порівняння кабозантинібу (60 мг/добу) й еверолімусу (10 мг/добу) у другій лінії терапії НКР (при прогресуванні хвороби на фоні чи після першої або другої лінії VEGF-таргетної терапії). У цьому дослідженні прийом кабозантинібу сприяв достовірному підвищенню ВБП та ЗВ, при цьому його перевага у відношенні ЗВ та ВБП зберігалася незалежно від групи ризику за MSKCC (T.K. Choueiri et al., 2016).
Імовірно, у майбутньому терапія при мНКР полягатиме у призначенні комбінованого лікування з використанням таргетних та імунних препаратів (інгібіторів контрольних точок) вже у першій лінії. Наразі проводиться низка клінічних досліджень з комбінаціями препаратів для лікування мНКР і найближчими роками очікуються їх результати.
Викликає інтерес дослідження, у якому вивчали безпеку й ефективність терапії кабозантинібом у пацієнтів із НКР та метастазуванням у центральну нервову систему (ЦНС) у реальній популяції. У дослідження було включено 12 пацієнтів із підтвердженими метастазами у ЦНС, які попередньо отримували щонайменше одну лінію терапії інгібіторами тирозинкінази. Дев’ять пацієнтів приймали кабозантиніб у дозі 60 мг/добу, а 3 – у дозі 40 мг/добу у зв’язку з їх незадовільним соматичним станом. Частота ОВ склала 50%, а частота контролю захворювання – 75%. Медіана ВБП і ЗВ сягала 5,8 та 8,8 міс відповідно, а однорічна ЗВ – 50% (G. Peverelli et al., 2019).
 Ярослав Миколайович Куляба представив клінічний випадок із власної практики.
Ярослав Миколайович Куляба представив клінічний випадок із власної практики.
Клінічний випадок
– Пацієнтка, 74 роки. Уперше звернулася за медичною допомогою у 2019 р., коли під час проведення комп’ютерної томографії (КТ) органів грудної клітки (ОГК), черевної порожнини (ЧП) та малого таза (МТ) із внутрішньовенним контрастуванням було виявлено ознаки неопластичного процесу правої нирки з інвазією листків фасції Герота та неможливістю виключення залучення капсули печінки на рівні VI‑VII сегментів, вторинну заочеревинну лімфаденопатію, вторинне ураження легень і поодинокі остеосклеротичні вогнища у ділянці тіла хребця F2 та тіла клубової кістки, які потребували динамічного спостереження.
12 лютого 2019 р. проведено позитронно-емісійну комп’ютерну томографію (ПЕТ-КТ), яка підтвердила метастатичне ураження легень.
20 лютого 2019 р., після правобічної лапароскопічної нефроадреналектомії встановлено діагноз світлоклітинна нирковоклітинна карцинома правої нирки pT3apN1(1/1)М1(pulm), правобічна лапароскопічна нефроадреналектомія 20.02.2020 (LVI0, Pn0, Ro). На післяопераційній КТ ОГК, ЧП і МТ візуалізувався один паракавальний лімфатичний вузол, розмір якого збільшився порівняно з попереднім дослідженням і становив 1,3 см у діаметрі. Динаміка метастатичних вузлів у легенях відсутня, в обох легенях зберігались множинні солідні вузли діаметром 0,3‑1,2 см.
Враховуючи отримані дані, як першу лінію лікування було призначено сунітиніб у дозі 50 мг/добу за схемою 4/2 (4 тижні з інтервалом між циклами 2 тижні). Була досягнута часткова відповідь на терапію сунітинібом, про що свідчило зменшення діаметра паракавального лімфатичного вузла до 9,5 мм та вогнищ у легенях до 5-8 мм.
10 червня 2019 р. при остеосцинтиграфії типових для вторинного ураження змін не виявлено. Під час контрольної КТ після 4 та 6 курсів терапії сунітинібом динаміки не виявлено. Проте після 8-го курсу лікування хвороба прогресувала, про що, зокрема, свідчило збільшення кількості та розмірів множинних патологічно змінених парааортокавальних лімфатичних вузлів, множинних солідних вузлів у легенях і вузлів середостіння, а також розвиток ексудативного правобічного плевриту. Варто відмітити, що загальний стан пацієнтки при цьому залишався задовільним, а серед побічних ефектів спостерігалося контрольоване підвищення артеріального тиску та долонно-підошвовий синдром. Таким чином, тривалість терапії сунітинібом склала 11 міс.
2 лютого 2020 р. розпочато другу лінію терапії із застосуванням еверолімусу 10 мг 1 раз на добу, проте лікування було припинене через 2 міс у зв’язку з вираженими побічними явищами (погіршення загального стану, носові кровотечі, кашель, задишка, шкірний висип і періодичне підвищення температури тіла). Прогресування хвороби також було підтверджене при проведенні контрольної КТ.
Для третьої лінії терапії було обрано пембролізумаб 200 мг 1 раз на 3 тижні у комбінації із акситинібом 5 мг 2 рази на добу. На фоні застосування цієї комбінації побічних ефектів не спостерігалося, загальний стан хворої залишався відносно задовільним, проте терапія була припинена через 2,5 міс у зв’язку із значним прогресуванням, виявленим при проведенні КТ.
У липні 2020 р. пацієнтка почала отримувати четверту лінію терапії – препарат Кабометикс® (кабозантиніб) у дозі 60 мг 1 раз на добу. Через 2,5 міс лікування кабозантинібом при проведенні контрольної КТ було підтверджено виражену позитивну динаміку та отримано часткову відповідь на терапію за критеріями RECIST v.1.1. Зокрема, було відмічено зменшення на 75% або розрішення вузлових утворень у легенях, плеврі, а також лімфатичних вузлів грудної порожнини, ЧП і МТ. Ознак накопичення випоту у плевральній порожнині не було. Через 5 міс прийому препарату стан хворої залишався задовільним, відхилень лабораторних показників не відмічалось. Проте при проведенні контрольної КТ було виявлено скупчення рідини у правій плевральній порожнині товщиною до 35 мм, появу рідини у порожнині перикарда і збільшення деяких вузлів середостіння та заочеревинного простору на 3-5 мм, що може бути пов’язано із розвитком гіпотиреозу як наслідку імунотерапії.
Було розпочато терапію гіпотиреозу на фоні прийому кабозантинібу. Серед побічних явищ можна відмітити періодичне підвищення артеріального тиску, слабо виражений долонно-підошвовий синдром і періодичну діарею із частотою дефекації до 3-4 разів на добу. Наразі продовжується динамічне спостереження та розглядаються можливі варіанти подальшого ведення пацієнтки.
Отже, згідно з даними клінічних досліджень і клінічної практики, приблизно 2/3 пацієнтів із мНКР первинно належать до групи проміжного та високого ризику. При цьому ще у частини хворих, які попередньо належали до групи низького ризику, захворювання все ж прогресує, а ризик змінюється на проміжний чи високий. Кабозантиніб (Кабометикс®) є препаратом, який продемонстрував вищу ефективність порівняно з сунітинібом у цих групах і був включений у клінічні рекомендації NCCN, EAU, ESMO як перша та друга лінія терапії при світлоклітинному НКР, переважно для лікування пацієнтів з проміжним і високим ризиком. Кабозантиніб (Кабометикс®) продемонстрував достатній рівень безпеки, прийнятну переносимість та обнадійливий протипухлинний ефект у хворих із метастатичним ураженням ЦНС при мНКР.
Підготувала Ольга Нестеровська
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 1 (68) 2021 р.



