22 березня, 2017
Эверолимус в лечении пациентов с субэпендимальными гигантоклеточными астроцитомами, ангиомиолипомами и поражениями легких или кожи, ассоциированными с туберозным склерозом

Выявление молекулярных путей и этиологических факторов, обусловливающих развитие туберозного склероза (ТС), привело к изменению парадигмы ведения пациентов и появлению новых методов лечения. Вследствие мутации генов TSC1 и TSC2 конститутивное нарушение регуляции сигнального пути мишени рапамицина у млекопитающих (mTOR) привело к изменению многих клеточных процессов, участвующих в росте различных опухолей. Ингибирующее воздействие на mTOR посредством применения эверолимуса, активного производного рапамицина, обеспечивает клинически значимое и статистически достоверное уменьшение опухолевой массы очагов поражения мозга (субэпендимальная гигантоклеточная астроцитома) и почек (ангиомиолипома), ассоциированных с ТС.
У пациентов, страдающих ТС, наблюдаются тяжелые инвалидизирующие нарушения, ассоциированные с многочисленными доброкачественными опухолями (гамартомами), наиболее часто локализованными в мозге, почках, легких, поражающими кожу.
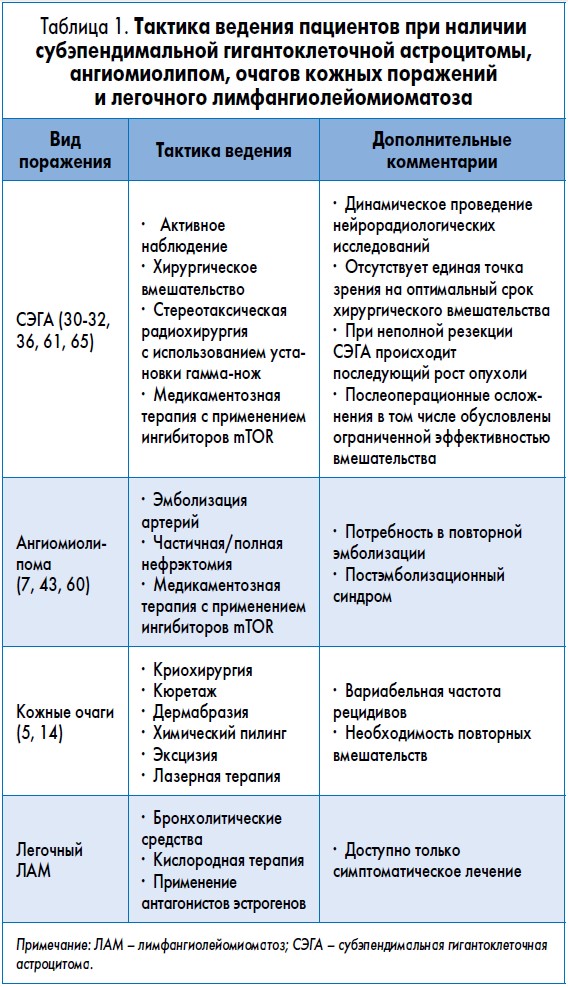
Подкомитетом консенсусной конференции (Tuberous Sclerosis Complex Clinical Consensus Conference) были рассмотрены и внесены изменения в рекомендации по наблюдению и тактике ведения пациентов с ТС. В руководствах по ведению пациентов с ТС представлены рекомендации, касающиеся скрининга и последующих обследований, а также сроки проведения клинических обследований, что поможет стандартизировать и совершенствовать медицинскую помощь пациентам. В соответствии с исторически сложившейся традицией ведение пациентов с гамартомами, ассоциированными с ТС, заключалось в комбинации активного и тщательного наблюдения, симптоматической медикаментозной терапии и хирургических вмешательств для уменьшения массы опухоли. До недавнего времени наиболее частым лечением при ряде форм ТС была хирургия. Отсутствие эффективного медикаментозного средства явилось причиной выжидательной тактики при лечении ТС. Только с появлением mTOR-блокаторов данная парадигма лечения была изменена и медикаментозная терапия была включена в международные рекомендации (табл. 1).
Ведущая роль сигнальных путей mTOR в этиологии ТС послужила основанием для применения ингибиторов mTOR в качестве таргетной терапии. Эверолимус снижает уровень фосфорилирования нисходящих эффекторов сигнального пути mTOR, ингибирует внутриклеточный сигнальный путь, который приводит к клеточной пролиферации. Блокада этого сигнала эверолимусом приводит к остановке деления клеток на стадии G1 клеточного цикла.
Фармакокинетические характеристики эверолимуса
 При приеме здоровыми добровольцами эверолимус быстро абсорбируется (на протяжении 30 мин), его максимальная концентрация в плазме крови составляет 44,2±13,3 мкг/л после приема однократной дозой. Время до достижения максимальной концентрации в крови (Tmax) при приеме препарата в дозе 4 мг составляет 0,5 ч (в диапазоне 0,5-1 ч). При приеме эверолимуса взрослыми пациентами в дозе 5 или 10 мг 1 раз в сутки время абсорбции составляет 1 ч. Среднее значение максимальной равновесной концентрации в крови составляет 32 нг/л (9 нг/л) и 61 нг/л (17 нг/д) при приеме в дозе 5 и 10 мг соответственно. Медиана времени до достижения максимальной концентрации составляет 1 ч. Пища с высоким содержанием жиров увеличивает среднее время до достижения максимальной концентрации на 1,25 ч и снижает максимальную концентрацию в сыворотке крови на 60%. Поэтому для предотвращения колебаний терапевтического действия эверолимуса его следует принимать натощак или с легкой пищей.
При приеме здоровыми добровольцами эверолимус быстро абсорбируется (на протяжении 30 мин), его максимальная концентрация в плазме крови составляет 44,2±13,3 мкг/л после приема однократной дозой. Время до достижения максимальной концентрации в крови (Tmax) при приеме препарата в дозе 4 мг составляет 0,5 ч (в диапазоне 0,5-1 ч). При приеме эверолимуса взрослыми пациентами в дозе 5 или 10 мг 1 раз в сутки время абсорбции составляет 1 ч. Среднее значение максимальной равновесной концентрации в крови составляет 32 нг/л (9 нг/л) и 61 нг/л (17 нг/д) при приеме в дозе 5 и 10 мг соответственно. Медиана времени до достижения максимальной концентрации составляет 1 ч. Пища с высоким содержанием жиров увеличивает среднее время до достижения максимальной концентрации на 1,25 ч и снижает максимальную концентрацию в сыворотке крови на 60%. Поэтому для предотвращения колебаний терапевтического действия эверолимуса его следует принимать натощак или с легкой пищей.
Эверолимус – субстрат изофермента CYP3A4 и Р-гликопротеина. Следовательно, одновременный прием с ингибиторами или активаторами изоферментов CYP3A4 влияет на его метаболическое преобразование, которое преимущественно происходит в кишечнике.
Эверолимус выводится главным образом с желчью, в меньшей степени с мочой. Средний период полувыведения составляет приблизительно 30 ч. При приеме здоровыми добровольцами средний период полувыведения эверолимуса при приеме в дозе 4 мг составил 32,2±6 ч. У пациентов с нарушением функций печени экспозиция эверолимуса увеличивается. Степень увеличения экспозиции зависит от степени тяжести нарушения функций печени – низкой, средней или высокой. При приеме пациентами, страдающими ТС, с СЭГА и/или ангиомиолипомой при наличии нарушения функций печени низкой или средней степени тяжести необходима коррекция дозы. Если польза превышает риск, допустимо назначение эверолимуса пациентам с почечной ангиомиолипомой, ассоциированной с ТС, даже при наличии нарушения функций печени высокой степени тяжести. Не рекомендуется применение эверолимуса у пациентов с СЭГА при наличии нарушения функций печени высокой степени тяжести.
Клиническая эффективность
Эффективность применения эверолимуса в терапии пациентов, страдающих ТС, впервые была продемонстрирована в открытом клиническом исследовании I/II фазы, проведенном с включением 28 пациентов с СЭГА, ассоциированной с ТС (NCT00411609). Основной период исследования длился 6 мес, после чего пациенты имели возможность продолжить лечение в рамках дополнительного этапа. На основании результатов данного исследования эверолимус был утвержден Управлением по конролю качества пищевых продуктов и лекарственных средств США (FDA) для применения в терапии пациентов с СЭГА, ассоциированной с ТС. Это исследование было первым, ходе которого продемонстрировано уменьшение размеров СЭГА в течение первых трех месяцев терапии и дальнейшее сохранение достигнутого эффекта. Пациенты в возрасте 3-34 лет получали эверолимус в начальной дозе 3 мг/м2 с последующим ее увеличением до уровня, обеспечивающего минимальную концентрацию в цельной крови 5-15 нг/мл. Средняя продолжительность лечения составляла 21,5 мес (диапазон 4,7-34,4 мес). Было достигнуто клинически значимое уменьшение объема первичных СЭГА, по оценке независимых экспертов, медиана сокращения составляла –0,8 см3 (95% доверительный интервал (ДИ) 0,4-1,2; p<0,001). Сообщения о новых очагах, повышении внутричерепного давления, увеличении степени тяжести гидроцефалии головного мозга, потребности в хирургической резекции или консервативной терапии отсутствовали. Получение эверолимуса ассоциировалось с достоверным уменьшением общей частоты клинических и субклинических эпилептических приступов (среднее изменение –1 приступ: р=0,02). Показатели по шкале оценки качества жизни детей с эпилепсией со временем улучшились (58,74±14 – до начала лечения; 63,4±12,4 – через 3 мес; 62,1±14,2 – через 6 мес). Результаты терапии, проводившейся на протяжении последующих трех лет, в ходе дополнительного этапа исследования недавно были опубликованы Krueger и соавт. Из 28 пациентов, включенных в основной этап исследования, 25 пациентам продолжали лечение в дополнительном трехлетнем этапе исследования вплоть до завершения сбора данных. После продолжения лечения медианной длительностью 34,2 мес начальный объем СЭГА (до начала лечения) 1,74 см3 через 36 мес снизился до 0,97 см3. Уменьшение объема на ≥30% в сравнении со значением до начала лечения через 24, 30 и 36 мес выявлено у 79,2; 64,7 и 77,8% пациентов соответственно, а уменьшение на ≥50% в те же периоды выявлено у 50; 41,2 и 55,6% пациентов соответственно. Через 24 мес уменьшение ангиофибром лица в сравнении с показателями при предыдущем посещении было отмечено у 8 из 9 пациентов (88,9%). Анализ данных подгрупп пациентов, включенных в исследование, показал достоверное изменение рассеяния белого вещества головного мозга у пациентов, получавших эверолимус, что свидетельствует о том, что лечение обеспечивает снижение поражения белого вещества головного мозга, вызванного генетическим нарушением, у пациентов, страдающих ТС. Отмечены достоверные изменения показателей фракционной анизотропии и радиальной диффузии в мозолистом теле, внутренней капсуле и коленчато-затылочном участке головного мозга пациентов, получавших эверолимус, тогда как у пациентов с ТС, соответствующих по возрасту и полу, из контрольной группы изменения отсутствовали. Средние (при 95% ДИ) показатели фракционной анизотропии после 12-18 мес получения эверолимуса (р<0,05) достоверно увеличились – на 0,04 (0,019-0,062) во всех трех областях головного мозга, что обусловлено уменьшением радиальной диффузии в мозолистом теле и коленчато-затылочном участке головного мозга (р<0,01 для каждой из областей).
Дальнейшие подтверждения эффективности эверолимуса получены в исследованиях III фазы EXIST-1 и EXIST-2 (табл. 2). Выборки пациентов в этих исследованиях репрезентативны с точки зрения эпидемиологии заболевания.
Безопасность и переносимость
Профиль безопасности эверолимуса, установленный во всех трех клинических исследованиях, был сопоставимым: тяжесть большинства нежелательных явлений (НЯ) не превышала 1 или 2 степени.
Стоматит (79%) и инфекционные заболевания верхних дыхательных путей (79%) были наиболее частыми НЯ в исследовании І/ІІ фазы; НЯ 3 степени тяжести отмечены у 10 пациентов, у одного отмечено одно явление (эпилепсия) 4 степени тяжести. Нарушений по результатам лабораторных анализов не было, за исключением повышения концентрации общего холестерина, липопротеинов низкой плотности и триглицеридов. Профиль безопасности, установленный в дополнительном этапе исследования, соответствует выводам анализа данных основного этапа. Ни один из пациентов не был отстранен от терапии эверолимусом в связи с НЯ – как в исследовании І/ІІ фазы, так и в исследовании EXIST-1; несколько пациентов в связи с НЯ прекратили участие в исследовании EXIST-2. Причинами отстранения от участия в исследовании пациентов из группы эверолимуса стал один случай уменьшения содержания фосфора в крови 2 степени тяжести; один пациент был отстранен в связи с повышенной чувствительностью к препарату 3 степени тяжести, ангионевротическим отеком 3 степени тяжести и бронхоспазмом 3 степени тяжести; еще один пациент был отстранен в связи со стойкими эпилептическими припадками, предположительно, имеющими причинно-следственную связь с исследуемым препаратом. В исследовании EXIST-1 наиболее частыми НЯ, отмеченными в группе эверолимуса и плацебо соответственно, были язвенный стоматит (32 и 5%), стоматит (31 и 21%), эпилептические припадки (23 и 26%) и пирексия (22 и 15%). Наиболее частыми НЯ 3 степени тяжести, отмеченными в группе эверолимуса и плацебо соответственно, были стоматит (8 и 3%), пирексия (6 и 0%) и эпилептические припадки (5 и 5%). В исследовании EXIST-2 наиболее частыми НЯ, отмеченными в группе эверолимуса и плацебо, были стоматит (48 и 8% соответственно), назофарингит (24 и 31%), угревая сыпь (22 и 5%) и головная боль (22 и 18%). Наиболее частыми НЯ 3 степени тяжести были афтозный и язвенный стоматит, которые развивались у 3% пациентов из группы эверолимуса и не были отмечены в группе плацебо. Явления 4 степени тяжести в обоих исследованиях наблюдались редко.
Следует отметить, что в исследованиях EXIST-1 и EXIST-2 зафиксировано несколько случаев вторичной аменореи. В ходе исследования EXIST-1 у трех из восьми девушек, получавших эверолимус, отмечены случаи аменореи, которая не наблюдалась в группе плацебо. В ходе исследования EXIST-2 случаи аменореи наблюдались у 7 из 52 пациенток из группы эверолимуса и у одной из 26 пациенток из группы плацебо. В связи с этим ведутся дальнейшие исследования возможности связи этого НЯ с получением эверолимуса.
Биомаркеры
Отсутствие регулирующих функций генов TSC1 и TSC2 ассоциируется с увеличением выработки факторов роста эндотелия сосудов (VEGF). Исследования показали, что ингибиторы mTOR угнетают выработку VEGF, рост опухолей и ангиогенез, как in vitro, так и in vivo.
В исследованиях EXIST-1 и EXIST-2 определялось воздействие эверолимуса на ряд ангиогенных биомаркеров. В сравнении с плацебо при получении эверолимуса в ходе обоих исследований отмечено устойчивое увеличение содержания VEGF-А – приблизительно на 30 и 60% соответственно. Параллельно отмечено снижение содержания коллагена IV типа (приблизительно на 25% в исследовании EXIST-1 и 45% в исследовании EXIST-2), а также растворимого рецептора VEGF (sVEGFR2) (приблизительно на 25% в обоих исследованиях). Стойкое снижение содержания рецепторов VEGF-D приблизительно на 60% отмечено у пациентов из группы эверолимуса в исследовании EXIST-2, однако не отмечено в исследовании EXIST-1. В обоих исследованиях у пациентов, получавших эверолимус, не зафиксировано изменений концентрации плацентного фактора роста, рецептора sVEGFR1 или c-Kit в плазме крови; изменения содержания ни одного из биомаркеров у пациентов из группы плацебо не выявлено. До начала лечения содержание рецепторов sVEGFR2 было больше на 40% и VEGF-D – выше в четыре раза, а рецепторов VEGF-А – приблизительно на 50% меньше у пациентов исследования EXIST-2 в сравнении с показателями, установленными в исследовании EXIST-1. Концентрация других биомаркеров в плазме крови пациентов, включенных в эти исследования, была одинаковой. Проведение дальнейших клинических исследований будет способствовать обеспечению определения новых прогностических биомаркеров, важных для оценки бремени заболевания, а также эффективности и безопасности терапии эверолимусом.
При ТС эверолимус утвержден к применению в терапии взрослых пациентов с почечной ангиомиолипомой, не требующей немедленного хирургического вмешательства, а также взрослых и детей в возрасте ≥3 лет с СЭГА, которым требуется терапевтическое, но не хирургическое вмешательство. Терапевтическая эффективность и безопасность эверолимуса подтверждены данными многоцентровых международных рандомизированных двойных слепых плацебо-контролируемых исследований. Продолжается проведение дополнительных этапов данных исследований для установления долговременной безопасности и эффективности эверолимуса в терапии пациентов с ТС. Ингибитор mTOR эверолимус является первым препаратом, утвержденным для медикаментозного лечения пациентов с ТС. Перспективность таргетной системной консервативной терапии с применением эверолимуса основана на ее эффективности при многочисленных проявлениях ТС и снижении интенсивности симптомов заболевания. В настоящее время эверолимус рассматривается как альтернатива хирургическим вмешательствам.
D.N. Franz. Everolimus in the treatment of subependymal giant cell astrocytomas, angiomyolipomas, and pulmonary
and skin lesions associated with tuberous sclerosis complex.
Biologics: Targets and Therapy 2013:7.
Подготовила Катерина Котенко






