16 січня, 2019
Лікування хвороб щитоподібної залози в загальній практиці
Хвороби щитоподібної залози (ЩЗ) можна розподілити на порушення функції (гіпо- та гіпертиреоз) і порушення структури (зоб, вузловий зоб, рак). Ведення таких пацієнтів зазвичай досить просте, але існують деякі типові помилки, що призводять до встановлення неправильного діагнозу, гіпердіагностики, невідповідного лікування.
У всьому світі провідною причиною хвороб ЩЗ є дефіцит йоду. Для боротьби із зазначеною проблемою в деяких країнах прийнято закон про обов’язкове застосування йодованої солі при виробництві хліба. Іншим поширеним фактором розвитку дисфункції ЩЗ є аутоімунні захворювання. Зокрема, в Австралії позитивні антитіла (АТ) до тканин ЩЗ виявляють у 10-15% населення. Зазвичай це АТ до тиреопероксидази (АТПО), які частіше є підвищеними в жінок, ніж у чоловіків. Еутиреоїдні пацієнти з позитивними АТ до тканин ЩЗ не потребують лікування, проте перебувають у групі підвищеного ризику розвитку дисфункції залози, особливо гіпотиреозу. У зв’язку з цим таким пацієнтам показане щорічне визначення сироваткового тиреотропного гормону (ТТГ), який є найбільш чутливим маркером порушень роботи ЩЗ. Прийнятими референтними значеннями норми ТТГ є 0,4-4,0 мОд/л. Концентрація ТТГ зростає з віком, тому деякі лабораторії застосовують вікові норми, в яких верхня межа становить до 7 мОд/л (для осіб старечого віку).
Гіпотиреоз
Класичними симптомами гіпотиреозу є втомлюваність, збільшення ваги, непереносимість холоду, болі в суглобах, закрепи, менорагія, сухість шкіри та волосся. Фізикальні ознаки включають блідість, загрубіння шкіри, брадикардію та зоб, які при помірному гіпотиреозі можуть бути відсутніми. Ці характеристики є неспецифічними та часто спостерігаються в осіб без хвороб ЩЗ, що зумовлює потребу в лабораторній діагностиці. Насамперед слід визначати сироватковий ТТГ. Якщо цей показник у межах норми, призначають додаткові тести: вільний тироксин (T4), вільний трийодтиронін (T3), рідше – антитіла до тканин ЩЗ. Визначення основного обміну та зворотного вільного T3 не має діагностичної цінності.
Клінічно виражений гіпотиреоз (високий ТТГ, низький вільний T4) зазвичай є симптоматичним, легко діагностується та потребує лікування. Проте частіше в загальній практиці спостерігається підвищений рівень ТТГ на тлі нормального T4, що може свідчити про субклінічний гіпотиреоз, спричинений аутоімунними захворюваннями ЩЗ чи системними захворюваннями нетиреоїдного походження, особливо у фазі реконвалесценції. У >50% пацієнтів з помірно підвищеним ТТГ (до 10 мОд/л) рівень цього гормону нормалізується без жодних втручань, тому не варто негайно призначати лікування хворим з такими показниками. Передусім потрібно повторити аналіз на ТТГ через 6-8 тиж, визначивши одночасно вільний T4 та АТПО, і рекомендувати лікування в разі повторного виявлення відхилень. За наявності гіпотиреозу візуалізаційні дослідження ЩЗ, у т. ч. ультразвукове дослідження (УЗД), не показані.
Важливість виявлення та лікування субклінічного гіпотиреозу досі залишається невизначеною. Рандомізовані контрольовані дослідження тироксину в таких осіб не виявили однозначного сприятливого впливу тиреоїдзамісної терапії на симптоми та якість життя, зокрема, у пацієнтів старшого віку та в разі помірного підвищення ТТГ (до 10 мОд/л). Однак показано, що нелікований субклінічний гіпотиреоз з рівнем ТТГ вище 10 мОд/л асоціюється з підвищеним ризиком розвитку кардіоваскулярних хвороб. Переваги лікування субклінічного гіпотиреозу є більш значущими для молодих осіб та в пацієнтів середнього віку в порівнянні з літніми людьми.
Замісна терапія гормонами ЩЗ показана при клінічно вираженому гіпотиреозі з рівнем ТТГ вище 10 мОд/л. Асимптоматичним чи малосимптоматичним пацієнтам зі стійким помірним субклінічним гіпотиреозом (ТТГ 4-10 Од/л) слід запропонувати вибір між лікуванням тироксином та спостереженням зі щорічним проведенням лабораторних аналізів.
Прогресування гіпотиреозу більш імовірне в АТПО-позитивних пацієнтів. Якщо незрозуміло, чи неспецифічні симптоми зумовлені субклінічним гіпотиреозом, чи просто співіснують з ним, доцільним є тримісячне пробне лікування тироксином. Замісна терапія гормонами ЩЗ не рекомендується, якщо наявні симптоми гіпофункції залози, але ТТГ перебуває в межах норми.
Стандартний засіб лікування гіпотиреозу – тироксин – зазвичай призначається в стартовій дозі 50-100 мг/добу з подальшою титрацією залежно від результату повторного аналізу функції ЩЗ, який необхідно провести через 6-8 тиж. У ослаблених хворих, осіб старшого віку та пацієнтів із симптоматичною ішемічною хворобою серця варто розпочинати лікування з менших доз (25 мг/добу). Тироксин слід приймати натще за 1 год до сніданку, але це може бути незручним для пацієнта та знижувати прихильність до лікування, тому достатньо регулярно вживати препарат.
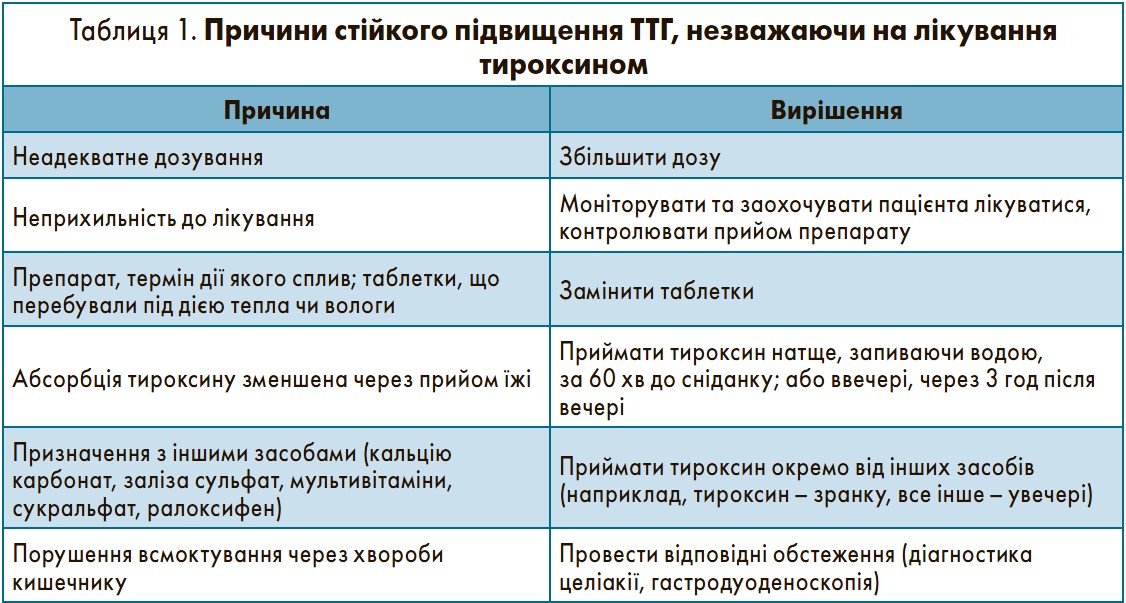
Цілями лікування гіпотиреозу є зниження вираженості симптомів і нормалізація ТТГ. У пацієнтів, які лікуються тироксином, сироватковий вільний T4 може бути нормальним або підвищеним, що не є показанням до зниження дози, якщо ТТГ перебуває в межах норми. Визначення вільного T3 для моніторування терапії тироксином не потрібне. У деяких хворих ТТГ залишається підвищеним, попри прийом адекватних доз тироксину. Основна причина цього – неприхильність до лікування; інші можливі фактори представлені в таблиці 1.
У певних пацієнтів симптоматика хвороби може утримуватися, незважаючи на прихильність до лікування та нормалізацію ТТГ. Зазначене можна пояснити 3 найбільш імовірними причинами.
По-перше, симптоми можуть бути не пов’язані з дисфункцією ЩЗ. У таких випадках слід передусім виключити коморбідні стани, зокрема целіакію (часто асоційована з аутоімунними хворобами ЩЗ) та депресію. По-друге, для деяких стандартна тиреоїдзамісна терапія може бути недостатньою. Деякі пацієнти почуваються краще в разі підвищення дози тироксину до досягнення низьких цільових значень ТТГ
(0,4-2,0 мОд/л) чи навіть показників нижче норми (0,1-0,4 мОд/л), хоча переваги такого підходу не були підтверджені в клінічних дослідженнях. Зазначена стратегія вважається безпечною, особливо в молодих пацієнтів без супутніх захворювань, у разі зниження ТТГ не нижче 0,1 мОд/л. По-третє, при аутоімунному тиреоїдиті підвищена продукція прозапальних цитокінів може бути причиною появи симптомів незалежно від функції ЩЗ. У деяких дослідженнях харчові добавки селену (100-200 мг/добу) знижували вміст маркерів запалення та поліпшували якість життя пацієнтів з хворобою Хашімото. Хоча селен не входить до стандартів лікування хвороб ЩЗ, слід розглянути можливість його призначення хворим зі стійкими симптомами.
Що стосується вторинного гіпотиреозу, у пацієнтів з хворобами гіпофіза сироватковий ТТГ є ненадійним показником діагностики хвороби та моніторингу лікування тироксином. Останній має включати визначення вільного T4 та клінічну оцінку стану пацієнта.
Гіпертиреоз
Клінічно виражений гіпертиреоз
Гіпертиреоз спостерігається рідше, ніж гіпотиреоз. Клінічна картина цього стану є досить типовою; основні симптоми включають схуднення, непереносимість тепла, відчуття серцебиття, задишку, тривожність, діарею, тремор, слабкість проксимальних м’язів. При фізикальному обстеженні можна виявити тремор, тахікардію, офтальмопатію, зоб, труднощі при вставанні з положення навпочіпки. Діагноз підтверджується за допомогою лабораторних аналізів (зниження ТТГ (зазвичай не визначається) та підвищення вільного T4 та/або вільного T3).
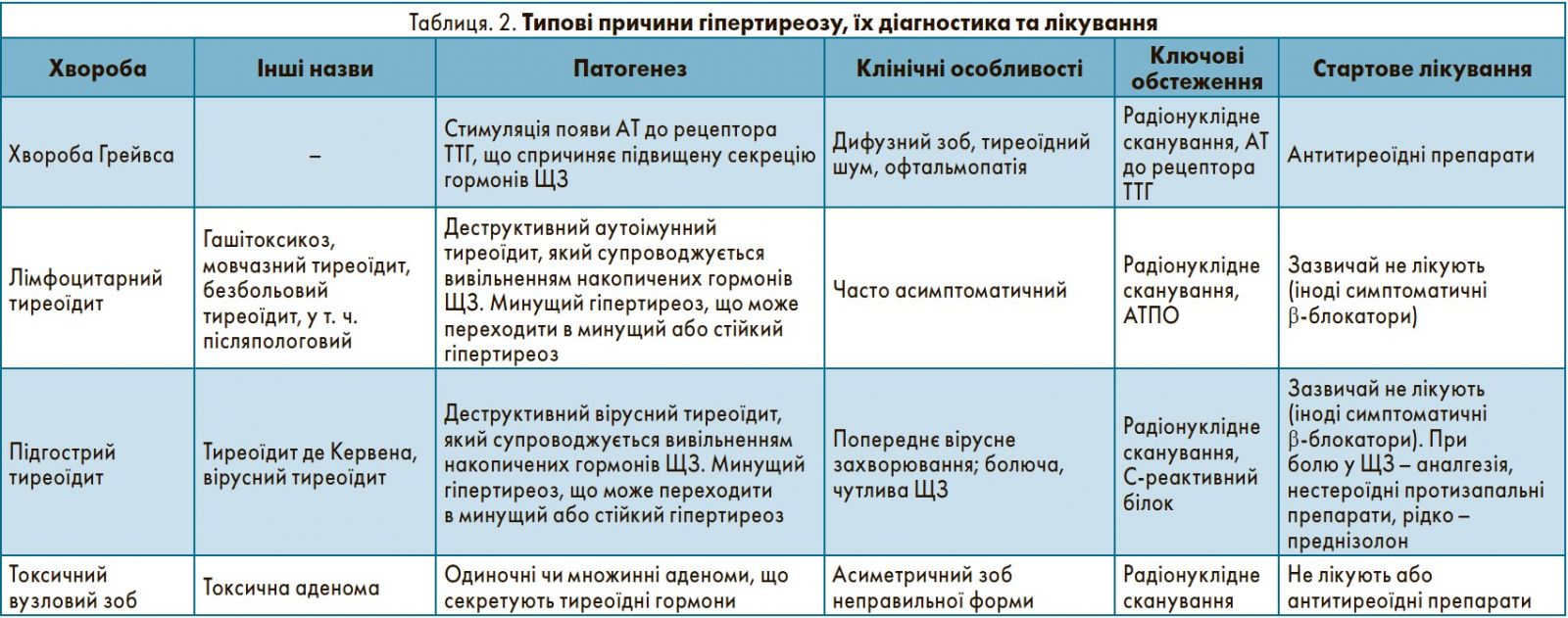
Основні причини гіпертиреозу – хвороба Грейвса, тиреоїдит, токсичний вузловий зоб (табл. 2). Встановлення точної причини є передумовою успішного лікування. Часто в діагностиці гіпертиреозу доцільним є радіонуклідне сканування залози, при цьому УЗД здебільшого не показано, оскільки не дозволяє розрізнити хворобу Грейвса та тиреоїдит, а також нерідко виявляє вузли, наявність яких не пов’язана з гіпертиреозом. Останнє призводить до помилок у діагнозі та подальших недоцільних обстежень.
Тиреоїдит зазвичай характеризується трифазним перебігом з переходом гіпертиреозу в гіпотиреоз, надалі – в еутиреоз. При підгострому (вірусному) тиреоїдиті переважно спостерігається повне відновлення функції залози, при цьому в разі аутоімунного тиреоїдиту з позитивними АТПО може тривало зберігатися гіпотиреоз. Часто такі пацієнти не потребують лікування в тиреотоксичній фазі, хоча α-блокатори можуть забезпечити симптоматичне полегшення. Рівні ТТГ, вільних T4 та T3 необхідно перевіряти кожні 6-8 тиж до нормалізації функції залози. Якщо зберігається гіпотиреоз, показана терапія тироксином.
Лікування хвороби Грейвса слід розпочинати з карбімазолу (15-20 мг/добу при незначному чи помірному гіпертиреозі, 30-40 мг – при тяжкому). Пацієнти, які добре відповідають на лікування, можуть приймати карбімазол курсом 18 міс для досягнення довготривалої ремісії. Іншими варіантами терапії є призначення радіоактивного йоду та тиреоїдектомія.
Токсичний вузловий зоб лікується хірургічно або за допомогою радіоактивного йоду. Хоча антитиреоїдні засоби також можуть застосовуватися, не варто надавати перевагу такому лікуванню: ремісія гіпертиреозу при цій хворобі малоймовірна, їх слід приймати пожиттєво.
Субклінічний гіпертиреоз
Помірний субклінічний гіпертиреоз з рівнями ТТГ у межах 0,1-0,4 мОд/л може бути наслідком наявності автономних вузлів ЩЗ або виявлятися в здорових осіб. Часто такий стан минає без лікування, тому тактикою вибору є спостереження з повторними регулярними обстеженнями. Субклінічний гіпертиреоз зі стійкими показниками ТТГ нижче 0,1 мОд/л класифікується як незначний гіпертиреоз і має лікуватися згідно з наведеними вище рекомендаціями.
Вузли та рак ЩЗ
Вузли, що пальпуються
Вузли ЩЗ, які можна пропальпувати, наявні приблизно в 5% населення світу. Більшість з них є доброякісними (колоїдні вузли, кісти, вузловий тиреоїдит, доброякісні новоутворення), і лише 5% – злоякісні пухлини. Великі нодулярні зоби можуть бути симптоматичними й потребувати хірургічного втручання для полегшення симптомів тиску на навколишні органи, але більшість вузлів ЩЗ є асимптоматичними. Загалом кажучи, основним спрямуванням діагностичного пошуку в разі наявності вузлів є оцінка ризику раку ЩЗ. Тактика діагностики вузлів, що пальпуються, представлена на рисунку. Ключове дослідження при вузлах – тонкоголкова аспіраційна біопсія під контролем УЗД. Якщо клінічна картина, ультразвукові характеристики та цитологія свідчать про доброякісну патологію, подальше обстеження не потрібне. Якщо цитологія має ознаки раку або результат невизначений, слід скерувати пацієнта до хірурга-ендокринолога. Якщо рівень ТТГ знижений, радіонуклідне сканування може виявити один чи кілька автономних («гарячих») вузлів, які рідко є злоякісними і зазвичай не потребують біопсії. Якщо ТТГ нормальний чи підвищений, радіонуклідне сканування не показане.
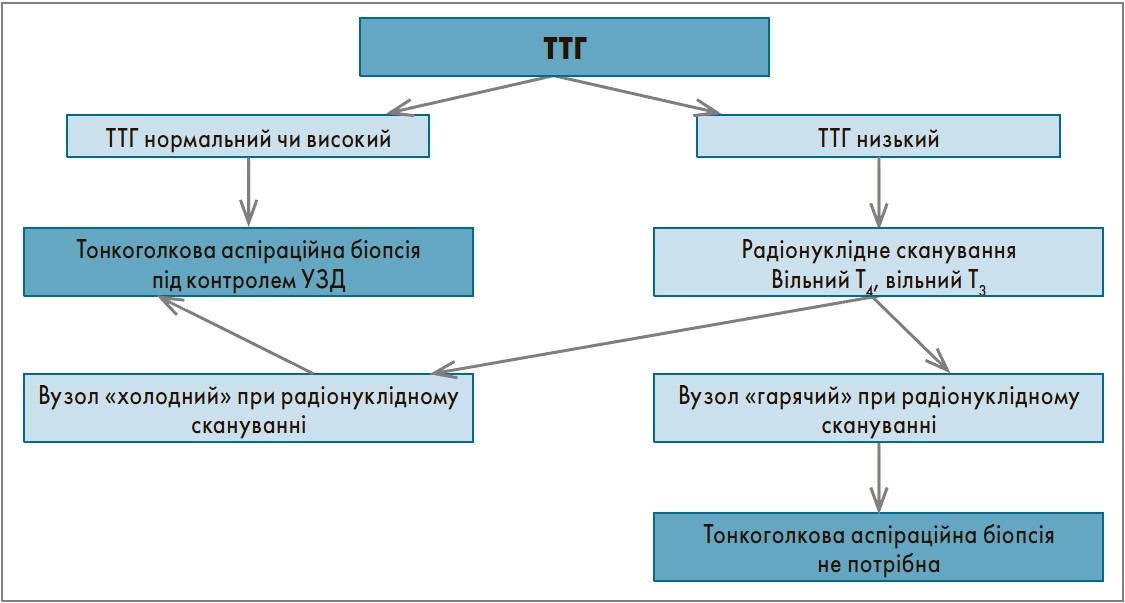 Рис. Алгоритм дослідження вузла ЩЗ, що пальпується
Рис. Алгоритм дослідження вузла ЩЗ, що пальпується
Тиреоїдні вузли та рак: ризик гіпердіагностики
Як зазначалося, близько 5% людей мають вузли ЩЗ, що пальпуються. Частота виявлення вузлів за допомогою УЗД є ще більшою і зростає до 70% в осіб старечого віку. Клінічно діагностований рак ЩЗ малоймовірний; ціложиттєвий ризик такої пухлини становить <1%, хоча при автопсії невеликі ракові пухлини ЩЗ виявляють у приблизно 36% людей. Основна частина цих пухлин – папілярний рак <1 см в діаметрі.
У більшості країн поширеність раку ЩЗ різко зростає. Це пов’язано в основному зі збільшенням виявлення невеликих папілярних ракових пухлин за допомогою УЗД. Оскільки більшість з них ніколи не проявляється клінічно, це є прикладом гіпердіагностики. Вражає така ситуація в Кореї, де скринінгове УЗД ЩЗ призвело до збільшення поширеності раку ЩЗ у 15 разів без відповідного зниження смертності, яка і так є дуже низькою.
Епідемії раку ЩЗ можна уникнути, якщо УЗД ЩЗ застосовувати розважливо й за такими правилами:
- УЗД ЩЗ слід проводити для оцінювання клінічно явних, видимих чи пальпованих вузлів ЩЗ чи зобу. Зазначене дослідження не рекомендується при гіпо- чи гіпертиреозі за відсутності зобу; у разі відчуття «комка» в горлі (globus hystericus), неспецифічних симптомів чи для скринінгу.
- Тонкоголкову аспіраційну біопсію варто проводити для вузлів >1 см у діаметрі за сонографічними вимірами. Менші вузли не потребують рутинної біопсії.
Хвороби ЩЗ у вагітних та в післяпологовому періоді
При вагітності секреція гормонів ЩЗ зростає на 30-50%. Це зумовлено стимулюючим впливом хоріонічного гонадотропіну на ЩЗ, підвищеним рівнем циркулюючого тироксинзв’язуючого глобуліну та руйнуванням гормонів ЩЗ у плаценті. Останні два фактори призводять до потреби у виділенні залозою більшої кількості гормонів. Материнський T4 проходить крізь плацентарний бар’єр та відіграє важливу роль у розвитку мозку плода до 18-20 тиж гестації, коли повністю дозріває власна ЩЗ плода. Помірний дефіцит йоду під час вагітності може порушувати розвиток мозку плода, а надходження цього мікроелементу з продуктами харчування може бути недостатнім у зв’язку з підвищеними потребами організму вагітної. Отже, вагітним жінкам або жінкам, що планують вагітність, слід приймати добавки йоду в дозі 150 мг/добу.
Досі не встановлено, чи потрібен загальнообов’язковий скринінг вагітних жінок на порушення функції ЩЗ. Його основною діагностичною цінністю є, ймовірно, виявлення рідкісних випадків явного гіпо- та гіпертиреозу, при яких показане лікування, хоча частіше виявляються незначущі порушення.
Загальні референтні значення ТТГ та вільного T4 для вагітних не підходять. Американська тиреоїдна асоціація рекомендує лабораторіям створити триместр-специфічні та метод-специфічні норми на основі показників місцевих популяцій. Однак більшість лабораторій користується стандартними значеннями: перший триместр – 0,1-2,5 мОд/л, другий триместр – 0,2-3,0 мОд/л, третій триместр – 0,3-3,0 мОд/л, хоча ці інтервали ґрунтуються на думках експертів та обмежених даних. Вивчення референтних значень, проведене в різних країнах, продемонструвало варіабельні результати. Здебільшого верхня межа ТТГ перевищує 2,5 чи 3,0 мОд/л, що свідчить про потребу в перегляді встановлених на сьогодні значень.
Гіпотиреоз
Явний гіпотиреоз під час вагітності асоційований з негативними наслідками, у т. ч. викиднями, прееклампсією, відшаруванням плаценти, передчасними пологами, низькою масою тіла при народженні, зниженим коефіцієнтом інтелекту в потомства. Вплив субклінічного гіпотиреозу точно не встановлений.
Існує мало клінічних досліджень застосування тироксину у вагітних. В одному з них така терапія в АТПО-позитивних еутиреоїдних жінок супроводжувалася зменшенням кількості викиднів і передчасних пологів. Недавнє випробування показало, що призначення тироксину вагітним жінкам (середній термін гестації – 12 тиж) з підвищеним ТТГ чи зниженим вільним T4 не мало жодного впливу на акушерські наслідки чи когнітивні функції потомства.
На сьогодні рекомендований такий підхід: жінкам з гіпотиреозом, які планують вагітність, слід оптимізувати дозу тироксину, орієнтуючись на цільові показники ТТГ у межах 0,4-2,5 мОд/л. При підтвердженні вагітності потрібно підвищити дозу препарату приблизно на 30%. Такого збільшення легко досягти, подвоївши дозу 2 дні на тиждень (інші дні – без змін). Сироватковий ТТГ необхідно перевіряти кожні 4-6 тиж до 20-го тиж гестації, надалі – один раз у третьому триместрі. Після пологів дозу тироксину необхідно знизити до рівня, який був до вагітності, провести аналіз ТТГ через 6-8 тиж після пологів. У жінок з підвищеним ТТГ під час вагітності рекомендується визначити вільний T4 та АТПО. Якщо ТТГ перевищує 4 мОд/л або виявляється зниження вільного T4, необхідно розпочати лікування тироксином у стартовій дозі 75-100 мг/добу.
Хоча Американське товариство ендокринології радить призначати тироксин вагітним жінкам з рівнем ТТГ 2,5-4,0 мОд/л, переваги такого лікування точно не встановлені. Американська тиреоїдна асоціація радить лікувати вагітних жінок з ТТГ >2,5 мОд/л лише в разі позитивного результату аналізу на АТПО.
Гіпертиреоз у вагітних
Явний гіпертиреоз під час вагітності фіксується рідко. У першому триместрі може спостерігатися гестаційний гіпертиреоз унаслідок стимулюючого впливу хоріонічного гонадотропіну на ЩЗ, особливо в жінок з дуже високими рівнями цього гормону, блюванням вагітних чи багатоплідною вагітністю. Такий гіпертиреоз зазвичай швидко минає без жодних втручань. Причиною стійкого гіпертиpeозу у вагітних в основному є хвороба Грейвса. Радіонуклідне сканування вагітним протипоказано, тому основним діагностичним обстеженням є визначення АТ до рецептора ТТГ. Разом з тим гіпертиреоз збільшує ризик переривання вагітності та інших небажаних явищ, отже, таких пацієнток необхідно негайно скерувати до ендокринолога.
Субклінічний гіпертиреоз при вагітності може бути і варіантом норми, і наслідком хвороб ЩЗ. Цей стан не асоціюється з негативними наслідками та часто не потребує лікування, однак слід ретельно моніторувати функцію ЩЗ у таких жінок.
Післяпологова дисфункція ЩЗ
Післяпологова дисфункція ЩЗ розвивається приблизно в 10% жінок протягом першого року після пологів. Гіпертиреоз може бути спричинений післяпологовим аутоімунним тиреоїдитом чи хворобою Грейвса, які можна розрізнити за допомогою визначення сироваткових АТПО чи радіонуклідного сканування (протипоказане жінкам, які годують груддю). Післяпологовий тиреоїдит може зумовлювати довготривалий гіпотиреоз у 10-20% жінок з цією патологією.
Walsh J. P. Managing thyroid disease in general practice. MJA 205 (4). – 2016. – P. 179-184.
Переклала з англ. Лариса Стрільчук
Медична газета «Здоров’я України 21 сторіччя» № 19 (440), жовтень 2018 р.