29 березня, 2025
Вплив психоемоційного стресу на менструальну функцію підлітків в умовах військової агресії
 Масштабний вплив на організм підлітків хронічного психоемоційного стресу внаслідок бойових дій, вимушеного переміщення та втрати звичного способу життя призводить до значних порушень у функціонуванні репродуктивної системи. Патофізіологічні механізми стресіндукованих змін охоплюють порушення в гіпоталамо-гіпофізарно-яєчниковій осі та пов’язані з ними метаболічні розлади. В межах пленуму ГО «Асоціація акушерів-гінекологів України» та науково-практичної конференції за міжнародної участі «Акушерство, гінекологія, репродуктологія: сьогодення та перспективи» доктор медичних наук, професор кафедри акушерства, гінекології та планування сім'ї Медичного інституту Сумського державного університету Ірина Миколаївна Нікітіна презентувала доповідь, в якій висвітлила актуальні питання порушень менструальної функції у підлітків в умовах війни.
Масштабний вплив на організм підлітків хронічного психоемоційного стресу внаслідок бойових дій, вимушеного переміщення та втрати звичного способу життя призводить до значних порушень у функціонуванні репродуктивної системи. Патофізіологічні механізми стресіндукованих змін охоплюють порушення в гіпоталамо-гіпофізарно-яєчниковій осі та пов’язані з ними метаболічні розлади. В межах пленуму ГО «Асоціація акушерів-гінекологів України» та науково-практичної конференції за міжнародної участі «Акушерство, гінекологія, репродуктологія: сьогодення та перспективи» доктор медичних наук, професор кафедри акушерства, гінекології та планування сім'ї Медичного інституту Сумського державного університету Ірина Миколаївна Нікітіна презентувала доповідь, в якій висвітлила актуальні питання порушень менструальної функції у підлітків в умовах війни.
За даними ООН, внаслідок повномасштабної російської агресії постраждало понад 30 тисяч мирних громадян України, з яких більш ніж 10 тисяч загинуло і понад 20 тисяч поранено. Серед них більше ніж 500 загиблих і понад тисячу поранених дітей. Станом на середину серпня 2024 р. понад 6,6 мільйона осіб в Україні стали внутрішньо переміщеними особами. До європейських країн виїхало майже 7 мільйонів українців, з яких 80% становлять жінки та діти.
Демографічна ситуація в Україні характеризується від’ємним приростом населення: на 6 народжень припадає 18 смертей на тисячу населення. Цей показник може погіршитися через довготривалий вплив стресових факторів на репродуктивне здоров’я підлітків – майбутніх батьків.
Приблизно 250 тисяч дітей регулярно зазнають обстрілів, що підвищує ризик фізичних травм та проблем із психічним здоров’ям. За оцінками ООН, щонайменше 7,5 мільйона дітей зазнають фізичних і психічних травм під час воєнних конфліктів. Гострий стрес, втрата житла, недоїдання та інфекційні захворювання, що супроводжують дітей під час воєнних конфліктів, підвищують імовірність розвитку хронічних неінфекційних захворювань у дорослому віці, зокрема цукрового діабету, серцево-судинних хвороб, хронічних захворювань нирок та репродуктивних розладів.
Патофізіологічні механізми впливу стресу на репродуктивну систему
Стрес у підлітковому віці особливо небезпечний через порушення режиму сну, відпочинку, харчової поведінки та фізичної активності. У період статевого дозрівання організм дитини більш сприйнятливий до впливу навколишнього середовища через обмежені адаптивні ресурси. Нестійкий баланс гіпоталамо-гіпофізарної системи під впливом несприятливих чинників легко порушується.
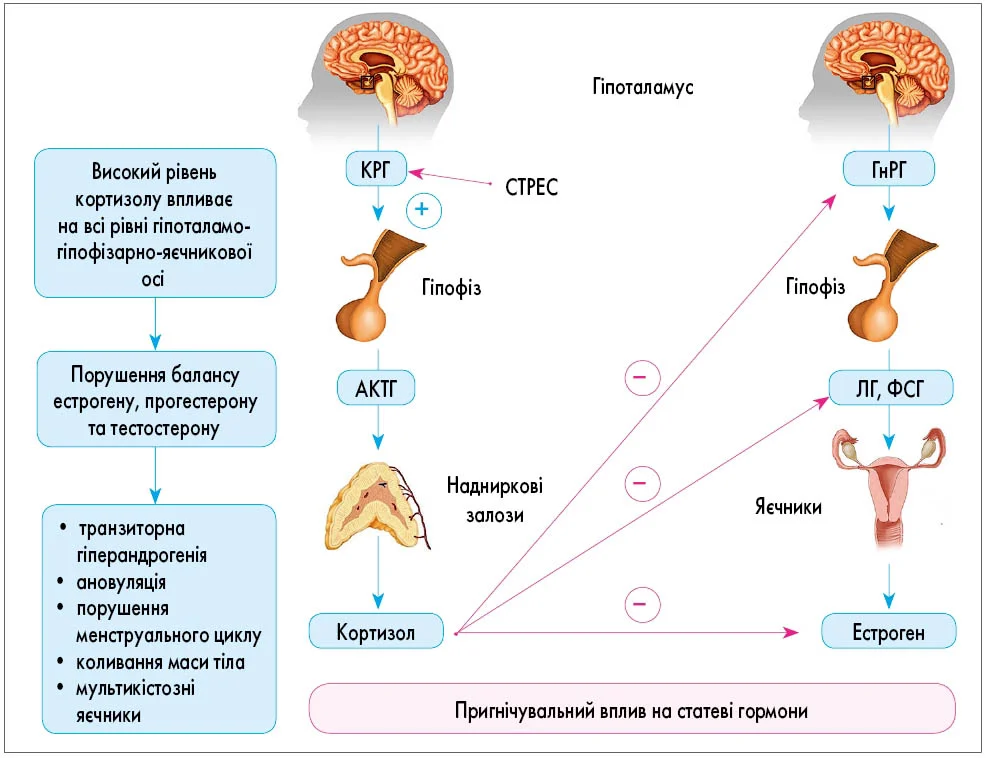
Стрес як захисна реакція на зовнішні подразники дає змогу адаптуватися до змін завдяки активній секреції гормонів надниркових залоз. Високий рівень кортизолу впливає на всі рівні гіпоталамо-гіпофізарно-яєчникової осі, сприяючи порушенню балансу естрогену, прогестерону та тестостерону. Наслідком є транзиторна гіперандрогенія, порушення менструального циклу, ановуляція, коливання маси тіла і розвиток полікістозу яєчників (рисунок).
Рисунок. Патофізіологічні механізми впливу стресу на репродуктивну систему
Примітки: КРГ – кортикотропін-рилізинг-гормон; AКТГ – адренокортикотропний гормон; ГнРГ – гонадотропін-рилізинг-гормон; ЛГ – лютеїнізуючий гормон; ФСГ – фолікулостимулювальний гормон.
У регуляції стресових процесів важливу роль відіграє пролактин, який підвищує рівень андрогенів, альдостерону, кортизолу та стимулює синтез катехоламінів у надниркових залозах. Динамічна взаємодія адренокортикотропного гормону (АКТГ) і пролактину спрямована на формування адаптаційної відповіді організму на стрес завдяки узгодженій секреції кортизолу і дегідроепіандростерону сульфату в надниркових залозах.
При хронічному стресі співвідношення кортизолу і дегідроепіандростерону сульфату зміщується в бік останнього, що призводить до гіперандрогенних станів та репродуктивних розладів. Гіперпролактинемія у дівчат може призводити до порушення статевого дозрівання, розладів менструального циклу (аменорея, олігоменорея), виникнення аномальних маткових кровотеч, а також до психічних розладів і метаболічних порушень.
Клінічні прояви та діагностика
Основними причинами звернення до гінеколога під час війни є порушення менструального циклу (близько 70% звернень). У 32% пацієнток діагностують гіперпролактинемію, також поширені дисменорея, аномальні маткові кровотечі, аменорея та олігоменорея. Нерегулярний менструальний цикл виявляють у понад 40% підлітків, водночас спостерігають збільшення тривалості менструацій та частоти аномальних маткових кровотеч.
Дисменорею спостерігають у 55% пацієнток, із них до 40% під час менструації потребують вживання знеболювальних препаратів. Важливо диференціювати первинну і вторинну дисменорею. Причинами вторинної дисменореї можуть бути ендометріоз (маніфестація можлива з 15 років), запальні захворювання органів малого таза, кісти та пухлини яєчників, цервікальний стеноз, поліпи матки, міома, внутрішньоматкові синехії та вроджені аномалії розвитку матки.
Метаболічні порушення виявляють приблизно у 25% обстежених підлітків, які мають метаболічний синдром та ожиріння. У цій групі частіше спостерігається олігоменорея, вторинна аменорея або надмірні менструації. Близько 56% підлітків із підтвердженим метаболічним синдромом мають щонайменше два з трьох Роттердамських критеріїв, через що потрапляють до групи високого ризику розвитку синдрому полікістозних яєчників.
Терапевтичні підходи
Лікування порушень менструального циклу потребує комплексного підходу, який насамперед враховує характер та етіологію порушень. При первинній дисменореї терапія спрямована на нормалізацію менструального циклу через пригнічення синтезу простагландинів. Для досягнення цієї мети застосовують анальгетики та спазмолітики, які доповнюють седативними препаратами для зменшення психоемоційного напруження. Важливим компонентом терапії є також застосування фітопрепаратів, які виявляють м’яку регулювальну дію на гормональний баланс. За наявності показань призначають гормональну терапію, яка обов’язково супроводжується адекватною вітамінотерапією для підтримання метаболічних процесів.
У разі аномальних маткових кровотеч у пубертатному періоді лікування проводять послідовно, починаючи з негормонального гемостазу. Якщо він виявляється неефективним, переходять до гормонального гемостазу, після чого обов’язково проводять протирецидивну терапію для запобігання повторним епізодам кровотеч.
! Особливої уваги потребують пацієнтки, які отримують психотропні препарати, оскільки нейролептики, антидепресанти та антипсихотики можуть спричинювати гіперпролактинемію.
У таких випадках терапевтичну стратегію розробляють спільно із психіатром. Насамперед розглядають можливість припинення прийому препарату, що спричинює підвищення рівня пролактину. Якщо це неможливо, проводять заміну на новіші препарати з меншим впливом на рівень пролактину. У разі коли зміна психотропної терапії неможлива, призначають агоністи дофаміну під ретельним наглядом обох спеціалістів.
За наявності метаболічних порушень терапію починають із модифікації способу життя та харчової поведінки. Паралельно впроваджують програму регулярних фізичних навантажень, адаптованих до можливостей пацієнтки. За наявності інсулінорезистентності призначають відповідні медикаментозні препарати. Важливим компонентом лікування є корекція дефіциту вітаміну D та інших мікронутрієнтів, які відіграють важливу роль у нормалізації метаболічних процесів та гормонального балансу.
Клінічний випадок № 1
Дівчина, 17 років, звернулась зі скаргами на порушення менструального циклу у вигляді затримок менструації на 10-14 днів та висипання на обличчі. З анамнезу відомо, що менархе настало в 10 років, спочатку менструації були регулярними, з помірною крововтратою в перші дні. Обтяжений сімейний анамнез: у матері діагностовано синдром полікістозних яєчників, цукровий діабет та ожиріння.
Під час об’єктивного обстеження виявлено клінічні ознаки гіперандрогенії, що підтверджено оцінкою за модифікованою шкалою Феррімана – Галлвея (>8 балів). Ультразвукове дослідження органів малого таза продемонструвало збільшення об’єму обох яєчників та їхню мультифолікулярну структуру.
Комплексне гормональне обстеження виявило порушення співвідношення гонадотропінів (ЛГ/ФСГ), лабораторні ознаки гіперандрогенії, знижений рівень прогестерону, дефіцит вітаміну D та зміни рівня антимюллерового гормону. Біохімічні показники характеризувалися гіперінсулінемією та підвищенням індексу НОМА, що свідчить про наявність інсулінорезистентності.
На підставі клініко-лабораторних даних встановлено діагноз: пубертатна олігоменорея; синдром полікістозних яєчників, що формується; гірсутний синдром; метаболічний синдром; інсулінорезистентність; гіперпролактинемія; дефіцит вітаміну D.
Призначено комплексне лікування, що охоплювало немедикаментозні методи (модифікація способу життя та харчової поведінки, дозовані фізичні навантаження, зокрема гімнастика та плавання) та медикаментозну терапію. Остання полягала в застосуванні флутаміду в дозі 125 мг на добу, каберголіну по 125 мкг двічі на тиждень, метформіну, препаратів міо-інозитолу, фолієвої кислоти та вітаміну D з регулярним моніторингом індексу НОМА та рівня глюкози крові.
Клінічний випадок № 2
Дівчинка звернулась зі скаргами на болісні менструації протягом останніх трьох місяців. Йшлося не лише про болісність, а й надмірну крововтрату під час менструацій.
На момент звернення пацієнтка для полегшення симптомів самостійно застосовувала під час менструацій нестероїдні протизапальні препарати та транексамову кислоту. При зборі сімейного анамнезу встановлено наявність ендометріозу в матері, що є важливим фактором ризику розвитку подібного стану в доньки.
Під час проведення ультразвукового дослідження органів малого таза явних патологічних змін не виявлено. Однак лабораторне обстеження продемонструвало зниження рівня феритину, що свідчить про розвиток прихованого залізодефіциту.
На підставі клініко-анамнестичних даних і результатів обстеження встановлено діагноз: дисменорея, прихований залізодефіцит.
Враховуючи тяжкість симптомів, наявність обтяженого сімейного анамнезу щодо ендометріозу та розвиток залізодефіциту, було призначено комплексне лікування:
- комбінований оральний контрацептив за схемою 21+7;
- препарати заліза для корекції залізодефіциту;
- рекомендовано контрольний огляд через 3 місяці для оцінювання ефективності призначеної терапії.
Отже, в умовах воєнних дій спостерігають значне зростання дисгормональних та метаболічних порушень у підлітків, що призводить до розладів менструального циклу у більш ніж 70% випадків. Своєчасне виявлення та адекватна корекція психоемоційних та обмінних розладів у підлітків сприяє профілактиці порушень менструального циклу та репродуктивної функції. Особливу увагу слід приділяти комплексному підходу до лікування та міждисциплінарній взаємодії спеціалістів для досягнення оптимальних результатів терапії.
Підготувала Олена Речмедіна
Тематичний номер «Педіатрія» № 1 (77) 2025 р.