25 квітня, 2022
Лікувальна тактика при отриманні патологічного цитологічного мазка шийки матки
За матеріалами конференції
 Незважаючи на наявність надійного тестового контролю, сучасні методи лікування та профілактики, рак шийки матки займає лідируючі позиції у структурі онкологічної патології. Ця тема не лишилася поза увагою під час Всеукраїнської науково-практичної конференції з міжнародною участю «Актуальні питання сучасного акушерства та гінекології», що відбулася минулого року. У рамках заходу асистент кафедри терапії та сімейної медицини Навчально-наукового інституту післядипломної освіти Тернопільського національного медичного університету ім. І. Я. Горбачевського, кандидат медичних наук Юлія Богданівна Якимчук спільно зі співавторами О. М. Якимчук та Т. В. Рудик висвітлили сучасні лікувальні стратегії при виявленні патологічного цитологічного мазка шийки матки.
Незважаючи на наявність надійного тестового контролю, сучасні методи лікування та профілактики, рак шийки матки займає лідируючі позиції у структурі онкологічної патології. Ця тема не лишилася поза увагою під час Всеукраїнської науково-практичної конференції з міжнародною участю «Актуальні питання сучасного акушерства та гінекології», що відбулася минулого року. У рамках заходу асистент кафедри терапії та сімейної медицини Навчально-наукового інституту післядипломної освіти Тернопільського національного медичного університету ім. І. Я. Горбачевського, кандидат медичних наук Юлія Богданівна Якимчук спільно зі співавторами О. М. Якимчук та Т. В. Рудик висвітлили сучасні лікувальні стратегії при виявленні патологічного цитологічного мазка шийки матки.
Ключові слова: рак шийки матки, кольпоскопія, вірус папіломи людини, цервікальна інтраепітеліальна неоплазія.
Рідинна цитологія широко використовується в сучасних умовах та визнана в усіх країнах, оскільки даний метод діагностики достовірно виявляє рак шийки матки (РШМ) як найбільш поширений онкологічний процес у структурі онкогінекологічної патології.
У травні 2018 року Генеральний директор Всесвітньої організації охорони здоров’я д-р Тедрос Аданом Гебреїсус звернувся із глобальним закликом до дій наступними словами: «Ми можемо усунути рак шийки матки як проблему суспільного здоров’я та зробити його хворобою минулого». Також він оприлюднив стратегію прискорення ліквідації РШМ, що включала наступні позиції:
- 90% жінок вакциновані від вірусу папіломи людини (ВПЛ);
- 70% жінок проходять регулярний скринінг на РШМ;
- у 90% жінок проліковані передракові стани та рак in situ.
Епідеміологія раку шийки матки
Доповідач зазначила, що епідеміологія РШМ має наступні статистичні показники (за даними Національного канцер-реєстру України):
- у 2017 році захворюваність на РШМ становила 21,7 випадку на 100 тис. жіночого населення (грубий показник) і посідала друге місце після раку молочної залози;
- у 2017 році у віковій групі 18‑29 років РШМ у загальній структурі злоякісних новоутворень становив 14,1%;
- у 2020 році було діагностовано 604 127 випадків РШМ, 341 831 жінка померла від даної патології – тобто кожні 5 хв одна пацієнтка помирає від РШМ.
Діагностичні методи виявлення раку шийки матки
Ю. Б. Якимчук зауважила, що встановлення діагнозу базується на «трьох китах» (згідно з Уніфікованим клінічним протоколом медичної допомоги «Дисплазія шийки матки. Рак шийки матки»; наказ МОЗ України від 02.04.2014 № 236):
- цитологія і/або ВПЛ-скринінг як первинний метод виявлення РШМ – найбільш точний, зручний у проведенні й порівняно дешевий;
- кольпоскопія;
- гістологічне дослідження біоматеріалу з ураженої ділянки.
У разі встановлення ASC-US (atypical squamous cells of undetermined significance, атипові клітини плоского епітелію невизначеного значення) ризик прихованого діагнозу LSIL (low-grade squamous intraepithelial lesions, інтраепітеліальні ураження низького ступеня) у жінок із ПАП (тест Папаніколау) становить до 30%, а HSIL (high grade squamous intraepithelial lesion, інтраепітеліальні ураження високого ступеня) досягає 10% (Raab S. S., 1999). У даному випадку доповідач рекомендувала проводити тест на ВПЛ, оскільки цей вірус у 98% випадків є причиною РШМ (згідно з Настановою 01088 «Злоякісні новоутворення в гінекології»). За негативних результатів тесту пацієнтка підлягає подальшому рутинному скринінгу, натомість як за умови виявлення ВПЛ необхідним є проведення кольпоскопії.
Основною метою кольпоскопії є визначення місця з найбільш вираженим ураженням для взяття прицільної біопcії, оскільки лише результат гістологічного дослідження біоптату може остаточно підтвердити або спростувати діагноз РШМ.
 У контексті доповіді Ю. Б. Якимчук поділилася власним досвідом діагностики РШМ і представила клінічний випадок ведення пацієнтки, у якої при кольпоскопічному дослідженні було отримано адекватну картину, лінія стику візуалізувалася повністю у цервікальному каналі. Виявлено зону трансформації 1-го типу з локалізацією ураження в межах зони трансформації циркулярно у 4 квадрантах, що становить 50% шийки матки. Аномальна кольпоскопічна картина II ступеня – щільні оцтово-білі обідки навколо залоз, щільний оцтово-білий епітелій, ознака внутрішньої межі. Така кольпоскопічна картина відповідає дисплазії епiтелію шийки матки тяжкого ступеня, внутрішньоепітеліальній карциномі (HSIL, цервікальна інтраепітеліальна неоплазія 3 [cervical intraethelial neoplasia, CIN]). Доповідач застерегла від помилкового вибору місця забору біоптату, оскільки це призводить до хибних результатів і в подальшому до невірної тактики лікування.
У контексті доповіді Ю. Б. Якимчук поділилася власним досвідом діагностики РШМ і представила клінічний випадок ведення пацієнтки, у якої при кольпоскопічному дослідженні було отримано адекватну картину, лінія стику візуалізувалася повністю у цервікальному каналі. Виявлено зону трансформації 1-го типу з локалізацією ураження в межах зони трансформації циркулярно у 4 квадрантах, що становить 50% шийки матки. Аномальна кольпоскопічна картина II ступеня – щільні оцтово-білі обідки навколо залоз, щільний оцтово-білий епітелій, ознака внутрішньої межі. Така кольпоскопічна картина відповідає дисплазії епiтелію шийки матки тяжкого ступеня, внутрішньоепітеліальній карциномі (HSIL, цервікальна інтраепітеліальна неоплазія 3 [cervical intraethelial neoplasia, CIN]). Доповідач застерегла від помилкового вибору місця забору біоптату, оскільки це призводить до хибних результатів і в подальшому до невірної тактики лікування.
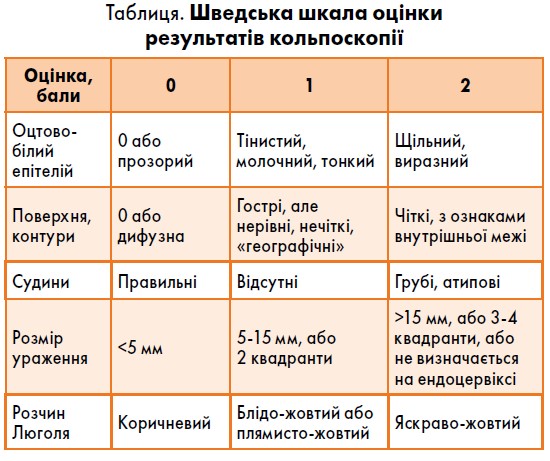
Для стандартизації результатів кольпоскопії була розроблена шведська шкала оцінки, що включає аналіз таких показників, як: оцтово-білий епітелій, поверхня та контури ураженої ділянки, характеристика судин, розмір ураження, зміна кольору розчину Люголя (таблиця). Комбіновано оцінюючи вищезазначені показники, за шкалою визначають ступінь ураження CIN та необхідність проведення біопсії патологічної ділянки.
Оцінка ≤5 балів може означати наявність цервікальної неоплазії, оцінка ≤8 балів у 90% випадків передбачає тяжке ураження CIN.
На підтвердження ефективності використання вищезазначеної шкали доповідач навела наступні клінічні випадки.
Клінічний випадок 1
На кольпофотограмі відзначається ураження шийки матки, що локалізоване в межах зони трансформації й відповідає 2-му типу. Лінія стику візуалізується повністю. Локалізація ураження в межах зони трансформації на 12 год, 20% шийки матки. Аномальна кольпоскопічна картина 1-го ступеня – тонкий оцтово-білий епітелій. Результат кольпоскопічного обстеження вказує на дисплазію епітелію шийки матки легкого ступеня. Відповідно до шкали, отримано результат 4 бали, що вказувало на відсутність необхідності проведення біопсії з гістологічним обстеженням.
Клінічний випадок 2
На кольпофотограмі відзначається ураження шийки матки, де лінія стику візуалізується повністю. Локалізація ураження в межах зони трансформації у 4 квадрантах, 60% шийки матки. Аномальна кольпоскопічна картина 1-го ступеня – тонкий оцтово-білий епітелій. Результат кольпоскопічного обстеження відповідає дисплазії епітелію шийки матки легкого ступеня. За підрахунками шкали отримано 7 балів, що вказувало на необхідність проведення біопсії, за результатами якої виявлено CIN I.
Лікування патології шийки матки
У випадку ураження низького ступеня (легкої дисплазії, CIN І) при задовільних результатах кольпоскопії (зона трансформації 1-го або 2-го типу) можливі два підходи: спостереження (рекомендовано) та активне лікування (може розглядатися при ознаках персистенції CIN І).
Ексцизійне лікування CIN I показане в наступних випадках:
- при довготривалій (понад 18‑24 міс) персистенції ураження, особливо у жінок віком ≥30 років;
- у пацієнток, які не мають репродуктивних планів і не погоджуються проходити регулярний контрольний огляд;
- у пацієнток із позитивним BIЛ-статусом.
Доповідач зазначила, що спостереження є оптимальною тактикою ведення молодих жінок та пацієнток, які планують вагітність. Режим спостереження включає в себе проведення цитологічного обстеження, ВПЛ-тестування та кольпоскопії кожні 6 міс, доки не буде отримано цитологічних і кольпоскопічних доказів регресії CIN I протягом 2 років. Крім того, жінкам із патологією шийки матки рекомендовано відмовитися від паління, оскільки ця шкідлива звичка знижує імунітет, сприяє персистенції ВПЛ і прогресуванню захворювання шийки матки.
Наступним важливим питанням, яке розглянула автор доповіді, було виявлення та лікування ко-інфекцій.
Ю. Б. Якимчук зауважила, що першим кроком є діагностика та лікування мікст-інфекцій, які провокують і підтримують виявлені порушення. Рекомендованим є обстеження на наявність та лікування інфекцій, що передаються статевим шляхом, таких як:
- трихомоніаз;
- сифіліс, гонорея, хламідіоз, сечостатевий мікоплазмоз;
- герпесвірусна інфекція;
- генітальний кандидоз.
Дані ко-інфекції створюють вторинні iмунодефіцитні стани, що дозволяє ВПЛ інтегруватися у клітини, а в подальшому – у геном.
Існує два варіанти розвитку ВПЛ у клітині:
- І варіант – транзиторна інфекція з можливим видаленням з організму за відсутності супутньої патології, що знижує імунітет пацієнта, оскільки ВПЛ проникає через цитоплазму, не впливаючи на ядро клітини й знаходячись у вільному (eпicoмальному) стані;
- ІІ варіант – за знижених захисних функцій організму розвивається інтегративна інфекція, що супроводжується проникненням ДНК вірусу у геном клітини із формуванням пухлинного клону клітини, що синтезують онкобілки Е6, Е7 (Кондратюк В.К.).
Другий крок у виявленні та лікуванні ВПЛ – це відновлення нормальної мікрофлори піхви, тоді як третій крок передбачає створення умов для елімінації вірусу організмом жінки.
Клінічний випадок 3
Пацієнтка, 25 років, не палить, скаржиться на непліддя протягом двох років. Дані рідинної цитології відповідають LSIL, ВПЛ 16 – 3,4×109 Lg, ВПЛ 35 – 5,2×109 Lg. Кольпоскопічний огляд вказує на LSIL, CIN І. Була призначена терапія імуномодулятором, що являє собою фрагменти клітинної стінки лактобактерій. При повторному огляді через 6 міс виявлено значні позитивні візуальні зміни ураженої ділянки та кольпоскопічні ознаки регресії.
Клінічний випадок 4
Пацієнтка, 30 років, не палить. Отримано результат рідинної цитології, що відповідає LSIL, ВПЛ 16 – 12,1×109 Lg, ВПЛ 33 – 7,2×109 Lg. Проведено кольпоскопію та прицільну біопсію, отримано результат – CIN I. Призначене спостереження й лікування супутньої мікст-інфекції та створення умов для елімінації ВПЛ. Після лікування повторено рідинну цитологію: LSIL, ВПЛ 16 – 8,7×109 Lg, ВПЛ 33 – 2,2×109 Lg. Динамічне спостереження проводилося протягом 12 міс. Рідинна цитологія: NILM (Negative for Intraepithelial Lesion or Malignancy), ВПЛ 16 – 1,7×109 Lg, ВПЛ 33 – негативний.
Однак у 12‑25% ВПЛ-позитивних жінок із LSIL протягом 4 років можливе її прогресування у HSIL.
Клінічний випадок 5
Пацієнтка, 35 років, палить. Pідинна цитологія відповідає LSIL, ВПЛ 16 – 17,1×109 Lg, ВПЛ 18 – 13,5×109 Lg. Після проведення кольпоскопії виявлена зона трансформації 2-го типу. Проведена прицільна бiопсія та цервікальний кюретаж, результат – CIN I. Контрольний огляд через 6 міс спостереження. Рідинна цитологія: LSIL, ВПЛ 16 – 8,7×109 Lg, ВПЛ 18 – 10,2×109 Lg. Пацієнтці було рекомендовано додатковий курс терапії імуномодулятором природного походження з широким спектром дії для елімінації ВПЛ.
Клінічний випадок 6
Пацієнтка, 28 років, не палить. Рідинна цитологія: HSIL, ВПЛ 16, 18, 31, 33. Кольпоскопічно виявлено патологічні зміни у 4 квадрантах, ознака внутрішньої межі. Діагноз – HSIL. Проведено біопсію ураженої ділянки з результатом CIN II. Пацієнтці запропоноване ексцизійне лікування.
Клінічний випадок 7
Пацієнтка, 30 років, палить. Pідинна цитологія: HSIL, ВПЛ 16 – 17,1×109 Lg, ВПЛ 18 – 13,5×109 Lg. За результатами кольпоскопії: щільний оцтово-білий eпітелій, ознака «гребеня». Результат біопсії відповідає CIN ІІІ. Проведено ексцизійне лікування. Диспансерне спостереження із призначенням цитології або ко-тестування (цитологія та ВПЛ-тест) кожні 6 міс протягом перших 2 років спостереження. Надалі пацієнтка обстежується 1 раз на рік.
Для комплексної терапії вторинних iмунодефіцитних станів, що проявляються у вигляді хронічних уповільнених рецидивуючих інфекційно-запальних процесів будь-якої локалізації, доповідач рекомендувала використовувати сучасні надійні засоби із групи імуномодуляторів природного походження з широким спектром дії. Оскільки головною мішенню для імуномодуляторів мікробного походження є фагоцитарні клітини, такі препарати посилюють функціональні властивості фагоцитів (фагоцитоз і внутрішньоклітинний кілінг поглинених мікроорганізмів) та проявляють цитолітичну активність проти клітин, ДНК яких було трансформовано папіломавірусами. Це сприяє збільшенню продукції прозапальних цитокінів, необхідних для ініціації гуморального і клітинного імунітету. Крім того, представники цієї групи лікарських засобів збільшують продукцію антитіл, активують утворення антигенспецифічних Т-хелперів і T-кілерів (Хаитов Р. М. и соавт., 2018).
У ході доповіді Ю. Б. Якимчук представила ще декілька клінічних випадків із власної практики.
Таким чином, проблема поширення раку шийки матки залишається однією з найактуальніших у сфері онкогінекології, тому вчасна діагностика патологічного стану є ключовою передумовою ефективного лікування.
Підготувала Вероніка Яремчук
Тематичний номер «Акушерство, Гінекологія, Репродуктологія» № 1-2 (47-48) 2022 р.



