22 лютого, 2019
Оценка влияния сахарного диабета на прогнозирование развития цирроза и других исходов неалкогольной жировой болезни печени с помощью неинвазивных методик диагностики фиброза, основанных на определении сывороточных индексов
Установлено, что пациенты с неалкогольной жировой болезнью печени (НАЖБП) и сопутствующим сахарным диабетом (СД) более подвержены риску развития цирроза и смерти, причиной которой являются заболевания печени. Именно поэтому точная оценка фиброза у этих больных является крайне важной.
Так, была изучена возможность применения неинвазивных методов диагностики фиброза печени, в частности сывороточных индексов Hepascore, шкалы фиброза при НАЖБП (NFS), APRI и FIB‑4 для определения исходов НАЖБП у пациентов с/без СД. Результаты исследования продемонстрировали, что у больных с СД точность вышеназванных тестов для прогнозирования цирроза, а также летальности и необходимости в трансплантации печени ниже, чем среди пациентов без СД.
Актуальность проблемы
НАЖБП – наиболее распространенное в мировой популяции хроническое заболевание печени. По прогнозам, в течение следующих 20 лет НАЖБП займет лидирующие позиции в структуре заболеваний печени и станет ведущей причиной смертности, связанной с печеночной патологией, что обусловлено глобальной эпидемией ожирения и СД в мире. Ожидается, что в ближайшие годы НАЖБП также будет основным показанием для проведения трансплантаций печени. Несмотря на это, лишь у небольшого числа пациентов с НАЖБП развивается терминальная стадия заболевания или возникают летальные случаи, связанные с осложнениями со стороны печени. Таким образом, выявление пациентов с наибольшим риском развития осложнений заболеваний печени остается ключевой клинической необходимостью для определения приоритетности их лечения, соответствия критериям клинических испытаний и мониторинга.
СД 2 типа (CД 2) стал неоспоримым фактором риска развития цирроза, декомпенсации функции печени и смерти среди пациентов с НАЖБП. Распространенность продвинутых стадий фиброза у пациентов диабетических клиник составляет 7-10%, а риск смерти от печеночной патологии у лиц общей популяции, имеющих СД, более чем в 2 раза выше по сравнению с таковыми без СД. Из этого следует, что наличие СД позволяет отнести пациентов с НАЖБП в группу риска, однако не является достаточно чувствительным или специфичным критерием для прогнозирования цирроза или исходов заболеваний печени. Поэтому точное определение наличия цирроза и прогноз исходов заболевания печени у пациентов с НАЖБП, страдающих СД, имеет важное значение и напрямую влияет на выбор клинической тактики относительно своевременного выявления гепатоцеллюлярной карциномы (ГЦК) и варикозно расширенных вен пищевода, необходимость проведения фармакотерапии, а также постоянного мониторинга и последующего динамического контроля.
Сегодня степень фиброза печени является наиболее сильным предиктором отдаленных клинических исходов у пациентов с НАЖБП, в том числе смертности, декомпенсации функции печени и ГЦК. Несмотря на то что биопсия печени остается золотым стандартом оценки стадии заболевания, инвазивность метода делает его непрактичным для широкого использования в качестве прогностического инструмента. Хорошей альтернативой считаются тест-панели, основанные на определении сывороточных показателей, что объясняется их широкой доступностью, простотой использования, стоимостью и приемлемостью для пациента. Несколько неинвазивных тестов, в том числе APRI, FIB‑4, Hepascore и NFS, продемонстрировали хорошую степень точности и высокую прогностическую ценность отрицательного результата для исключения продвинутых стадий фиброза. Вдобавок, будучи надежными предикторами прогрессирующего фиброза печени, некоторые сывороточные панели показали способность прогнозирования общей и/или связанной с проблемами печени смертности у пациентов с НАЖБП.
Несмотря на внедрение неинвазивных методов оценки фиброза в клиническую практику, очевидным остается возможное влияние на их результаты различных факторов со стороны пациента, что может снизить точность и ограничить интерпретацию тестов. Как было отмечено при анализе результатов теста BARD для определения прогрессирующего фиброза, одним из таких факторов у пациентов с НАЖБП может быть СД 2, который способствовал уменьшению показателей фиброза у пациентов с СД 2. Эти данные не были подтверждены, а вопрос, связан ли СД со снижением точности или ухудшением прогностической способности других тестов для диагностики фиброза, основанных на анализе крови, остается открытым. Поэтому целью исследования стало изучение влияния СД на 4 непатентованных алгоритма (NFS, Hepascore, APRI и FIB‑4), прежде всего, для определения цирроза, а также прогнозирования общей смертности, исходов заболеваний печени и ГЦК у пациентов с НАЖБП.
Характеристика пациентов и методы исследования
С 2006 по 2015 год в отделении гепатологии больницы им. сэра Чарльза Гарднера (Западная Австралия) было проведено когортное исследование пациентов с диагнозом НАЖБП, которые предварительно были внесены в биобанк отделения. Критериями включения в исследование были: установленный диагноз НАЖБП по данным биопсии печени (наличие >5% стеатоза или жировой инфильтрации), подтвержденный визуализационными методами (УЗИ брюшной полости, магнитно-резонансной или компьютерной томографией); наличие данных для расчета показателей Hepascore, NFS, FIB‑4 и APRI; проведение наблюдения за больным на протяжении более чем 6 мес после расчета показателей фиброза. Критерии исключения предусматривали: наличие сопутствующих заболеваний печени, в том числе вирусного гепатита, гемохроматоза, дефицита α1-антитрипсина, болезни Вильсона, аутоиммунных и лекарственных поражений печени по результатам общеклинических и лабораторных исследований; ранее проведенную трансплантацию печени; наличие признаков декомпенсации функции печени и ГЦК до даты включения в исследование; вторичные причины НАЖБП; ВИЧ-инфекцию; среднесуточное потребление алкоголя >20 г для мужчин и >10 г для женщин в анамнезе.
Были получены такие необходимые клинические и лабораторные данные, как возраст, пол и этническая принадлежность, индекс массы тела, показатели аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), холестерина, триглицеридов, глюкозы натощак, билирубина, количества тромбоцитов, международного нормализованного отношения, щелочной фосфатазы, креатинина и альбумина. Учитывались сопутствующие заболевания, в том числе СД 2, гипертония, ишемическая болезнь сердца и метаболический синдром. Диагноз СД 2 типа устанавливался на основе наличия СД в анамнезе, использования антидиабетических препаратов и/или уровня глюкозы в плазме натощак ≥110 мг/мл или уровня глюкозы в крови по результатам двухчасового перорального теста на толерантность к глюкозе ≥126 мг/ мл. Показатели фиброза неинвазивных диагностических методов рассчитывались по опубликованным формулам.
Гистологическая оценка биоптатов печени проводилась одним и тем же специалистом по шкале NASH-CRN. Стадии фиброза классифицировались следующим образом: F0 – фиброз отсутствует; F1 – перисинусоидальный/перивенулярный фиброз 3-й зоны; F2 – фиброз в 3-й зоне и перипортальный фиброз; F3 – септальный/мостовидный фиброз; F4 – цирроз. F3 и F4 рассматривались как продвинутые стадии фиброза.
Последующее наблюдение за больными предусматривало проведение клинических исследований в гепатологической клинике на протяжении 6 месяцев. Согласно стандартам пациентам с циррозом печени проводилось плановое УЗИ для исключения ГЦК каждые 6 мес и эндоскопический скрининг на предмет наличия варикозно расширенных вен. Первичным исходом во время наблюдения считалась смерть от заболевания печени или необходимость в трансплантации печени. Вторичные исходы включали возникновение первого эпизода декомпенсации функции печени и ГЦК. Печеночная декомпенсация определялась как первое возникновение одного из следующих признаков: асцита, печеночной энцефалопатии, спонтанного бактериального перитонита, кровотечения из варикозно расширенных вен, гепаторенального синдрома. ГЦК была диагностирована в соответствии со стандартными критериями.
Результаты
Общие характеристики
В исследование были включены 284 пациента (из них 152 (53%) женщины; средний возраст равнялся 54±13 лет). 233 (94%) пациента были представителями европеоидной расы, 151 (53%) участник имел диагноз СД 2). Больные с СД 2 составили более старшую возрастную группу (57,5±11,7 vs 50,5±13,6 года) и изначально имели более высокие показатели фиброза. У всех пациентов с циррозом был ранее поставленный диагноз СД со средним сроком между установлением этих диагнозов 8,9 года (в диапазоне 3-26 лет). НАЖБП была подтверждена в 241 (84%) случае биопсией печени и в 43 (16%) – неинвазивными методами.
Клинические исходы: смерть, декомпенсация функции печени и ГЦК
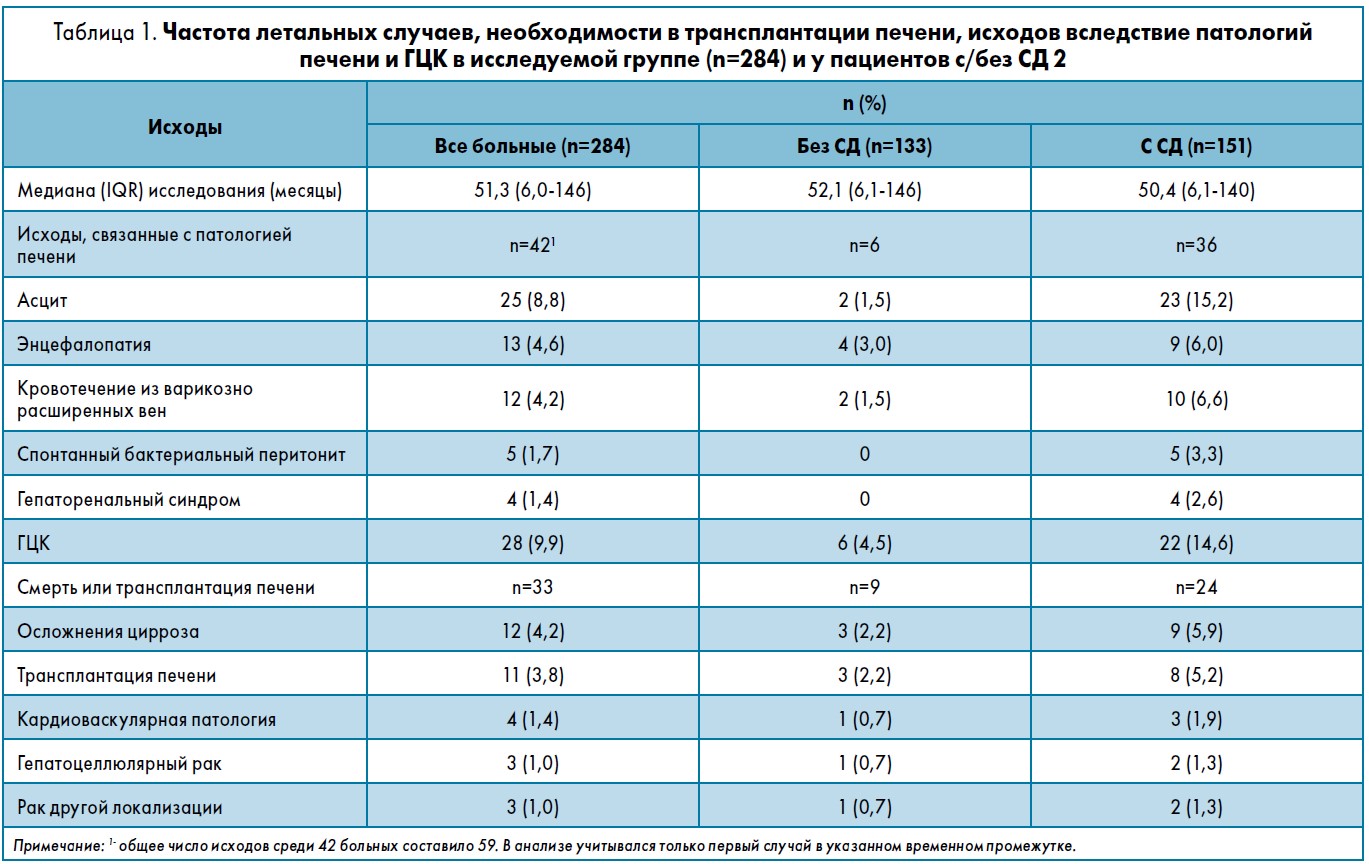
На протяжении периода наблюдения, медиана которого составила 51 мес (6,1-146 мес), у 33 (11,6%) больных был зафиксирован летальный исход или проведена трансплантация печени; 42 (14,8%) пациента имели декомпенсацию функции печени, а у 28 (9,9%) была диагностирована ГЦК (табл. 1). Смерть 33 пациентов в большинстве случаев (36,4%) была связана с осложнениями цирроза, а в трех (9,0%) – с ГЦК. Сердечно-сосудистые заболевания и внепеченочные злокачественные новообразования заняли второе место среди наиболее распространенных причин смерти, на которые пришлось 12,1% всех случаев. Во время исследования 11 пациентам была выполнена пересадка печени. Преимущественными проявлениями декомпенсации функции печени были асцит, энцефалопатия и кровотечение из варикозно расширенных вен (перечислены в порядке уменьшения частоты). Больные с СД имели более высокую вероятность развития декомпенсации функции печени, ГЦК и смерти от осложнений со стороны печени, также они больше нуждались в трансплантации печени по сравнению с пациентами без СД.
Точность неинвазивных методик диагностики фиброза, основанных на определении сывороточных индексов, в отношении прогнозирования фиброза
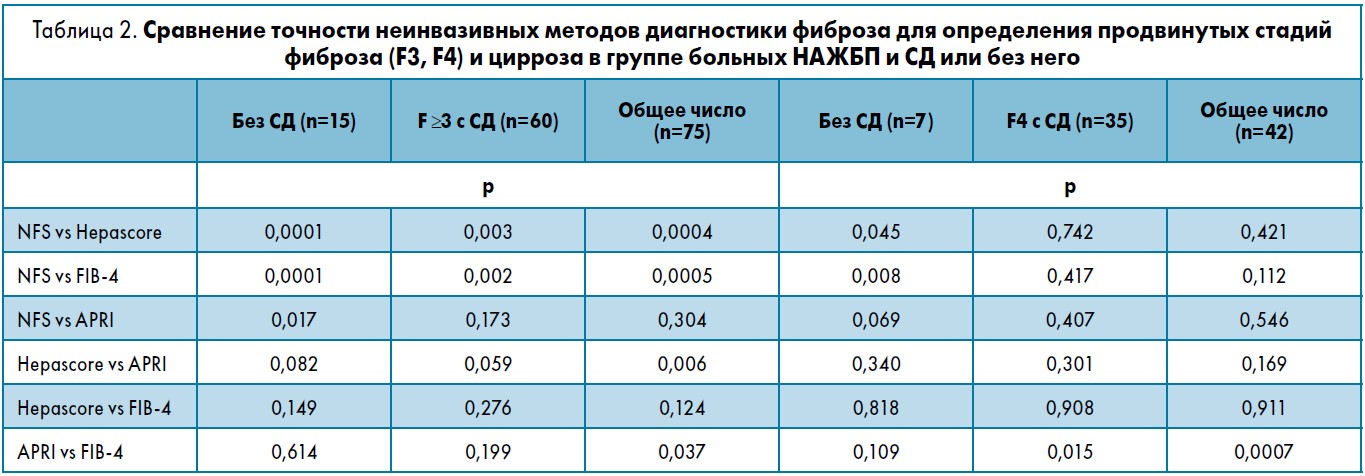
Среди больных, у которых наличие НАЖБП было доказано гистологически, 117 не имели СД, а 124 страдали СД. В диагностике продвинутых стадий фиброза в подгруппе пациентов, которым была проведена биопсия (≥F3-F4, n=75), Hepascore и FIB‑4 продемонстрировали значительно более точные результаты, чем APRI и NFS (табл. 2). При этом статистически значимые значения были лишь у Hepascore. FIB‑4 и Hepascore являлись более точными методами неинвазивной диагностики фиброза, чем NFS, как среди больных с СД, так и без него.
Для прогнозирования цирроза у всех исследуемых (F4, n=42) только тест FIB‑4 оказался более точным, чем APRI. При сравнении пациентов с/без СД точность Hepascore, FIB‑4 и APRI была значительно выше у больных без СД, а NFS вовсе не продемонстрировал отличий между группами.
Поскольку на точность проведенных тестов может влиять возраст пациентов, анализ результатов был повторен с учетом возраста, однако существенных различий найдено не было.
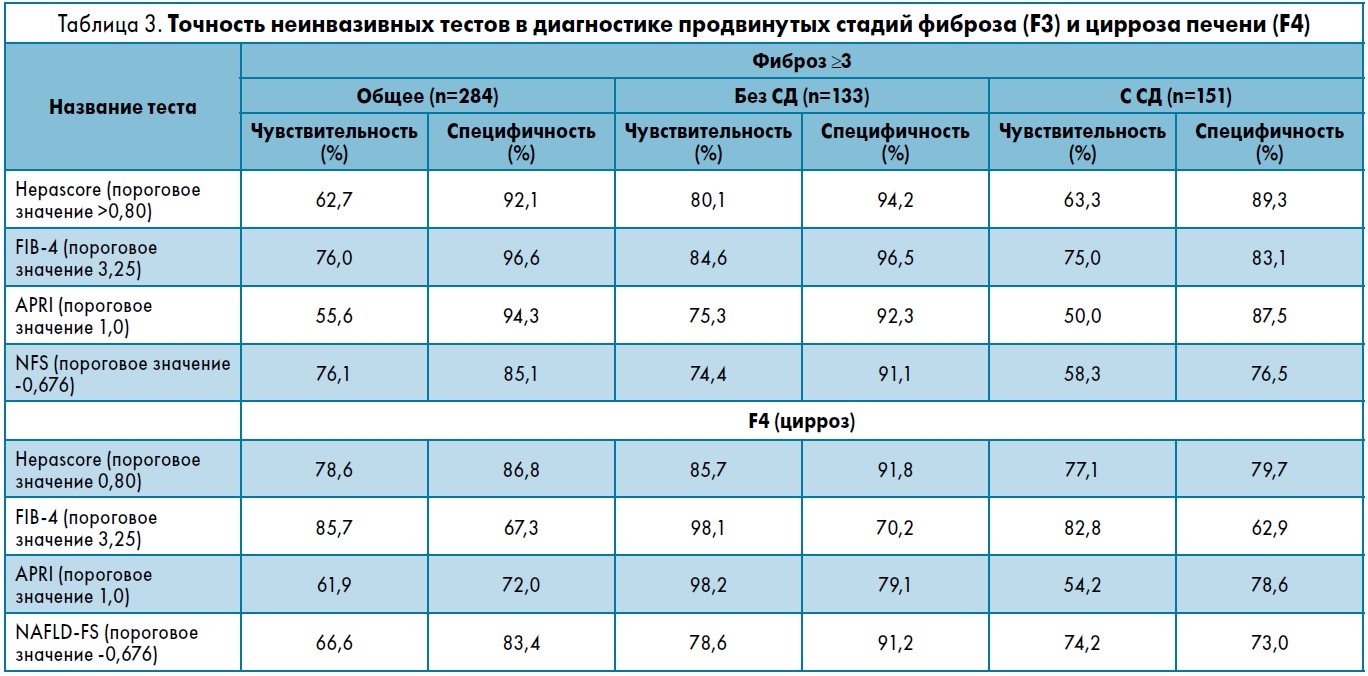
Сопоставимость результатов анализов биомаркеров различных тестов для определения продвинутых стадий фиброза была довольно высокой между FIB‑4, APRI и NFS, но недостаточной между Hepascore и другими тестами. В целом процент соответствия результатов был ниже у пациентов с СД по сравнению с пациентами без него. Для диагностики продвинутых стадий фиброза и цирроза каждый тест имел в целом более высокие показатели чувствительности и специфичности у больных без СД по сравнению с пациентами с СД (табл. 3).
Точность неинвазивных методик диагностики фиброза, основанных на определении сывороточных индексов, в отношении прогнозирования клинических исходов и смертности
Основные значения всех неинвазивных методик диагностики фиброза продемонстрировали высокую точность для прогнозирования ГЦК и декомпенсации функции печени. Однако для прогнозирования последней у больных с СД все тесты, кроме NFS, были значительно менее точными, чем у пациентов без СД. Важно отметить, что в группе больных без СД точность NFS была ниже в прогнозировании декомпенсации функции печени в сравнении с FIB‑4 и Hepascore. Все диагностические модели являлись менее точными для прогнозирования ГЦК у пациентов с СД по сравнению с пациентами без него, но имели достаточную точность для прогнозирования общей смертности. Результаты оставались сопоставимыми, когда анализ проводился исключительно среди пациентов, которым была выполнена биопсия печени (n=241), при этом на фоне СД неинвазивные тесты были менее точны для прогнозирования декомпенсации функции печени (кроме NFS) и ГЦК по сравнению с больными без СД.
Анализ соответствия результатов различных неинвазивных тестов для оценки клинических исходов продемонстрировал самое высокое сходство между APRI и FIB‑4 во всех группах. При наличии СД соответствие результатов всех методов было меньше.
Прогнозирование клинических исходов и смертности
Среди больных СД с высокими исходными показателями тестов на протяжении 5 лет наблюдалась повышенная частота случаев декомпенсации функции печени, которая варьировала в пределах 23-37%, а также ГЦК – 13-25%. Тем не менее у пациентов с исходно низкими показателями фиброза риск развития декомпенсации функции печени также был неприемлемо высоким (NFS – 21%, FIB‑4 – 15%, APRI – 15%), за исключением результатов по шкале Hepascore (1,5%). Не было найдено отличий в общей частоте возникновения декомпенсации функции печени (21 vs 23%) или ГЦК (27 vs 13%) на протяжении 5 лет среди больных СД с низкими или повышенными цифрами NFS.
Напротив, в течение всего периода наблюдения ни у одного пациента без СД с низкими исходными показателями фиброза не развивалась декомпенсация функции печени или ГЦК, что демонстрирует прекрасную отрицательную прогностическую ценность неинвазивных методов диагностики фиброза у пациентов без СД. Среди пациентов с повышенными исходными показателями фиброза общая частота случаев декомпенсации функции печени и ГЦК варьировала от 5 до 12% и от 7 до 18% соответственно.
Обсуждение
Указанные исследования продемонстрировали, что у пациентов с НАЖБП точность четырех выбранных неинвазивных методик определения фиброза для прогнозирования цирроза и исходов заболеваний печени значительно ниже на фоне СД.
У больных без СД, которые имели низкие показатели фиброза, в течение 5-летнего периода не развивались осложнения со стороны печени. Имплементация этих данных в клиническую практику отстрочила бы проведение повторного осмотра этих пациентов на 5-летний период. С другой стороны, у пациентов с СД и низкими показателями NFS, FIB‑4 или APRI частота декомпенсации функции печени составляет 15-21%, а ГЦК – 10-27% в течение 5 лет, что свидетельствует о том, что эти алгоритмы не подходят для прогнозирования результатов или принятия решений о лечении пациентов с СД.
Было отмечено несколько спе-цифических отличий между проанализированными неинвазивными тестами. В то время как точность Hepascore для прогнозирования цирроза и декомпенсации функции печени у пациентов с СД была ниже по сравнению с таковой у пациентов без него, статистические данные у пациентов с СД дали прекрасные результаты. Низкие показатели Hepascore у пациентов с СД в дальнейшем были ассоциированы с предельно низкой общей частотой декомпенсации функции печени и развития ГЦК (0,5 и 0% соответственно), поэтому Hepascore целесообразно использовать для прогноза исходов заболеваний печени у этой категории больных.
Другая находка заключается в том, что не было обнаружено значительного различия в точности определения декомпенсации функции печени с помощью NFS у больных с/без СД. Примечательно, что для расчета индекса NFS используется наличие СД или нарушенной толерантности к глюкозе. Поэтому лишь немногие пациенты с СД имеют NFS ниже «безопасного» уровня и только 13 из 153 (9%) пациентов с СД в исследовании имели показатель ниже -1,455. Таким образом, использование NFS для исключения будущих событий у больных с СД ограничено.
Низкая эффективность неинвазивных методик при СД может быть отчасти связана с недостаточной информативностью показателей АСТ и АЛТ, которые используются для подсчета APRI, FIB‑4 и NFS. S.A. Harrison и соавт. ранее продемонстрировали, что вероятность возникновения развитого фиброза печени при соотношении AST/ALT >0,8 резко снижается именно на фоне СД. На животных моделях также было показано, что при гипергликемии могут наблюдаться видимые колебания аминотрансфераз в виде повышения цитозольного АСТ, что объясняется усилением глюконеогенеза в печени. Стоит подчеркнуть, что СД наименьшим образом влиял на показатели Hepascore, в алгоритме которого не учитываются уровни АСТ и АЛТ.
Еще одним важным результатом исследования стало то, что каждый неинвазивный метод диагностики фиброза был более точным для прогнозирования декомпенсации функции печени, чем общей выживаемости, что подтверждает их специфичность в плане исходов заболеваний печени и подчеркивает отсутствие влияния на их результаты других сопутствующих заболеваний, например сердечно-сосудистой патологии.
APRI – наиболее простой неинвазивный тест, требующий для получения результата только показателей АСТ и количества тромбоцитов. Он имел и самую низкую точность в прогнозировании декомпенсации функции печени. Этот результат подтверждается другими ранее выполненными исследованиями, демонстрирующими, что точность APRI значительно ниже, чем у методов, предусматривающих более сложные алгоритмы, таких как FIB‑4, NFS, Hepascore и FibrometerV2G. Он также имеет более низкую точность для прогнозирования фиброза по сравнению с другими более сложными методами. Таким образом, APRI не должен быть предпочтительным среди других неинвазивных методов диагностики фиброза печени, основанных на определении сывороточных показателей у пациентов с НАЖБП.
Альтернативным неинвазивным методом оценки фиброза печени, который позволяет прогнозировать результаты у пациентов с НАЖБП, является эластография. В одном из исследований, включивших 360 пациентов, было продемонстрировано, что Fibroscan был более точным, чем сывороточные индексы Hepascore или FibrometerV2G, для прогнозирования фиброза, но не смерти вследствие развития печеночных осложнений. Ограничением эластографии является невозможность проведения сканирования при ожирении или его неинформативность, а также ограниченная доступность метода. Использование неинвазивных панелей, основанных на анализе сывороточных маркеров, изучаемых в данном исследовании, – доступный и недорогой прогностический инструмент, который может легко применяться на практике.
Проведенная работа показала, что наличие СД значительно влияет на диагностическую и прогностическую ценность широко используемых неинвазивных тестов для диагностики фиброза при НАЖБП, тогда как у пациентов без СД показатели этих методов являются достаточно точными. У пациентов с СД NFS, APRI и FIB‑4 не продемонстрировали надежности в плане исключения риска будущих негативных исходов.
Таким образом, пациенты с НАЖБП, страдающие СД, должны быть отнесены в группу риска с повышенной вероятностью возникновения цирроза, ГЦК и смерти вследствие осложнений заболеваний печени. Стандартные неинвазивные методы диагностики фиброза, основанные на анализе показателей сыворотки крови, менее точны для диагностики цирроза печени, прогнозирования ГЦК и декомпенсации функции печени у пациентов с НАЖБП и сопутствующим СД, поскольку они достоверно исключают цирроз и риск будущей декомпенсации печени у пациентов с НАЖБП без СД. Поэтому для оценки фиброза у пациентов с НАЖБП и СД актуальным вопросом является разработка новых прогностических моделей.
Адаптированный перевод с англ.
Татьяны Радионовой
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 4 (44) грудень 2018 р.