30 жовтня, 2020
Хіміоіндукована гепатотоксичність в онкологічних хворих і сучасні погляди на її корекцію
 Епідеміологічна ситуація в світі загалом та в Україні зокрема дала поштовх для широкого впровадження дистанційних освітніх заходів. Науково-практична конференція з онлайн-трансляцією UkraineOncoGlobal‑2020, що відбулася 15 липня (м. Київ), є черговим прикладом втілення концепції безперервного професійного розвитку в сучасних умовах. У рамках заходу було представлено доповіді провідних вітчизняних фахівців, які висвітлювали різноманітні актуальні питання лікування онкологічних хворих. Серед них було розглянуто питання проявів гепатотоксичності у пацієнтів, які отримують протипухлинну терапію, та підходи до її коригування. Доповідь, присвячена цьому аспекту, була представлена Наталією Миколаївною Отченаш (лікар-онколог КНП «Обласний центр онкології», м. Харків).
Епідеміологічна ситуація в світі загалом та в Україні зокрема дала поштовх для широкого впровадження дистанційних освітніх заходів. Науково-практична конференція з онлайн-трансляцією UkraineOncoGlobal‑2020, що відбулася 15 липня (м. Київ), є черговим прикладом втілення концепції безперервного професійного розвитку в сучасних умовах. У рамках заходу було представлено доповіді провідних вітчизняних фахівців, які висвітлювали різноманітні актуальні питання лікування онкологічних хворих. Серед них було розглянуто питання проявів гепатотоксичності у пацієнтів, які отримують протипухлинну терапію, та підходи до її коригування. Доповідь, присвячена цьому аспекту, була представлена Наталією Миколаївною Отченаш (лікар-онколог КНП «Обласний центр онкології», м. Харків).
– Гепатотоксичність, або ураження печінки лікарськими засобами, – це патологічний процес, який розвивається у печінці при використанні лікарських агентів у терапевтичних дозах. Важливо зазначити, що у 47% онкологічних хворих гепатотоксичність є причиною відтермінування хіміотерапії (D. Santini et al., 2003; B. Vincenzi et al., 2011), що, у свою чергу, може призводити до гірших результатів лікування. Загалом частота розвитку гепатотоксичності під час проведення системної протипухлинної терапії варіює від 14,3 до 100% (J. Floyd et al., 2006; E. Petit et al., 2008; F.A. Rodrigues-Frias et al., 2007; A. Tannapfel et al., 2008). При цьому у клінічній практиці під час проведення хіміотерапії лікарі діагностують лише 50,6% випадків гепатотоксичності, а відповідне лікування з приводу гепатотоксичних проявів отримують лише 30,4% пацієнтів (А.Н. Козюлін та ін., 2010). Це свідчить, на жаль, про недостатню настороженість лікарів щодо цієї патології.
Виділяють такі фактори ризику ушкодження печінки лікарськими засобами:
- токсичний потенціал лікарського засобу (реактивні метаболіти, мітохондріальні ефекти, виснаження молекул, які беруть участь у детоксикації, наприклад глутатіону);
- генетичні фактори, що впливають на метаболізм лікарських засобів, детоксикацію, транспорт і т.ін.;
- фактори навколишнього середовища (початковий стан функції печінки, вік, стать, кількість лікарських засобів, які отримує пацієнт, фонові системні захворювання).
Лікарські засоби можуть мати два варіанти ушкоджувальної дії на печінку. Пряма гепатотоксична дія виникає внаслідок безпосереднього ушкодження клітинних структур (мітохондрії, мікрофіламенти тощо), блокади транспортних насосів, денатурації білків. Окрім цього, для прямого гепатотоксичного ефекту наявна залежність ризику ушкодження від дози, а також короткий з встановленими строками період маніфестації. Непряма гепатотоксична дія виникає внаслідок дії метаболітів або імуноалергічного ураження печінки, не залежить від дози та характеризується непрогнозованою тривалістю маніфестації.
Встановлені механізми ушкодження печінки лікарськими засобами. До них належать руйнування мембрани гепатоцитів, актинових волокон жовчних проток (що призводить до порушення секреції жовчі), розладу транспортного насоса MRP3 (з подальшим порушенням екскреції у білірубін органічних сполук лікарського препарату), вплив на цитохром Р450, який забезпечує метаболізм лікарських засобів, активацію каспаз і блокування функції мітохондрій.
Причинами розвитку токсичного гепатиту в онкологічних хворих можуть бути не лише протипухлинні лікарські засоби, а й хірургічні втручання на печінці та хронічне ураження органа. Різноманітні протипухлинні засоби зумовлюють різну гепатотоксичність, але слід пам’ятати, що всі вони тією чи іншою мірою чинять гепатотоксичний вплив.
Причинами гепатотоксичного ефекту протипухлинних препаратів є активація і розпад більшості цитостатиків у печінці. Окрім цього, метаболіти справляють прямий токсичний вплив на цей орган. Морфологічні зміни печінки, що виникають у результаті цитолізу, супроводжуються функціональними змінами.
Механізми гепатотоксичності протипухлинних препаратів мають відмінності. Алкілувальні засоби призводять до розвитку центролобулярного чи перипортального ушкодження, холестазу, на фоні якого у низці випадків розвивається запалення. Антиметаболіти спричиняють розвиток венооклюзійної хвороби, холестаз і чинять пряму цитотоксичну ушкоджувальну дію на гепатоцити. Похідні нітрозосечовини призводять до виснаження внутрішньопечінкових запасів глутатіону, що істотно підвищує ризик окисного ушкодження печінки. Протипухлинні антибіотики ушкоджують мембрану гепатоцитів з утворенням вільних радикалів. Алкалоїди барвінку й таксани викликають токсичне ушкодження печінки, в тому числі неалкогольний стеатогепатит. Препарати платини спричиняють жировий гепатоз, неалкогольний стеатогепатит і венооклюзійну хворобу. Інтерферони й інтерлейкіни активують Т-кілери та підвищують експресію прозапальних цитокінів, можуть чинити прямий токсичний вплив на гепатоцити. Гормональні засоби можуть призводити до розвитку холестазу. Таргетна терапія здатна спричиняти синусоїдальну дилатацію.
Гепатотоксичність нерідко має тривалий латентний період і проявляється ізольованим підвищенням активності сироваткових трансаміназ. Тому ушкодження печінки може діагностуватися лише при поглибленому обстеженні й часто у віддалений термін. У зв’язку з цим необхідно ретельно збирати інформацію щодо лікарських засобів, які приймає пацієнт, включаючи дозування та тривалість терапії. Важливо з’ясувати, чи наявні захворювання печінки, оскільки дія препарату може їх обтяжити.
Діагностичний мінімум при підозрі на гепатотоксичний вплив лікарського засобу включає визначення рівня аланінамінотрансферази (АЛТ), аспартатамінотрансферази (АСТ), лужної фосфатази (ЛФ), білірубіну, міжнародного нормалізованого відношення (МНВ), клінічний аналіз крові та ультразвукове дослідження печінки. Необхідно виключити наявність вірусних, ішемічного й аутоімунного гепатитів, алкогольного ураження печінки, обструктивних захворювань жовчних шляхів, пухлинного ураження печінки. Важливо ретельно зібрати анамнез щодо прийому лікарських засобів і визначити домінуючий тип ураження печінки.
Розроблені шкали для встановлення й оцінки взаємозв’язку між прийомом препарату та розвитком ураження печінки (RUCAM, DILIN та ін.). Критерії діагностики ушкодження печінки наведені в таблиці.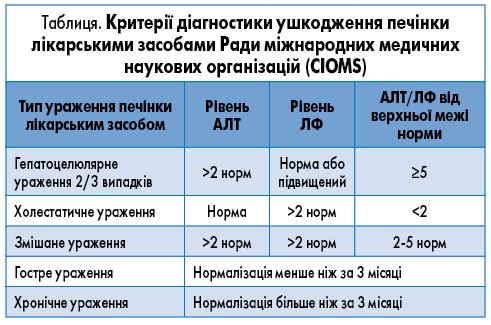
Пункційна біопсія печінки не потрібна, якщо ураження печінки лікарським засобом доведено та відбувається нормалізація функціональних показників печінки протягом 6 місяців. У разі тяжкого і прогресуючого перебігу пункційну біопсію печінки можна виконувати з метою диференційної діагностики від аутоімунного гепатиту.
Діагностика гепатотоксичності під час проведення системної протипухлинної терапії має певні особливості. Підвищення рівня АЛТ – найчутливіший тест для ранньої діагностики ушкодження печінки лікарськими засобами. Підвищення вмісту АСТ виникає при мітохондріальних гепатоцитопатіях. Якщо коефіцієнт де Рітіса (АСТ/АЛТ) становить <1, то підвищення рівня трансаміназ трактується як запальний тип відповіді, >1 – як некротичний тип. Нормалізація рівня АЛТ при сприятливому перебігу відбувається протягом декількох тижнів. Повторне чи прогресуюче підвищення рівня трансаміназ свідчить про прогресування ураження печінки.
Критерії відміни препарату, що спричинив гепатотоксичність, при гепатоцелюлярному типі включають:
- підвищення вмісту АЛТ більш ніж у 8 разів за норму в будь-який момент від початку прийому препарату;
- підвищення рівня АЛТ більш ніж у 5 разів за норму протягом більше 2 тижнів;
- підвищення вмісту АЛТ більш ніж у 3 рази за норму у поєднанні з підвищенням більш ніж у 2 рази рівнем білірубіну;
- підвищення МНВ більш ніж у 1,5 разу від норми.
Критеріями холестатичного типу гепатотоксичних проявів будуть підвищення вмісту білірубіну більш ніж у 3 рази за норму та збільшення протромбінового часу і МНВ більш ніж у 1,5 разу за норму.
Профілактика та лікування при гепатотоксичних реакціях у онкологічних хворих включає призначення гепатотропної терапії – лікарських засобів, які перешкоджають руйнуванню клітинних мембран і стимулюють регенерацію гепатоцитів, тим самим позитивно впливаючи на функцію печінки. Гепатотропні препарати підвищують стійкість печінки до патологічних факторів, посилюють її дезінтоксикаційну функцію шляхом підвищення активності ферментних систем і сприяють відновленню її функції при різних ушкодженнях (у тому числі токсичного характеру).
Основними вимогами до ефективного та безпечного гепатопротектора є достатньо повна абсорбція, наявність ефекту першого проходження через печінку, виражена здатність зв’язувати або запобігати утворенню високоактивних ушкоджувальних сполук, зменшувати надмірно виражене запалення, пригнічувати фіброгенез, стимулювати регенерацію печінки, природний метаболізм при патології печінки, екстенсивну ентерогепатичну циркуляцію, а також відсутність токсичності.
Вибір гепатотропного препарату має відбуватись у першу чергу з урахуванням принципів доказової медицини. Слід зважати, що всі хронічні захворювання печінки супроводжуються дефіцитом адеметіоніну, який є обов’язковим компонентом метаболізму гепатоцита. Адеметіонін синтезується в організмі з метіоніну й аденозину за допомогою ферменту адеметіонінсинтетази, функція якого порушується при захворюваннях печінки. Дефіцит адеметіоніну відіграє ключову роль у патогенезі захворювань печінки. Зниження рівня адеметіоніну погіршує ураження печінки, що призводить до запальних процесів, а згодом – і до незворотних структурних і дистрофічних змін печінки.
Адеметіонін – основний учасник процесів метилювання в організмі, який є основним донором метильних груп для понад сотні біохімічних реакцій метилювання. Первинний синтез адеметіоніну відбувається у печінці, а основними споживачами є печінка та мозок. При нестачі адеметіоніну змінюються характеристики клітинних мембран. Порушення метаболізму при дефіциті адеметіоніну призводить до дефіциту метилфолату і, відповідно, до дефіциту глутатіону – основного антиоксидантного й антитоксичного агента. Дефіцит адеметіоніну може спричиняти розвиток патологічної втоми та когнітивних порушень у пацієнтів із захворюваннями печінки. Однією з причин цього є те, що при зниженні рівня адеметіоніну в головному мозку порушується синтез нейромедіаторів (серотоніну, дофаміну, норадреналіну). Встановлено, що антидепресанти не ефективні за наявності холестатичних захворювань печінки.
Гептрал® – це аналог ендогенного адеметіоніну. Схема застосування препарату Гептрал® залежить від показань. Двоетапний курс лікування з метою досягнення швидкого і стійкого результату включає внутрішньовенне чи внутрішньом’язове введення препарату у дозі 500-1000 мг на добу протягом 14 днів (до стійкої нормалізації функціонального стану печінки) з подальшим переходом на пероральний прийом по 1 таблетці 500 мг 2-3 рази на добу між вживанням їжі. За наявності хронічної печінкової недостатності з внутрішньопечінковим холестазом у період ремісії курсові дози становлять 500-1000-1500 мг на добу перорально. При затяжному перебігу гепатиту, спричиненого лікарськими засобами, який супроводжується внутрішньопечінковим холестазом, патогенетично обґрунтоване призначення курсових доз 500-1000 мг на добу з тривалістю лікування щонайменше 2 місяці. Можливе додаткове призначення урсодезоксихолевої кислоти 10-15 мг/кг маси тіла за 2-3 рази до розрішення холестазу.
Аналіз даних 16 клінічних досліджень (понад 3400 пацієнтів), у яких вивчали вплив адеметіоніну на патологічну втому та астенію, показав, що патологічна втома була характерна для 80% пацієнтів із захворюваннями печінки, а ефективність адеметіоніну відзначалась вже з 7-го дня терапії. Адеметіонін має опосередковану (дезінтоксикаційна й антиоксидантна функція) та пряму нейропротекторну дію (активує процеси метилювання в головному мозку і підвищує синтез нейромедіаторів та нейросинаптичну передачу). Гептрал® є аналогом ендогенного адеметіоніну, завдяки чому він сприяє швидкому (з 7-го дня) відновленню рівня адеметіоніну при захворюваннях печінки, структури та функції гепатоцитів зі швидким клінічним результатом. Препарат характеризується високим рівнем терапевтичної активності при застосуванні як в ін’єкційній, так і в таблетованій формах.
Онкологічні хворі, які отримують системну протипухлинну терапію, мають періодично проходити біохімічний моніторинг та отримувати відповідну супровідну терапію. При значних проявах гепатотоксичності необхідно відкласти чи відмінити застосування препаратів, що її спричинили. Поліпрагмазія має бути зведена до мінімуму, слід враховувати взаємодію всіх лікарських засобів, які отримує пацієнт. Гептрал® – гепатотропна патогенетична терапія, яка продемонструвала свою ефективність у клінічних дослідженнях, забезпечує окрім цього ще й виражений нейропротекторний ефект, що не менш важливо для онкологічних хворих, які отримують хіміотерапію.
Підготувала Олена Поступаленко
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 4 (65) 2020 р.




