2 грудня, 2020
Когнітивний профіль пацієнтів, які перенесли COVID-19: клінічні предиктори нейропсихологічних порушень
Обґрунтування. Когнітивні прояви, пов’язані з тяжкістю нової коронавірусної інфекції (COVID-19), невідомі. Раннє виявлення нейропсихологічних проявів може модифікувати ризик незворотного порушення та подальшого нейрокогнітивного зниження.
Методи. В одноцентрове когортне дослідження було послідовно включено всіх дорослих пацієнтів віком від 20 до 60 років із підтвердженою інфекцією COVID-19. Нейропсихологічну оцінку проводив один і той самий підготовлений нейропсихолог з 22 квітня по 16 червня 2020 року. Пацієнтів із раніше відомими когнітивними порушеннями, будь-якою патологією центральної нервової системи чи психіатричними захворюваннями було виключено. Демографічні, клінічні, фармакологічні та лабораторні дані були отримані з медичної документації.
Результати. Загалом 35 пацієнтів відповідали критеріям включення та були залучені до дослідження.
У пацієнтів із головним болем, аносмією, дисгевзією, діареєю й у тих, хто потребував кисневої терапії, показники субтестів пам’яті, уваги та виконавчої функції були нижчими порівняно з безсимптомними пацієнтами. Пацієнти з головним болем і клінічною гіпоксією мали нижчий показник загального когнітивного індексу (р=0,002; р=0,010). Показник Т <30 спостерігався в доменах пам’яті, уваги та семантичної швидкості (2 [5,7%]), робочої пам’яті та розумової гнучкості (3 [8,6%]), у фонетичній швидкості (4 [11,4%]). Вищі показники тривоги та депресії (р=0,047; р=0,008) були виявлені в пацієнтів із когнітивними скаргами.
Висновки. У нашій когорті хворих на COVID-19 нерідко зустрічалися неврологічні прояви, включно з когнітивними порушеннями. Неврологічні симптоми під час захворювання, діарея та киснева терапія були факторами ризику нейрокогнітивних порушень. Когнітивні скарги були пов’язані з тривогою та депресією.
Вірус SARS-CoV-2 (коронавірус тяжкого гострого респіраторного синдрому-2) є етіологічним чинником коронавірусної хвороби (COVID-19), пандемія котрої швидко набирає обертів. Найпоширенішими симптомами цього захворювання є лихоманка, сухий кашель, утома та задишка. У тяжчих випадках розвиваються пневмонія та дихальна недостатність, через які пацієнти часто потребують госпіталізації.
Лікарі дедалі частіше виявляють неврологічні прояви у хворих на COVID‑19. Найчастішими з них є головний біль, міалгія, втрата смаку та нюху (Mao et al., 2020). Ці симптоми можуть бути наслідком прямого впливу вірусу на центральну нервову систему (ЦНС), результатом пара- чи постінфекційного імуноопосередкованого патологічного процесу, неврологічним ускладненням системного негативного впливу COVID‑19 (Li et al., 2020; Helms et al., 2020).
Подібно до раніше відомого SARS-CoV, збудник COVID‑19 використовує рецептори ангіотензинперетворювального ферменту‑2 (ACE2) для проникнення в клітини (Hoffmann et al., 2020). Це зумовлює необхідність вивчення експресії рецепторів АСЕ2 у ЦНС для визначення безпосереднього впливу COVID‑19 на тканину мозку (Baig et al., 2020).
Mao та співавт. (2020) встановили, що 36,4% пацієнтів із COVID‑19 мали неврологічні прояви. У кількох серіях спостережень повідомлялося про міалгію, головний біль, запаморочення, сплутаність свідомості й епілептичні напади (Li et al., 2020; Wu et al., 2020; Chen et al., 2020; Guan et al., 2020; Arentz et al., 2020). Було опубліковано випадки енцефалопатії й інсульту, пов’язаних із легким і середньотяжким перебігом COVID‑19, імовірно, через протромботичний і прозапальний характер коронавірусної інфекції.
Добре відомо, що вірусні інфекції ЦНС (Warren-Gash et al., 2019), запальні процеси в головному мозку (Sartori et al., 2012) та церебральна гіпоксія (McMorris et al., 2017) можуть спричиняти тимчасові чи стійкі когнітивні порушення. Лімбічна система, зокрема гіпокамп, і пов’язані з нею мозкові структури, такі як базальні ганглії, містять значно більше прозапальних ферментів, аніж інші ділянки головного мозку. Тому існує підвищений ризик розвитку порушень таких нейрокогнітивних процесів, як пам’ять, увага й емоції (Sartori et al., 2012; Raz і Rodrigue, 2006). Пацієнти з хронічною гіпоксією на тлі легеневих захворювань можуть мати гірші показники тестів з оцінки уваги, виконавчих функцій і швидкості обробки інформації. Когнітивні порушення корелюють із тяжкістю легеневої хвороби та свідчать на користь діагнозу енцефалопатії підкіркового типу (Areza-Fegyveres et al., 2010).
Когнітивні порушення внаслідок набутих уражень мозку є частою скаргою в пацієнтів неврологічного профілю, адже вони спричиняють труднощі в повсякденній діяльності та роботі, мають значні негативні функціональні й емоційні наслідки не тільки для самого пацієнта, але й для членів його сім’ї.
Наскільки відомо авторам статті, раніше не проводили досліджень із вивчення розповсюдженості та клінічного визначення когнітивних порушень у хворих на COVID‑19. Оскільки є підстави припускати безпосередній вплив SARS-CoV на ЦНС, найімовірніше, лікарі стикатимуться з більшою частотою нейрокогнітивних скарг у пацієнтів, які одужують після COVID‑19. Ця проблема має велике наукове та клінічне значення, адже когнітивні розлади внаслідок COVID‑19 можуть бути зворотними та мати інші відмінності від порушень вищих нервових функцій, спричинених нейродегенеративними захворюваннями. У цьому дослідженні автори мали на меті оцінити вплив COVID‑19 на нейрокогнітивні показники.
Методи
Дизайн дослідження й учасники
У когортне дослідження включали дорослих пацієнтів з інфекцією SARS-CoV‑2, які проходили обстеження в університетській лікарні Mútua Terrassa з 21 квітня (дата оцінки першого пацієнта) по 16 червня 2020 р. У всіх осіб, включених у дослідження, інфекція SARS-CoV‑2 була підтверджена позитивним результатом полімеразно-ланцюгової реакції мазка з носоглотки та/або позитивною серологією.
Вік пацієнтів варіював від 24 до 60 років. Осіб старшого віку виключали з випробування, щоб уникнути похибки, пов’язаної з віковим зниженням когнітивних функцій. Також із дослідження виключали осіб із попередніми когнітивними порушеннями та будь-якими іншими захворюваннями ЦНС.
Випробування було схвалено місцевим комітетом із питань етики, всі пацієнти підписали інформовану згоду.
Збір даних і методи оцінки
Клінічні дані в лікарні було зібрано проспективно. Надалі автори ретроспективно проаналізували електронну базу медичних карток усіх пацієнтів із лабораторно підтвердженою інфекцією SARS-CoV‑2. Було оцінено демографічні показники, наявність супутніх захворювань, результати аналізів крові, у тому числі рівнів феритину та D‑димеру, симптоми при зверненні, ускладнення, проведене лікування, когнітивні скарги в динаміці, наслідки захворювання. Ускладнення включали гіпоксичну дихальну недостатність, енцефаліт й інсульт. Наслідки захворювання включали тривалість перебування в стаціонарі, тривалість симптомів, необхідність інвазивної механічної вентиляції, статус під час виписки.
Автори відібрали низку тестів для оцінки когнітивних функцій і створили нейропсихологічну батарею, специфічну для досліджуваної популяції пацієнтів. Усі тести валідовані та використовуються на міжнародному рівні. До складу батареї тестів увійшли: тест оцінки словесної пам’яті TAVEC (Test de Aprendizaje Verbal Espana-Complutense); субтест візуального відтворення WMS-IV (Wechsler Memory Scale IV); низка тестів із проєкту NEURONORMA – прямий і зворотний рахунок (Digits Forward and Backward), тест із поєднанням літер і цифр (Letter and Numbers), тест послідовних з’єднань TMT (Trail Making Test A and B), символьно-цифровий тест SDMT (Symbol Digit Modalities Test), тест Струпа, тест вербальної семантичної та фонетичної швидкості, тест копіювання складної фігури FCRO (Figure Complex Rey – Osterrieth), Бостонський тест найменування BNT (Boston Naming Test). Для загальної оцінки когнітивних функцій було використано когнітивний індекс (ICog), що розраховували як середнє арифметичне стандартизованих показників окремих тестів. Нарешті, для оцінки симптомів тривоги та депресії використовували шкалу HAD (Hospital Anxiety and Depression Scale).
Тестування проводилося між 10 і 35 днями після виписки з лікарні кваліфікованим нейропсихологом і тривало приблизно 1 год.
Результати
Демографічні та клінічні характеристики
У період із квітня по червень 2020 р. в університетській лікарні Mútua Terrassa в 454 пацієнтів виявили позитивний результат лабораторного аналізу на SARS-CoV‑2. Після виключення осіб віком понад 60 років, із попередніми когнітивними порушеннями чи будь-якими іншими ураженнями ЦНС або психіки для аналізу було відібрано 35 пацієнтів.
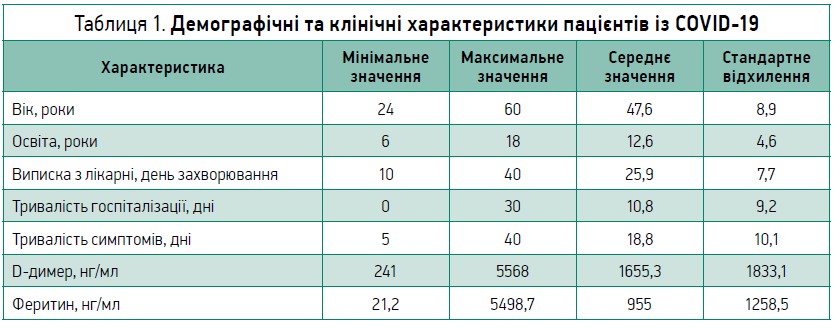
Трохи більше половини становили жінки (54,3%). Середній вік пацієнтів – 47,6±8,9 років. Інші демографічні та клінічні характеристики учасників дослідження представлено в таблиці 1.
Найпоширенішими симптомами на початку захворювання були: лихоманка – в 16 хворих (45,7%), кашель – у 10 (28,6%), утома – в 6 (17,1%), головний біль – у 2 (5,7%), міалгія – в 1 (2,9%). При подальшому перебігу інфекції 33 пацієнти (94,3%) мали проблеми з диханням, 31 (88,6%) – кашель, 34 (97,1%) – лихоманку, 30 (85,7%) – міалгії, 31 (88,6%) – утому, 22 (62,9%) – головний біль, 20 (57,1%) – аносмію, 20 (57,1%) – дисгевзію, 14 (40%) – діарею, 4 (11,4%) – ураження шкіри. Госпіталізації до відділення інтенсивної терапії (ВІТ) потребували 7 пацієнтів (20%), кисневої терапії – 21 (60%).
Середня тривалість перебування в лікарні становила 10,86 дня, а середня тривалість симптомів – 18,8 дня.
Лабораторні дослідження показали, що в чоловіків рівень феритину був вищим, аніж у жінок (1765,9 vs 346,9; р=0,010). Чоловіки також мали вищі рівні D‑димеру (2415,5 vs 1047,2), хоча ця різниця не було статистично значущою (р=0,067). У пацієнтів, яким була потрібна інтенсивна терапія, було виявлено вищі рівні феритину (р=0,034) та D‑димеру (р=0,001). Такі самі результати отримано для хворих, які потребували кисневої терапії під час госпіталізації (р=0,024 та р=0,031 відповідно).
Нейропсихологічні дані
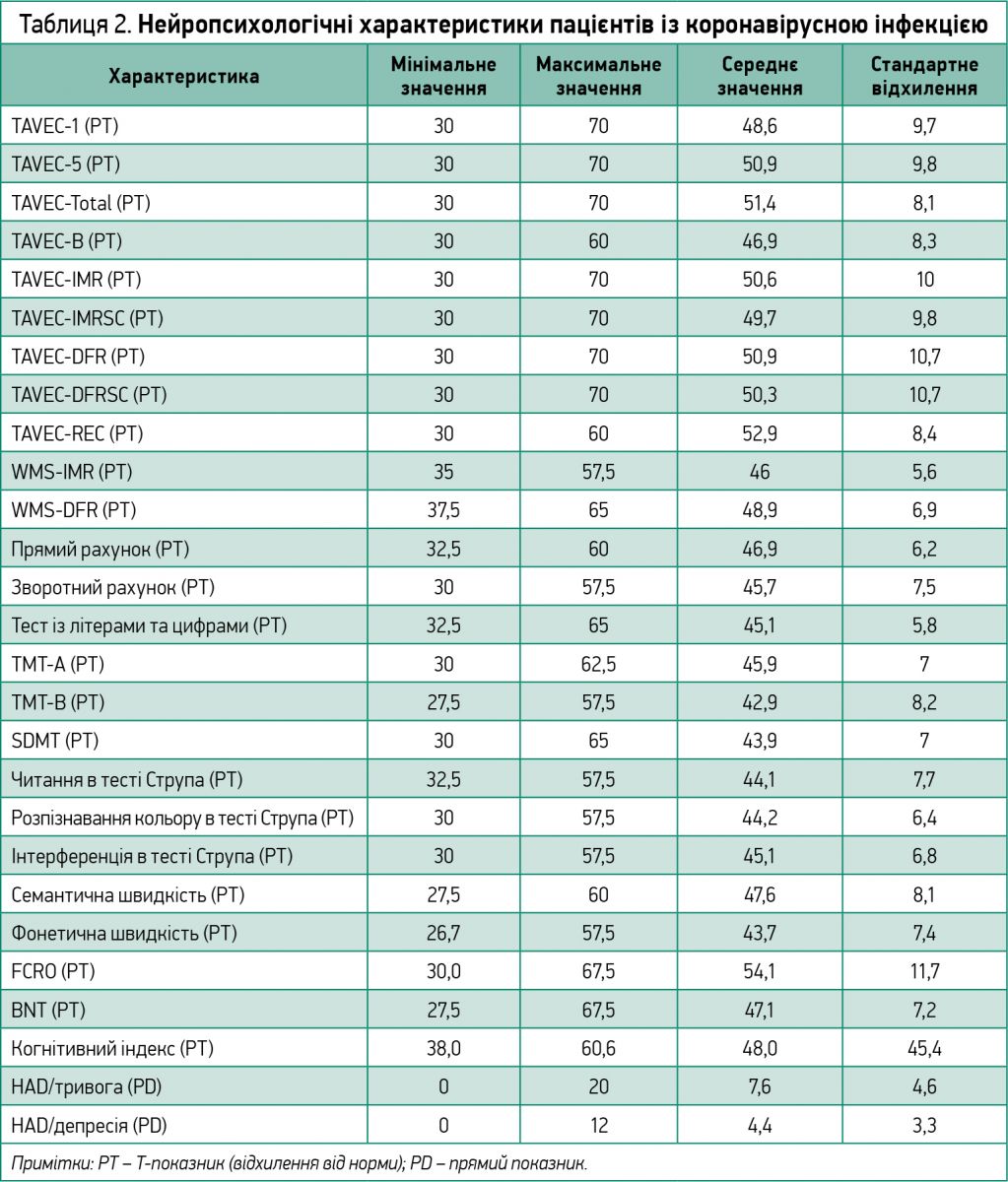
Із досліджуваної когорти 12 пацієнтів (34,3%) мали скарги на когнітивні порушення. Нейропсихологічні характеристики представлено в таблиці 2.
Патологічні показники нейропсихологічних тестів спостерігалися: TAVEC‑1 – у 2 хворих (5,7%), TAVEC‑5 – у 2 (5,7%), TAVEC-Total – в 1 (2,9%), TAVEC-B – у 2 (5,7%), TAVEC-IMR – в 1 (2,9%), TAVEC-IMRSC – у 2 (5,7%), TAVEC-DFR – у 2 (5,7%), TAVEC-DFRSC – у 3 (8,6%), TAVEC-REC – у 2 (5,7%), зворотний рахунок – у 3 (8,6%), TMT-A – в 1 (2,9%), TMT-B – у 3 (8,6%), SDMT – у 2 (5,7%), називання кольорів у тесті Струпа – в 1 (2,9%), інтерференція в тесті Струпа – в 1 (2,9%), семантична швидкість – у 2 (5,7%), фонетична швидкість – у 4 (11,4%), FCRO – в 1 (2,9%), BNT – в 1 (2,9%).
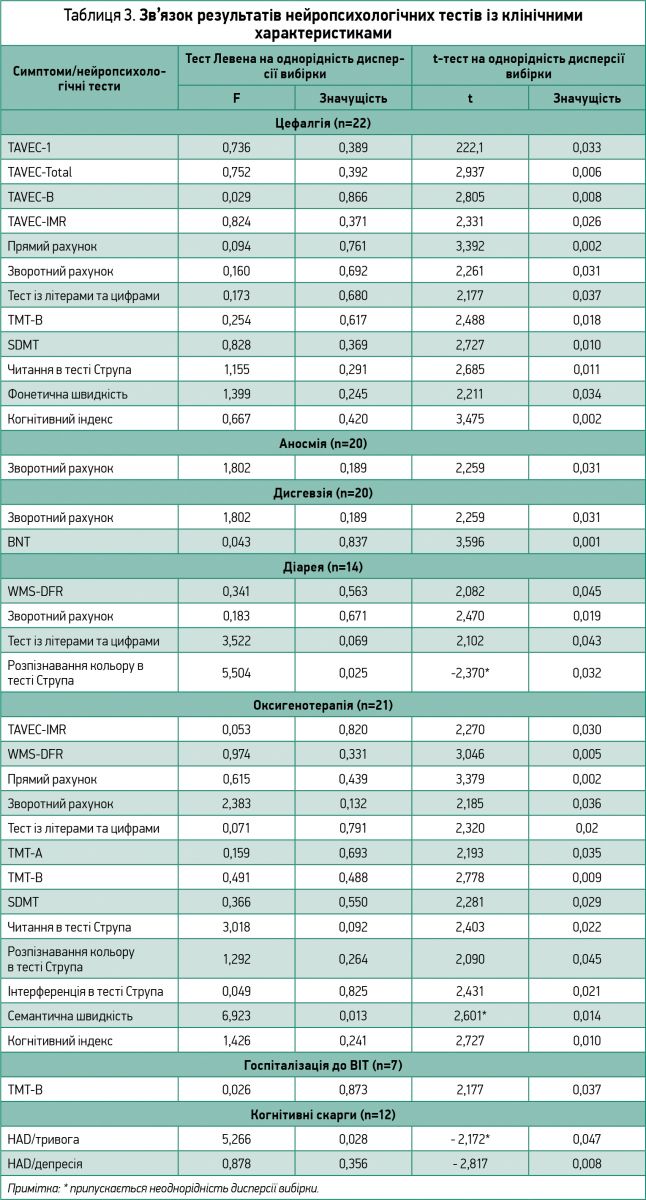
Було проведено аналіз зв’язку між результатами нейропсихологічних тестів і клінічними характеристиками, що відзначалися більш ніж у 5 пацієнтів. Лихоманка, кашель, утома та міалгія були виключені з аналізу через те, що практично всі пацієнти мали такі скарги. Водночас ураження шкіри виключили через недостатню кількість спостережень. У таблиці 3 представлено клінічні характеристики, що достовірно підвищували ризик когнітивних порушень у пацієнтів із COVID‑19.
Пацієнти з такими неврологічними симптомами, як головний біль, аносмія та дисгевзія, мали гірші показники робочої пам’яті порівняно з хворими без цих симптомів (р=0,031, р=0,031 і р=0,031 відповідно). Пацієнти з головним болем також виявили нижчі показники тестів з оцінки кодування пам’яті (р=0,006), уваги (р=0,002), складної робочої пам’яті (р=0,037), швидкості обробки інформації (р=0,010), виконавчих функцій (р=0,034, р=0,018) і загального когнітивного індексу (р=0,002). Пацієнти з дисгевзією також мали нижчі показники тесту найменування (р=0,001).
Хворі, котрі відзначали діарею, мали нижчі показники відкладеної зорової пам’яті (р=0,045), робочої пам’яті (р=0,019) та складної робочої пам’яті (р=0,043).
У пацієнтів, які потребували інтенсивної терапії, було виявлено нижчі показники тестів з оцінки виконавчих функцій (р=0,037). У хворих, які потребували кисневої терапії, спостерігалися нижчі показники словесної пам’яті (р=0,030), зорової пам’яті (р=0,005), уваги (р=0,002), робочої пам’яті (р=0,036), складної робочої пам’яті (р=0,027), швидкості обробки інформації (р=0,035, р=0,029), виконавчих функцій (р=0,009, р=0,014) і загального когнітивного індексу (р=0,010).
Цікаво, що не було виявлено відмінностей у показниках нейропсихологічних тестів у пацієнтів, які мали скарги на зниження когнітивних функцій після COVID‑19, і тих, які не мали. Водночас у підгрупі хворих із когнітивними скаргами було виявлено гірші показники тестів на тривогу та депресію (р=0,047 і р=0,008 відповідно).
Обговорення
Раніше не повідомлялося про зв’язок між COVID‑19 і когнітивними порушеннями. Зважаючи на наявність інших неврологічних проявів при COVID‑19 і когнітивний дефіцит після інших вірусних інфекцій, автори припустили, що така асоціація є дуже ймовірною.
В учасників проведеного дослідження перебіг COVID‑19 відповідав типовому опису цього захворювання (Li et al., 2020; Wu et al., 2020; Chen et al., 2020; Guan et al., 2020; Arentz et al., 2020). У вивченій когорті найчастішим симптомом була лихоманка, за якою слідували кашель, міалгія, втома та головний біль.
Чоловіки демонстрували вищі рівні D‑димеру та феритину, ніж жінки. Згідно з іншими дослідженнями, тяжкий перебіг COVID‑19 частіше трапляється в чоловіків, можливо, внаслідок вищих рівнів рецепторів ACE2 (Sama et al., 2020).
Подібно до інших респіраторних вірусів SARS-CoV‑2 теоретично може потрапляти в ЦНС гематогенним або ретроградним нейронним шляхом. Друга гіпотеза підтверджується тим фактом, що 57% пацієнтів у проведеному дослідженні мали порушення нюху. Неврологічні симптоми, такі як головний біль, втрата нюху та смаку, мали сильну кореляцію з порушеннями вищих нервових процесів, зокрема уваги, пам’яті та виконавчих функцій. Із перелічених вище неврологічних симптомів головний біль був найсильніше пов’язаний із гіршими показниками нейропсихологічних тестів. Це підтверджує нейротропність SARS-CoV‑2, яка описана в попередніх дослідженнях (Mao et al., 2020; Li et al., 2020).
Автори також виявили когнітивні порушення в пацієнтів, які потребували кисневої терапії під час госпіталізації. Це можна пояснити постійною гіпоксією, спричиненою ураженням легень унаслідок COVID‑19 (Areza-Fegyveres et al., 2010).
Головний біль та оксигенотерапія незалежно одне від одного були основними клінічними характеристиками, пов’язанами з когнітивними порушеннями. Саме в пацієнтів із цими ознаками був істотно знижений загальний когнітивний індекс.
Пацієнти з діареєю також мали гірші показники нейропсихологічного тестування. Автори не визначали, чи була діарея спричинена інфекцією, чи була побічним явищем фармакологічного лікування. Цей момент було би корисно врахувати в подальших дослідженнях.
У дослідженій госпітальній когорті 12 (34,3%) пацієнтів мали когнітивні скарги після COVID‑19. Цікаво, що не було знайдено відмінностей у показниках нейропсихологічних тестів у пацієнтів із когнітивними скаргами та без них. Водночас пацієнти, котрі скаржилися на погіршення когнітивних функцій, мали значно вищі показники тривоги та депресії. Пацієнти з когнітивними скаргами пов’язували їх із дефіцитом уваги й аномією (деморалізація, ослаблення зв’язку із суспільством, переживання відчуженості від людей, порожнечі життя тощо). Емоційний дистрес, у тому числі тривога, депресія та безсоння, можуть відігравати суттєву роль у суб’єктивному сприйнятті когнітивних скарг. Це підкреслює важливість раннього виявлення тривоги та депресії, щоб уникнути пізніших когнітивних скарг у пацієнтів із COVID‑19.
Обмеження дослідження
Це випробування має кілька обмежень. Воно включало лише 35 учасників. Звісно, було би краще включити більше пацієнтів, щоб оцінити вплив інших симптомів, зокрема міалгії чи втоми, на когнітивні функції. Проте така кількість учасників була зумовлена найперше тим, що з дослідження виключали осіб старшого віку, щоб уникнути впливу вікових когнітивних порушень. Нейропсихологічну оцінку проводили якомога раніше після госпіталізації, щоб отримати свіжий когнітивний профіль, пов’язаний з інфекцією. Частина даних отримана з електронних медичних карток, тому деякі симптоми могли бути не зафіксовані, якщо вони були занадто легкими чи з інших причин проігноровані пацієнтами. Можливо, автори пропустили деяких пацієнтів із гіпоксичним ураженням ЦНС, що могло бути виявлено на МРТ. У майбутніх дослідженнях слід ширше використовувати нейровізуалізацію, а також здійснити довгострокову оцінку когнітивного дефіциту, щоб визначити можливість розвитку нейродегенеративних або цереброваскулярних захворювань після COVID‑19.
Висновки
- Пацієнти, котрі перенесли COVID‑19, можуть мати когнітивні порушення незабаром після виписки з лікарні.
- Неврологічні симптоми, такі як головний біль, аносмія та дисгевзія, були основними факторами ризику когнітивних порушень, пов’язаних з увагою, пам’яттю та виконавчими функціями.
- Потреба в кисневій терапії та діарея також були пов’язані з дефіцитом пам’яті, уваги та виконавчих функцій.
- Тривога та депресія асоціювалися з когнітивними скаргами, хоча суттєвих відмінностей у показниках нейропсихологічних тестів у пацієнтів із когнітивними скаргами та без них виявлено не було.
- Клініцисти мають бути обізнаними щодо можливості розвитку когнітивної дисфункції після COVID‑19, виявляти й довгостроково спостерігати таких пацієнтів, щоб уникнути подальшого прогресування нейропсихологічних порушень.
Список літератури знаходиться в редакції.
Almeria M., Cejudo J., Sotoca J., Deus J., Krupinski J. Cognitive profile following COVID‑19 infection: clinical predictors leading to neuropsychological impairment. Brain Behav. Immun. Health. 2020 Dec; 9: 100163.
Переклала з англ. Наталя Александрук
Медична газета «Здоров’я України 21 сторіччя» № 21 (490), 2020 р.