26 грудня, 2020
Практичні аспекти індивідуалізації інсулінотерапіїв пацієнтів із цукровим діабетом 2 типу
10-12 червня відбулося чергове засідання добре відомого науково-освітнього проекту «Школа ендокринолога». Структуру заходу було побудовано з урахуванням питань, з якими найчастіше стикаються як ендокринологи, так і лікарі суміжних спеціальностей у своїй рутинній практиці. Саме інтерактивний підхід до презентації доповідей забезпечує належний рівень засвоєння актуальної інформації в області ендокринології та метаболічних порушень, щоби в подальшому впроваджувати її в практичну лікарську діяльність. Спікери у своїх доповідях освітили широкий спектр важливих тем, зокрема патологію гіпофізу, щитоподібної та паращитоподібних залоз, аспекти жіночого та чоловічого репродуктивного здоров’я та завжди актуальні проблеми діабетології.
.jpg) Особистим досвідом індивідуалізації інсулінотерапії (ІТ) у пацієнтів із цукровим діабетом (ЦД) 2 типу на прикладі реальних клінічних випадків поділилася завідувачка кафедри ендокринології Львівського національного медичного університету ім. Данила Галицького, доктор медичних наук, професор Аліна Мечиславівна Урбанович.
Особистим досвідом індивідуалізації інсулінотерапії (ІТ) у пацієнтів із цукровим діабетом (ЦД) 2 типу на прикладі реальних клінічних випадків поділилася завідувачка кафедри ендокринології Львівського національного медичного університету ім. Данила Галицького, доктор медичних наук, професор Аліна Мечиславівна Урбанович.
Клінічний випадок 1
Фізикально-лабораторні характеристики пацієнта
Пацієнтка К., 59 років, зі стажем ЦД 2 типу 12 років, звернулася зі скаргами на прибавку у вазі 5 кг за рік, профузну пітливість уві сні, яскраві сновидіння, періодичні периферичні набряки. Хвора підозрювала, що ці симптоми були пов’язані з гіпоглікемією, тому періодично неконтрольовано зменшувала дозу інсуліну ввечері, що супроводжувалося вираженою гіперглікемією зранку.
На момент первинної консультації вага пацієнтки становила 82 кг при зрості 165 см (індекс маси тіла (ІМТ) = 30,15 кг/м2), рівень глікозильованого гемоглобіну (HbA1c) – 9,1%.
Супутні захворювання включали дисліпідемію та артеріальну гіпертензію, які були діагностовані 15 років тому. Крім того, останні 10 років пацієнтка перебуває на обліку в психіатра та періодично приймає антидепресанти.
Лікування на момент звернення: інсулін НПХ 42 Од у 2 прийоми, метформін 2000 мг, бісопролол 5 мг, лозартан 50 мг, розувастатин 20 мг.
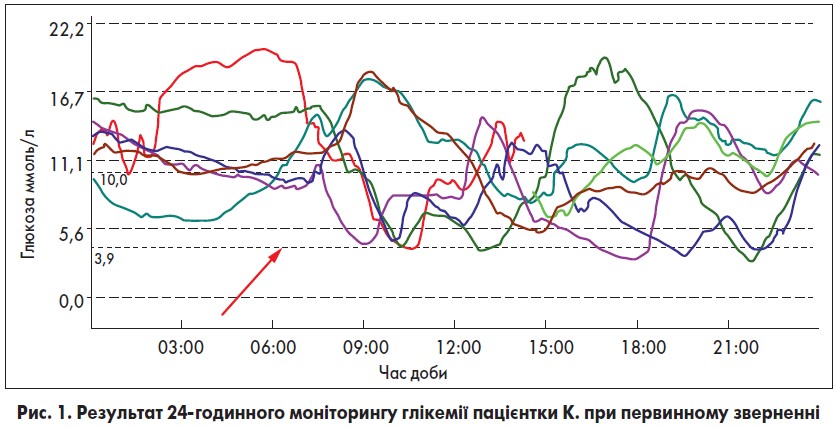
Пацієнтці провели 24-годинний моніторинг рівня глікемії, який виявив повну відсутність компенсації ЦД, з епізодами гіпо- та гіперглікемії. Нічна гіпоглікемія реєструвалася о 3:00, а рівень глюкози плазми під час епізодів гіперглікемії підіймався понад 17 ммоль/л, що відображено на рисунку 1.
Вибір препарату для цукрознижувальної терапії
Отримані показники однозначно потребували зміни цукрознижувальної терапії (ЦЗТ). Виявлені скачки рівня глюкози плазми пов’язані з добовою варіативністю дії базального інсуліну НПХ, тому було прийняте рішення перейти на більш сучасні аналоги інсуліну.
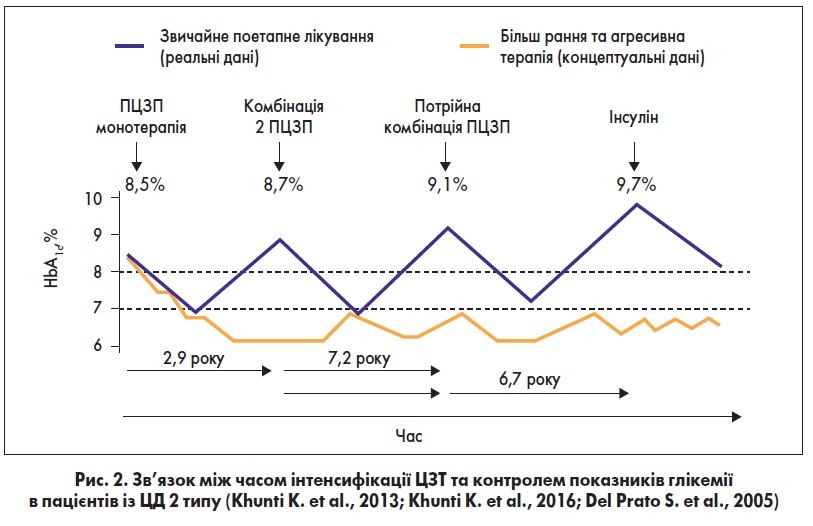
Варіативність дії різних видів інсуліну оцінювалася в низці клінічних досліджень, результати яких відображені на рисунку 2 (Heise et al., 2012).
Як можна побачити з рисунка, добова варіативність дії менша в аналогових інсулінів проти інсуліну НПХ, а найкращий профіль варіативності серед них однозначно має інсулін деглюдек (препарат Тресіба® ФлексТач® від фармацевтичної компанії Novo Nordisk, Данія). Це забезпечує високу прогнозованість дії і, відповідно, робить деглюдек найбільш безпечним для пацієнтів.
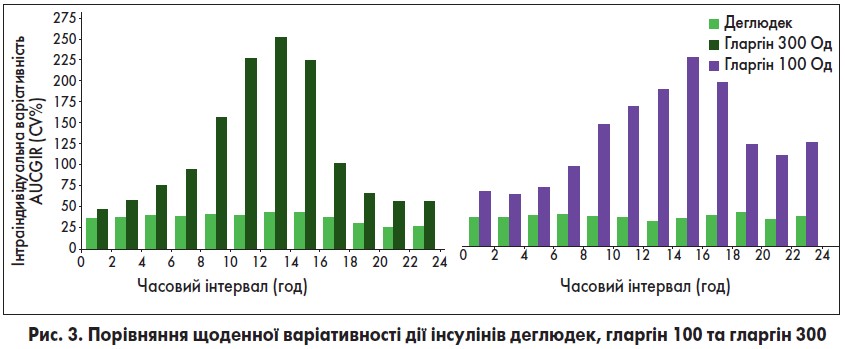
У дослідженні Heise вивчалася прогнозованість дії інсуліну деглюдек в порівнянні з інсуліном гларгін 100 і гларгін 300. Індивідуальна варіативність цукрознижувального впливу, що оцінювався за площею під фармакокінетичною кривою, яка описує залежність «концентрація/час» для швидкості інфузії глюкози (AUCGIR), зображена на рисунку 3.
Таким чином, інсулін деглюдек краще імітує ендогенну базальну секрецію та дію інсуліну, ніж гларгін 100/300.
В Європейському багатоцентровому ретроспективному обсерваційному дослідженні EU-TREAT оцінювалася ефективність інсуліну деглюдек після переведення з інших базальних інсулінів у пацієнтів із ЦД 1 та 2 типу (Siegmund T. et al., 2017; Schultes B. et al., 2017).
Дослідження тривало 6-12 міс та охопило 2550 пацієнтів, серед яких 70% мали підвищений ризик гіпоглікемії. Критеріями включення були ЦД 1 або 2 типу та використання базального інсуліну (± болюсний інсулін) протягом ≥6 міс до переведення на інсулін деглюдек. Мінімум інформації, необхідний для участі в дослідженні, включав вік, рівень HbA1c, тривалість лікування інсуліном, значення розрахункової швидкості клубочкової фільтрації (ШКФ) за останні 12 місяців.
Первинною кінцевою точкою була динаміка HbA1c за 6 міс після переведення на інсулін деглюдек. Вторинні кінцеві точки включали динаміку: HbA1c за 12 міс після переведення на інсулін деглюдек, глікемії натще, середніх доз базального і болюсного інсулінів, частоти епізодів гіпоглікемії та маси тіла через 6 та 12 міс після переведення на інсулін деглюдек.
Основними причинами переходу з інших базальних інсулінів на інсулін деглюдек були висока варіативність глікемії, високий ризик гіпоглікемій та висока доза інсуліну. Останнє напряму пов’язане з підвищенням вірогідності розвитку онкологічних захворювань. Детальна структура індивідуальних особливостей пацієнтів, які були кандидатами для переходу на терапію інсуліном деглюдек, показана на рисунку 4.
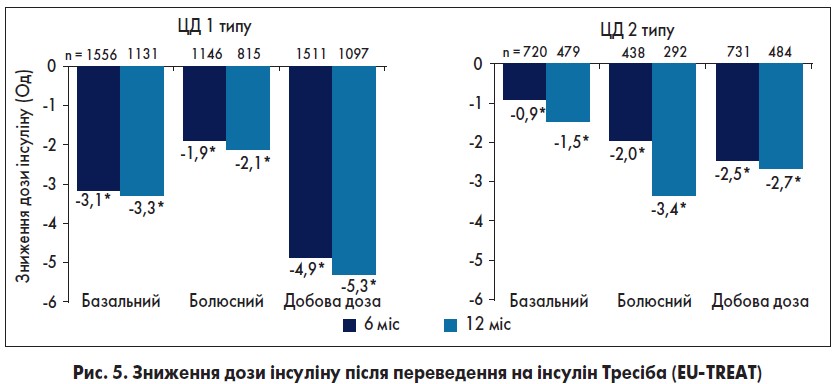
Результати дослідження EU-TREAT виявилися вражаючими. Уже через 6 міс спостереження в пацієнтів із ЦД 1 типу, які отримували інсулін деглюдек, спостерігалося зниження частоти всіх гіпоглікемій на 21%, легких нічних – на 44% (через 12 міс – на 52%) та тяжких – на 85%. У пацієнтів із ЦД 2 типу динаміка була ще краще. Через півроку лікування інсуліном деглюдек загальна частота гіпоглікемій знизилася на 61%, легких нічних – на 90%, а тяжких – на 92%. Через рік спостереження в пацієнтів на інсуліні деглюдек взагалі не було зареєстровано тяжких гіпоглікемій. Ще однією важливою перевагою переходу на інсулін деглюдек було зниження дози інсуліну, яку отримують пацієнти (рис. 5).
Як показали результати, лікування інсуліном деглюдек уже через 6 міс демонструє зниження місячної дози інсуліну і, своєю чергою, ускладнень, пов’язаних із хронічним передозуванням інсуліну, на 75 Од у пацієнтів із ЦД 2 типу та аж на 150 Од у хворих на ЦД 1 типу.
Оскільки глікемічний профіль пацієнтки К. характеризувався значною варіативністю глікемії та схильністю до гіпоглікемій, саме інсулін деглюдек (Тресіба® ФлексТач®) був обраний в якості ЦЗТ в доповнення до метформіну.
Розрахунок дози інсуліну
Необхідно враховувати той факт, що пацієнтам із ЦД 2 типу слід знизити дозу на 20% від дози попереднього базального інсуліну, з подальшим індивідуальним підбором дози, при переході на деглюдек з:
- базального інсуліну, який застосовувався 2 рази на день;
- інсуліну гларгін 300 Од/мл.
Пацієнтка К. отримувала 42 Од інсуліну НПХ, тому при переході на інсулін деглюдек дозу було зменшено на 20%, тобто до 34 Од/добу.
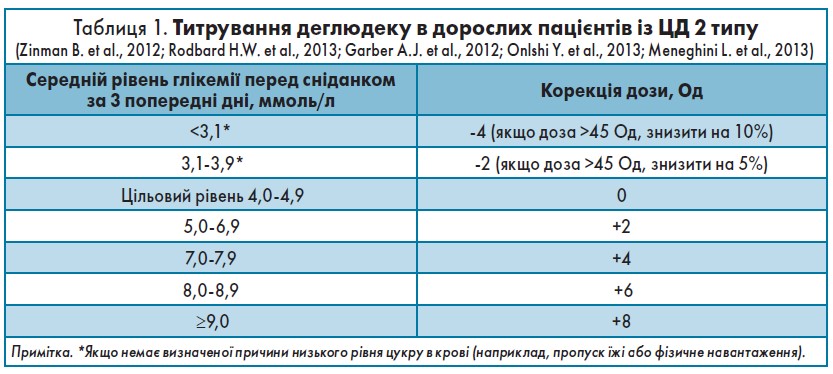
Титрувати інсулін деглюдек потрібно 1 раз на тиждень, оцінюючи середній рівень глікемії перед сніданком за попередні 3 дні. Корекція дози відповідно до рівня глікемії відображена в таблиці 1.
Результати лікування
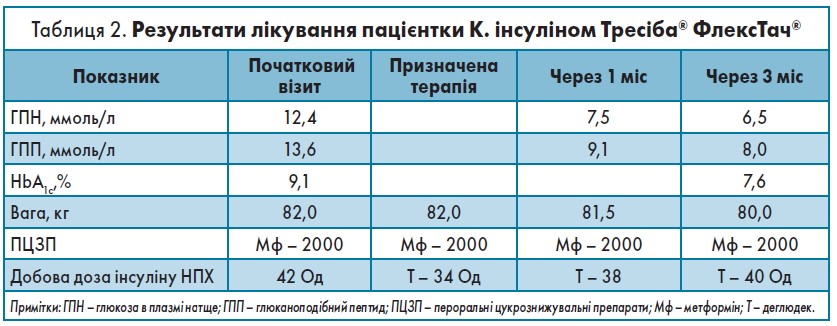
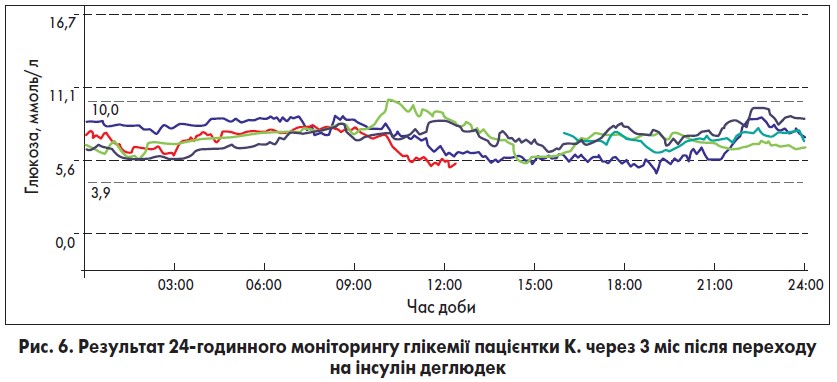
Окрім змін у ЦЗТ пацієнтка була повторно проконсультована психіатром і отримала відповідну корекцію порушень настрою, що підвищило прихильність хворої до лікування в цілому. Динаміка результатів терапії та 24-годинний моніторинг рівня глікемії через 3 міс терапії інсуліном деглюдек показані в таблиці 2 та на рисунку 6.
Уже через 3 міс після переходу на деглюдек у пацієнтки мінімізувалася варіативність глікемії, не реєструвалися епізоди гіпоглікемії, а рівень HbA1c знизився на 1,5%, тому можна очікувати, що при наступному контролі він досягне цільових 7%. Крім покращення лабораторних показників відбулися позитивні зміни і в якості життя пацієнтки: вона схудла на 2 кілограми, настрій її покращився, зросла активність.
Таким чином, інсулін деглюдек дає можливість не тільки ефективно контролювати ЦД пацієнтам зі значною варіативністю глікемії та ризиком виникнення гіпоглікемій, але й досягти цього завдяки нижчій дозі інсуліну, що оберігає пацієнтів від деяких серйозних ускладнень, зокрема підвищеного ризику розвитку онкологічних захворювань.
Клінічний випадок 2
Фізикально-лабораторні характеристики пацієнта
Пацієнт Б., 48 років, стаж ЦД 2 типу 7 років.
На момент первинного звернення вага хворого становила 98 кг при зрості 181 см (ІМТ=29,99 кг/м2), рівень HbA1c – 8,95%. З анамнезу життя відомо, що хворий працює на митниці за графіком «доба через три», тому регулярно піддається впливу стресових ситуацій і нерегулярно харчується. При огляді: [артеріальний тиск] АТ – 150/90 мм рт. ст., [частота серцевих скорочень] ЧСС – 76/хв, периферичних набряків немає.
Супутні захворювання: дисліпідемія та артеріальна гіпертензія, діагностовані 8 років тому.
Лікування на момент звернення: метформін 850 мг 3 р./добу, дапагліфлозин 10 мг/добу, олмесартан 40 мг, розувастатин 10 мг.
Пацієнта дообстежили та отримали такі результати біохімічних досліджень: креатинін плазми – 6,47 мкмоль/л, ШКФ –
109 мл/хв/1,73м2, холестерин – 6,47 ммоль/л, [ліпопротеїни низької щільності] ЛПНЩ – 4,7 ммоль/добу, [аспартатамінотрансфераза] АСТ – 49 Од/л, [аланінамінотрансфераза] АЛТ – 51 Од/л. Глікемія впродовж доби коливалася в межах 9,0-15,0 ммоль/л.
 Цільовий показник HbA1c становив 6,5-7,0%, тому були внесені зміни в ЦЗТ: метформін 850 мг 3 р./добу був замінений на метформін XR2000 1 р./добу та було призначено 14 Од інсуліну НПХ. Дозу дапагліфлозину не корегували. За час перебування в стаціонарі дозу інсуліну НПХ було дотитровано до 28 Од/добу.
Цільовий показник HbA1c становив 6,5-7,0%, тому були внесені зміни в ЦЗТ: метформін 850 мг 3 р./добу був замінений на метформін XR2000 1 р./добу та було призначено 14 Од інсуліну НПХ. Дозу дапагліфлозину не корегували. За час перебування в стаціонарі дозу інсуліну НПХ було дотитровано до 28 Од/добу.
Через 2 тиж після стаціонарного лікування в пацієнта, який перебував на роботі, унаслідок стресової ситуації розвинувся гіпоглікемічний стан, який потребував виклику «швидкої».
Вибір препарату для ЦЗТ
З анамнезу пацієнта відомо, що режим його харчування був абсолютно неврегульованим: він міг цілий день не їсти на роботі, а ввечері перед сном переїдав. При застосуванні інсуліну НПХ, який характеризується найвищою серед базальних інсулінів варіативністю, це загрожує виникненням гіпоглікемій. Таким чином, потрібен інсулін, який, з одного боку, ефективно знижує рівень HbA1c та рідко викликає гіпоглікемії, а з другого – може індивідуально вводитися пацієнтом під найбільший прийом їжі.
У програмі клінічних досліджень BOOST оцінювався інсулін деглюдек/аспарт (Райзодег®) проти інсуліну гларгін в якості препарату для старту ІТ в пацієнтів із ЦД 2 типу (Onishi et al., 2013).
Так, відкрите 26-тижневе дослідження BOOST JAPAN охопило 296 пацієнтів, які були поділені на 2 групи: перша (n=147) отримувала деглюдек/аспарт 1 раз на день ± ПЗЦП, друга (n=149) – інсулін гларгін 100 1 раз на день ± ПЗЦП. Критеріями включення були: ЦД 2 типу; попередня терапія ≥1 ПЦЗП понад 3 міс в максимальній дозі; HbA1c 7,0-10,0%; ІМТ ≤35 кг/м2, вік ≥20 років.
Стартова доза інсуліну в обох групах дослідження становила 10 Од 1 раз на добу. Деглюдек/аспарт вводився 1 раз на день під найбільший прийом їжі за рішенням пацієнта, а інсулін гларгін 100 Од – 1 раз на день перед сніданком або нічним сном (за рішенням пацієнта).
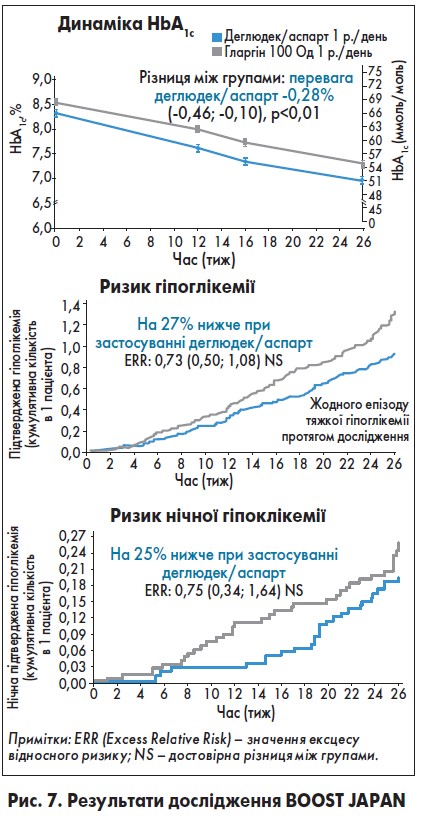
Вплив інсулінів деглюдек/аспарт та гларгін 100 на динаміку HbA1c і ризик гіпоглікемії та нічної гіпоглікемії відображені на рисунку 7.
Таким чином, деглюдек/аспарт 1 раз на день, якщо порівняти з інсуліном гларгін 100 Од, більш ефективно знижував рівень HbA1c, глікемію натще та після прийому їжі і водночас на 27% рідше викликав епізоди гіпоглікемії і на 25% – нічної гіпоглікемії.
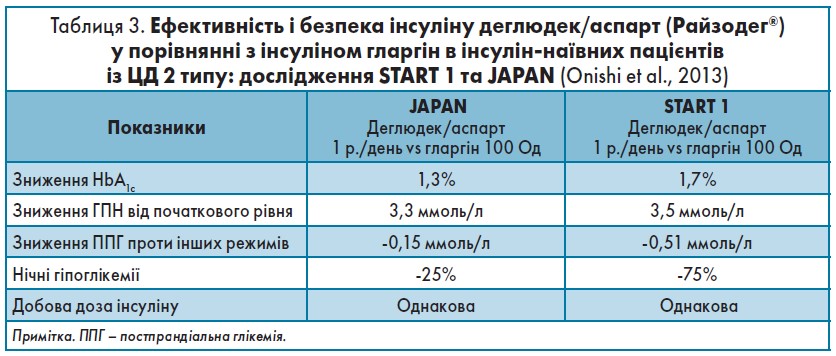
У таблиці 3 представлені основні первинні й вторинні кінцеві точки, отримані в дослідженні BOOST JAPAN та START 1, результати якого зіставні з висновками BOOST JAPAN.
Через епізоди гіпоглікемії та нерегулярне харчування, характерні для нашого пацієнта, було прийняте рішення перейти на інсулін деглюдек/аспарт.
Розрахунок дози інсуліну
Перехід на препарат інсуліну деглюдек/аспарт з інших інсулінів не викликає жодних труднощів, адже пацієнти можуть бути переведені на деглюдек/аспарт у тій самій добовій дозі базального інсуліну, яку вони отримували раніше.
Титрування дози здійснюється 1 раз на тиждень, з огляду на середнє значення рівня ГПН за попередні 3 дні. Схема титрування проста: при ГПН вище цільової додається 2 Од інсуліну, при ГПН нижче цільової віднімається 2 Од інсуліну, а при досягненні цільових значень доза не змінюється.
Результати лікування
Через 3 міс лікування інсуліном деглюдек/аспарт у пацієнта стабілізувалися показники глікемії, рівень HbA1c практично досягнув бажаного, були відсутні прояви гіпоглікемії, які значуще погіршували якість життя хворого та загрожували виникненням низки серйозних ускладнень. Основні результати терапії представлені в таблиці 4.
Інсулін деглюдек/аспарт – це легкий старт ІТ, який дає можливість триваліше контролювати рівень глікемії натще і після прийому їжі, застосовуючи всього один препарат. Простота використання, а саме – введення інсуліну під найбільший прийом їжі, та менший ризик виникнення гіпоглікемій, особливо вночі, забезпечують високу прихильність хворих до лікування. Деглюдек/аспарт ідеальний для активних працюючих людей з нерегулярним графіком роботи та харчування, оскільки дає можливість досягти ефективного контролю ЦД, не змінюючи при цьому звичний ритм життя.
Таким чином, на вибір цукрознижувальної тактики, крім цільового рівня HbA1c, впливає ще низка клініко-лабораторних показників, починаючи від глікемічного профілю й способу життя пацієнтів до особливостей їхнього психоемоційного стану, що обов’язково слід ураховувати для оптимальної індивідуалізації лікування хворих на ЦД.
Список літератури знаходиться в редакції.
Підготувала Ганна Кирпач
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 3 (51) 2020 р.