15 січня, 2021
Європейські рекомендації щодо первинної протигрибкової профілактики у дорослих пацієнтів онкогематологічного профілю
У 2005 р. Європейська група з трансплантації крові та кісткового мозку (EBMT), Європейська організація з вивчення та лікування онкологічних захворювань (EORTC), Європейська асоціація боротьби з лейкозами (ELN) та Міжнародне товариство з вивчення послабленої імунної реактивності (ICHS) започаткували проведення Європейської конференції з питань інфекцій при лейкозах (ECIL). Її основною метою було створення рекомендацій з лікування та профілактики бактеріальних, вірусних і грибкових інфекцій у пацієнтів з лейкозами, а також у хворих, яким проводиться трансплантація гемопоетичних стовбурових клітин (ТГСК) [1]. Від самого початку роботи конференції однією з її ключових тематик стала профілактика інвазивних грибкових захворювань (ІГЗ).
Комітет ECIL прагне регулярно оновлювати свої рекомендації на підставі доступних доказів. Під час п’ятого та шостого засідань ECIL, проведених відповідно 19-21 вересня 2013 р. та 11-12 вересня 2015 р. у м. Ніцца (Франція), відбувся детальний перегляд рекомендацій щодо протигрибкової профілактики у дорослих. Їх остаточна версія була розміщена на вебсайті ECIL (www.ecil-leukaemia.com).
Порівняно з попередніми версіями рекомендацій (включаючи опубліковані у 2011 р.), основні зміни у новій редакції документа включають:
- впровадження нової системи оцінювання доказів, згідно з якою оцінка сили рекомендацій скорочена з п’яти до трьох рівнів (A – вагомі докази, що підтримують використання втручання або ж свідчать проти нього; В – помірні докази на підтримку рекомендації чи проти втручання; С – недостатні докази на підтримку рекомендації);
- розширення рекомендацій і на інші гематологічні захворювання, окрім гострого мієлолейкозу (ГМЛ) і стану після трансплантації алогенних гемопоетичних стовбурових клітин (ГСК). Внаслідок застосування нових терапевтичних підходів (у тому числі біологічних препаратів) останнім часом ІГЗ все частіше реєструють при багатьох онкогематологічних захворюваннях (включаючи лімфопроліферативні) [5]. Отже, група вважала за потрібне розширити свій аналіз і надати фахівцям у галузі онкогематології рекомендації щодо первинної профілактики грибкових інфекцій у цих популяціях пацієнтів.
Рекомендації
ГМЛ
Пацієнти з ГМЛ або мієлодиспластичним синдромом (МДС), котрі проходять послідовні цикли мієлосупресивної хіміотерапії, мають численні фактори ризику розвитку ІГЗ. Зокрема, вони включають похилий вік, тривалу та глибоку нейтропенію і моноцитопенію, застосування пуринових аналогів, наявність постійних катетерів, аліментарний мукозит та індивідуальну генетичну схильність [17]. Більш того, нещодавно у пацієнтів з ГМЛ були виявлені наявні ще до госпіталізації фактори, які згодом підвищують цей ризик: хронічне обструктивне захворювання легень, вплив грибкових патогенів, пов’язаний з особливостями професійної діяльності або хобі, відсутність високоефективних систем очищення повітря, інфікування вірусом грипу H1N1 та відсутність відповіді на індукційну хіміотерапію [18, 19].
Після впровадження у клінічну практику профілактики флуконазолом на початку 1990-х років у світі спостерігався чіткий епідеміологічний зсув у структурі ІГЗ у бік інфекцій, спричинених цвілевими грибами. Домінуючим видом у Європі став Aspergillus – частота інвазивного аспергільозу при ГМЛ варіює від 5 до 24%, тоді як частота кандидемії становить <2% [20]. У європейському багатоцентровому дослідженні з оцінювання поширеності (аудит PIMDA за участю 17 країн) загальна частота підтвердженого та ймовірного аспергільозу у пацієнтів з ГМЛ, що отримували індукційну хіміотерапію, становила 8,1% [21]. З огляду на ці високі показники були запропоновані відповідні профілактичні заходи. Зокрема, загальноприйнятою практикою у багатьох європейських онкоцентрах стало призначення первинної протигрибкової хіміопрофілактики [22, 23].
Враховуючи очікувану частоту ІГЗ близько 8%, під час оновлення рекомендацій не розглядалися та не включалися в аналіз дослідження за участю <200 пацієнтів, оскільки вони не мали достатньої потужності для оцінювання потенційної користі протигрибкової профілактики. У цей оновлений аналіз було включено в цілому 6 досліджень [10, 11, 13, 26-28].
Рекомендації ECIL (табл. 1). У пацієнтів з ГМЛ або МДС, котрі отримують інтенсивну хіміотерапію з метою індукції ремісії, як препарати першого вибору для первинної протигрибкової профілактики розглядаються азоли.
! На підставі результатів великого відкритого дослідження препаратом вибору вважається посаконазол (рівень доказовості I A). Його можна призначати у формі пероральної суспензії (200 мг через кожні 8 год) [13] або кишково-розчинних таблеток* (300 мг через кожні 24 год після прийому у навантажувальній дозі 300 мг через кожні 12 год у перший день) [30]. При застосуванні посаконазолу частота підтверджених і ймовірних ІГЗ знижувалася з 8 до 2%, а частота інвазивного аспергільозу – з 7 до 1% [13].
Також слід відзначити, що ефективність профілактики посаконазолом була чітко вищою, ніж флуконазолом (P=0,001), хоча те саме й не було встановлено у порівнянні з ітраконазолом (Р=0,22) [13]. Проте ітраконазол отримав рекомендацію лише рівня I B, оскільки він гірше переноситься, спричиняє більше реакцій медикаментозної взаємодії та потребує моніторингу сироваткової концентрації [11, 26, 27]. Великі дослідження з оцінювання профілактики вориконазолом за участю пацієнтів з ГМЛ/МДС не проводилися, але цей препарат отримав рекомендацію рівня II B для застосування у дозі 200 мг через кожні 12 год на підставі результатів використання під час нейтропенічної фази перед приживленням трансплантованих алогенних ГСК. Врешті у центрах із низькою частотою розвитку інвазивних грибкових інфекцій, спричинених цвілевими грибами (тобто менше 8%), все ще прийнятним варіантом (I B) залишається призначення флуконазолу (400 мг через кожні 24 год). Умовою такого призначення є те, що воно становить частину інтегрованої стратегії ведення, яка включає ранню діагностику інфекцій, зумовлених цвілевими грибами, із поєднанням скринінгу біомаркерів і візуалізаційних досліджень [33].
Рекомендації щодо ехінокандинів і внутрішньовенних ліпідних лікарських форм амфотерицину В залишаються незмінними, оскільки все ще недостатньо даних щодо дози, частоти та тривалості застосування, а також щодо ефективності та безпеки (II C) [3]. Єдиним винятком є аерозольний ліпосомальний амфотерицин В (10 мг 2 рази на тиждень) у випадку його призначення у комбінації з пероральним флуконазолом (400 мг через кожні 24 год для профілактики інфекції, викликаної дріжджовими грибами; I B) [35]. Категорично не рекомендується застосовувати звичайний амфотерицин В, а також його аерозольну форму (I A проти застосування) або розчин для внутрішньовенного введення (II A проти застосування) у разі доступності ліпідних форм.
МДС
У той час як деякі підгрупи пацієнтів з МДС отримують інтенсивну терапію, подібну до такої при ГМЛ (з алогенною ТГСК або без неї), більшості хворих проводиться лише підтримуюче лікування (трансфузії, стимулятори еритропоезу), застосовується леналідомід або гіпометилюючі препарати. Однак ці пацієнти з МДС низького або проміжного ризику зазвичай мають численні спонтанні або набуті фактори ризику розвитку інфекції, включаючи тривалу нейтропенію та функціональні дефекти нейтрофілів, порушення з боку В-, Т- і NK-клітин, перевантаження залізом та асоційовані з похилим віком супутні захворювання [36]. Проте у дослідженнях, присвячених лікуванню пацієнтів з МДС гіпометилюючими препаратами або леналідомідом, ІГЗ як ускладнення згадуються рідко або взагалі не згадуються [36]. У трьох проспективних європейських реєстрах інвазивних захворювань, спричинених цвілевими грибами, частка пацієнтів з МДС серед включеної популяції гематологічного профілю виявилася незначною [37-39]. Отже, ECIL не рекомендує проводити первинну протигрибкову профілактику у пацієнтів з МДС низького та проміжного ризику (за винятком тих пацієнтів, яким проводиться інтенсивна індукція ремісії, подібна до такої при ГМЛ, та/або алогенна ТГСК), оскільки вони мають низький ризик ІГЗ (<2%).
Гострий лімфобластний лейкоз
У ретроспективному аналізі SEIFEM‑2004 за участю 1173 дорослих пацієнтів з гострим лімфобластним лейкозом (ГЛЛ) частота ІГЗ становила 6,5%; найчастішими з них були інвазивний аспергільоз і кандидоз [40]. Враховуючи ретроспективну природу аналізу та складність діагностування ІГЗ, їх істинна частота може бути недооцінена. У той час як профілактика протигрибковими препаратами з класу азолів стала стандартом лікування інших груп пацієнтів з аналогічним ризиком (наприклад, з ГМЛ), для пацієнтів з ГЛЛ наразі не існує схваленого стандарту терапії. За відсутності переконливих даних щодо ефективності та токсичності слід розглянути обережне застосування профілактики флуконазолом для запобігання інфекціям, спричиненим дріжджовими грибами (III C).
Хронічні мієлопроліферативні новоутворення
При хронічних мієлопроліферативних новоутвореннях (МПН) первинна протигрибкова профілактика не рекомендується. Однак пацієнтів з МПН, яким проводиться інтенсивна терапія (подібна до такої при ГМЛ) або алогенна ТГСК, слід вести згідно з відповідними рекомендаціями. Слід зазначити, що у пацієнтів, у яких ІГЗ розвиваються на тлі терапії інгібіторами тирозинкінази, необхідно враховувати взаємодії цих препаратів з протигрибковими засобами з класу азолів [44].
Пацієнти з мієломою схильні мати декілька факторів ризику розвитку ІГЗ, включаючи часте застосування високих доз кортикостероїдів, пов’язану з мієломою вроджену імунну недостатність і супутні захворювання, а також незадовільну функцію кісткового мозку при інтенсивному попередньому лікуванні [45]. Однак у кількох великих епідеміологічних дослідженнях і проспективних реєстрах повідомляли про дуже низьку частоту (<1%) інфекцій, спричинених дріжджовими та цвілевими грибами, серед осіб, які отримували звичайну комбіновану хіміотерапію [37-39, 41]. Поки очікуються подальші епідеміологічні дані, первинна протигрибкова профілактика не рекомендована пацієнтам, котрі отримують лікування з приводу мієломи.
Хронічний лімфобластний лейкоз
У ретроспективному багатоцентровому італійському дослідженні (SEIFEM‑2004) частота ІГЗ у пацієнтів з хронічним лімфобластним лейкозом (ХЛЛ) складала 0,5% [41]. З огляду на цей доволі низький показник первинна протигрибкова профілактика не рекомендується, хоча вона може бути розглянута у пацієнтів з пролонгованою нейтропенією (>6 міс), осіб похилого віку та хворих із прогресуючим і рефрактерним ХЛЛ.
Лімфома
Пацієнти з лімфомою мають низький ризик ІГЗ. У вищезгаданому дослідженні SEIFEM‑2004, що включало 844 пацієнти з лімфомою Ходжкіна та 3475 пацієнтів з неходжкінськими лімфомами, частота ІГЗ складала 0,7 та 1,6% відповідно [41].
Аутологічна ТГСК
Пацієнти, яким проводиться аутологічна ТГСК (з приводу будь-якого основного захворювання), мають низький ризик розвитку ІГЗ. Первинна протигрибкова профілактика не рекомендується, хоча слід розглядати введення флуконазолу (400 мг через кожні 24 год) для профілактики кандидозної інфекції слизових оболонок під час нейтропенічної фази (III B) [50-53].
Алогенна ТГСК
У період до приживлення трансплантата основними факторами ризику є гострий лейкоз, трансплантація пуповинної крові та попередня грибкова інфекція [54]. Крім того, високий ризик розвитку ІГЗ під час приживлення трансплантата характерний для реципієнтів донорських ГСК при наявності щонайменше одного з таких факторів: перевантаження залізом, рання або рецидивуюча цитомегаловірусна інфекція, гостра реакція трансплантат проти хазяїна (РТпХ), сповільнене приживлення (нейтропенія протягом більше 3 тижнів), застосування кортикостероїдів у високих дозах (2 мг/кг або більше) протягом понад 1 тижня [54].
Що ж стосується фаз після приживлення трансплантата, історично основними факторами ризику розвитку ІГЗ є гостра і хронічна РТпХ [54]. Крім того, як стани високого ризику після приживлення трансплантата мають розглядатися вторинна нейтропенія та рецидивуюча цитомегаловірусна інфекція [54]. Врешті, у пацієнтів з гострою РТпХ, котрі отримують кортикостероїди, додатковим фактором ризику розвитку інфекцій, спричинених цвілевими грибами, є вік понад 40 років [56].
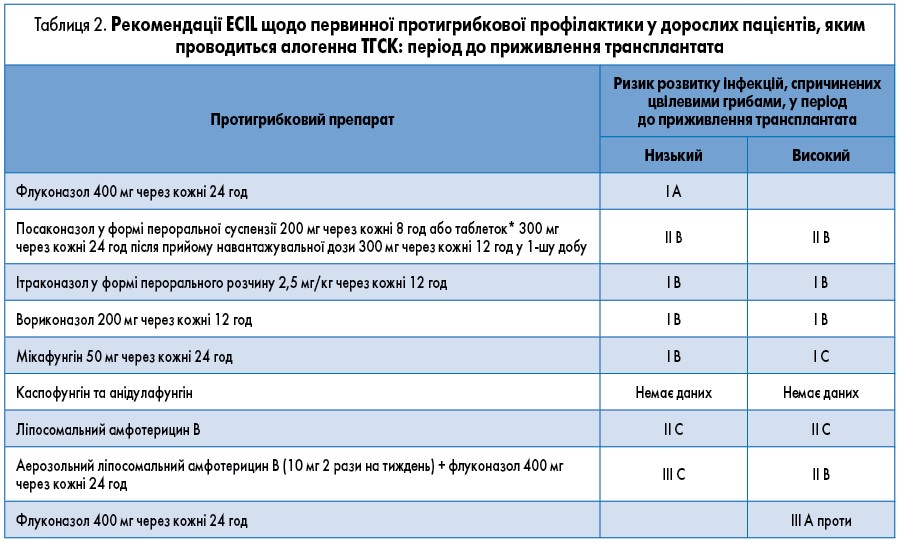
Період до приживлення (табл. 2). Флуконазол (400 мг/добу), як і раніше, рекомендується для застосування у центрах із низькою захворюваністю на інфекції, спричинені цвілевими грибами (тобто <5%), але лише у поєднанні з комбінованим діагностичним підходом до виявлення (біомаркери та/або комп’ютерна томографія) та лікування цих інфекцій (I A) [33]. Показано, що введення ітраконазолу (200 мг в/в через кожні 24 год, за яким слідує пероральний прийом розчину у дозі 200 мг через кожні 12 год) забезпечувало кращий порівняно з флуконазолом захист проти інвазивних грибкових інфекцій, спричинених цвілевими грибами, з аналогічним захистом проти кандидозу. Однак токсичність препарату й аспекти переносимості обмежують корисність його профілактичного застосування (I B) [12].
Хоча немає специфічних великих проспективних досліджень з оцінювання профілактики посаконазолом під час фази до приживлення трансплантата, на підставі результатів, отриманих при аналізі даних під час нейтропенічної фази у пацієнтів з ГМЛ/МДС, цьому препарату була надана рекомендація рівня II B [13].
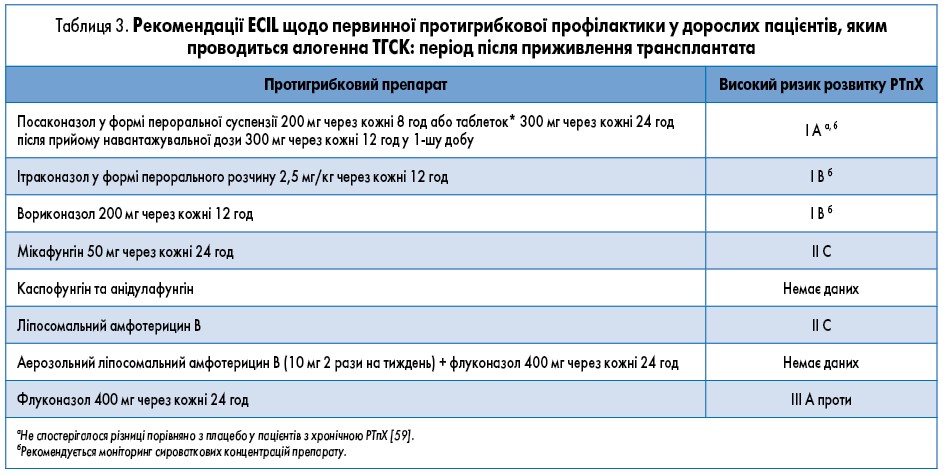
Період після приживлення трансплантата (табл. 3). Враховуючи значно підвищений під час РТпХ ризик розвитку інвазивних інфекцій, зумовлених цвілевими грибами, а також асоційовану з нею високу смертність, наполегливо рекомендується відмовитися від використання флуконазолу для профілактики у пацієнтів з РТпХ високого ризику (III A).
! На підставі результатів великого подвійного сліпого дослідження посаконазол (пероральна суспензія або кишково-розчинні таблетки*/розчин для внутрішньовенного введення) є препаратом вибору для протигрибкової профілактики (I A) [59].
Наразі існує реальна потреба у виявленні будь-яких змін в епідеміології грибкових інфекцій у пацієнтів онкогематологічного профілю з огляду на швидке зростання доступності нових терапевтичних засобів з імуносупресивними властивостями. ECIL надає оновлену версію рекомендацій з протигрибкової профілактики для основних груп дорослих пацієнтів з гематологічними злоякісними новоутвореннями. Вони мають допомогти лікарям розпізнати ризик, із яким стикаються їхні пацієнти, та своєчасно вжити ефективних заходів для його зниження.
Стаття друкується у скороченні.
Повний список літератури, що включає 62 джерела, знаходиться в редакції.
Maertens J.A. et al. European guidelines for primary antifungal prophylaxis in adult haematology patients: summary of the updated recommendations from the European Conference on Infections in Leukaemia. Antimicrob Chemother. 2018; 73: 3221-3230.
doi: 10.1093/jac/dky286.
Реферативний переклад з англ. підготувала Інга Боброва
*В Україні посаконазол доступний лише у лікарській формі суспензії для перорального застосування.
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 6 (67) 2020 р.