16 січня, 2021
Застосування пірацетаму в сучасній медичній практиці. Огляд доказової бази
Пірацетам – це циклічне похідне гамма-аміномасляної кислоти (ГАМК), він є ноотропним засобом, що діє на мозок, покращуючи когнітивні функції, такі як здатність до навчання, пам’ять, увага, а також розумову працездатність у здорових осіб і хворих із когнітивними порушеннями. Ефекти пірацетаму пов’язані зі стимуляцією нуклеотидного метаболізму в нейронах, підвищенням рівня глюкози й утилізації кисню в головному мозку, а також із посиленням холінергічних і дофамінергічних механізмів передачі збудження в нервовій тканині. Пірацетам має властивість дозозалежного зв’язування з фосфоліпідним подвійним шаром клітинних мембран, причому він відновлює їхню структуру, таким чином, підвищується плинність і поліпшується функція мембран.
Механізмів впливу препарату на центральну нервову систему, ймовірно, кілька: зміна швидкості поширення збудження в головному мозку; посилення метаболічних процесів у нервових клітинах; поліпшення мікроциркуляції шляхом впливу на реологічні характеристики крові без спричинення при цьому судинорозширювальної дії. Пірацетам покращує зв’язки між півкулями головного мозку та синаптичну провідність у неокортикальних структурах. Пірацетам пригнічує агрегацію тромбоцитів і відновлює еластичність мембрани еритроцитів, зменшує адгезію еритроцитів, чинить протекторну або відновлювальну когнітивну дію при порушенні функції головного мозку (гіпоксії, отруєнні, електросудомній терапії) або після цих станів. Пірацетам знижує вираженість і тривалість вестибулярного ністагму. Пірацетам швидко всмоктується після перорального прийому з біодоступністю близько 100%.
Пірацетам являє собою ноотропний препарат, який застосовується для симптоматичного лікування патологічних станів, котрі супроводжуються погіршенням пам’яті та когнітивними розладами. Пірацетам добре вивчений у вітчизняних і закордонних дослідженнях. Ще одне поле застосування пірацетаму в медицині – астенія. Астенічні симптоми (втома, знесилення, слабкість) спричиняють значне занепокоєння як у пацієнта, так і в лікаря, оскільки можуть бути наслідками низки різноманітних хвороб. Астенія (давньогрецьк. ἀσθένεια – безсилля, слабкість) – психопатологічний стан, що характеризується слабкістю, втомлюваністю, емоційною лабільністю, гіперстезією, порушенням сну. Астенічний синдром є одним із найпоширеніших у практиці лікаря та спостерігається в усіх категорій населення. На частку скарг, що пов’язані з астенією, припадає більш ніж 60%.
Астенія – поліморфний синдром. Спектр її дії включає наступні групи симптомів: фізичні (м’язова слабкість, зниження витривалості), когнітивні (зниження пам’яті, уваги, здатності до концентрації, неуважність), вегетативні (тахікардія, гіпервентиляція, гіпергідроз), больові (кардіалгії, дорсалгії, абдоміалгії), емоційні (тривожність, лабільність або нестійкість настрою, диссомнія) (Юдельсон Я.Б., 2003).
В одне з досліджень (2004) було включено 60 пацієнтів віком понад 18 років з органічним емоційно-лабільним розладом. Середній вік включених у дослідження хворих становив 51 рік, 73% були жінки. Учасникам дослідження призначався пірацетам у добовій дозі 1,2 г (група 1) або 4,8 г (група 2). Тривалість лікування в обох групах склала 6 тижнів. Для оцінки ефективності ноотропної терапії застосовувалися загальний клініко-психопатологічний метод, шкала загального клінічного враження (CGI), візуальна аналогова шкала астенії та суб’єктивна шкала оцінки астенії (MFI‑20). Оцінку безпеки терапії контролювали на основі загального аналізу крові та сечі, а також електрокардіограми.
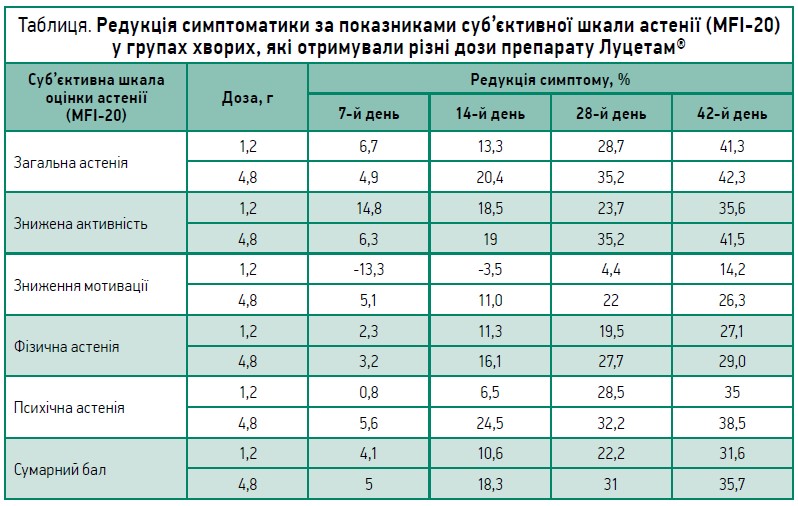
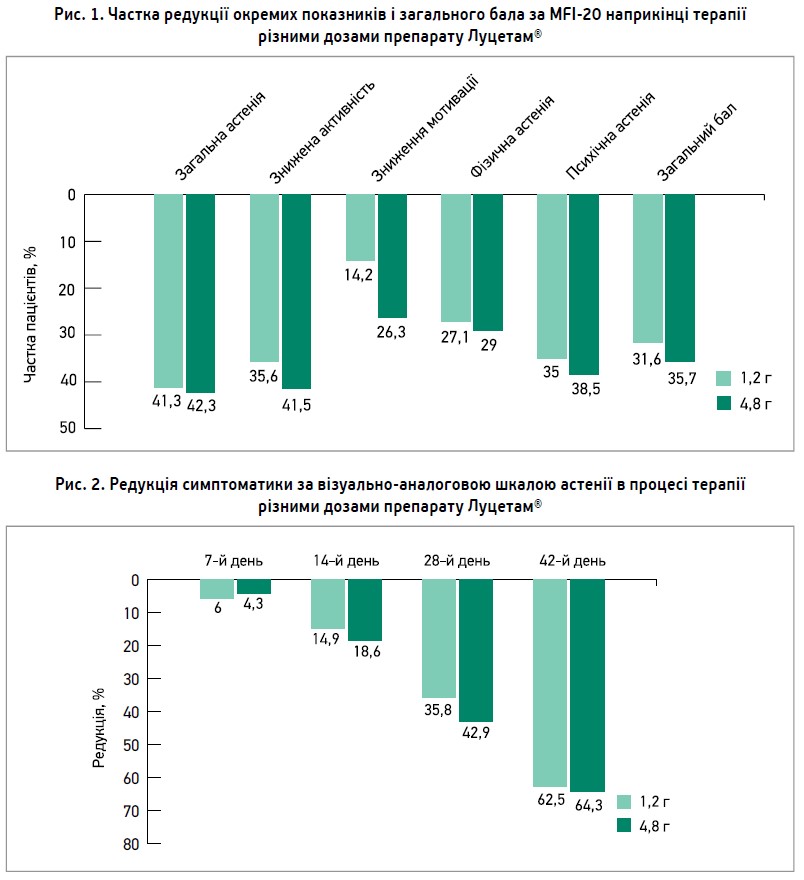
У процесі терапії тяжкість загального стану різною мірою зменшувалася в усіх пацієнтів. Уже на 7-й день лікування в групі хворих, які отримували пірацетам у дозі 1,2 г/добу, частка пацієнтів із вираженою тяжкістю стану скоротилася з 33,3 до 13,3%, із середньою – з 66,7 до 33,3%. У групі лікування пірацетамом у дозі 4,8 г/добу на 7-й день терапії вже не було пацієнтів із вираженою тяжкістю загального стану; частки осіб із середньотяжким і легким станом становили 33,3 та 66,7% відповідно. На 28-й день терапії пацієнти із середньою та вираженою тяжкістю стану були відсутні в обох групах, при цьому у 20% хворих групи пірацетаму 4,8 г/добу визначалася мінімальна вираженість розладів. Наприкінці лікування (42-й день) у всіх учасників дослідження було зафіксовано повне зникнення розладів або зниження їхньої тяжкості до рівня мінімальних клінічних проявів. У групі пірацетаму 4,8 г/добу кількість осіб без ознак розладів дорівнювала 53,3%, у групі 1,2 г/добу – 33,3%. Аналіз окремих показників шкали MFI‑20 виявив найбільшу редукцію за показниками загальної астенії та зниженої активності (табл., рис. 1). Оцінка за візуальною аналоговою шкалою підтвердила поступове зменшення вираженості симптомів астенії в ході лікування (рис. 2). Препарат відмінно переносився, жоден пацієнт не припинив лікування передчасно. Сумарна поширеність побічних явищ не залежала від призначуваної дози. Автори зробили висновок, що пірацетам є високоефективним при лікуванні астенічного розладу. Підвищення дози до 4,8 г/добу супроводжувалося покращенням результатів лікування без зростання кількості побічних ефектів і змін їхнього спектра.
В огляді літератури R.K. de Souza (2020) було проведено аналіз баз даних SciELO, Google Scholar і PubMed (2000-2018) і виявлено низку різнопланових досліджень, присвячених застосуванню пірацетаму при різних хворобах. Далі стисло викладено отримані результати.
Дослідження щодо застосування пірацетаму після інсульту та в лікуванні когнітивних розладів із позицій доказової медицини почали
проводити з початку 1990-х років. Одним із перших стало подвійне сліпе плацебо-контрольоване дослідження впливу пірацетаму на відновлення та реабілітацію після інсульту (Enderby Р. et al., 1994). Його результати продемонстрували, що пірацетам покращує здатність до навчання і пам’ять, а отже, може сприяти відновленню та реабілітації. Цей висновок був зроблений на підставі спостереження ефектів пірацетаму в групі, котра включала 158 пацієнтів, які проходили реабілітацію після гострого інфаркту головного мозку в басейні сонної артерії.
В іншому дослідженні було переконливо продемонстровано поліпшення мови в пацієнтів з афазією, котрі протягом 12 тижнів після інсульту отримували терапію пірацетамом. Як відомо, афазія є поширеним симптомом у людей, які перенесли інсульт, тоді як пірацетам сприяє відновленню функцій мозку, включаючи поліпшення мови (Huber W., 1999).
Кокранівський огляд 2001 року, який був присвячений фармакотерапії постінсультної афазії і включив результати 10 досліджень (ретельно відібраних із-поміж 52 із цієї проблеми), підтвердив ефективність пірацетаму в лікуванні афазії після інсульту (Greener J. et al., 2001).
Загалом ефективність пірацетаму у відновленні мовних функцій визначається впливом на когнітивні функції, інтенсифікацією мозкового кровотоку та метаболізму в мовних центрах, а також полегшенням міжпівкульової передачі інформації та кортикоталамічних зв’язків.
В експериментальних дослідженнях L. Grossman і співавт. (2011) та J. Samartgis і співавт. (2012) було виявлено сприятливий вплив пірацетаму на пам’ять. K. Winnicka та співавт. (2005) також стверджують, що пірацетам покращує пам’ять і здатність до навчання в умовах гіпоксії. Цей препарат запобігає розвитку дефіциту пам’яті, спричиненому надмірним вживанням алкоголю (Yang Y. et al., 2017). Ю. А. Фресенко (2009) показав, що пірацетам здатний запобігати амнезії після загальної анестезії, а Y. L. Wang і співавт. (2016) – при застосуванні пропофолу.
Особливий інтерес представляють великі багатоцентрові дослідження ефективності пірацетаму в літніх пацієнтів із різноманітною психоневрологічною симптоматикою. У цих дослідженнях проводилася кількісна оцінка покращення загального самопочуття після лікування. Слід звернути увагу на те, що застосування пірацетаму разом із покращенням у когнітивній сфері супроводжувалося редукцією супутньої психопатологічної симптоматики – депресивних й інших розладів.
У відкритому багатоцентровому дослідженні 5306 пацієнтів (віком 14-96 років) з ознаками цереброваскулярної недостатності приймали пірацетам 1,2 г/добу протягом 4 тижнів. Після 4 тижнів терапії пірацетамом покращення загального стану відзначено у 88% пацієнтів, відсутність змін – в 11,5%, погіршення – в 0,5%. При цьому число пацієнтів із запамороченням скоротилося з 3265 до 960 (покращення на 70,6%), зі зниженням мотивації – з 3803 до 1185 (68,8%), із вираженою стомлюваністю – з 4255 до 1474 (65,4%), із депресією – з 2238 до 830 (62,9%), зі зниженням концентрації уваги – з 4676 до 1759 (62,4%), зі зниженням адаптації – з 1566 до 623 (60,2%), із дзвоном у вухах – із 2064 до 888 (57%), із погіршенням сприйняття – з 4518 до 2086 (53,8%), із порушенням сну – з 3024 до 1690 (44,1%). Переносимість препарату була оцінена як дуже хороша: лише в 339 (6,6%) пацієнтів спостерігалися незначні побічні ефекти: порушення сну, шлунково-кишкові розлади, збудження, головний біль.
Подібні дані отримані в ході іншого багатоцентрового дослідження, в якому оцінювали ефективність пірацетаму в 11 654 пацієнтів, середній вік яких становив 64 роки. Більш ніж у 70% пацієнтів відзначалося порушення пам’яті. Інші розлади були представлені запамороченням (650 пацієнтів), артеріальною гіпертензією (423), головним болем (320) і депресією (213). Лікування пірацетамом здійснювали протягом 90 днів у різних дозуваннях: у пацієнтів віком до 60 років – по 2,4 г/добу, у пацієнтів віком понад 60 років – 3 г/добу. Пацієнтів обстежували перед початком терапії, на 45-й і 90-й день лікування. Результати дослідження продемонстрували високу ефективність пірацетаму: 70% лікарів і 90% пацієнтів відзначили позитивний ефект препарату й лише 7% пацієнтів скаржилися на побічні ефекти.
У зв’язку зі здатністю покращувати мозковий кровоток і функціонування мітохондрій, пірацетам можна застосовувати як нейропротектор при хірургічних операціях, що супроводжуються гіпоперфузією мозку. Інфузія пірацетаму перед проведенням хірургічної реваскуляризації забезпечувала кращу короткочасну пам’ять й увагу на післяопераційному етапі, ніж застосування плацебо (Uebelhack R. et al., 2003). Аналогічні результати виявив і метааналіз Y. Fang і співавт. (2013), а також подвійні сліпі дослідження S. Holinski (2008, 2011).
Застосування пірацетаму (4-50 мг/кг) покращує когнітивні функції (пам’ять, увагу, виконавчі функції) та координацію рухів у пацієнтів із травмою голови (Заваденко Н. Н., Гузілова Л. С., 2008). К. Б. Ованесов і співавт. (2002) повідомили, що використання пірацетаму протягом 4 тижнів у пацієнтів, які перенесли тяжкі травми головного мозку, сприяло збільшенню чутливості сітківки та зменшенню часу сенсомоторної реакції. На думку авторів, це підвищення чутливості пов’язане з ноотропним впливом пірацетаму на ГАМК‑ергічні процеси сітківки.
Покращення оксигенації й обміну речовин у мозку на тлі застосування пірацетаму також здатне зменшувати дистрес плода під час пологів. У дослідженні G. J. Hofmeyr і R. Kulier (2012) 96 жінок із підозрою на дистрес плода під час пологів було розподілено на групи плацебо та пірацетаму. Застосування останнього асоціювалося з тенденцією до зменшення кількості кесаревих розтинів.
Луцетам® (EGIS, Угорщина) є європейським препаратом пірацетаму, ефективність якого була підтверджена у вітчизняних і закордонних клінічних дослідженнях.
Луцетам® представлений у формі таблеток (0,4; 0,8 та 1,2 г пірацетаму), а також розчину для ін’єкцій в ампулах (1 або 3 г пірацетаму). Подібна різноманітність лікарських форм і дозувань пірацетаму дозволяє використовувати різні схеми терапії залежно від форми патології та її симптомів, віку пацієнта, наявності супутніх захворювань й індивідуальної реакції на лікування. Результати вивчення ефективності Луцетаму свідчать про його виражену дію на когнітивні та вегетативні порушення, можливість застосовування в лікуванні пацієнтів із психоорганічним синдромом, запамороченням, дислексією та широким спектром інших патологічних станів, а також про хорошу переносимість препарату Луцетам®.
Підготувала Лариса Стрільчук
Медична газета «Здоров’я України 21 сторіччя» № 23 (492), 2020 р.