17 квітня, 2021
Цефдінір – новий антибіотик для лікування респіраторних інфекцій у дорослих і дітей
У сучасних клінічних настановах як емпіричну антибіотикотерапію нетяжких респіраторних інфекцій рекомендовано використовувати пероральні цефалоспорини III покоління [1‑3]. Крім високої активності щодо передбачуваних збудників, цим препаратам властиві сприятливий профіль безпеки та хороша переносимість, здатність створювати високі концентрації в сироватці крові, а також у вогнищі запалення. Віднедавна на фармацевтичному ринку України представлений цефалоспорин ІІІ покоління цефдінір (3-ДІНІР, Корпорація «Артеріум») [4]; препарат доступний у формі капсул 300 мг для лікування дорослих і підлітків віком від 13 років, а вже незабаром з’явиться спеціальна дитяча форма – порошок для оральної суспензії, що призначений для використання в дітей від 6 міс до 12 років. Молекула цефдініру не широко представлена в Україні, тому цей антибіотик є новим не лише для лікарів і пацієнтів, а й для локальних інфекційних патогенів. Отже, в подальші роки можна сподіватися на низьку резистентність мікроорганізмів до цього препарату.
Антибактеріальна активність
Цефдінір є активним щодо більшості штамів таких мікроорганізмів in vitro, а також у разі клінічних інфекцій [5]:
- грампозитивні бактерії: Staphylococcus aureus (лише метицилінчутливі штами), Streptococcus pneumoniae (лише пеніцилінчутливі штами), Streptococcus pyogenes;
- грамнегативні бактерії: Haemophilus influenzae, Haemophilus parainfluenzae, Moraxella catarrhalis.
 Окрім того, in vitro продемонстрована активність цефдініру проти Staphylococcus epidermidis (метицилінчутливих штамів), Streptococcus agalactiae, стептококів групи Viridans, Citrobacter koseri, Escherichia coli, Klebsiella pneumoniae та Proteus mirabilis.
Окрім того, in vitro продемонстрована активність цефдініру проти Staphylococcus epidermidis (метицилінчутливих штамів), Streptococcus agalactiae, стептококів групи Viridans, Citrobacter koseri, Escherichia coli, Klebsiella pneumoniae та Proteus mirabilis.
Молекула цефдініру містить амінотіазолову групу, що підвищує зв’язувальну здатність із РВР (бактеріальним пеніцилін-зв’язувальним білком) і покращує протимікробну активність, а також вінілову групу, що полегшує абсорбцію в разі перорального прийому. Афінність цефдініру до РВР S. aureus, H. influenzae й E. coli є вищою порівняно з такою цефіксиму, цефаклору й цефалексину.
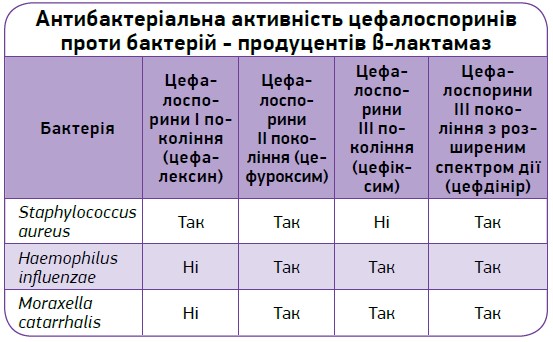
Цефдінір стійкий до гідролізу 13 основних β-лактамаз, включно з β-лактамазами ТЕМ‑1/ТЕМ‑2 H. influenzae та BRO‑1/BRO‑2 M. catarrhalis [6].
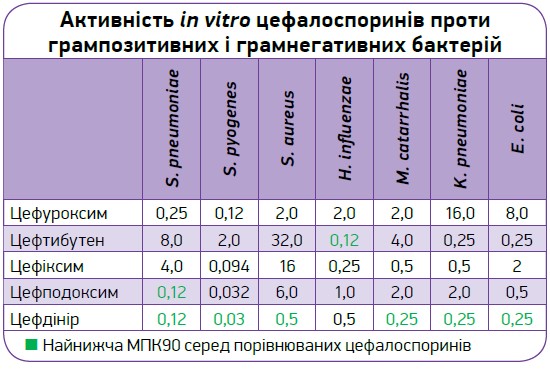 Цефдінір має високу активність проти більшості респіраторних патогенів із нижчими показниками МПК90 (мінімальної концентрації, котра пригнічує ріст 90% ізолятів) порівняно з іншими цефалоспориновими антибіотиками [7-10].
Цефдінір має високу активність проти більшості респіраторних патогенів із нижчими показниками МПК90 (мінімальної концентрації, котра пригнічує ріст 90% ізолятів) порівняно з іншими цефалоспориновими антибіотиками [7-10].
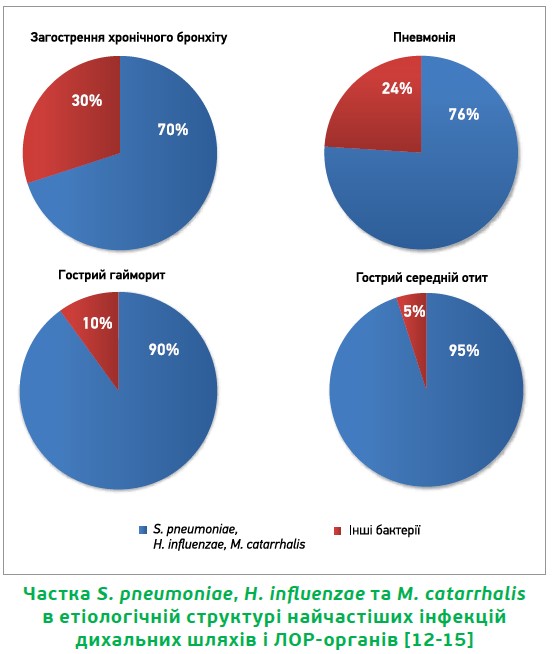
Відповідно до інструкції [11], 3-ДІНІР показаний для лікування дітей і дорослих із легкими та помірно тяжкими інфекціями, спричиненими H. influenzae/parainfluenzae (включно зі штамами, що продукують β-лактамази), S. pneumoniae (лише пеніцилінчутливі штами) та M. catarrhalis (включно зі штамами, що продукують β-лактамази):
- негоспітальною пневмонією;
- загостренням хронічного бронхіту;
- гострим бактеріальним середнім отитом;
- гострим гайморитом.
 Окрім того, 3-ДІНІР може застосовуватися для лікування фарингіту/тонзиліту, зумовленого S. pyogenes, і неускладнених інфекцій шкіри й м’яких тканин, спричинених S. aureus (включно зі штамами, що продукують β-лактамази) та S. pyogenes [11].
Окрім того, 3-ДІНІР може застосовуватися для лікування фарингіту/тонзиліту, зумовленого S. pyogenes, і неускладнених інфекцій шкіри й м’яких тканин, спричинених S. aureus (включно зі штамами, що продукують β-лактамази) та S. pyogenes [11].
Клінічна та бактеріологічна ефективність
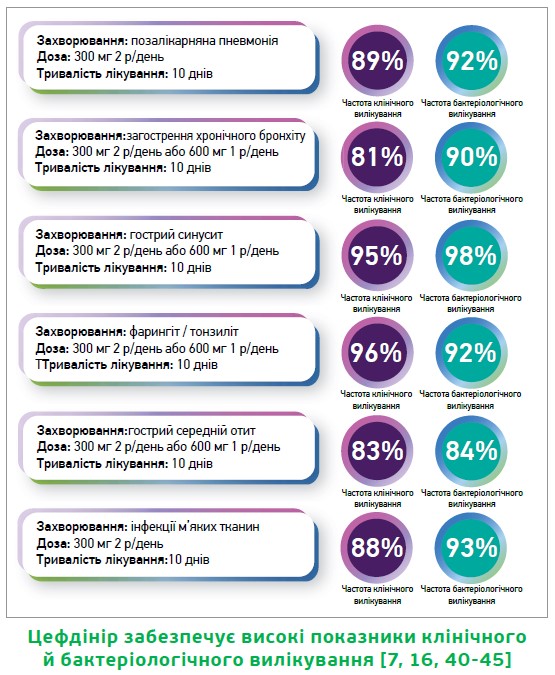
У рандомізованих контрольованих дослідженнях цефдінір продемонстрував високі показники клінічного та бактеріологічного вилікування.
У випробуванні Drehobl і співавт. цефдінір 300 мг 2 р/день і цефаклор 500 мг 3 р/день забезпечили мікробіологічну ерадикацію в >92% пацієнтів із позалікарняною пневмонією. Клінічна відповідь (вилікування + покращення) була досягнута у 89% групи цефдініру й у 86% групи цефаклору [16].
У дорослих пацієнтів із загостренням хронічного бронхіту цефдінір 300 мг 2 р/добу протягом 5 або 10 днів або 600 мг 1 р/добу протягом 10 днів забезпечив високу клінічну (74-81%) і бактеріологічну ефективність (85-90%) [17].
У пацієнтів із гострим бактеріальним верхньощелепним синуситом цефдінір 600 мг 1 р/день або 300 мг 2 р/день продемонстрував клінічну та бактеріологічну ефективність, зіставну з такою амоксициліну/клавуланату 500/125 мг 3 р/день (тривалість лікування в обох групах – 10 днів) [18].
 У міжнародному дослідженні Henry та співавт. порівнювали 10-денні схеми застосування цефдініру 600 мг 1 р/добу та левофлоксацину 500 мг 1 р/добу в дорослих із гострим бактеріальним риносинуситом (ГБРС). Загальні показники клінічного одужання протягом 9-14 днів перевищили 83% без статистичних відмінностей між групами. Гнійні виділення з носа зникли чи зменшилися в 97% пацієнтів у кожній групі лікування [19].
У міжнародному дослідженні Henry та співавт. порівнювали 10-денні схеми застосування цефдініру 600 мг 1 р/добу та левофлоксацину 500 мг 1 р/добу в дорослих із гострим бактеріальним риносинуситом (ГБРС). Загальні показники клінічного одужання протягом 9-14 днів перевищили 83% без статистичних відмінностей між групами. Гнійні виділення з носа зникли чи зменшилися в 97% пацієнтів у кожній групі лікування [19].
У метааналізі J. A. Hadley та співавт. порівняли цефдінір 600 мг 1 р/день, цефдінір 300 мг 2 р/день й амоксицилін/клавуланат 500/125 мг 3 р/день у пацієнтів із ГБРС. Клінічна відповідь (відсутність ознак і симптомів синуситу) на 7-14-й день лікування була подібною для цефдініру 1 р/добу (90%), цефдініру 2 р/добу (87%) й амоксициліну/клавуланату (91%). Загальний показник ерадикації збудників становив 88% для цефдініру (1-2 р/день) і 85% для амоксициліну/клавуланату [20].
У дослідженні Adler і співавт. у дітей із гострим середнім отитом 10-денна терапія цефдініром (7 мг/кг 2 р/добу чи 14 мг/кг 1 р/добу) була ефективнішою за лікування амоксициліном/клавуланатом. На 11-16-й день від початку лікування показник клінічного успіху становив 76,4% для цефдініру 1 р/день, 73,9% для цефдініру 2 р/день та 68,5% для амоксициліну/клавуланату [21].
У дітей із фарингітом, спричиненим β-гемолітичним стрептококом групи А (S. pyogenes), цефдінір 14 мг/кг/добу (1 або 2 р/день) продемонстрував значно кращі результати лікування, ніж пеніцилін. Частота клінічного вилікування для цефдініру 1 р/день, цефдініру 2 р/день і пеніциліну становила 97,4; 96,0 та 86,3% відповідно, частота ерадикації S. pyogenes через 4-9 днів після завершення терапії – 94,3; 94,3 та 70,0% відповідно [22].
 Можливість застосування в ступінчастій терапії
Можливість застосування в ступінчастій терапії
Цефдінір може призначатися перорально як протягом усього курсу антибіотикотерапії, так і на другому етапі ступінчастої терапії після стартового парентерального застосування цефалоспоринів. Стратегія ступінчастої терапії робить лікування комфортнішим за рахунок зменшення кількості ін’єкцій, дає змогу скоротити терміни перебування пацієнта в стаціонарі (а отже, й знизити ризик нозокоміальних інфекцій) і зменшити вартість лікування [23]. При проведенні ступінчастої терапії на тлі поліпшення клінічного стану пацієнта допускається перехід із парентерального введення одного антибіотика на пероральний прийом іншого, що належить до того самого класу та покоління [24]. Наприклад, після короткострокової парентеральної терапії цефалоспорином III покоління цефтріаксоном (який не випускається в лікарській формі для перорального прийому) можна перейти на пероральну терапію препаратом 3-ДІНІР, який також належить до цефалоспоринів III покоління й має схожий спектр антибактеріальної дії. У нещодавньому дослідженні ступінчаста терапія цефтріаксоном (у середньому 3 дні) та цефдініром (у середньому 7 днів) продемонструвала дуже високу ефективність – 99% [25].
Безпека та переносимість
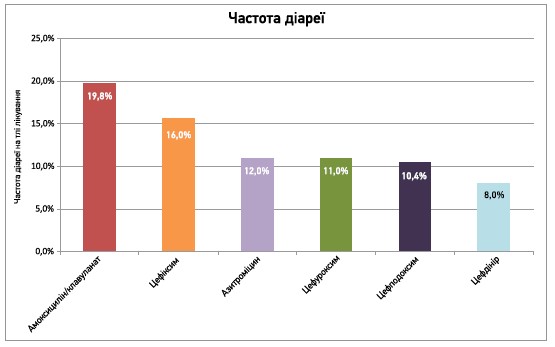
Цефдінір має сприятливий профіль безпеки та переносимості в пацієнтів усіх вікових груп; більшість його побічних ефектів є легкими та минають самостійно. У клінічних дослідженнях лише 2% пацієнтів припинили прийом цефдініру через небажані реакції, потенційно пов’язані з лікуванням. Частота розвитку діареї при лікуванні цефдініром є зіставною з амоксициліном і значно нижчою порівняно з амоксициліном/клавуланатом [5].
 Цефдінір практично не метаболізується й виводиться переважно нирками, при цьому корекція дози рекомендується лише хворим із тяжкою нирковою недостатністю (кліренс креатиніну <30 мл/хв). У пацієнтів із порушенням функції печінки, а також у хворих похилого віку зміна режиму дозування не потрібна [5].
Цефдінір практично не метаболізується й виводиться переважно нирками, при цьому корекція дози рекомендується лише хворим із тяжкою нирковою недостатністю (кліренс креатиніну <30 мл/хв). У пацієнтів із порушенням функції печінки, а також у хворих похилого віку зміна режиму дозування не потрібна [5].
На сьогодні випадків передозування цефдініром у людей не описано. В експериментальних дослідженнях гострої токсичності однократне пероральне введення цефдініру дозою 5600 мг/кг не спричиняло розвитку жодних побічних реакцій [5].
За класифікацією Управління з контролю якості продуктів харчування та лікарських засобів США (FDA), цефдінір має категорію безпеки під час вагітності В (як і амоксицилін чи азитроміцин) [5]. Після прийому цефдініру дозою 600 мг він не визначався в грудному молоці; отже, його застосування у вагітних і жінок, які годують грудним молоком, можна вважати безпечним [5].
Низка цефалоспоринів, які в структурі своїх молекул містять метилтіотріазоловий бічний ланцюг або метилтіодіокситріазинове кільце (цефоперазон, цефтріаксон, цефамандол тощо), в поєднанні з алкоголем можуть зумовлювати дисульфірам-подібні реакції (аж до летального наслідку). Молекула цефдініру не містить цих сполук, тому його застосування разом з алкоголем є безпечним [30].
Cмакова привабливість педіатричної форми
Діти молодшого віку віддають перевагу тим продуктам харчування, що мають знайомий і солодкий смак [31]. Більшість препаратів, які застосовуються в педіатрії, мають незнайомий і гіркий смак, тому пройти повний курс лікування – складне завдання для дітей та їхніх батьків. Недотримання призначеної схеми антибіотикотерапії може погіршувати результати лікування, спричиняти ускладнення й підвищувати ризик селекції резистентних штамів мікроорганізмів [32].
 Значення органолептичних властивостей педіатричних форм антибіотиків добре описане в медичній літературі [33, 34]. У дослідженні K. Sunakawa та співавт. опитування 192 родин виявило, що повний курс призначеної антибіотикотерапії не пройшла ¼ дітей, при цьому відмова дитини приймати препарат через неприємний смак була другою найчастішою причиною низького комплаєнсу (перша причина – рішення батьків, що дитині стало краще) [35]. У дослідженні al-Shammari та співавт. за участю 414 пацієнтів, які звернулися до сімейного лікаря (65,9% дітей), провідними причинами неприхильності до короткочасної антибіотикотерапії були швидке збільшення вираженості симптомів, гіркий смак препарату, забудькуватість і часте дозування [36]. У багатьох інших випробуваннях продемонстровано, що кращий смак антибіотиків достовірно корелює з вищим комплаєнсом.
Значення органолептичних властивостей педіатричних форм антибіотиків добре описане в медичній літературі [33, 34]. У дослідженні K. Sunakawa та співавт. опитування 192 родин виявило, що повний курс призначеної антибіотикотерапії не пройшла ¼ дітей, при цьому відмова дитини приймати препарат через неприємний смак була другою найчастішою причиною низького комплаєнсу (перша причина – рішення батьків, що дитині стало краще) [35]. У дослідженні al-Shammari та співавт. за участю 414 пацієнтів, які звернулися до сімейного лікаря (65,9% дітей), провідними причинами неприхильності до короткочасної антибіотикотерапії були швидке збільшення вираженості симптомів, гіркий смак препарату, забудькуватість і часте дозування [36]. У багатьох інших випробуваннях продемонстровано, що кращий смак антибіотиків достовірно корелює з вищим комплаєнсом.
Смак і запах цефдініру у формі суспензії вивчали в 6 рандомізованих сліпих перехресних дослідженнях порівняно з амоксициліном/клавуланатом, цефпрозилом і азитроміцином. Дітям віком від 4 до 8 років пропонували оцінити смак і запах кожного препарату за візуально-аналоговою шкалою зі «смайлами», вираз яких відповідав оцінці від 1 (дуже погано) до 5 (дуже добре). З-поміж 715 учасників 85% оцінили смак цефдініру як «добрий» або «дуже добрий»; це був найкращий показник серед протестованих антибіотиків (у середньому 63%). Запах цефдініру як «добрий» або «дуже добрий» визначили 71% дітей проти 64% для амоксициліну/клавуланату, цефпрозилу й азитроміцину. Отже, ці дослідження довели, що діти сприймають смак і запах цефдініру краще, ніж такі інших антибіотиків.
Окрім смаку, важливим є смакове задоволення (англ. palatability, від palate – піднебіння), що формується в центральній нервовій системі за участю опіоїдних рецепторів [38]. Смакове задоволення залежить від багатьох факторів, як-от запах, смак, текстура й об’єм дози, а також від попереднього смакового досвіду. У дослідженні Steele та співавт., що проводилося в США серед лікарів, вивчали смакове задоволення для найчастіше застосовуваних антибіотиків у вигляді суспензії [39]. Для кожної суспензії за шкалою від 0 (найгірше) до 5 (найкраще) лікарі сліпим методом оцінювали запах, текстуру, смак і післясмак; сумарна оцінка визначала смакову задоволеність. У результаті цефдінір отримав значно кращі оцінки, ніж інші антибіотики.
Ключові переваги цефдініру
- Стабільність щодо більшості β-лактамаз, унікальний профіль розподілу в тканинах
- Розширений спектр антибактеріальної активності, що охоплює всі основні респіраторні патогени
- Нижчі значення МПК90 порівняно з іншими цефалоспоринами
- Висока частота клінічного й бактеріологічного вилікування
- Сприятливий профіль безпеки в усіх вікових групах, можливість призначення під час вагітності й лактації
- Зручність застосування – 1 або 2 рази на добу, незалежно від уживання їжі
- Висока смакова привабливість педіатричної лікарської форми
Список літератури знаходиться в редакцій.



