22 березня, 2026
Потенційна імуномодулювальна роль Енгістолу при SARS-CoV‑2-індукованому ушкодженні легень: результати пілотного експериментального дослідження
Наприкінці 2019 року з’явилися перші повідомлення про нову коронавірусну інфекцію SARS-CoV‑2, яка вже в березні 2020 року була оголошена Всесвітньою організацією охорони здоров’я (ВООЗ) пандемією. За даними ВООЗ, протягом перших років пандемії було зареєстровано сотні мільйонів випадків COVID‑19 та мільйони летальних наслідків у всьому світі (WHO, 2023). COVID‑19 став безпрецедентним викликом для систем охорони здоров’я через високий рівень госпіталізації, значну потребу в інтенсивній терапії та тривалі наслідки для пацієнтів.
У перші хвилі пандемії частка госпіталізованих пацієнтів серед підтверджених випадків коливалася в межах 10-20%, а ≈3-5% хворих потребували лікування у відділенні інтенсивної терапії (Guan W.J. et al., 2020; Richardson S. et al., 2020). Летальність значно зростала в пацієнтів із розвитком дихальної недостатності та потребою в штучній вентиляції легень (Huang C. et al., 2020). Крім гострої фази, значна частка пацієнтів мала довготривалі наслідки, включаючи персистуючі респіраторні симптоми, зниження дифузійної здатності легень та постковідний синдром (Nalbandian A. et al., 2021).
Саме ураження легень визначає тяжкість перебігу COVID‑19. У більшості госпіталізованих пацієнтів розвивається вірусна пневмонія з двобічним інтерстиціальним ураженням. У частки хворих процес прогресує до гострого респіраторного дистрес-синдрому і тяжкої гіпоксемії (Guan W.J. et al., 2020; Huang C. et al., 2020).
Патоморфологічні дослідження показали, що ушкодження легень при COVID‑19 характеризується дифузним альвеолярним ураженням, гіперплазією пневмоцитів ІІ типу, вираженою запальною інфільтрацією та мікротромбозом судин (Ackermann M. et al., 2020; Carsana L. et al., 2020). Важливо, що тяжкість перебігу визначається не лише вірусним навантаженням, а й дисрегульованою запальною відповіддю. Це відображається в зниженні смертності при застосуванні системних глюкокортикоїдів у пацієнтів, які потребують кисневої підтримки, тобто при клінічно значущому легеневому запаленні (RECOVERY Collaborative Group; Horby P. et al., 2021).
Отже, контроль легеневого ураження є ключовою терапевтичною мішенню при COVID‑19. Незважаючи на наявність противірусної та протизапальної терапії, питання раннього впливу на запальні механізми з метою зменшення ушкодження легеневої тканини залишається актуальним для прикладної медицини.
Сучасні терапевтичні стратегії спрямовані переважно або на пригнічення вірусної реплікації, або на контроль уже сформованої системної запальної відповіді. Водночас можливості профілактичного впливу на локальні імунозапальні процеси в легенях до розвитку вираженого ушкодження залишаються обмеженими. Саме тому триває пошук молекул із потенційною імуномодулювальною дією, здатних впливати на перебіг інфекції без прямої імуносупресії.
Енгістол – це лікарський засіб із доведеною клінічною ефективністю, який застосовується для лікування та профілактики респіраторних інфекцій. Препарат має багаторічну історію застосування: у медичній практиці він використовується вже понад 80 років, що свідчить про накопичений клінічний досвід, терапевтичну цінність та довіру з боку лікарів і пацієнтів. Такий тривалий період використання дозволив сформувати значний масив клінічних спостережень, які підтверджують його ефективність у підтримці противірусної резистентності та регуляції імунної відповіді (Hanferian R.A. et al., 2019). Енгістол має також значний міжнародний досвід застосування: препарат використовується в різних країнах світу, включно з Європою, Північною Америкою та Азією, що свідчить про універсальність його терапевтичного профілю та можливість інтеграції у різні системи охорони здоров’я (Hanferian R.A. et al., 2019).
Окрему увагу привертає сприятливий профіль безпеки препарату. Дані клінічних і експериментальних досліджень свідчать про добру переносимість Енгістолу та можливість його застосування у широких групах пацієнтів, включно з дітьми, особами літнього віку та пацієнтами з коморбідною патологією. У клінічних роботах також показано, що препарат може використовуватися як компонент комплексної терапії респіраторних інфекцій і характеризується низьким ризиком небажаних реакцій (Herzberger G. et al., 1997; Matusiewicz R., 1997; Heilmann A., 1994). Наявність такого профілю безпеки має важливе клінічне значення, оскільки дозволяє розглядати Енгістол як засіб підтримки імунної відповіді без надмірної стимуляції або пригнічення захисних механізмів організму.
У попередніх дослідженнях було показано, що Енгістол може впливати на різні ланки імунної відповіді, зокрема підвищувати фагоцитарну активність імунних клітин, стимулювати продукцію інтерферонів та модулювати цитокінову відповідь при вірусних інфекціях (Wronski S. et al., 2018; Roeska K., Seilheimer B., 2010; Wagner H., 1986; Enbergs H., 2006). Експериментальні роботи також демонструють його здатність зменшувати вірус-індуковане запалення дихальних шляхів і підтримувати ефективність противірусного захисту організму (Wronski S. et al., 2018; Roeska K., Seilheimer B., 2010).
Водночас патогенез тяжких вірусних інфекцій, зокрема COVID‑19, значною мірою визначається не лише вірусним навантаженням, а й дисрегульованою імунною відповіддю. Саме тому сучасні терапевтичні стратегії дедалі більше орієнтуються на патогенетичний підхід – регуляцію запального процесу та обмеження тканинного ушкодження.
У цьому контексті особливий інтерес викликають результати експериментального дослідження на моделі SARS-CoV‑2-інфекції, у якому оцінювали потенційний вплив Енгістолу на розвиток вірус-індукованого ушкодження легеневої тканини. Отримані дані дозволяють розширити уявлення про можливі патогенетичні механізми дії препарату при вірусних респіраторних інфекціях (Yang D. et al., 2023).
Методи
Дизайн дослідження та експериментальна модель
Дослідження було виконано на тваринній моделі, що відтворює характерні респіраторні прояви COVID‑19 у людини. В роботі використано сирійських золотистих хом’яків (LVG golden Syrian hamsters) віком 6-7 тиж – модель, що демонструє розвиток вірусної пневмонії з альвеолярним ушкодженням і запальною інфільтрацією після інтраназального зараження SARS-CoV‑2 (Yang D. et al., 2023).
До дослідження було включено 36 самців сирійських золотистих хом’яків. Деяким тваринам проводили псевдоінфікування – інтраназально вводили фосфатно-сольовий буфер (PFU) замість вірусної суспензії, що дозволяло сформувати контрольні групи без вірусного навантаження.
Після рандомізації сформували 5 груп: 2 контрольні (псевдоінфікування + плацебо; псевдоінфікування + Енгістол) і 3 експериментальні (інфікування SARS-CoV‑2 + плацебо; інфікування SARS-CoV‑2 + Енгістол у дозах 6,4 або 1,6 мл/кг/добу).
Такий дизайн забезпечував можливість одночасної оцінки безпечності препарату в умовах відсутності інфекції, його впливу на перебіг SARS-CoV‑2-інфекції та потенційної дозозалежності ефекту щодо легеневого ушкодження.
Профілактичний режим введення
Препарат або плацебо вводили підшкірно 1 р/добу за 7 днів до інфікування (D‑7) та продовжували до 3-го дня після інфікування. Такий підхід обрали для моделювання саме профілактичного впливу – із формуванням можливого імуномодулювального ефекту до контакту з вірусом (Yang D. et al., 2023).
Інфікування проводили на день 0 – через 2 год після чергового введення препарату або плацебо. Тваринам інтраназально вводили 2×10⁵ PFU SARS-CoV‑2 (ізолят USA-WA1/2020) в об’ємі 100 мкл. У контрольних групах замість вірусної суспензії інтраназально вводили фосфатно-сольовий буфер, що відповідало процедурі псевдоінфікування (Yang D. et al., 2023).
Клінічне спостереження
Після інфікування тварин щодня зважували та проводили клінічне спостереження. Динаміку маси тіла використовували як непрямий показник тяжкості перебігу інфекції, що дозволяло оцінювати загальний стан організму впродовж гострої фази захворювання (Yang D. et al., 2023).
Для подальшого лабораторного аналізу тварин виводили з експерименту на 1-шу та 4-ту добу після інфікування. На кожній часовій точці досліджували по 3 тварини з кожної групи, що забезпечувало порівняльну оцінку ранніх та розгорнутіших морфологічних і вірусологічних змін.
Визначення вірусного навантаження
5 часток правої легені гомогенізували з подальшим визначенням вірусного титру методом бляшкоутворення (plaque assay). Кількісна оцінка дозволяла визначити рівень реплікації SARS-CoV‑2 у легеневій тканині та оцінити можливий вплив Енгістолу на вірусне навантаження (Yang D. et al., 2023).
Гематологічні показники
Проводили загальний аналіз крові з оцінкою клітинного складу, що дозволяло охарактеризувати системну запальну відповідь на інфекцію та оцінити можливий вплив Енгістолу на гематологічні показники (Yang D. et al., 2023).
Гістопатологічна оцінка
Одну частку лівої легені фіксували, вона зазнавала стандартної гістологічної обробки, згодом її фарбували гематоксиліном та еозином (Г-Е). Під час мікроскопічної оцінки аналізували товщину альвеолярних перегородок, вираженість запальної інфільтрації, наявність гіперплазії епітелію та ступінь консолідації легеневої тканини.
Морфологічний аналіз розглядався як основний критерій оцінки впливу Енгістолу на тяжкість легеневого ушкодження в моделі SARS-CoV‑2-індукованої інфекції (Yang D. et al., 2023).
Отже, дослідження було спроєктоване як контрольований профілактичний експеримент із можливістю паралельної оцінки вірусної реплікації, системної запальної відповіді та структурних змін легеневої тканини.
Результати
Клінічні показники та вірусне навантаження
Після інтраназального інфікування SARS-CoV‑2 у тварин розвивалися типові для цієї моделі клінічні прояви, включно зі зниженням маси тіла впродовж гострої фази інфекції. Порівняльний аналіз динаміки маси тіла між групами не продемонстрував суттєвих відмінностей між інфікованими тваринами, які отримували плацебо, та тими, що отримували Енгістол у досліджуваних дозах (Yang D. et al., 2023).
Визначення вірусного титру в легеневій тканині методом бляшкоутворення також не виявило достовірного зниження вірусного навантаження під впливом Енгістолу. Реплікація SARS-CoV‑2 у легенях інфікованих тварин була зіставною в групах плацебо й активного втручання (Yang D. et al., 2023).
Аналогічно аналіз гематологічних показників не засвідчив значущих змін клітинного складу крові між відповідними групами (Yang D. et al., 2023). Отже, препарат не продемонстрував вираженого впливу на системні показники перебігу інфекції або на рівень вірусної реплікації.
Гістопатологічні зміни легеневої тканини
Натомість під час морфологічного аналізу було виявлено відмінності у вираженості легеневого ушкодження, що відображено на рисунку.
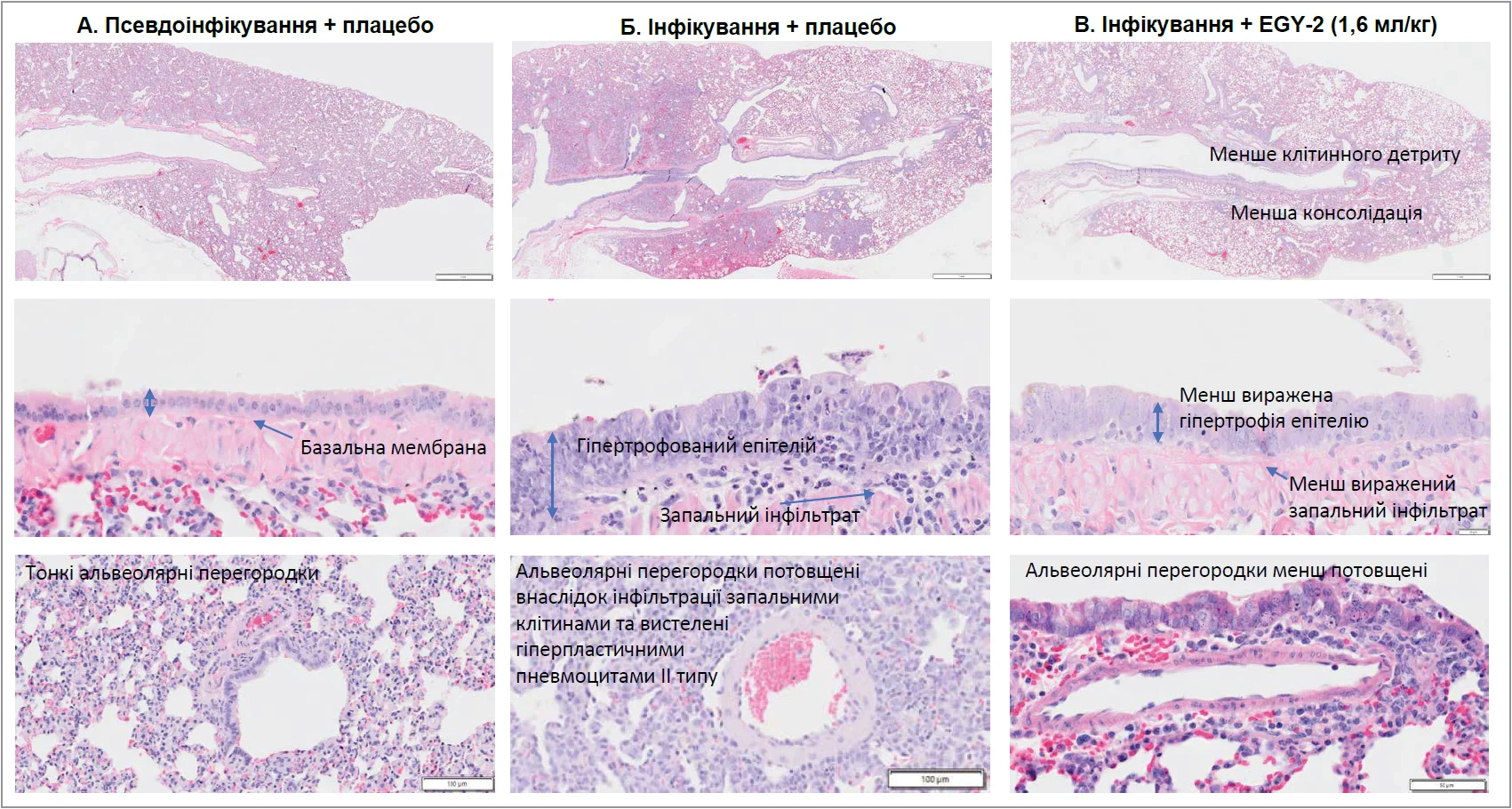 Рис. Морфологічні зміни легеневої тканини в сирійських золотистих хом’яків у моделі SARS-CoV‑2-інфекції
Рис. Морфологічні зміни легеневої тканини в сирійських золотистих хом’яків у моделі SARS-CoV‑2-інфекції
A. Контрольна група (псевдоінфікування + плацебо): нормальна структура легеневої тканини з тонкими альвеолярними перегородками. Б. Інфікування SARS-CoV‑2 + плацебо: виражені патологічні зміни, характерні для вірусної пневмонії, включно з гіпертрофією епітелію, інфільтрацією запальних клітин, потовщенням альвеолярних перегородок й ознаками консолідації легеневої тканини. В. Інфікування SARS-CoV‑2 + Енгістол (1,6 мл/кг/добу): зменшення вираженості запального процесу, менша інфільтрація запальними клітинами, менш виражена гіпертрофія епітелію та менше потовщення альвеолярних перегородок порівняно з групою плацебо.
У тварин, інфікованих SARS-CoV‑2, які отримували плацебо, спостерігали характерні для моделі зміни: виражену нейтрофільну інфільтрацію, проліферативне запалення, потовщення альвеолярних перегородок і гіперплазію пневмоцитів ІІ типу. Запальні інфільтрати часто формували осередки з підвищеною клітинністю, що супроводжувалося зменшенням площі добре аерованої легеневої тканини (Yang D. et al., 2023).
У групі інфікованих тварин, які отримували Енгістол у дозі 1,6 мл/кг/добу, якісна гістологічна оцінка продемонструвала менш виражену інфільтрацію запальними клітинами, меншу товщину альвеолярних перегородок та зниження ступеня консолідації легеневої тканини порівняно із групою плацебо (Yang D. et al., 2023). Морфологічна картина свідчила про зменшення інтенсивності запального процесу.
Водночас у групі з вищою дозою препарату (6,4 мл/кг/добу) переконливого додаткового зменшення морфологічних змін не продемонстровано (Yang D. et al., 2023).
Висновки
Пілотне експериментальне дослідження на моделі SARS-CoV‑2-індукованої інфекції продемонструвало, що профілактичне застосування Енгістолу не впливає на рівень вірусної реплікації або системні клінічні показники перебігу інфекції. Водночас у тварин, які отримували препарат, спостерігалося зменшення вираженості морфологічних ознак ушкодження легеневої тканини, зокрема інтенсивності запальної інфільтрації та ступеня консолідації легені.
Отримані результати свідчать, що дія препарату, імовірно, реалізується не через прямий противірусний ефект, а шляхом активації імунологічних механізмів і модифікації локальної запальної відповіді. Такий патогенетичний вплив може сприяти обмеженню запального ушкодження легеневої тканини та потенційно зменшувати тяжкість наслідків інфекційного процесу.
Оскільки контроль легеневого ураження залишається ключовою терапевтичною мішенню при COVID‑19 та інших тяжких ГРВІ, питання раннього впливу на запальні механізми є критично актуальним для прикладної медицини. У цьому контексті результати дослідження підкреслюють важливість стратегій, спрямованих не лише на контроль вірусної реплікації, а й на системну регуляцію імунозапальної відповіді організму.
Враховуючи вищезазначене, Енгістол можемо розглядати як важливий компонент комплексної терапії, що забезпечує патогенетичний контроль інфекційного процесу. Його здатність модифікувати локальну відповідь та зменшувати морфологічні ознаки ушкодження легеневої тканини (інфільтрацію та консолідацію) дозволяє обмежити патологічні зміни ще на ранніх етапах. Отже, застосування Енгістолу може сприяти підтримці організму та потенційному зменшенню тяжкісті клінічних наслідків вірусних респіраторних інфекцій.Окрему увагу слід приділити профілю безпеки препарату. Тривалий досвід застосування свідчить про його добру переносимість, що є важливою характеристикою для засобів, які можуть використовуватися у широких групах пацієнтів, зокрема в осіб із підвищеним ризиком розвитку ускладнень респіраторних інфекцій.
Література
- World Health Organization. WHO Coronavirus (COVID‑19) Dashboard. WHO, 2023. Доступ 26.02.2026, https://data.who.int/dashboards/covid19/cases.
- Guan W.J., Ni Z.Y., Hu Y. et al. Clinical Characteristics of Coronavirus Disease 2019 in China. N Engl J Med., 2020; 382 (18): 1708-1720. doi:10.1056/NEJMoa2002032.
- Richardson S., Hirsch J.S., Narasimhan M. et al. Presenting Characteristics, Comorbidities, and Outcomes Among 5700 Patients Hospitalized With COVID‑19 in the New York City Area. JAMA, 2020; 323 (20): 2052-2059. doi:10.1001/jama.2020.6775.
- Huang C., Wang Y., Li X. et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet, 2020; 395 (10223): 497-506. doi:10.1016/S0140-6736(20)30183-5.
- Nalbandian A., Sehgal K., Gupta A. et al. Post-acute COVID‑19 syndrome. Nat Med., 2021; 27: 601-615. doi:10.1038/s41591-021-01283-z.
- Ackermann M., Verleden S.E., Kuehnel M. et al. Pulmonary Vascular Endothelialitis, Thrombosis, and Angiogenesis in Covid‑19. N Engl J Med., 2020; 383 (2): 120-128. doi:10.1056/NEJMoa2015432.
- Carsana L., Sonzogni A., Nasr A. et al. Pulmonary post-mortem findings in a large series of COVID‑19 cases from Northern Italy. Lancet Infect Dis., 2020; 20 (10): 1135-1140. doi:10.1016/S1473-3099(20)30434-5.
- RECOVERY Collaborative Group, Horby P., Lim W.S. et al. Dexamethasone in Hospitalized Patients with Covid‑19. N Engl J Med., 2021; 384 (8): 693-704. doi:10.1056/NEJMoa2021436.
- Hanferian R.A., Daihes N.A., Karneeva O.V., Garashchenko T.I., Kim I.A. Antiviral and immunomodulatory effects of Engystol. Meditsinsky Sovet. 2019; 8: 116-120. DOI: https://doi.org/10.21518/2079-701X‑2019-8-116-120.
- Herzberger G., Weiser M. Homeopathic Treatment of Infections of Various Origins: A Prospective Study. Biomedical Therapy, 1997; 14: 123-127.
- Matusiewicz R. The effect of a homeopathic preparation on the clinical condition of patients with corticosteroid-dependent bronchial asthma. Biomed Ther., 1997; 15: 70-74.
- Heilmann A. A combination injection preparation as a prophylactic for flu and common colds. Biological Therapy, 1994; VII (4): 249-253.
- Wronski S., Dannenmaier J., Schild S., Macke O., Müller L., Burmeister Y., Seilheimer B., Müller M. Engystol reduces onset of experimental respiratory syncytial virus-induced respiratory inflammation in mice by modulating macrophage phagocytic capacity. PLoS One, 2018 Apr 19; 13 (4): e0195822. doi:10.1371/journal.pone.0195822.
- Roeska K., Seilheimer B. Antiviral activity of Engystol® and Gripp-Heel®: an in-vitro assessment. J Immune Based Ther Vaccines, 2010 Nov 16; 8: 6. doi:10.1186/1476-8518-8-6.
- Enbergs H. Effects of the homeopathic preparation Engystol® on interferon-γ production by human T-lymphocytes. Immunol Invest 2006; 35:19-27
- Denys A et al. Efficacy of preoperative immunoprophylaxis in patients with neoplastic diseases (II). Int Rev Allergol Immunol 1999;5(1);46-50. 5.
- Yang D., Xue Y., Taylor S., Ihms E.A., Weyer K., Zalduondo L., Seilheimer B., Fitzpatrick E., Jonsson C. Engystol may reduce lung pathology in SARS-CoV‑2 infected hamsters: a pilot study. In: 4th Edition of Infectious Diseases Congress – Abstract Book. 2023.
Підготувала Ганна Кирпач
Медична газета «Здоров’я України 21 сторіччя» № 3 (614), 2026 р



