19 липня, 2021
Від метаболічного синдрому до нефропротекції: лайфхаки ведення пацієнтів з артеріальною гіпертензією та коморбідністю
11 травня у форматі вебінару за підтримки компанії Acino відбувся міждисциплінарний клінічний розбір «Від метаболічного синдрому до нефропротекції». Модератор заходу – Ольга Миколаївна Барна, завідувачка кафедри загальної практики (сімейної медицини) Національного медичного університету ім. О. О. Богомольця (м. Київ), доктор медичних наук, професор. До професійної дискусії долучилися кардіолог і ендокринолог – Дмитро Андрійович Лашкул, професор кафедри внутрішніх хвороб № 1 та симуляційної медицини Запорізького державного медичного університету, доктор медичних наук, а також Яніна Андріївна Саєнко, провідний науковий співробітник відділу діагностики та лікування метаболічних захворювань ДНУ «Центр інноваційних медичних технологій НАН України» (м. Київ), кандидат медичних наук.
На початку вебінару професор О.М. Барна зазначила, що контроль факторів ризику (ФР) більшою мірою впливає на кінцеві точки артеріальної гіпертензії (АГ), ніж лікування (навіть високотехнологічне). Наразі виокремлюють декілька рівнів профілактики (Hong K.N. et al., 2017): преморбідна – корекція поведінки, способу життя (дотримання дієти, контроль маси тіла, адекватна фізична активність, відмова від куріння, мінімізація негативного впливу навколишнього середовища); первинна – контроль ФР, як-от дисліпідемія, АГ, цукровий діабет (ЦД), метаболічний синдром; вторинна й третинна – попередження загострення процесу в пацієнтів із проявами атеросклеротичної хвороби серця, ураження периферичних судин, серцевої недостатності (СН), цереброваскулярних хвороб.
АГ і ЦД мають багато точок дотику як у контексті причин розвитку, так і з погляду наслідків. Хворого із ЦД часто називають «особливим кардіологічним пацієнтом» з огляду на вкрай високий кардіоваскулярний ризик, що вираженіше прослідковується в жіночій популяції. Зокрема, ризик появи АГ у хворих на діабет зростає удвічі, коронарних подій – у 2-4, СН – в 3-5, інсульту – в 3, захворювань периферичних судин – у 2-4. Нерідко в спеціалізованій пресі зустрічається теза «діабет = серцево-судинні захворювання» (Long A.N., Dagogo-Jack S., 2011).
В рамках вебінару фахівці презентували 3 клінічних випадки й обговорили стратегії лікування пацієнтів з АГ залежно від коморбідності, особливу увагу сфокусувавши на поєднанні АГ з порушеннями вуглеводного обміну та методах профілактики.
Клінічний випадок 1
Пацієнт Р., 42 роки, звернувся до сімейного лікаря з метою контрольного огляду.
Анамнез: офісний працівник, веде малорухливий спосіб життя, не курить, епізодично вживає алкоголь (2 напої/тиж), режим харчування – фастфуд, полюбляє швидкі вуглеводи. Лікарські засоби не застосовує, крім періодичного використання дезлоратадину під час загострення алергічного риніту.
Об’єктивно: пацієнт підвищеного харчування (зріст – 178 см, маса тіла – 105 кг, індекс маси тіла (ІМТ) перевищує 33 кг/м2, окружність талії (ОТ) – 96 см). Рівень артеріального тиску (АТ) під час огляду – 148/88 мм рт. ст.
Дані лабораторних обстежень: рівень HbA1c – 6,1%, глюкоза крові натще – 6,7 ммоль/л, глюкозотолерантний тест (ГТТ) через 2 год – 8,1 ммоль/л, загальний холестерин (ХС) – 5,4 ммоль/л, ХС ліпопротеїнів низької щільності (ЛПНЩ) – 2,25 ммоль/л. Аналіз сечі на наявність мікроальбуміну – в межах норми.
Діагноз: предіабет. Аліментарно-конституційне ожиріння I ст. АГ (стадія I, ступінь 1, низький ризик, ASCVD = 2%).
Призначення: дієта, фізичні вправи, засіб на основі порошку листя моринги маслянистої (Моринга-Йоруба) 2 р/день, валсартан 80 мг (Діокор Соло) вранці, повторне обстеження через 2 міс.
Дані лабораторних досліджень при повторному обстеженні через 2 міс (протягом зазначеного періоду пацієнт дотримувався рекомендацій лікаря): АТ – 132/75 мм рт. ст, рівень HbA1c – 5,6%, глюкоза крові натще – 5,8 ммоль/л, ГТТ через 2 год – 7,1 ммоль/л, загальний ХС – 5,3 ммоль/л, ХС ЛПНЩ – 2,2 ммоль/л. Аналіз сечі на наявність мікроальбуміну – в межах норми.
Діагноз: АГ (стадія I, ступінь 1, низький ризик, ASCVD = 1%). Аліментарно-конституційне ожиріння I ст.
Рекомендовано: продовжувати прийом валсартану 80 мг (Діокор Соло) вранці, дотримуватися дієти та фізичної активності.
? Чи правильним, на вашу думку, є призначення немедикаментозних стратегій і монотерапії антигіпертензивним препаратом (АГП) цьому пацієнту?
Д.А. Лашкул: Останнім часом фахівці акцентують увагу на використанні комбінованої антигіпертензивної терапії, однак я хотів би зауважити, що ефективність немедикаментозних методів у багатьох випадках зіставна з такою фармакотерапії. Зокрема, в описаного пацієнта модифікація способу життя забезпечила відчутні позитивні зміни.
Згідно з настановами Європейського товариства кардіологів / Європейського товариства з АГ (ESC/ESH, 2018), до пацієнтів, яким показана стартова монотерапія АГП, належать хворі з АГ низького ризику ступеня 1 (АТ <150/90 мм рт. ст.), пацієнти дуже похилого віку (≥80 років) і т. зв. крихкі (тендітні) пацієнти. Лише після використання зазначеної опції рекомендується призначати фіксовані комбінації.
? В описаному клінічному випадку сімейний лікар призначив валсартан 80 мг (Діокор Соло) – блокатор рецепторів до ангіотензину II (БРА). Коли варто віддавати перевагу БРА, а в яких ситуаціях доцільно використати інгібітори ангіотензинперетворювального ферменту (АПФ)?
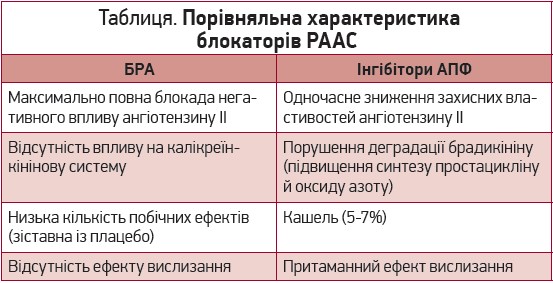
Д.А. Лашкул: Наразі в арсеналі лікарів існують 5 класів АГП, серед яких провідними є блокатори ренін-ангіотензин-альдостеронової системи (РААС). За наявності АГ вони розглядаються як засоби вибору (табл.). Доведена здатність блокаторів РААС запобігати серцево-судинним подіям.
До особливостей дії БРА належать блокувальний вплив на АТ1-рецептори до ангіотензину II (останні відповідають за вазоконстрикцію, вивільнення альдостерону, оксидативний стрес, активацію симпатичної нервової системи, інгібування вивільнення реніну, реабсорбцію нирками натрію та рідини, клітинний ріст і проліферацію), а також стимулювальна дія на АТ2-рецептори до ангіотензину II й опосередковані ними ефекти, як-от вазодилатація, апоптоз, антипроліферація, вивільнення оксиду азоту, продукція брадикініну, антидіурез.
За моїми спостереженнями, для пацієнтів, яким призначають АГП, пріоритетним є переносимість лікування. Дані досліджень, зокрема спостереження G. Mancia та співавт. (2011) за участю понад 130 тис. пацієнтів, свідчать, що прихильність до терапії БРА є вищою порівняно з такою за прийому інгібіторів АПФ.
Чому ж саме валсартан? Якщо йдеться про обрання конкретного представника класу, варто аналізувати наявну доказову базу. На сьогодні найбільша кількість наукових даних серед сартанів накопичена стосовно валсартану. Вчені досліджували його вплив у різних когортах пацієнтів: із ФР, супутньою ішемічною хворобою серця, інфарктом міокарда, СН. Наразі валсартан посідає важливе місце в настановах з лікування АГ.
Оскільки пацієнт Р. мав ФР, порушення вуглеводного обміну при первинному візиті, це стало додатковим аргументом на користь призначення БРА. Дані досліджень (Elliot W.J. et al., 2007) свідчать, що серед усіх АГП із найменшим ризиком розвитку ЦД асоціюються саме БРА.
? За рахунок яких механізмів реалізується протидіабетична дія БРА?
Я.А. Саєнко: У прогресуванні та регресі ЦД задіяні адипонектин і лептин (однак наголошу, що їхній рівень не потрібно визначати рутинно у всіх пацієнтів із ЦД). Валсартан сприяє зниженню рівня лептину, котрий стимулює оксидативний стрес і провокує цитокіновий шторм, та підвищенню концентрації адипонектину, що здійснює протидіабетичний вплив.
Через взаємозв’язок з АТ1- та АТ2-рецепторами ангіотензину II забезпечується апоптоз великих за розміром адипоцитів; цим опосередкований і механізм зниження маси тіла в хворих. Водночас валсартан зменшує інсулінорезистентність (покращує засвоєння вуглеводів скелетними м’язами, жировою тканиною та печінкою, знижує синтез глюкози печінкою); нормалізує ліпідний обмін; пригнічує запалення й атерогенез (зменшує продукцію запальних цитокінів і збільшує таку оксиду азоту.
? Чому в цьому випадку лікування предіабету розпочали із засобу Моринга-Йоруба, а не з метформіну?
Я.А. Саєнко: В описаній ситуації допустимі 2 шляхи: порекомендувати рослинний засіб Моринга-Йоруба чи застосувати метформін. У власній практиці я використовую обидва варіанти (частіше призначаю метформін, оскільки така тактика є більш доказово обґрунтованою).
Однак існують категорії пацієнтів, які прихильні до фітотерапії чи категорично відмовляються від фармакотерапевтичного лікування. Таким хворим краще запропонувати саме засіб Моринга-Йоруба, адже він сприяє нормалізації ліпідного профілю, зниженню маси тіла, апетиту й рівня глюкози крові, що й підтверджує наведений клінічний випадок. Досягнення позитивної клінічної динаміки мотивуватиме пацієнтів дослухатися до порад лікаря в подальшому й підвищуватиме комплаєнс.
Клінічний випадок 2
Пацієнтка Н., 58 років, на плановому огляді в кардіолога скаржиться на головний біль, підвищення АТ.
Анамнез: страждає на АГ протягом 10 років, нерегулярно застосовує лізиноприл 20 мг/добу. Протягом останніх 3 міс відзначає появу сухого кашлю. Веде малорухливий спосіб життя, не курить.
Об’єктивно: пастозність гомілок і стоп. Пацієнтка підвищеного харчування (зріст – 162 см, маса тіла – 90 кг, ІМТ перевищує 34 кг/м2, ОТ – 92 см).
Дані лабораторних та інструментальних обстежень: АТ – 168/104 мм рт. ст. Рентгенографія органів грудної клітки – без патологічних змін. Рівень HbA1c – 5,9%, глюкоза крові натще – 6,6 ммоль/л, ГТТ через 2 год – 8,4 ммоль/л, загальний ХС – 5,9 ммоль/л, ХС ЛПНЩ – 2,87 ммоль/л, креатинін – 115 мкмоль/л. Клінічний аналіз сечі: щільність – 1014, білок – 2 г/л, альбумін – 15 мг/ммоль, еритроцити – 1 в полі зору, лейкоцити – 3 в полі зору, швидкість клубочкової фільтрації (ШКФ) – 52 мл/хв/1,73 м2.
Діагноз: АГ, стадія II, ступінь 2, ризик високий. Хронічна хвороба нирок (ХХН; гіпертензивна нефропатія) 3а стадії, альбумінурія А2. Аліментарно-конституційне ожиріння I ст. Предіабет.
Призначено: дотримуватися дієти та виконувати фізичні вправи; припинити використання лізиноприлу через побічний ефект у вигляді кашлю; застосовувати комбінацію валсартан 160 мг / гідрохлортіазид 12,5 мг (Діокор 160) 1 р/день уранці, розувастатин 10 мг (Клівас) увечері; з’явитися на огляд через 2 тиж для корекції дози АГП.
Повторний огляд через 2 тиж: кашель не турбує, АТ – 138/89 мм рт. ст., пастозність стоп.
Дані лабораторних обстежень: рівень HbA1c – 5,8%, глюкоза крові натще – 6,5 ммоль/л, ГТТ через 2 год – 8,3 ммоль/л, загальний ХС – 5,5 ммоль/л, ХС ЛПНЩ – 2,32 ммоль/л, креатинін – 125 мкмоль/л.
Діагноз: АГ, стадія II, ступінь 2, ризик високий. ХХН (гіпертензивна нефропатія) 3а стадії, альбумінурія А2. Аліментарно-конституційне ожиріння I ст. Предіабет.
Рекомендовано: дотримуватися дієти та виконувати фізичні вправи; застосовувати комбінацію валсартан 160 мг / гідрохлортіазид 12,5 мг (Діокор 160) 1 р/день уранці, розувастатин 10 мг (Клівас) увечері, метформін 500 мг увечері; з’явитися на огляд через 1 міс для корекції дози АГП.
? Чим ви керувалися під час призначення пацієнтці Н. комбінації БРА та діуретика?
Д.А. Лашкул: У переважної більшості пацієнтів з АГ тактикою вибору є призначення фіксованих комбінацій: інгібітори АПФ або БРА + діуретик чи інгібітори АПФ або БРА + антагоністи кальцію (АК). Показання для використання комбінації БРА й діуретика – СН, набряковий синдром, ЦД, ізольована систолічна АГ, інсульт в анамнезі, діабетична та недіабетична нефропатія, схильність до тахіаритмії.
У пацієнтки Н. спостерігається зниження ШКФ, що свідчить про порушення функції нирок. Дисфункцію нирок у пацієнта з АГ спричиняють різні фактори. Якщо АГ зумовлює ХХН, констатують гіпертензивну нефропатію. Відповідно до результатів досліджень зниження ШКФ асоціюється зі збільшенням ризику розвитку кардіоваскулярних подій, атеросклеротичних змін. У пацієнтів із ШКФ <60 мл/хв/1,73 м2 така ймовірність зростає майже на 40%. Саме тому, говорячи про профілактику ренокардіальних порушень, слід зосередитися на контролі АТ (зменшення споживання натрію й білка сприяє зниженню альбумінурії) та блокуванні впливу ангіотензину II.
? Пацієнт з АГ, порушеннями вуглеводного обміну й ХХН: який діагностичний мінімум у цьому випадку?
Я.А. Саєнко: Існує величезна проблема з недостатнім визначенням ШКФ у пацієнтів із предіабетом і ЦД. Чомусь вважається, що насамперед хворі на ЦД 1 типу страждають на ХХН, проте визначати цей показник варто у всіх пацієнтів. Зазвичай на момент встановлення діагнозу ЦД (або навіть предіабету) в пацієнта вже виявляється ХХН, що може мати різний ґенез, у т. ч. бути спричиненою АГ.
Критично важливим моментом є оцінка альбумінурії. Визначати цей параметр слід у кожного пацієнта з порушенням вуглеводного обміну (проба у випадковій порції сечі; просте дослідження, яке виконують майже всі лабораторії). Альбумінурія – важливий прогностичний маркер, але не розвитку дисфункції нирок, а появи серцево-судинного захворювання. Враховуйте, що появу білка в сечі також здатні спровокувати інтенсивне фізичне навантаження, порушення дієти, тому важливо відрізняти ці стани.
Найвищий пілотаж у діагностиці – співвідношення альбуміну та креатиніну».
? Прокоментуйте, будь ласка, призначення лікаря для корекції АТ.
Я.А. Саєнко: Підтримую обрану тактику. Рекомендації KDIGO (2021) містять поради щодо початку лікування інгібіторами РААС (БРА чи інгібіторами АПФ) пацієнтів з високим АТ, ХХН і суттєво підвищеною альбумінурією (G1-G4, A3) без діабету.
Таким хворим варто рекомендувати досягнення показників АТ 120-130/80 мм рт. ст. за допомогою АГП. Використання, наприклад, валсартану забезпечує позитивний вплив щодо профілактики прогресування ХХН у хворих із предіабетом/ЦД. Продемонстрована відсутність негативного впливу БРА як у монотерапії, так і в комбінації з іншими АГП на показник ШКФ (Burnier M. et al., 2019).
Як уже згадували, валсартан має позитивний, доведений і відчутний вплив на дисбаланс адипонектину та лептину (ФР прогресування ХХН): збільшує рівень адипонектину й зменшує такий лептину.
? Правила призначення інгібіторів АПФ і БРА за ХХН.
Я.А. Саєнко: При зниженні ШКФ <60 мл/хв/1,73 м2 цільова доза для більшості інгібіторів АПФ має бути зменшена на 50%; за ШКФ <30 мл/хв/1,73 м2 – на ¾; при вихідному рівні калію >5,5 ммоль/л не варто призначати інгібітори АПФ.
Титрують дозу під ретельним контролем стану пацієнта, рівнів АТ, креатиніну та калію. Показники креатиніну з розрахунком ШКФ і калію сироватки визначають перед призначенням препарату, згодом - 1 р/7-10 днів (3-5 днів за ШКФ <30 мл/хв/1,73 м2) до досягнення дози, рекомендованої для цього препарату з урахуванням ШКФ.
Діокор Соло рекомендований і не потребує корекції дози при ШКФ >10 мл/хв/1,73 м2.
Діокор 80 мг і Діфорс рекомендовані та не потребують корекції дози за ШКФ >30 мл/хв/1,73 м2.
? Як розрахувати ШКФ?
Я.А. Саєнко: «Зазвичай застосовують формулу CKD-EPI. Як на мене, найпростіший спосіб розрахувати ШКФ – за допомогою смартфону (з використанням спеціальних додатків). Це суттєво економить час, адже процес потребує лише декілька хвилин.
? Чи слід зазначати в діагнозі ХХН її клінічний варіант («гіпертензивна нефропатія», «діабетична нефропатія» тощо)?
Я.А. Саєнко: Можна зазначити, але в більшості пацієнтів спостерігається змішаний ґенез ХХН. Обов’язково слід установити та зазначити в діагнозі стадію ХХН.
? Чи спостерігали ви в клінічній практиці реальне збільшення ШКФ у динаміці лікування? Якщо так, то через який час (орієнтовно) можна на нього очікувати? Чи успіхом є уже те, що показник не знижується?
Я.А. Саєнко: Спостерігаю регрес значення ШКФ досить часто. Звичайно, він не настає через 1-2 тиж лікування. Хорошого й стабільного результату вдається досягти приблизно через півроку за умови адекватного лікування – прийому цукрознижувальних засобів, АГП, статинів.
Клінічний випадок 3
Пацієнт В., 58 років, що має ЦД 2 типу, звернувся до ендокринолога з метою контрольного огляду.
Об’єктивно: пацієнт підвищеного харчування (зріст – 182 см, маса тіла – 100 кг, ІМТ перевищує 30 кг/м2, ОТ – 92 см). Має обмежену фізичну активність, не курить, епізодично вживає алкоголь (1 напій/тиж). Рівень АТ під час огляду – 160/100 мм рт. ст.
Анамнез: протягом 3 років має ЦД 2 типу, приймає метформін (Глюкофаж) у дозі 2000 мг 2 р/день, периндоприл/амлодипін 5/5 мг.
Дані лабораторних обстежень: рівень HbA1c – 6,6%, глюкоза крові натще – 6,0 ммоль/л, загальний ХС – 5,4 ммоль/л, ХС ЛПНЩ – 2,37 ммоль/л, креатинін – 178 мкмоль/л. Клінічний аналіз сечі: щільність – 1014, білок – 1,9 г/л, альбумін – 28 мг/ммоль, еритроцити – 1 в полі зору, лейкоцити – 3 в полі зору; ШКФ – 42 мл/хв/1,73 м2.
Діагноз: ЦД 2 типу. Аліментарно-конституційне ожиріння I ст. АГ, стадія II, ступінь 2, ризик дуже високий. ХНН, стадія 3Б, змішаного ґенезу (діабетична й гіпертензивна).
Рекомендовано: дотримуватися дієти та виконувати фізичні вправи, валсартан/амлодипін 160/10 мг (Діфорс 160) уранці, продовжувати прийом метформіну 1000 мг 2 р/день (з огляду на ШКФ), розувастатин 10 мг (Клівас) увечері.
? Чи правильну тактику обрав лікар-ендокринолог щодо ведення цього хворого?
Д.А. Лашкул: Авторитетні закордонні настанови визначають комбінацію блокаторів РААС і АК як оптимальний стандарт лікування. Таке поєднання допомагає покращити терапевтичну ефективність і нівелювати негативні впливи, притаманні кожному із класів АГП.
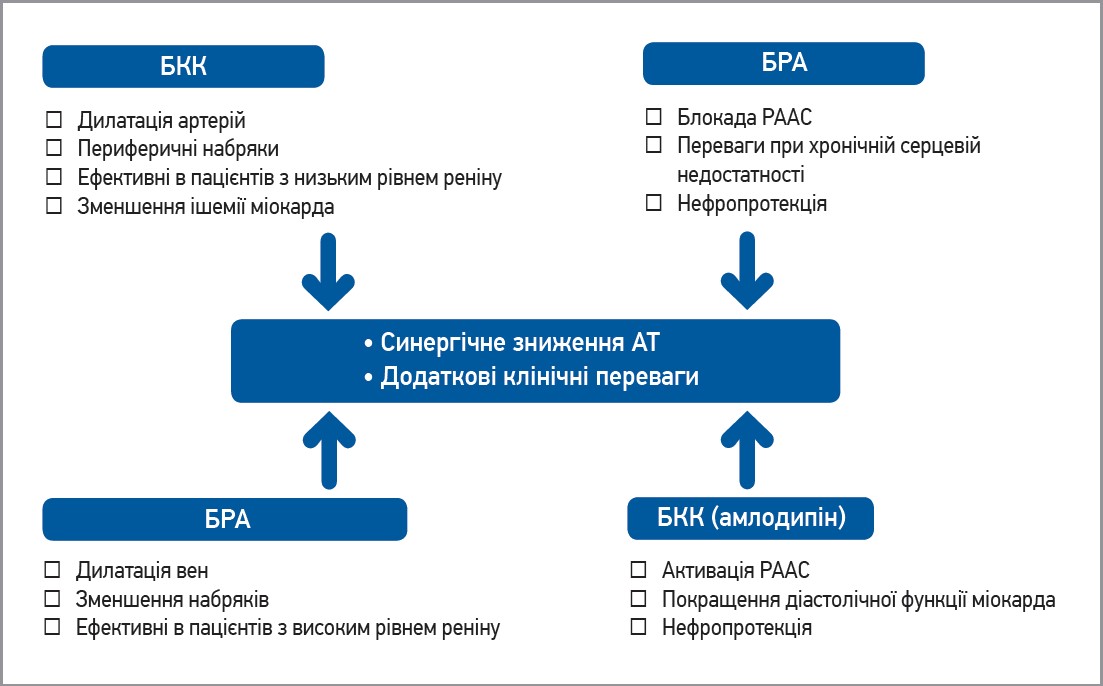
У дослідженнях призначення комбінації валсартану й АК після використання інгібіторів АПФ + АК супроводжувалося додатковим зниженням рівня АТ (рис.).
Рис. Механізми синергічної взаємодії БРА й АК
? Чому периндоприл/амлодипін замінили на валсартан/амлодипін (Діфорс 160)?
Я.А. Саєнко: В описаному клінічному випадку пацієнт спочатку приймав комбінацію периндоприл/амлодипін, однак з огляду на ШКФ 42 мл/хв/1,73 м2, таке призначення замінили на валсартан/амлодипін (Діфорс 160). Комбінація валсартан/амлодипін забезпечує довготривалі переваги щодо нефропротекції порівняно з комбінацією периндоприл/амлодипін.
Довгострокове лікування БРА супроводжується кращими показниками виживання пацієнтів з діабетичною нефропатією, ніж такими на тлі прийому інгібіторів АПФ (Robles N.R. et al., 2009).
Загалом під час обрання терапії раджу керуватися даними авторитетних клінічних досліджень, надавати перевагу якісним препаратам, зокрема засобам швейцарської компанії Acino.
Спікери резюмували, що менеджмент пацієнтів з АГ є досить різноплановим; він має ураховувати стадію, ступінь АГ, супутні стани та ФР. На пильну увагу заслуговують хворі з коморбідністю: предіабетом, ЦД і (особливо!) порушенням функції нирок. Блокатори РААС є АГП першої лінії. БРА, що належать до блокаторів РААС, характеризуються численними перевагами: високою прихильністю пацієнтів до лікування, здатністю запобігати появі ЦД і прогресуванню ХХН. Особливе місце серед представників класу БРА має валсартан завдяки наявності потужної доказової бази та фіксованих комбінацій з гідрохлортіазидом і амлодипіном.
UA-DIOC-PIM-062021-037
Підготувала Олександра Марченко
Медична газета «Здоров’я України 21 сторіччя» № 11-12 (504-505), 2021 р.