23 жовтня, 2021
Соматично обтяжена резистентна депресія: тактика терапії
У квітні в онлайн-форматі відбулася ІІІ науково-практична конференція з міжнародною участю «Психосоматична медицина: наука та практика». Під час лекцій та майстер-класів були розглянуті основні питання щодо напрямів сучасних досліджень у сфері психосоматичної медицини, досягнення і перспективи в Україні. Також було піднято вкрай актуальну тему сьогодення – психосоматичні аспекти пандемії COVID‑19 у різних клінічних галузях медицини, як-от діагностика, терапія, реабілітація. Із доповіддю на тему «Соматично обтяжена резистентна депресія: тактика терапії» виступила д. мед. н., професорка кафедри медичної психології, психосоматичної медицини та психотерапії Національного медичного університету імені О.О. Богомольця (м. Київ) Олена Олександрівна Хаустова.
Депресія як поширене коморбідне захворювання
Депресія – одне з найпоширеніших супутніх захворювань багатьох хронічних соматичних патологій, до яких належать серцево-судинні, метаболічні, запальні та неврологічні (Gold et al., 2020). Депресивні розлади є дуже різноманітними й поділяються за клінічними формами, патерном і початком виникнення, тяжкістю, станом ремісії.
Із точки зору психосоматичної медицини на стресові тригери реагує не тільки нервова система розвитком тривоги, депресії або інсомнії, але й додатково приєднується відповідь імунної системи у формі запалення, інфекції, алергії та болю, а також ендокринної, що проявляється зміною тиреоїдно-адренало-гонадної панелі.
Типові представники другої частини першої хвилі пандемії COVID‑19 – пацієнти соматичного профілю, які вчасно не звертаються по медичну допомогу, що погіршує їхній психічний стан (O’Shea 2020).
У дослідженні S.M. Gold et al. (2020) був виявлений зв’язок між коморбідною депресією та соматичною патологією, посилений двоспрямованим шляхом, що включає такі фактори: поведінкові (незбалансоване харчування, куріння, знижена фізична активність), біологічні (нейроендокринні порушення, запалення), фармакологічні (побічні ефекти антидепресантів [АД], як-то збільшення маси тіла) та вплив середовища.
У період пандемії COVID‑19 актуальність впливу середовища набуває неабиякого значення, результатом чого є утворення так званого circulus vitiosus (замкненого кола). Людина примусово соціально ізолюється, що призводить до самотності та вимушених поведінкових, емоційних і когнітивних змін, таких як неналежне харчування, невміння долати стрес, відчуття покинутості. Вона не може опанувати своє хронічне захворювання, наслідком чого є погіршення пам’яті, брак енергійності, зменшення мотивації до життя та недбалість у лікуванні. Це спричиняє поглиблення хронізації захворювання та депресії, яка знову ж таки збільшує соціальну ізоляцію (Longman et al., 2013).
Відповідь на терапію АД залежить від стану активних молекул, клітин і тканин організму. Початкові молекулярні та клітинні наслідки стресу можуть прогресувати до серйозних структурних модифікацій нейронів і лімбічних ділянок мозку, причетних до перебігу депресії. Послідовні зміни на молекулярному рівні здатні призвести до клітинної дестабілізації та реконструкції. Довгострокові наслідки стрес-індукованих молекулярних та клітинних перебудов зумовлюють морфологічні зміни, що характеризуються дефіцитом функції нейронів та «підключення» до нейронної мережі. Терапевтичний ефект типового лікування АД спрямований на зменшення негативних наслідків стресу на молекулярно-клітинно-морфологічному/тканинному рівнях (Duric, Duman, 2012).
Важливість контролю лабораторно-інструментальних показників
У рутинній практиці психіатра вкрай важливим є контроль лабораторно-інструментальних показників пацієнта.
Маркери позитивної динаміки лікування депресії:
- Клінічні: коротка тривалість нелікованої хвороби; рання реакція на лікування.
- Нейровізуалізація: висока основна активність у корі переднього відростка за даними магнітно-резонансної томографії (МРТ), електроенцефалографії, позитронно-емісійна томографія (ПЕТ).
- Біохімічне дослідження крові: збільшення вмісту нейротропного фактора мозку в плазмі крові у відповідь на лікування; зниження рівня інтерлейкіну‑6 під час терапії.
Маркери негативної динаміки лікування депресії:
- Клінічні: низький рівень функціонування до розвитку захворювання; психіатрична коморбідність – тривога, посттравматичний стресовий, обсесивно-компульсивний розлади, кумулятивність; стресові життєві події; жорстоке поводження з дітьми; терапевтична резистентність.
- Нейровізуалізація: мікрогліальна активація (за даними ПЕТ); низький базовий об’єм гіпокампа (за даними МРТ).
- Біохімічне дослідження крові: високий рівень фактора некрозу пухлини α після лікування; високий базовий вміст С-реактивного білка.
Важливими умовами, що впливають на одужання пацієнта, є загальна тяжкість хвороби, психосоціальні й біологічні провокувальні фактори, загальні та специфічні етіологічні чинники (пошкодження мозку, соматотропне лікування), а також особливості попередньої терапії АД (порушення режиму лікування, соматичні побічні ефекти).
Терапія депресії
Препаратами першої лінії лікування пацієнтів із депресією є селективні інгібітори зворотного захоплення серотоніну (СІЗЗС). У разі їх неефективності слід перейти на подвійні антидепресанти або комбіновані стратегії, якщо ж депресія резистентна – надати перевагу стимуляції мозку електросудомною терапією (Kessler et al., 2005; Herrmann, 1995).
Есциталопрам є активною речовиною препарату Ессобел (компанії «Нобель Ілач») та типовим засобом першої лінії для лікування великого депресивного розладу. Ессобел – це алостеричний інгібітор зворотного захоплення серотоніну, який має дві головні переваги перед іншими представниками групи СІЗЗС: збільшує синаптичну концентрацію серотоніну та стимулює серотонінергічні ефекти у ЦНС. Він чинить виразну дію на три компоненти депресивного стану: тимічний, тривожний та апатодинамічний. Ессобел ефективний при лікуванні тужливих, тривожних і анергетичних депресій.
Лікування депресії з супутніми станами
Що стосується вибору методів лікування депресії у пацієнтів із коморбідними станами, препарати для терапії першої лінії включають:
- хронічний біль – трициклічні антидепресанти (ТЦА), інгібітори зворотного захоплення серотоніну й норадреналіну (ІЗЗСН) (дулоксетин);
- деменція, постінсультні стани – циталопрам, есциталопрам, сертралін;
- цукровий діабет – флуоксетин, циталопрам, есциталопрам, сертралін, пароксетин;
- глаукома – есциталопрам, флуоксетин, циталопрам, сертралін, бупропіон.
Ниркова та печінкова недостатність
При нирковій недостатності слід надавати перевагу агомелатину, моклобеміду, ТЦА, тразодону, вортіоксетину. Помірний ризик побічних подій відзначено за приймання СІЗЗС, міртазапіну, дулоксетину.
Не рекомендовано застосовувати сертралін (через ризик виникнення серотонінового синдрому при діалізі), флуоксетин (слід призначати обережно при виразній нирковій недостатності), венлафаксин (варто зменшити дозу на 25‑50% при легкому та помірному порушенні функції нирок, якщо кліренс креатиніну <30 мл/хв – на 50%).
При печінковій недостатності препаратами вибору є пароксетин і вортіоксетин. Помірний ризик побічних реакцій пов’язаний із терапією СІЗЗС та ТЦА (найчастіше), міртазапіном, дулоксетином, моклобемідом, тразодоном, венлафаксином. Не рекомендовано застосовувати агомелатин (необхідний моніторинг функціонування печінки до початку та на 3, 6, 12, 24-му тижнях лікування; збільшуючи дозу, слід проводити тести з тією ж частотою, що й на початку терапії) та інгібітори моноаміносидази (іМАО) через гепатотоксичні властивості, які можуть прискорити розвиток коми.
За наявності епілепсії в анамнезі протипоказаний бупропіон, перевагу слід надавати агомелатину, моклобеміду, іМАО, СІЗЗС (есциталопраму).
Серцево-судинні захворювання
Не рекомендовано призначати іМАО та ТЦА пацієнтам кардіологічного профілю: з ішемічною хворобою серця (ІХС), дефектами провідності, застійною серцевою недостатністю (СН) та літнім особам; протипоказані вони хворим після інфаркту міокарда (ІМ). Препаратами вибору є агомелатин, міртазапін, дулоксетин, тразодон, вортіоксетин та СІЗЗС.
СІЗЗС. Сертралін є засобом вибору в пацієнтів після ІМ, проте одночасне приймання з аспірином та іншими антикоагулянтами може збільшити ймовірність кровотеч, особливо в осіб похилого віку. Циталопрам слід застосовувати з обережністю особам із високим ризиком пролонгації інтервалу QTc або тахікардії типу «пірует», які нещодавно перенесли ІМ.
ІЗЗСН. Слід уникати призначення венлафаксину хворим із високим ризиком розвитку злоякісної шлуночкової аритмії або неконтрольованою гіпертензією.
Інші антидепресанти. При застосуванні бупропріону пацієнтам з ІХС слід відмовитися від куріння через швидку зміну концентрації препарату за наявності нікотину.
Варто з обережністю призначати міртазапін особам з ІХС та після ІМ, тразодон – за наявності в анамнезі ІХС, атріовентрикулярної блокади або інших порушень провідності у хворих після ІМ.
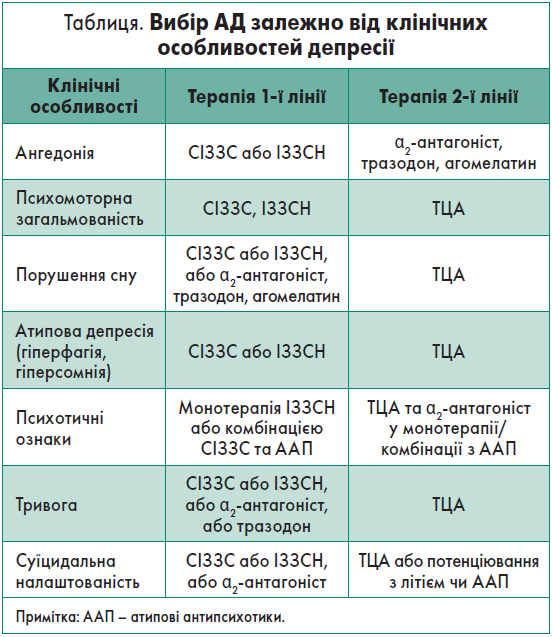
У таблиці наведено дані щодо вибору АД залежно від клінічних особливостей депресії.
Резистентна депресія у похилому віці
Серед дорослих віком від 55 років поширеність великого депресивного розладу загалом становить близько 2% у світі; 10‑20% всіх осіб похилого віку страждають на клінічно значущий депресивний синдром. Поширеність вища серед пацієнтів у лікарнях та будинках престарілих віком від 85 років.
Нелікована депресія може призвести до різних негативних наслідків, таких як функціональні порушення, підвищений ризик нейрокогнітивних розладів, зростання захворюваності та смертності, вживання заборонених речовин / алкоголю, частоти госпіталізацій, рівня самогубств. Особливістю перебігу депресії в осіб похилого віку є те, що вони часто не реагують на фармакотерапію першого ряду і потребують переведення на інший засіб або посилення лікування (Liu et al., 2020).
Для аугментації у таких пацієнтів слід застосовувати терапію третьої лінії, яка включає приєднання додаткового препарату, як-то:
- нормотимік – карбонат літію;
- атиповий нейролептик – арипіпразол у дозі 2‑15 мг, оланзапін по 2,5‑10 мг, кветіапін у дозі 150‑300 мг.
На противагу кветіапіну та оланзапіну, ефективним при тривозі та ажитації, арипіпразол застосовують при резистентних депресіях, що мають меланхолійний ефект. На вітчизняному ринку арипіпразол представлений препаратом Абізол (компанії «Нобель Ілач») у дозуванні 5 і 10 мг. Оскільки початкова доза арипіпразолу при лікуванні резистентної депресії становить 2,0‑2,5 мг, таке дозування препарату є досить зручним для застосування пацієнтом.
Таким чином, стратегії, які існують нині, дозволяють пацієнтам успішно долати депресію. Люди, які з цим впоралися, стають сильнішими, адже ця боротьба може бути каталізатором виживання та подолання соматичних захворювань.
Підготував Денис Соколовський
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 3 (58) 2021 р.