13 грудня, 2021
Нові перспективи хірургічного і терапевтичного лікування пацієнтів із пухлинами голови та шиї в Україні
 25-26 листопада відбулася науково-практична конференція з міжнародною участю «Пухлини голови та шиї – нові перспективи хірургічного і терапевтичного лікування хворих в Україні». Про які перспективи йшлося, ми поговорили з організатором заходу, експертом МОЗ України за спеціальністю «Онкологія», завідувачем кафедри онкології ДЗ «Запорізька медична академія післядипломної освіти МОЗ України», доктором медичних наук, професором Олексієм Олексійовичем Ковальовим.
25-26 листопада відбулася науково-практична конференція з міжнародною участю «Пухлини голови та шиї – нові перспективи хірургічного і терапевтичного лікування хворих в Україні». Про які перспективи йшлося, ми поговорили з організатором заходу, експертом МОЗ України за спеціальністю «Онкологія», завідувачем кафедри онкології ДЗ «Запорізька медична академія післядипломної освіти МОЗ України», доктором медичних наук, професором Олексієм Олексійовичем Ковальовим.
? Шановний Олексію Олексійовичу, злоякісні пухлини голови та шиї є однією з найскладніших проблем сучасної онкології. Яких успіхів у лікуванні хворих досягнуто сьогодні і чого нам очікувати у найближчому майбутньому?
– Пухлини голови та шиї – це справжня «проблема у проблемі». Про існування таких пухлин було відомо у давнину. Археологи виявили докази саркоми лицевих кісток у неандертальців, раку шкіри у єгипетських і неаполітанських мумій, назофарингеальної карциноми – у арагонських мумій (рис. 1-2).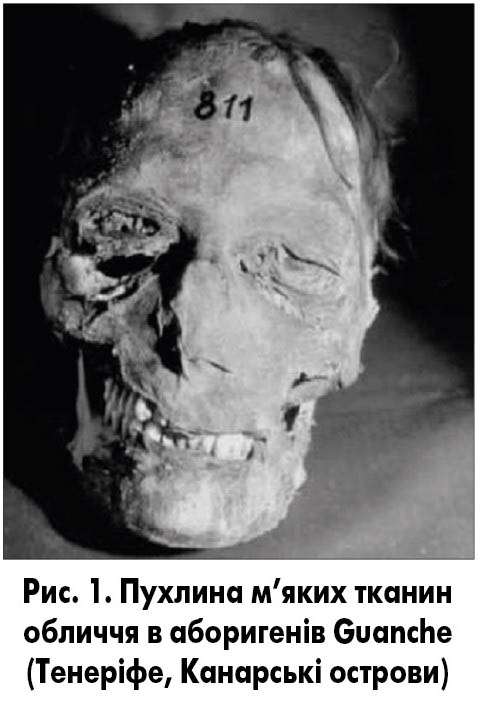
Сьогодні частота раку голови та шиї досить висока, проте вона дуже відрізняється в різних географічних регіонах світу. Це залежить від переважання певних етіологічних факторів, поведінки людей, їх звичок, які можуть відрізнятися залежно від країни і континенту.
Пухлини голови та шиї – збірний термін, що включає кілька різних типів раку. 10% таких пухлин можуть розвиватися з лімфоцитів, клітин сполучної тканини або слинної залози, проте найчастішою формою (90%) є плоскоклітинна карцинома. Гістологічно вона може різнитися – від добре диференційованої зроговілої до недиференційованої незроговілої. Поняття «пухлини голови та шиї» охоплює плоскоклітинний рак губи, слизової оболонки щік, твердого піднебіння, передньої частини язика, дна ротової порожнини, ретромолярного трикутника, ротоглотки (корінь язика, м’яке піднебіння, мигдалики), задньої стінки глотки, гортані, надгортанника, голосової щілини, під’язикового м’яза, носової порожнини та приносових пазух.
? Чому у різних країнах захворюваність на плоскоклітинний рак голови та шиї відрізняється?
– Це залежить від етіологічних чинників. Сьогодні головними причинами розвитку плоскоклітинної карциноми ротової порожнини є вплив тютюнового диму та міцних алкогольних напоїв, у яких містяться основні канцерогени людської цивілізації. Справді, цигарка, якщо нею правильно користуватися, вбиває. При вдиханні тютюнового диму в організм людини потрапляє не лише нікотин. У ньому містяться ацетальдегід, поліциклічні ароматичні вуглеводні, нітрозометиламін, миш’як, тар, ізопрен, ацетон, кадмій, ціаніди, аміак, нітрометан, солі важких металів, а також полоній-210 – всі доведені класичні канцерогени, що спричиняють рак ротової порожнини, легені та злоякісні пухлини інших локалізацій.
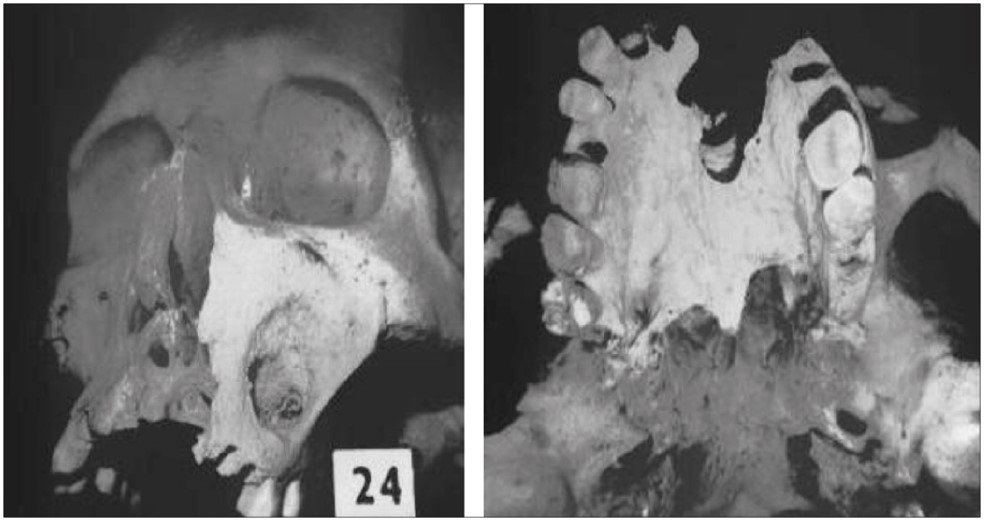 Рис. 2. Назофарингеальна карцинома в арагонської мумії XIV ст.
Рис. 2. Назофарингеальна карцинома в арагонської мумії XIV ст.
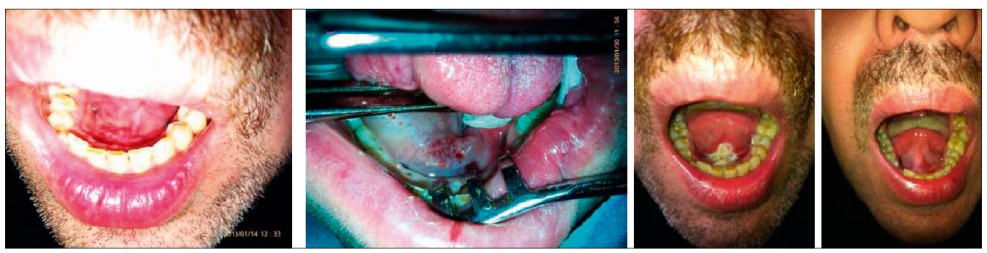
Екзотичною формою злоякісної пухлини ротової порожнини, пов’язаної з курінням тютюну та жуванням бетелю, яку виявляють переважно у населення північних районів Індії, є рак чутта. Чутта – це саморобна сигара, виготовлена з особливого сорту місцевого тютюну, дим якого містить велику кількість нікотину, алкалоїдів і твердих часток. Чутту курять в оберненому вигляді, утримуючи її палаючий кінець у роті, внаслідок чого у курців швидко розвивається рак піднебіння (рис. 3). Обернене куріння поширене також у Панамі у праль, які під час прання білизни тримають вогник цигарки в роті, щоб він не погас через розбризкування води.
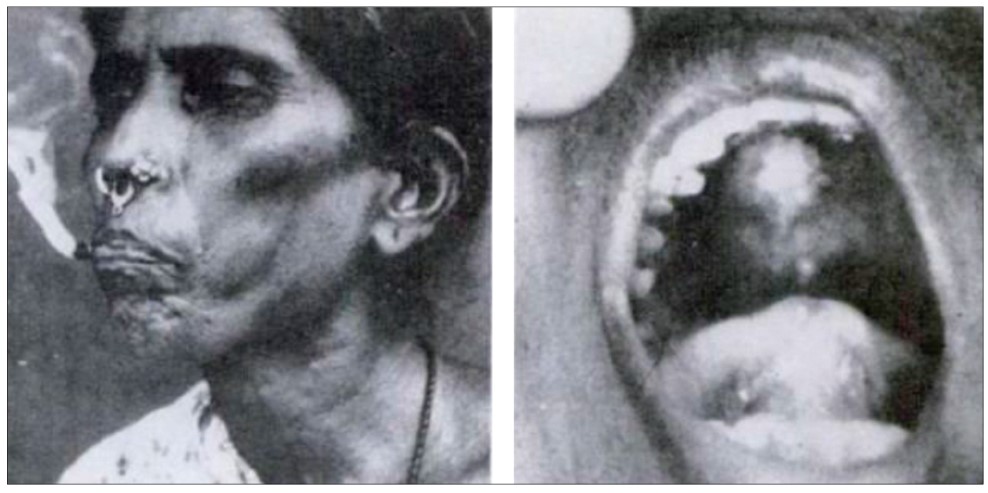 Рис. 3. Обернене куріння і рак чутта у мешканців північних районів Індії
Рис. 3. Обернене куріння і рак чутта у мешканців північних районів Індії
Це приклади впливу звичок і способу життя людей, які проживають у країнах «тютюнового поясу», що впливають на частоту захворюваності на рак голови та шиї. Проте ризик формування плоскоклітинної карциноми значно підвищений і в північних країнах так званого горілчаного поясу, де населення споживає міцні алкогольні напої.
Ще на початку XX ст. було встановлено, що у людей, які беруть участь у виробництві дистильованих напоїв і мають до них вільний доступ, частіше розвивалися злоякісні пухлини голови та шиї порівняно з тими, хто з релігійних чи інших причин повністю утримувався від вживання алкоголю.
Алкольні напої – це багатокомпонентні суміші, які можуть містити кілька канцерогенних сполук, що одночасно підвищують ризик розвитку раку, – етанол, ацетальдегід, альфа-токсини, етилкарбамат, нітрозоаміни, сивушні олії, поліциклічні вуглеводні фенантрен, бензантрацен, бензопірен, хризен і навіть волокна азбесту, які використовують для злужнення та фільтрації вина, пива й джину. Люди з тяжкою алкогольною залежністю, до категорії яких належать також особи з карциномою ротової порожнини, нерідко вживають сурогатний алкоголь (лак для волосся, засоби після гоління, рідину для запальничок, спиртові розчини для полоскання рота), що містять не тільки дуже високу концентрацію етанолу, а й вищі спирти, токсичні концентрації метанолу та інші хімічні отрути.
Протягом кількох десятиліть проводилися дослідження щодо вивчення впливу домашнього та промислового алкоголю на ризик розвитку різних неоплазій. У 1988 р. Міжнародне агентство з дослідження раку оголосило алкоголь доведеним канцерогеном для людини групи 1, таким самим як миш’як, бензол та азбест. У доповіді експертів Всесвітньої організації охорони здоров’я зазначено, що у 2010 р. майже 340 000 випадків смерті та 9000 втрачених років життя зумовлені раком, асоційованим із надмірним вживанням алкогольних напоїв. Найвища частота раку голови та шиї, пов’язаного з вживанням алкоголю, спостерігається у країнах Східної Європи, найнижча – у Північній Африці та на Близькому Сході. Сьогодні більше половини населення країн Східної Європи не знає, що алкоголь є канцерогеном і що навіть легке та помірне його споживання підвищує ризик розвитку раку. Дані Всесвітньої організації охорони здоров’я про те, що у 2011 р. у Європі кожен десятий випадок раку у чоловіків та один із тридцяти випадків у жінок був викликаний вживанням алкоголю, залишаються невідомими як для населення, так і для медичної громадськості.
Особливу роль відіграє той факт, що спирт діє як розчинник і полегшує проникнення канцерогенів тютюну через клітинні мембрани. Це означає, що люди, які п’ють алкогольні напої та курять, зазнають набагато вищого (приблизно в 35 разів) ризику розвитку раку ротової порожнини, трахеї та стравоходу.
Крім тютюнового диму та алкоголю у розвитку плоскоклітинної карциноми певну роль відіграють іонізуюче й неіонізуюче випромінювання. Достатньо згадати «радієвих дівчат» початку минулого століття, які змочували власною слиною пензлики для розфарбовування радіоактивними фарбами циферблатів годинників, що світяться, після чого у них розвивалися злоякісні пухлини ротової порожнини і щелеп.
Надмірне ультрафіолетове випромінювання є причиною раку губи. Ця проблема особливо актуальна для Австралії, де сонячна активність висока протягом усього року.
? Чи наявні ще якісь фактори ризику розвитку плоскоклітинного раку голови та шиї крім тютюнового диму, алкогольних напоїв та ультрафіолетового випромінювання?
– Численною групою таких факторів ризику є віруси людського раку. Вони з’явилися на Землі близько 50 тис. років тому, а пізніше, з епохи палеоліту та верхнього неоліту, почали заражати людей. Очевидно, саме це пояснює існування назофарингеальних карцином у наших далеких предків, виявлених палеопатологами в єгипетських і неаполітанських мумій.
Сьогодні відомо про існування восьми онкогенних вірусів, які Міжнародне агентство з дослідження раку визначає як доведені для людини канцерогени групи 1А. До вірусів, асоційованих із плоскоклітинною карциномою голови та шиї, належать п’ять видів: вірус папіломи людини (ВПЛ), вірус Епштейна – Барр (ВЕБ), вірус гепатиту В (ВГВ), вірус гепатиту С (ВГС) і вірус карциноми клітин Меркеля (рис. 4). Роль цих патогенів у канцерогенезі настільки важлива, що сьогодні робляться спроби створити молекулярну класифікацію раку голови та шиї, а також розробити терапевтичні стратегії індивідуалізованого лікування хворих залежно від наявності тієї чи іншої інфекції.
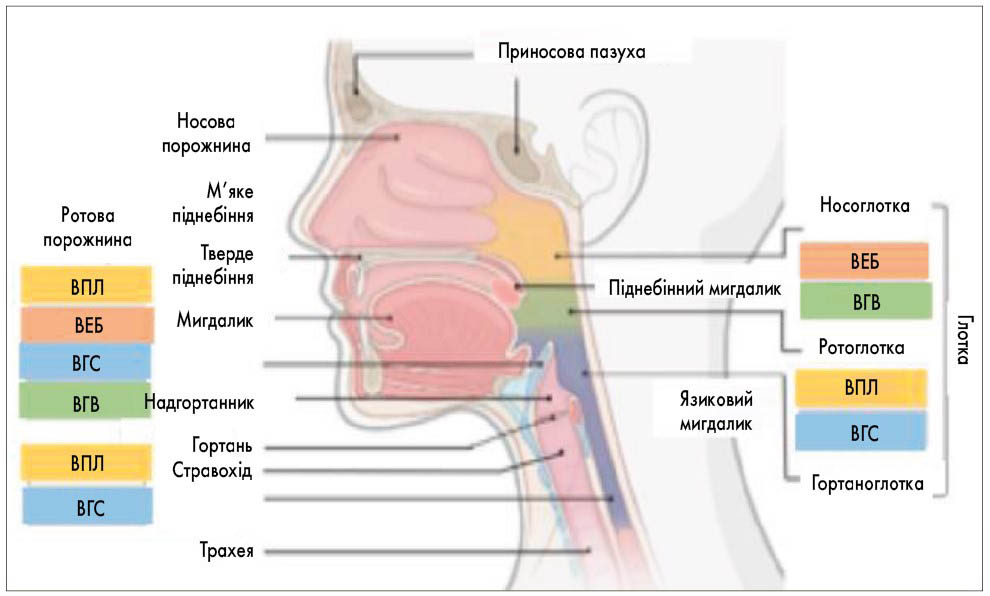 Рис. 4. Онкогенні віруси, асоційовані з плоскоклітинним раком голови та шиї різних локалізацій (за L. Mahmutovic, E. Bilajac, A. Hromic-Jahjefendic, 2021)
Рис. 4. Онкогенні віруси, асоційовані з плоскоклітинним раком голови та шиї різних локалізацій (за L. Mahmutovic, E. Bilajac, A. Hromic-Jahjefendic, 2021)
Те, що вірус папіломи людини відповідає за розвиток плоскоклітинного раку шийки матки, довів німецький вірусолог Харольд цур Хаузен, який за дослідження в цій галузі у 2008 р. став лауреатом Нобелівської премії.
На початку 1980-х рр. фінський учений Карі Сюр’янен показав, що механізм розвитку плоскоклітинної карциноми мигдалика, ротоглотки та гортані дуже нагадує канцерогенез цервікальної карциноми. Сьогодні відомо, що більш ніж у 70% випадків рак голови та шиї зумовлений ВПЛ, а у 90% хворих виявляють найбільш агресивний штам ВПЛ – 16. У чоловіків ВПЛ-позитивний (ВПЛ+) рак розвивається частіше, ніж у жінок.
На молекулярному рівні ВПЛ+ та ВПЛ-негативний (ВПЛ-) рак голови та шиї значно відрізняються. Так, для ВПЛ+ раку характерна надекспресія p16 і не характерні мутації TP53 і TP16, для ВПЛ- характерна експресія p53, bcl-2 та EGFR. Залишається не зрозумілим, чому у близьких анатомічних ділянках ротової порожнини, ротоглотки, гортані, приносових пазух поширеність ВПЛ-інфекції різна. Так, практично всі випадки раку мигдалика пов’язані з ВПЛ, при раку ротоглотки частота цієї інфекції нижча, а при раку ротової порожнини та гортані ще нижча.
Прогноз та виживаність при вірусасоційованому раку кращі (62 проти 26%).
Було зроблено висновок, що тестування на ВПЛ-інфекцію необхідно проводити всім пацієнтам з діагностованим раком ротоглотки, а в майбутньому, можливо, доведеться розглядати два типи раку окремо з наукового, діагностичного, епідеміологічного та клінічного погляду.
Серйозна проблема полягає в тому, що немає єдиної думки, як ідентифікувати рак, спричинений ВПЛ. У різних дослідженнях його частота значно варіює – від 0% при карциномі ротової порожнини та гортані до 93% при карциномі ротоглотки.
ДНК вірусу виявлено слині та злущених клітинах ротової порожнини, проте це має більше значення для проведення скринінгу раку голови та шиї у групах високого ризику, ніж для виявлення вірусних часток у самій пухлині. Ризик розвитку вторинного раку ротоглотки підвищений у пацієнтів, які отримували променеву терапію з приводу раку шийки матки. Можливими причинами можуть бути статева поведінка, горизонтальна передача вірусу з рота до рота зі слиною, генетична або імунологічна схильність до онкогенних ефектів вірусу. До групи підвищеного ризику розвитку раку мигдалика і язика потрапляють чоловіки жінок з інвазивним раком шийки матки і карциномою in situ. Можливо, при позитивному результаті скринінгового ВПЛ-тесту у жінки дослідження необхідно проводити і її партнеру.
Вірус Епштейна – Барр (вірус герпесу людини 4 типу) є одним із найпоширеніших вірусів у людській популяції. Він інфікує приблизно 90-95% дорослих у всьому світі. ВЕБ здатний проявляти подвійний тропізм та інфікувати В-лімфоцити й епітеліальні клітини, відповідаючи тим самим приблизно за 1% всіх видів пухлин – лімфому Беркітта, дифузну великоклітинну лімфому, лімфому Ходжкіна, карциному шлунка. Ця інфекція наявна у 100% хворих на незроговілу анапластичну карциному носоглотки. ДНК вірусу можна виявити в плазмі крові хворого, хоча для якісного та кількісного визначення можуть бути використані зразки тканин, отримані за допомогою щітки та мазка.
На сьогодні не схвалено жодного лікарського препарату проти ВЕБ-асоційованої карциноми. Оскільки у відповідь на цю інфекцію розвивається лише клітинний імунітет і антитіла до ВЕБ не виробляються, профілактичні вакцини, подібні до Гардасил або Церварікс, створити не вдається. Головною перспективою, яка зможе радикально змінити парадигму лікування цих хворих, є не профілактичні, а терапевтичні анти-ВЕБ вакцини. Важливо, що вони підвищують CD8+ та CD4+ Т-клітинну відповідь та виключають будь-який зв’язок із варіаціями людського лейкоцитарного антигену (HLA) або відмінностями у штамах ВЕБ.
Повідомляється, що вакцини добре переносяться і мають обмежену токсичність. Їх можна виробляти серійно за невисокою вартістю. Результати їх застосування стабільні та відтворювані. Для впровадження у клінічну практику потрібно мінімум навченого персоналу й обладнання. Сьогодні застосування терапевтичних анти-ВЕБ вакцин вивчають у пацієнтів різного етнічного походження.
Вірус гепатиту B, який уражає понад 300 млн людей у всьому світі і щорічно є причиною смерті більше 1 млн осіб, має подвійний тропізм: він здатний заражати як гепатоцити, так і B-клітини, реплікуватись у лімфоцитах і мононуклеарах периферичної крові. ВГВ є канцерогенним патогеном і асоціюється з гепатоцелюлярною карциномою, раком підшлункової залози, а також неходжкінською лімфомою. Інфікування ВГВ може бути непрямим фактором ризику розвитку раку голови та шиї. Припускають, що канцерогенез залежить від взаємодії вірусів гепатиту та Епштейна – Барр.
Вірус гепатиту С передається між людьми винятково через прямі контакти. Цей вірус має потрійний тропізм і може інфікувати В-лімфоцити, гепатоцити та клітини слинних залоз. Крім гепатоцелюлярної карциноми ВГС асоційований із карциномами, які пов’язані з курінням і вживанням алкогольних напоїв, – раком підшлункової залози, легені та нирки, а також з неходжкінською лімфомою. Позапечінковим проявом хронічної інфекції ВГС є червоний плоский лишай ротової порожнини – передракова форма плоскоклітинної карциноми.
Загальна поширеність ВГС у пацієнтів з діагнозом рак голови та шиї коливається від 7,8 до 12,8%. Найвища асоціація наявна у пацієнтів віком 40-50 років. Доведено зв’язок ВГС із ВПЛ при раку ротоглотки та фарингеальному раку (крім раку носоглотки). Факторами ризику є поєднання інфекції з курінням, вживанням алкогольних напоїв і наркотиків, гастроезофагеальним рефлюксом та професійними контактами з азбестом. Враховуючи високу поширеність гепатиту С у світі, слід заохочувати гепатологів до додаткового спостереження за пацієнтами з відомими хронічними вірусними інфекціями, що могло б допомогти у ранній діагностиці раку голови та шиї. Після проведення доступної сьогодні противірусної терапії ризик розвитку плоскоклітинної карциноми ротової порожнини знижується на 35%.
Поліомавіруси є частиною природної мікрофлори людини і присутні в клітинах здорової шкіри. Вони стають онкогенними на тлі природного та набутого імунодефіциту. 97% карцином клітин Меркеля (первинна пухлина та метастази) містять поліомавірус HPyV5. Він також асоційований із хронічним лімфолейкозом, неходжкінською лімфомою, раком слинних залоз і немеланомним епітеліальним раком шкіри. Поліомавірус клітин Меркеля (MCPyV) є етіологічним фактором плоскоклітинної карциноми голови та шиї й у 16-36% випадків зустрічається при III стадії раку глотки, язика та мигдалика.
? Які досягнення та тенденції сучасного хірургічного лікування пухлин голови та шиї?
– За останні два десятиліття підходи до хірургічного лікування раку кардинально змінилися. Цьому сприяли досягнення технічної революції, завдяки якій з’явилися унікальні технології – 3D, комп’ютерне моделювання та використання роботів.
Операції на органах голови та шиї виконуються у дуже складній анатомічній зоні. Для видалення пухлини хірурги поки що використовують традиційні відкриті операції, які вимагають великого розрізу тканин обличчя від нижньої губи до вуха та середини шиї. Щоб дістатися до задньої частини ротової порожнини та горла, необхідно розтинати нижню щелепу. Крім високої смертності та тяжких ускладнень, у хворих розвиваються функціональні порушення мовлення та ковтання, які супроводжуються неприйнятними косметичними дефектами.
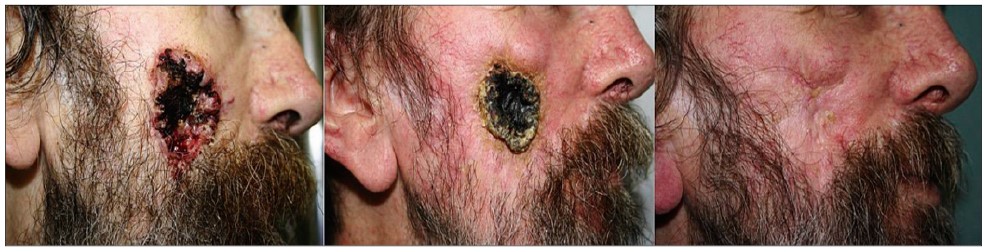
Ми давно використовуємо можливості мініінвазивних хірургічних втручань (радіочастотна термоабляція, фотодинамічна терапія – рис. 5, електрохімічний лізис) для лікування плоскоклітинного раку губи, ротової порожнини та язика.
Рис. 5. Успішне лікування хворого із плоскоклітинною карциномою ротової порожнини методом фотодинамічної терапії (А.М. Рябошапка, кафедра онкології ДЗ «Запорізька медична академія післядипломної освіти МОЗ України»)
Останні технологічні досягнення, у тому числі мініінвазивна ендоскопічна лазерна мікрохірургія та роботизована хірургія, здійснили революцію в галузі лікування хворих на плоскоклітинну карциному голови та шиї.
Трансоральна роботизована хірургія за допомогою системи да Вінчі (TORS), розроблена для лікування пухлин ротоглотки, була вперше застосована у 2007 р. Сьогодні понад 50 установ у 20 країнах світу використовують цю технологію, і напрям швидко розвивається. Переваги TORS очевидні (рис. 6). Вона дозволяє зменшити тривалість і травматизм операції, скоротити час анестезії та перебування у лікарні, уникнути крововтрати, знизити до мінімуму інтенсивність післяопераційного болю, ризик ранової інфекції, усунути необхідність накладання трахеостоми та гастростоми, запобігти косметичним деформаціям. У пацієнтів, яких лікували за допомогою TORS, немає необхідності використовувати назогастральний зонд для ентерального харчування, оскільки вони рано починають вживати їжу перорально. Функція ковтання у всіх оперованих відновлюється до 6-го тижня, лише 1% пацієнтів протягом цього часу не повертається до нормальної дієти. Після трансоральних радикальних операцій при ВПЛ+ плоскоклітинній карциномі голови та шиї прогноз хороший, часто немає потреби призначати ад’ювантну хіміопроменеву терапію.
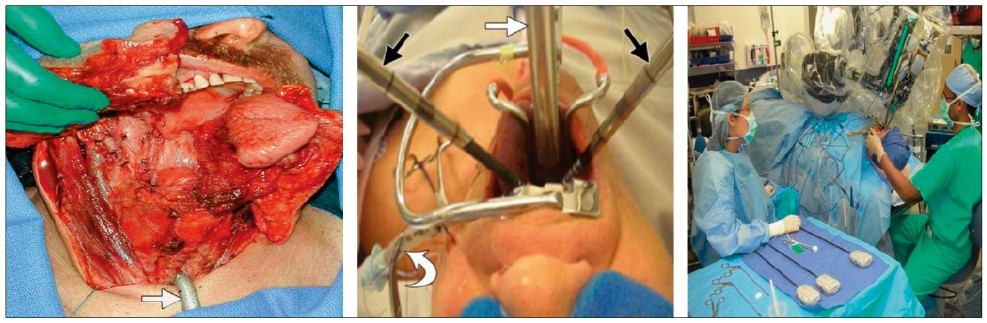 Рис. 6. Класична і трансоральна роботасистована хірургія орофарингеальної зони (за L.A. Loevner et al., 2013; R.M. Satava, 2003)
Рис. 6. Класична і трансоральна роботасистована хірургія орофарингеальної зони (за L.A. Loevner et al., 2013; R.M. Satava, 2003)
Інноваційні досягнення в хірургії раку голови та шиї сприяли створенню нових протоколів лікування хворих, і ймовірно, що в найближче десятиліття парадигма терапії цього захворювання повністю зміниться.
У всьому світі роботизована трансоральна хірургія стала повсякденною практикою, хоча ще 10 років тому її застосовували лише кілька добре підготовлених хірургів. Не виключено, що із швидким розвитком технологій та інформатики у найближчому майбутньому ці операції можуть виконуватися віддалено через кіберпростір. Цей напрям стрімко розвивається. Дуже важливо, щоб Україна на цьому шляху не відстала від технологічного прогресу.
? Розкажіть, будь ласка, про особливості медикаментозної терапії цієї групи пацієнтів. Чи є досягнення у сфері терапевтичного лікування хворих на плоскоклітинну карциному голови та шиї?
– Лікування пацієнтів з місцево-поширеною та метастатичною формою плоскоклітинного раку голови та шиї є складним завданням. Усі хворі цієї групи потребують корекції анемії, нутритивної підтримки й активної аналгетичної терапії, оскільки інтенсивність больового синдрому у них може сягати 9-10 балів за візуальною аналоговою шкалою. Проблема клінічного харчування частково може бути вирішена за допомогою сипінгів або за необхідності – ентерального зондового годування. Проблему резистентного болю у таких хворих ми успішно долаємо за допомогою радіочастотної термоабляції гілок трійчастого нерва (рис. 7) – ефективного методу, який, на відміну від хімічних блокад, можна використовувати одноразово. 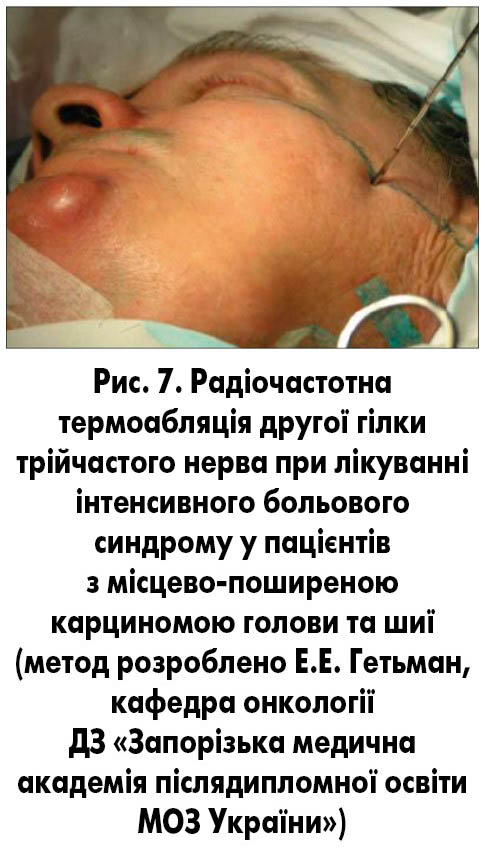
Під час хіміотерапії або поєднання променевої терапії з анти-EGFR моноклональним антитілом цетуксимабом (єдиний таргетний препарат, рекомендований для цієї групи хворих) у більшості пацієнтів неминуче виникають ускладнення у вигляді мукозиту й ураження шкіри (рис. 8). Гострі токсичні ефекти зберігаються протягом тривалого часу, хоча статистику цих ускладнень нерідко занижують чи недооцінюють.
Метааналіз результатів лікування 230 пацієнтів із раком голови та шиї дозволив встановити, що наслідки токсичності зберігаються більш ніж 180 днів після завершення лікування. 43% хворих, які ще зазнають у цей час токсичність 3 ступеня або вище, через дисфункцію гортані продовжують харчуватися через гастростому. Найвищий ризик тривалої токсичності у літніх пацієнтів з вищою стадією Т і локалізацією раку в гортані або глотці.
Слід зазначити, що навіть при використанні променевої терапії з модульованою інтенсивністю (IMRT), що дозволяє не пошкоджувати опроміненням привушні слинні залози, у третини пацієнтів все одно розвивається ксеростомія 2 ступеня та вище. Такі ускладнення, як порушення ковтання та сухість у роті, під час терапії ігнорувати не можна. Багато фахівців слушно вважають, що функціональний результат лікування та відсутність токсичності мають не менше значення, ніж досягнення терапевтичного ефекту.
Перспективним напрямом лікування пацієнтів з місцево-поширеним і метастатичним раком голови та шиї, що дає змогу уникнути неприйнятної токсичності та досягти хороших клінічних результатів, є імунотерапія анти-PD-L1 антитілами. На підставі аналізу результатів дослідження Keynote-048 Управління з контролю якості харчових продуктів і лікарських препаратів США зареєструвало пембролізумаб у монорежимі, а також у комбінації з хіміопрепаратами (цисплатином і 5-фторурацилом) у 1-й та 2-й лініях терапії. Це абсолютно новий та обнадійливий підхід у лікуванні плоскоклітинної карциноми голови та шиї.
? На минулій конференції великий інтерес учасників викликала доповідь учених зі Стокгольма про електрохіміотерапію. Ця технологія поки маловідома для українських онкологів, оскільки була недоступна. Розкажіть, будь ласка, на чому ґрунтується ефект цього методу впливу на пухлину та які перспективи його використання в Україні.
– Електрохіміотерапія, або електропорація, – це порівняно новий метод локальної абляції, який поєднує внутрішньовенне введення цитостатиків (наприклад, цисплатину або блеоміцину) із впливом на клітини пухлини постійного струму з короткими та інтенсивними імпульсами (8 імпульсів тривалістю 100 мікросекунд). Електричне поле у тканинах створюється за допомогою спеціального приладу (генератора) й електродів, які пункційно імплантують у пухлину. Залежно від глибини її розташування (поверхнева чи вісцеральна) електроди можуть мати різну форму та довжину (рис. 9).
Ще у 1960-х рр. було відомо, що під впливом зовнішнього електричного поля в клітинних мембранах з’являються тимчасові отвори – мікроперфорації, які можна використовувати для електроперенесення різних ліків та молекул усередину клітин. Таким чином, в електрохіміотерапії одночасно використовуються два способи протипухлинного впливу – фізичний і хімічний. На відміну від радіочастотної, мікрохвильової або лазерної абляції, при яких тканини руйнуються в результаті дії високих температур з утворенням зони коагуляційного некрозу, метод електропорації не пов’язаний із термічним впливом, є безпечнішим і його можна використовувати в різних клінічних ситуаціях, у тому числі при лікуванні раку язика та слизової оболонки ротової порожнини.
 Рис. 9. Прилад для електрохіміотерапії (електропорації) IQWaveTM компанії Scandinavian ChemoTech AB уже цього року буде доступний в Україні
Рис. 9. Прилад для електрохіміотерапії (електропорації) IQWaveTM компанії Scandinavian ChemoTech AB уже цього року буде доступний в Україні
Важливо відзначити, що фізико-хімічна основа методу електропорації дозволяє впливати на всі типи пухлин. Опубліковані доклінічні та клінічні результати однозначно це підтверджують. За останні 20 років доведена ефективність електрохіміотерапії при лікуванні поверхневих і глибоких пухлин шкіри (рис. 10), слизових оболонок та вісцеральних органів незалежно від їх гістологічної структури й розташування. Протоколи для стандартних операцій за допомогою електрохіміотерапії вперше було опубліковано у Європейському Союзі ще у 2006 р.
Рис. 10. Результати лікування злоякісного новоутворення методом електрохіміотерапії (за G. Bertino, G. Sersa, F. De Terlizzi, 2016)
Останнім часом зріс інтерес до використання методу при лікуванні пухлин голови та шиї, вже наявні європейські протоколи з динамічної електропідсиленої хіміотерапії (D-EECT) для лікування раку цих локалізацій. Відомо, що електрохіміотерапія не тільки активно вивчається, а й вже застосовується при нерезектабельних карциномах молочної, підшлункової залози, гліомах головного мозку, саркомах м’яких тканин та інших високорезистентних до лікування злоякісних новоутвореннях.
Європейський проект EURECA об’єднав центри Італії, Іспанії, Великобританії, Нідерландів, Данії та інших країн у рамках Міжнародної мережі INSPECT з обміну досвідом у галузі електрохіміотерапії. Створено базу даних і реєстр пацієнтів ISRCTN, яких лікували за допомогою такого методу. Нещодавно були розроблені нові методи електропорації для впливу на вісцеральні пухлини з використанням хірургічного, ендоскопічного або черезшкірного доступу до ділянки лікування.
Наукові досягнення шведської компанії Scandinavian ChemoTech AB істотно просунули вперед цей напрям. Портативний прилад IQWaveTM є новим і сучаснішим технологічним рішенням, ніж його попередники. Модифікація насамперед полягає у зменшенні розмірів апарата (його вага становить близько 5 кг), що дозволяє легко доставити обладнання в будь-яку клініку, якщо воно відсутнє в цьому лікувальному закладі. Це дає можливість виконати процедуру хірургічної електрохіміотерапії амбулаторно або стаціонарно. У приладі IQWaveTM реалізована більш сучасна технологія створення електричного поля, і тому режими D-EECT дозволяють руйнувати пухлину саме за рахунок хімічної електропорації, а не електричного некрозу тканин шкіри, слизових оболонок і паренхіми вісцеральних органів. D-EECT є безпечним, простим та ефективним клінічним методом, спрямованим на лікування великих пухлинних мас. Цей метод відкриває новий напрям і створює хороші перспективи в лікуванні неоперабельних, хіміо- та радіорезистентних пухлин. Можна щиро привітати рішення компанії Scandinavian ChemoTech AB зареєструвати цю технологію в Україні. Електрохіміотерапія стане ще одним методом, який дасть змогу покращити лікування наших пацієнтів із складними пухлинами різних локалізацій.
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 5 (72) 2021 р.