19 серпня, 2025
Карциноми гепатобіліарного тракту
Стандарт медичної допомоги
Карциноми гепатобіліарного тракту (КГТ) – це рак, що характеризується високою летальністю та охоплює спектр інвазивних карцином, які виникають у печінці (гепатоцелюлярна карцинома (ГЦК)), жовчних протоках (внутрішньопечінкова і позапечінкова холангіокарцинома (ХК)) та жовчному міхурі. ХК охоплюють усі пухлини, що походять з епітелію жовчних протоків. Рання діагностика і початок лікування пацієнтів із КГТ сприяють запобіганню ускладненням і покращенню якості життя пацієнтів. Стандарт призначений забезпечити організацію надання медичної допомоги, зокрема діагностики, лікування та подальшого спостереження пацієнтів із КГТ і раком жовчного міхура (РЖМ) на всіх етапах медичної допомоги.
Загальна частина
Назва діагнозу: Карциноми гепатобіліарного тракту.
Коди стану або захворювання. НК 025:2021 «Класифікатор хвороб та споріднених проблем охорони здоров’я»:
С22 Злоякісне новоутворення печінки та внутрішньопечінкових жовчних проток;
С23 Злоякісне новоутворення жовчного міхура;
C24 Злоякісне новоутворення інших та неуточнених частин жовчовивідних шляхів.
Розділ I. Організація надання медичної допомоги пацієнтам із карциномами гепатобіліарного тракту
Положення стандарту медичної допомоги (СМД). Медичну допомогу пацієнти із КГТ отримують в закладах охорони здоров’я (ЗОЗ), що надають спеціалізовану медичну допомогу. Вона потребує міждисциплінарної співпраці та інтегрованого ведення пацієнтів мультидисциплінарною командою фахівців, що мають відповідну кваліфікацію і досвід лікування злоякісних новоутворень печінки.
Лікарі різних спеціальностей повинні бути обізнані щодо основних факторів ризику і клінічних проявів КГТ з метою раннього виявлення і направлення пацієнта до відповідного ЗОЗ.
Обґрунтування. Ефективна взаємодія між учасниками процесу вважається найкращою практикою обстеження і лікування, а також невіддільною частиною скоординованої допомоги в онкології.
Заходи з раннього (своєчасного) виявлення цього виду злоякісних пухлин дають змогу суттєво поліпшити стан пацієнта.
Критерії якості медичної допомоги
Обов’язкові
- Пацієнтів, у яких під час візуалізаційного дослідження виявлено підозріле утворення в жовчному міхурі, печінці чи жовчних протоках, направляють до ЗОЗ, що надає спеціалізовану медичну допомогу, для підтвердження або спростування діагнозу і проведення спеціального лікування.
- Існують локально узгоджені письмові документи, що координують та інтегрують медичну допомогу для забезпечення діагностики і лікування пацієнтів із КГТ.
- Забезпечення пацієнтам після радикального лікування дотримання графіка оглядів і обстежень, пацієнтам із захворюванням, що прогресує після завершення спеціального лікування, – адекватного знеболення, проведення інших заходів з паліативної допомоги, а також симптоматичного лікування відповідно до чинних галузевих стандартів у сфері охорони здоров’я.
- Надання інформації пацієнтам, які отримали спеціальне протипухлинне лікування, щодо його можливих віддалених побічних ефектів, необхідності проведення періодичних обстежень у зв’язку з високою небезпекою виникнення рецидиву або іншої пухлини, а також рекомендацій щодо способу життя, режиму харчування і фізичних навантажень.
Бажані
5. Членів сім’ї/осіб, які здійснюють догляд, за згодою пацієнта, забезпечують у доступній формі інформацією щодо стану пацієнта, плану обстеження, лікування і подальшого спостереження.
6. Надання психоемоційної підтримки пацієнтам із КГТ та членам їхніх сімей, щоб послабити психологічний дистрес.
Розділ II. Діагностика і стадіювання карцином гепатобіліарного тракту
Положення СМД. Діагноз КГТ встановлюють у ЗОЗ, що надають спеціалізовану медичну допомогу, на основі збору анамнестичних даних, фізикального обстеження пацієнта, лабораторних, радіологічних методів дослідження та за результатами морфологічного дослідження біопсії пухлинного утворення (окрім резектабельних пухлин; панель 1).
Для визначення плану лікування пацієнтам, яким встановлено діагноз КГТ і РЖМ, можуть бути призначені додаткові обстеження, проведена періопераційна підготовка та визначений прогноз захворювання.
Панель 1
Морфологічна та молекулярна класифікація КГТ
Макроскопічно – на три патерни росту:
- мас-формуючий: солідна маса в паренхімі печінки;
- перидуктальний інфільтрат: інфільтрати вздовж портальних гілок, що спричиняють стриктури жовчних проток;
- внутрішньопротоковий ріст: папілярне або поліпоподібне зростання всередині розширеної жовчної протоки.
Мікроскопічно внутрішньопечінкова холангіокарцинома (ВПХК) представлена добре сформованою фіброзною стромою або із залозами у великій кількості. Залози вистелені клітинами з різним ступенем атипії та плеоморфізму.
Зазвичай це високодиференційована аденокарцинома з легкою атипією; однак також може бути вогнищева атипія з вираженим плеоморфізмом.
Часто трапляються мультицентричні пухлини і периневральна інвазія.
Гістологічні варіанти включають муцинозні, кільцеподібні, світлоклітинні, лімфоепітеліомоподібні, щитоподібно-фолікулоподібні, аденосквамозні та саркоматоїдні.
ВПХК поділяють на малий і великий протоковий типи.
- Малий протоковий тип:
- локалізація – периферична паренхіма печінки;
- формування маси;
- кубоподібні клітини, що утворюють невеликі трубчасті або анастомозуючі залози;
- нечаста лімфоваскулярна/периневральна інвазія;
- CD56, N-кадгерин, CRP позитивний;
- підтипи включають холангіолокарциному, ВПХК із малюнком, подібним до мальформації протокової пластинки.
- Великий протоковий тип:
- локалізація – проксимальніше до воріт печінки;
- перидуктальний інфільтрат або мас-формуючий патерн;
- високі стовпчасті клітини, які утворюють великі залози всередині відкритого просвіту; зазвичай містять муцин;
- біліарна інтраепітеліальна неоплазія, внутрішньопротокова біліарна неоплазія, інтрадуктальна тубулопапілярна неоплазія є прекурсорами;
- характерна лімфоваскулярна/периневральна інвазія;
- MUC5AC, MUC6, S100P і TFF1 позитивні.
Обґрунтування. Понад 90% ХК є аденокарциномами. Вони поділяються за характером росту на три гістологічні типи: мас-формування, протокова інфільтрація та внутрішньопротоковий ріст. ХК діагностують в усіх відділах жовчовивідної системи.
ВПХК – первинне злоякісне новоутворення печінки, для якого характерне виникнення солідних пухлинних вогнищ, що походять з епітелію внутрішньопечінкових жовчних проток. Основними факторами ризику розвитку ВПХК є хронічні захворювання печінки незалежно від етіології, а саме: первинний склерозуючий холангіт, гепатолітіаз, цироз печінки, вірусний гепатит В і С, печінкові гельмінтози, запальні захворювання кишечника (ЗЗК), цукровий діабет, ожиріння, вживання алкоголю та паління.
ВПХК впродовж тривалого часу може не мати клінічних симптомів, проте пацієнт скаржиться на втомлюваність, підвищення температури, втрату маси тіла, біль у правому підребер’ї. Жовтяниця – нехарактерний симптом для ВПХК, вона частіше розвивається при інвазії позапечінкових жовчних проток внаслідок заміщення великої частини паренхіми печінки пухлиною або оклюзії пухлиною печінкових вен.
Позапечінкові ХК (ППХК) трапляються частіше, ніж внутрішньопечінкові. Вони виникають у будь-якому місці позапечінкової жовчної протоки – від місця з’єднання правої та лівої печінкової протоки до загальної жовчної протоки включно із внутрішньопечінковою частиною. Далі їх класифікують на хілярні або дистальні пухлини. Хілярні ХК (які також називають пухлинами Клацкіна) виникають у місці з’єднання правої та лівої печінкових проток або поблизу нього; дистальні ХК – це позапечінкові ураження, що виникають у позапечінкових жовчних протоках над фатеровим соском і нижче від місця злиття лівої та правої жовчних проток. Хілярні ХК – найпоширеніший тип позапечінкових ХК.
Основними факторами ризику розвитку ППХК є гепато- та холангіолітіаз, вірусний гепатит В і С, кісти холедоха, токсини (діоксин, полівінілхлорид, алкоголь), ЗЗК, печінкові гельмінтози, неалкогольна жирова хвороба печінки.
Для ППХК характерна маніфестація захворювання з механічної жовтяниці, що зумовлена обструкцією позапечінкових жовчних проток.
Клінічна картина IgG4-асоційованого холангіту, що проявляється стриктурами жовчних проток та обструктивною жовтяницею, може бути подібною до ППХК. Тому у пацієнтів із непереконливим діагнозом ППХК необхідно визначити рівень IgG4 в сироватці крові, щоб уникнути недоцільної хірургічної резекції. Пацієнтів з IgG‑4-асоційованою холангіопатією направляють на лікування до лікаря-гастроентеролога.
РЖМ є найпоширенішим видом КГТ. Переважна більшість випадків РЖМ – це аденокарциноми. Поширеність РЖМ неухильно зростає з віком; у жінок його діагностують частіше, ніж у чоловіків. Для РЖМ характерний місцевоінвазивний ріст та інвазія в судини, широке метастазування у регіонарні лімфатичні вузли та віддалені метастази.
Жовчнокам’яна хвороба з наявністю хронічного запалення є найпоширенішим фактором ризику РЖМ, причому ризик зростає зі збільшенням розміру каменів. Кальцифікацію стінки жовчного міхура («порцеляновий» жовчний міхур), що є результатом хронічного запалення, також розглядають як фактор ризику РЖМ. Інші фактори ризику: аномальне з’єднання головної протоки підшлункової залози та жовчної протоки, поліпи жовчного міхура (> 1 см), хронічний черевний тиф, первинний склерозуючий холангіт і ЗЗК. Аденоміоматоз жовчного міхура також є потенційним, хоча й дещо суперечливим фактором ризику.
Пацієнтам із високим ризиком розвитку РЖМ необхідно провести профілактичну холецистектомію. Інші можливі клінічні прояви РЖМ охоплюють підозріле утворення, виявлене під час ультразвукового дослідження (УЗД), обструкцію жовчних проток із жовтяницею чи хронічним болем у правому верхньому квадранті живота, а також маніфестацію захворювання із жовтяниці, що пов’язана з пухлинною інвазією позапечінкових жовчних проток.
РЖМ часто діагностують на пізній стадії, оскільки на ранніх стадіях він може мати безсимптомний перебіг. Пізніше він набуває агресивного характеру і може швидко поширюватися. Клінічна картина РЖМ подібна до жовчних кольок або хронічного холециститу, тому його часто діагностують випадково під час холецистектомії через доброякісне захворювання жовчного міхура або під час аналізу результатів патоморфологічного дослідження після холецистектомії, виконаної для лікування симптоматичної жовчнокам’яної хвороби.
Критерії якості медичної допомоги
Обов’язкові
- Діагностичні заходи під час первинного обстеження пацієнтів із підозрою на ВПХК, ППХК та РЖМ передбачають збір анамнестичних даних, фізикальне обстеження, спрямоване на виявлення, зокрема і неспецифічних, ознак (невмотивоване підвищення температури, апатія, втрата маси тіла, загальна слабкість і біль у верхній частині живота) та морфологічне дослідження біопсії пухлинного утворення (окрім резектабельних пухлин). Пацієнти із ППХК можуть звертатися із жовтяницею, що супроводжується ознаками обструкції жовчних проток. Проводять діагностику супутніх захворювань.
- Початкове оцінювання функції печінки передбачає вимірювання рівнів білірубіну, аспартатамінотрансферази, аланінамінотрансферази, лужної фосфатази, визначення протромбінового часу як міжнародного нормалізованого співвідношення, альбуміну та рівня тромбоцитів (корелюючого для портальної гіпертензії); загальний клінічний аналіз крові; азот сечовини та креатинін для оцінювання функції нирок.
- Діагностика ВПХК, ППХК, РЖМ передбачає проведення багатофазової комп’ютерної томографії (КТ) або магнітно-резонансної томографії (МРТ) черевної порожнини та органів малого таза із внутрішньовенним контрастуванням для оцінювання ураження печінки, магістральних судин, регіонарних лімфатичних вузлів і віддалених органів. Для виключення вторинного ураження органів грудної клітки і для стадіювання пухлини виконують КТ органів грудної клітки з/без внутрішньовенного контрастування. Стадіювання пухлин здійснюють за системою TNM (див. табл. 1-6).
- Для підтвердження діагнозу перед початком подальшого лікування проводять передопераційну біопсію пацієнтам із нерезектабельним (включно із пухлинами з віддаленими метастазами в лімфатичні вузли навколо черевного стовбура або в ділянці борозни черевної частини аорти й нижньої порожнистої вени) або метастатичним захворюванням (включно із віддаленими метастазами, метастазами у лімфатичні вузли за межами ділянки воріт печінки, а також обширним ураженням воріт печінки, що спричиняє жовтяницю або проникає в судини). Виконують трепан-біопсію утворення.
- Для оцінювання функціональної резервної здатності печінки у пацієнтів із цирозом використовують класифікацію за шкалою Чайлда – П’ю.
|
Таблиця 1. Стадіювання пухлин внутрішньопечінкових жовчних проток за системою TNM (8ме вид., 2017 р., Американський об’єднаний комітет із питань раку – American Joint Committee on Cancer, AJCC) |
|
|
Стадіювання |
Визначення |
|
T – Первинна пухлина |
|
|
TX |
Первинну пухлину не можна оцінити |
|
T0 |
Немає ознак первинної пухлини |
|
Tis |
Карцинома in situ (внутрішньопротокова пухлина) |
|
T1 |
Поодинока пухлина розміром < 5 см або > 5 см без інвазії судин |
|
T1a |
Поодинока пухлина розміром < 5 см без інвазії судин |
|
T1b |
Поодинока пухлина розміром > 5 см без інвазії судин |
|
T2 |
Поодинока пухлина із внутрішньопечінковою інвазією судин або множинні пухлини з інвазією судин або без неї |
|
T3 |
Пухлина перфорує вісцеральну очеревину |
|
T4 |
Пухлина вражає локальні позапечінкові структури шляхом прямої інвазії |
|
N – Регіонарні лімфовузли |
|
|
NX |
Регіонарні лімфовузли не можна оцінити |
|
N0 |
Немає метастазів у регіонарні лімфатичні вузли |
|
N1 |
Наявні метастази в регіонарні лімфатичні вузли |
|
M – Віддалені метастази |
|
|
M0 |
Немає віддалених метастазів |
|
M1 |
Наявні віддалені метастази |
|
Таблиця 2. Прогностичні групи (за системою AJCC) |
|||
|
Стадія |
T |
N |
M |
|
0 |
Tis |
N0 |
M0 |
|
IA |
T1a |
N0 |
M0 |
|
IB |
T1b |
N0 |
M0 |
|
II |
T2 |
N0 |
M0 |
|
IIIA |
T3 |
N0 |
M0 |
|
IIIB |
T4 |
N0 |
M0 |
|
Будьяка стадія T |
N1 |
M0 |
|
|
IV |
Будьяка стадія T |
Будьяка стадія N |
M1 |
|
Гістологічний ступінь злоякісності (G) |
|||
|
GX Ступінь злоякісності не можна оцінити |
|||
|
G1 Високодиференційована пухлина |
|||
|
G2 Помірно диференційована пухлина |
|||
|
G3 Низькодиференційована пухлина |
|||
|
Таблиця 3. Стадіювання перихілярних пухлин жовчних проток за системою TNM (8ме вид., 2017 р., AJCC) |
|
|
Стадіювання |
Визначення |
|
T |
Первинна пухлина |
|
TX |
Первинну пухлину не можна оцінити |
|
T0 |
Немає ознак первинної пухлини |
|
Tis |
Карцинома in situ/дисплазія високого ступеня |
|
T1 |
Пухлина обмежена жовчною протокою, з поширенням на м’язовий шар або фіброзну тканину |
|
T2 |
Пухлина проростає за стінку жовчної протоки в навколишню жирову тканину, або пухлина інвазує прилеглу паренхіму печінки |
|
T2a |
Пухлина проростає за стінку жовчної протоки в навколишню жирову тканину |
|
T2b |
Пухлина інвазує прилеглу паренхіму печінки |
|
T3 |
Пухлина інвазує гілки ворітної вени або печінкової артерії з одного боку |
|
T4 |
Пухлина інвазує головний стовбур ворітної вени чи її гілки з двох боків або загальну печінкову артерію; або гілки жовчних проток другого порядку з двох боків з ураженням гілок ворітної вени або печінкової артерії з протилежного боку |
|
N |
Регіонарні лімфовузли |
|
NX |
Регіонарні лімфовузли не можна оцінити |
|
N0 |
Немає метастазів у регіонарні лімфатичні вузли |
|
N1 |
Ураження від одного до трьох лімфатичних вузлів, до яких зазвичай належать хілярні лімфовузли, лімфовузли вздовж міхурової протоки, загальної жовчної протоки, печінкової артерії, задні панкреатодуоденальні лімфовузли та лімфовузли вздовж ворітної вени |
|
N2 |
Ураження чотирьох або більше лімфатичних вузлів на ділянках, описаних для N1 |
|
M |
Віддалені метастази |
|
M0 |
Немає віддалених метастазів |
|
M1 |
Віддалені метастази |
|
Таблиця 4. Прогностичні групи (за системою AJCC) |
|||
|
Стадія |
T |
N |
M |
|
0 |
Tis |
N0 |
M0 |
|
I |
T1 |
N0 |
M0 |
|
II |
T2a–b |
N0 |
M0 |
|
IIIA |
T3 |
N0 |
M0 |
|
IIIB |
T4 |
N0 |
M0 |
|
IIIC |
Будьяка стадія T |
N1 |
M0 |
|
IVA |
Будьяка стадія T |
N2 |
M0 |
|
IVB |
Будьяка стадія T |
Будьяка стадія N |
M1 |
|
Гістологічний ступінь злоякісності (G) |
|||
|
GX Ступінь злоякісності не можна оцінити |
|||
|
G1 Високодиференційована пухлина |
|||
|
G2 Помірно диференційована пухлина |
|||
|
G3 Низькодиференційована пухлина |
|||
|
Таблиця 5. Стадіювання пухлин дистальних відділів жовчних проток за системою TNM (8ме вид., 2017 р., AJCC) |
|
|
Стадіювання |
Визначення |
|
Т |
Первинна пухлина |
|
TX |
Первинну пухлину не можна оцінити |
|
Tis |
Карцинома in situ/дисплазія високого ступеня |
|
T1 |
Пухлина інвазує стінку жовчної протоки на глибину менше ніж 5 мм |
|
T2 |
Пухлина інвазує стінку жовчної протоки на глибину 512 мм |
|
T3 |
Пухлина інвазує стінку жовчної протоки на глибину понад 12 мм |
|
T4 |
Пухлина вражає черевний стовбур, верхню брижову артерію та/або загальну печінкову артерію |
|
N |
Регіонарні лімфовузли |
|
NX |
Регіонарні лімфовузли не можна оцінити |
|
N0 |
Немає метастазів у регіонарні лімфатичні вузли |
|
N1 |
Метастази в 13 регіонарні лімфовузли |
|
N2 |
Метастази в 4 або більше регіонарних лімфовузлів |
|
M |
Віддалені метастази |
|
M0 |
Немає віддалених метастазів |
|
M1 |
Віддалені метастази |
|
Таблиця 6. Прогностичні групи (за системою AJCC) |
|||
|
Стадія |
T |
N |
M |
|
0 |
Tis |
N0 |
M0 |
|
I |
T1 |
N0 |
M0 |
|
IIA |
T1 |
N1 |
M0 |
|
|
T2 |
N0 |
|
|
IIB |
T2 |
N1 |
M0 |
|
|
T3 |
N0 |
|
|
|
T3 |
N1 |
|
|
IIIA |
T1 |
N2 |
M0 |
|
|
T2 |
N2 |
|
|
|
T3 |
N2 |
|
|
IIIB |
T4 |
N0 |
M0 |
|
|
T4 |
N1 |
|
|
|
T4 |
N2 |
|
|
IV |
Будьяка стадія T |
Будьяка стадія N |
M1 |
|
Гістологічний ступінь злоякісності (G) |
|||
|
GX Ступінь злоякісності не можна оцінити |
|||
|
G1 Високодиференційована пухлина |
|||
|
G2 Помірно диференційована пухлина |
|||
|
G3 Низькодиференційована пухлина |
|||
Діагностика ВПХК
6. Для оцінювання резектабельності ВПХК та її стадіювання пацієнтам із жовтяницею проводять (до дренування) консультацію хірурга-онколога. Товстоголкову біопсію проводять лише після визначення статусу резектабельності та трансплантабельності.
7. У разі ускладненого диференційного діагнозу між ВПХК і ГЦК проводять тестування на альфа-фетопротеїн (АФП), особливо у пацієнтів із хронічними захворюваннями печінки.
8. У разі сумнівного діагнозу ВПХК розглядають доцільність проведення серологічних досліджень на вірусні гепатити. Якщо діагностовано гепатит, пацієнта направляють на консультацію до лікаря-інфекціоніста, лікаря-гастроентеролога, лікування проводять відповідно до чинних галузевих стандартів у сфері охорони здоров’я.
9. Біопсію проводять, коли наявні сумніви щодо природи пухлини (диференційна діагностика між ВПХК і ГЦК, наявність пухлин в анамнезі або печінкові метастази, які можуть імітувати ВПХК). Оптимальним методом біопсії для ВПХК є трепан-біопсія.
Діагностика ППХК
10. Для діагностики ППХК проводять магнітно-резонансну холангіопанкреатографію (МРХПГ) та/або КТ із внутрішньовенним контрастуванням для оцінювання поширення пухлини (до хірургічного дренування/стентування жовчних проток).
11. За наявності жовтяниці у пацієнтів із ППХК призначають неінвазивну холангіографію з візуалізацією.
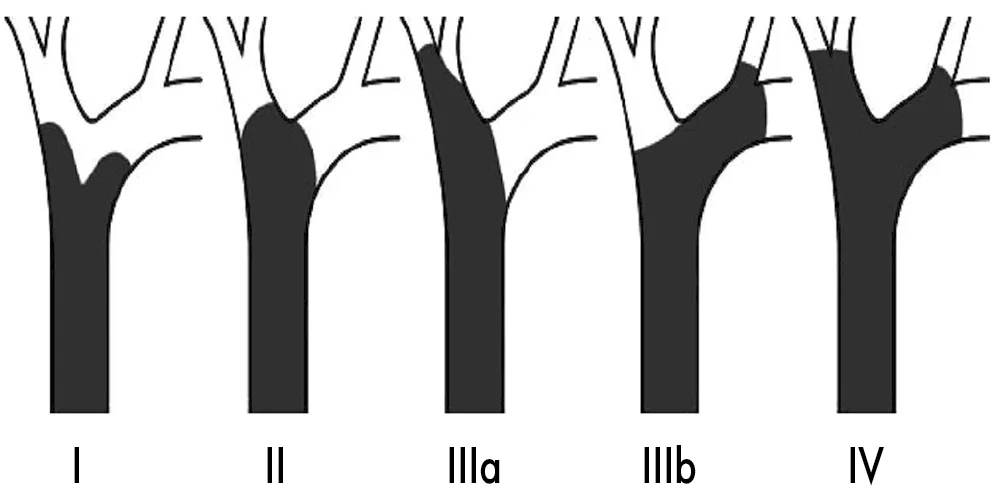
12. У разі ППХК для стадіювання рівня ураження жовчних проток і визначення тактики лікування застосовують класифікацію за Бісмут – Корлетт (табл. 7).
13. Пацієнтам із гілярною ХК, які можуть бути кандидатами на трансплантацію, протипоказана черезочеревинна біопсія. Оптимальним методом діагностики є трепан-біопсія.
14. У разі резектабельного захворювання перед хірургічним видаленням пухлини слід розглянути виконання лапароскопічної діагностики для виключення дисемінованого захворювання.
15. Пацієнтам із сумнівним діагнозом ППХК та підозрою на холангіопатію необхідно визначити рівень IgG4 в сироватці крові для проведення диференційної діагностики з IgG‑4-асоційованою холангіопатією та уникнення недоцільної хірургічної резекції. Пацієнтів з IgG‑4-асоційованою холангіопатією необхідно скерувати до лікаря-гастроентеролога.
|
Таблиця 7. Система класифікації гілярних холангіокарцином за Бісмут – Корлетт |
|
|
Тип I |
Стриктура обмежена загальною печінковою протокою, нижче рівня злиття правої та лівої печінкових проток |
|
Тип II |
Стриктура на рівні злиття правої та лівої дольових проток |
|
Тип IIIa |
Стриктура тип II і поширюється на початок правої дольової протоки (злиття правої задньої та передньої секційних проток) |
|
Тип IIIb |
Стриктура тип II і поширюється на початок лівої дольової протоки (впадіння 2го, 3го і 4го сегментарних проток) |
|
Тип IV |
Стриктура поширюється на початок і правої, і лівої дольових проток (тобто комбінація типів IIIa та IIIb) або мультифокальне ураження |
Діагностика РЖМ
16. Пацієнтам, у яких виявлено новоутворення жовчного міхура і за результатами клінічних та радіологічних ознак підозрюють резектабельне захворювання, проведення передопераційної біопсії не рекомендовано.
17. За наявності або підозри на хронічне захворювання печінки необхідно провести серологічну діагностику на вірусні гепатити і консультації лікаря-інфекціоніста, лікаря-гастроентеролога.
18. Пацієнтів, у яких виявлено РЖМ за результатами патоморфологічного обстеження препарату після холецистектомії через доброякісне захворювання, слід дообстежити за такими ж принципами, як і пацієнтів із первинним РЖМ.
19. У разі виникнення інтраопераційної підозри на РЖМ під час холецистектомії через доброякісне утворення рекомендовано виконати лапароскопічну діагностику для виключення вторинного ураження очеревини, за можливості провести інтраопераційну біопсію пухлини та завершити операцію, направивши пацієнта до ЗОЗ, що надає спеціалізовану медичну допомогу онкологічним хворим.
20. Пацієнтам із нерезектабельним або метастатичним захворюванням для визначення подальшого лікування виконують трепан-біопсію утворення.
21. Для оцінювання глибини інвазії пухлини у стінку жовчного міхура, наявності метастазів у лімфовузлах та віддалених метастазів, виявлення ступеня прямої інвазії пухлини у прилеглі органи/жовчовивідну систему або інвазії в магістральні судини рекомендовано провести візуалізацію (КТ та/або МРТ) із контрастуванням органів черевної порожнини, таза та, за необхідності, грудної клітки.
Бажані
22. За необхідності застосовують неінвазивну МРХПГ, ендоскопічну ретроградну холангіопанкреатографію або черезшкірну черезпечінкову холангіографію, якщо терапевтичне втручання не заплановане.
23. У разі клінічної необхідності рекомендовано визначення рівня сироваткових маркерів: АФП, СА 19-9, РЕА.
24. Пацієнтам із резектабельним захворюванням (на основі візуалізаційних досліджень) та після огляду мультидисциплінарної команди, за необхідності, рекомендоване проведення ПЕТ/КТ для виключення віддалених метастазів і метастазів у регіонарні лімфатичні вузли.
25, За необхідності, пацієнтам із резектабельним захворюванням можна розглянути виконання додаткових методів оцінювання функції печінки (оцінювання індексів ALBI, APRI; УЗ- або МР-еластометрія, гепатосцинтиграфія, функціональна МРТ із гепатоспецифічним контрастом).
26, За необхідності, для діагностики дистальної ППХК може бути використано ендоскопічне УЗД.
27 За необхідності, пацієнтам із нерезектабельним, нетрансплантабельним або метастатичним захворюванням, що є кандидатами на проведення системної терапії, можна розглянути виконання панелі молекулярних досліджень для визначення тактики лікування. Доцільність направлення на генетичне консультування і потенційне тестування на мутації зародкової лінії можна розглядати у пацієнтів, що відповідають будь-якій із цих характеристик: молодий вік на момент встановлення діагнозу; обтяжений особистий анамнез або рак у сімейному анамнезі; відсутність відомих факторів ризику захворювання печінки; наявність мутацій, виявлених під час тестування пухлини, які, за підозрами, можуть бути причиною змін у генах зародкової лінії.
Розділ IIІ. Лікування пацієнтів із карциномами гепатобіліарного тракту
Положення СМД. Спеціальне протипухлинне лікування пацієнтів із КГТ здійснюють виключно у ЗОЗ, що надають спеціалізовану медичну допомогу онкологічним хворим. Для вибору оптимальної та ефективної стратегії лікування, за якої можна досягти найкращого прогнозу захворювання зі збереженою якістю життя, ведення пацієнтів із КГТ передбачає мультидисциплінарний підхід.
План лікування пацієнтів, який склав консиліум фахівців (лікар хірург-онколог, лікар-онколог, лікар-радіолог, лікар із променевої терапії, лікар-гастроентеролог) та погодив із пацієнтом, має враховувати стадію і поширеність захворювання, рівень збереження функції печінки і загальний стан пацієнта. Лікування РЖМ передбачає проведення холецистектомії з резекцією прилеглої паренхіми печінки, променевої та системної терапії.
Обґрунтування. Лікування пухлин жовчовивідної системи часто ускладнене наявністю супутніх захворювань печінки (ГЦК, цироз, портальна гіпертензія, гострі вірусні гепатити, імунодефіцитні стани, гостре пошкодження нирок тощо) та впливає на вибір методу лікування у пацієнтів із КГТ і потребує мультидисциплінарного підходу. Крім того, поширеність та дія КГТ на функцію печінки можуть впливати на ефективність лікування, тому під час вибору його методу потрібно врахувати ризики можливих токсичних ефектів від лікування і потенційні переваги.
Симптоматичне лікування механічної жовтяниці, пов’язаної із ППХК, можна здійснювати і в ЗОЗ, що надають спеціалізовану онкологічну медичну допомогу, і в хірургічних стаціонарах загального профілю.
Методи лікування КГТ залежать від того, яку оцінку резектабельності пацієнта визначила мультидисциплінарна команда. Пацієнти можуть бути умовно поділені на три категорії: ті, що підлягають хірургічному лікуванню, нерезектабельні та пацієнти з віддаленими метастазами.
Для пацієнтів із резектабельним захворюванням хірургічне видалення є єдиним потенційно радикальним методом лікування, хоча більшість пацієнтів не відповідають вимогам для хірургічного втручання через пізню стадію захворювання на момент встановлення діагнозу. Принципи хірургічного втручання наведені на панелі 2.
Панель 2
Принципи хірургічного втручання
Пацієнти мають бути операбельними (за медичними показаннями).
На момент планування оперативного лікування пацієнт повинен мати результати дослідження (КТ/МРТ черевної порожнини та малого таза із внутрішньовенним контрастуванням, КТ органів грудної клітки з/без контрастування). Обсяг резекції печінки залежить від розмірів та локалізації пухлини і може варіювати від атипової до великої анатомічної резекції залежно від можливості забезпечити R0-статус.
Резекція печінки має бути методом вибору за таких обставин:
- збережена функція печінки (результати лабораторного обстеження);
- можливість забезпечити достатній хірургічний кліренс (R0);
- адекватний майбутній залишковий об’єм печінки у відсотках (загалом 30% у пацієнтів без хронічного захворювання печінки) за умови можливості збереження адекватного притоку/відтоку крові та жовчі.
Для оцінювання післяопераційних ризиків застосовують розрахунок майбутнього залишкового об’єму печінки у відсотках.
У пацієнтів із недостатнім майбутнім залишковим об’ємом печінки слід розглянути використання методик індукції гіпертрофії майбутнього залишку печінки (портовенозна емболізація, комбінація портовенозної емболізації та емболізації печінкових вен).
Інвазія позапечінкових жовчних проток, біфуркації ворітної вени, гирл печінкових вен та нижньої порожнистої вени не є протипоказаннями до хірургічного лікування.
Протипоказаннями до резекції є пухлини з віддаленими метастазами в лімфатичні вузли за межами воріт печінки (найчастіше навколо черевного стовбура або в ділянці борозни черевної частини аорти й нижньої порожнистої вени) або віддалені метастази (найчастіше в печінку та очеревину).
Резекція печінки сумнівна, проте може бути проведена після ретельного обговорення мультидисциплінарною командою за таких обставин: лімітоване і резектабельне багатовогнищеве ураження (відповідає Т2 за AJCC); погранично-резектабельне ураження регіонарних лімфатичних вузлів.
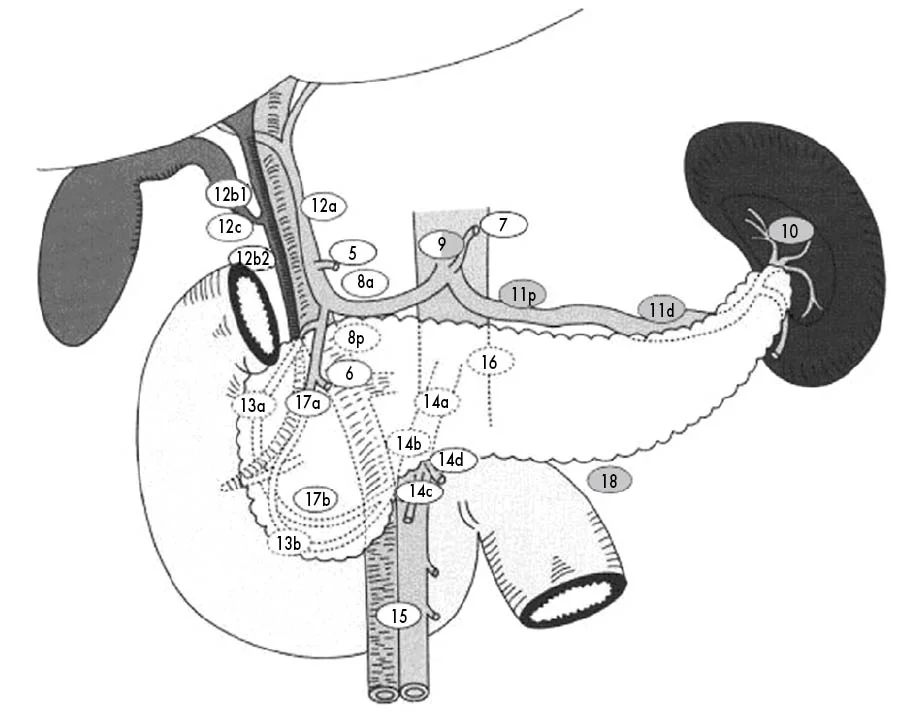
Лімфодисекція має включати лімфатичні вузли 12, 13, 8 груп, її потрібно виконати для ретельного стадіювання захворювання. Макроскопічна лімфаденопатія за межами воріт печінки потребує інтраопераційного патоморфологічного дослідження, оскільки метастатична лімфаденопатія за межами воріт печінки є протипоказанням для хірургічного лікування.
Після хірургічного видалення пухлини з низьким хірургічним кліренсом (R1) або позитивними регіонарними лімфовузлами слід розглянути доцільність проведення ад’ювантної хімієпроменевої терапії.
Пацієнтів із нерезектабельним захворюванням через місцеве поширення пухлини слід розглянути щодо трансплантабельності. Загалом пацієнтів із нерезектабельною перихілярною ППХК, радіальний розмір якої менше 3 см, без внутрішньо-, позапечінкових метастазів та без регіонарної лімфаденопатії слід розглядати щодо трансплантабельності і направити в центр трансплантації.
Потенційному кандидату на трансплантацію до визначення статусу трансплантабельності не рекомендовано виконувати біопсію.
Для лікування пацієнтів із нерезектабельним захворюванням внаслідок місцевого поширення пухлини може бути використана системна терапія або локорегіонарні методи (радіочастотна абляція, трансартеріальна хімієемболізація).
Оптимальний метод лікування для пацієнтів із нерезектабельним та метастатичним захворюванням – системна терапія, а біопсія пухлини перед початком лікування є обов’язковою вимогою. Оптимальним методом діагностики є трепан-біопсія.
Критерії якості медичної допомоги
Обов’язкові
- Пацієнтів із вперше встановленим діагнозом ППХК, ВПХК, РЖМ направляють до ЗОЗ, що надають спеціалізовану медичну допомогу пацієнтам з онкологічною патологією.
- Для визначення стратегії лікування проводять оцінювання резектабельності та стадіювання пухлини.
- Біопсія пухлини перед початком лікування є обов’язковою вимогою для пацієнтів із нерезектабельним і метастатичним захворюванням.
- Проведення діагностичної лапароскопії рекомендовано для пацієнтів із будь-якою підозрою (за результатами радіологічних досліджень) на метастатичне захворювання за неможливості черезшкірної біопсії.
- Неоад’ювантна терапія при резектабельному захворюванні ППХК може бути запропонована певним пацієнтам, що є сумнівними кандидатами на хірургічне лікування (наприклад, мультифокальне ураження чи масивна лімфаденопатія воріт печінки), після обговорення мультидисциплінарною командою.
- Після хірургічного видалення пухлини з низьким хірургічним кліренсом (R1) або позитивними регіонарними лімфовузлами слід розглянути доцільність проведення ад’ювантної хімієпроменевої терапії.
- Пацієнтам із нерезектабельним, метастатичним захворюванням при збереженому соматичному статусі або тим, які не є кандидатами на хірургічне втручання через стан здоров’я або супутнє захворювання, призначають проведення системної терапії (табл. 8).
- Метастатичне ураження печінки, очеревини та інших зон, а також метастатична лімфаденопатія за межами воріт печінки є протипоказаннями до хірургічного лікування.
- У разі випадкового виявлення підозрілого утворення під час операції через холецистектомію та неможливості залучити до втручання фахівців відповідної кваліфікації слід задокументувати усі результати і скерувати пацієнта до спеціалізованого ЗОЗ. Біопсію не проводять, оскільки це може призвести до перитонеальної дисемінації.
- У разі можливості залучити до розпочатої холецистектомії фахівців необхідної кваліфікації та наявності відповідної переконливої клінічної картини раку необхідно провести радикальну резекцію. Якщо діагноз не можна чітко встановити, в деяких випадках можна розглянути доцільність проведення інтраопераційної експрес-біопсії перед радикальною резекцією.
- У разі випадкового виявлення патологічних результатів патоморфологічного дослідження препарату після звичайної холецистектомії слід повторно оцінити результат патоморфологічного дослідження щодо стадії пухлини (T), статусу країв резекції, виключити віддалені метастази і направити пацієнта до ЗОЗ, що надає спеціалізовану медичну допомогу пацієнтам з онкологічними захворюваннями.
|
Таблиця 8. Принципи системної терапії |
||
|
Пріоритетні схеми |
Інші рекомендовані схеми |
Корисні за певних обставин |
|
Неоад’ювантна терапія |
||
|
Пріоритетні схеми
|
Інші рекомендовані схеми
|
|
|
Ад’ювантна терапія |
||
|
Пріоритетні схеми
|
Інші рекомендовані схеми
|
|
|
Препарати, що використовуються одночасно з променевою терапією |
||
|
||
|
Первинне лікування нерезектабельного й метастатичного захворювання |
||
|
Пріоритетні схеми Дурвалумаб + гемцитабін + цисплатин |
Інші рекомендовані схеми
|
Таргетна терапія:
У разі пухлин із позитивними результатами тестування на HER2:
У разі пухлин із MSIH/dMMR:
|
|
Терапія раку жовчовивідної системи подальших ліній у разі прогресування захворювання |
||
|
Пріоритетні схеми FOLFOX |
Інші рекомендовані схеми
|
Пембролізумаб Таргетна терапія:
У разі пухлин із позитивними результатами тестування на HER2:
У разі пухлин із MSIH/dMMR:
У разі ХК із мутаціями IDH1:
|
Лікування ВПХК
12. Для пацієнтів із мультифокальним внутрішньопечінковим ураженням ВПХК (Т2 за AJCC), за можливості досягнення хірургічного кліренсу (R0) та збереження після втручання достатнього об’єму майбутнього залишку печінки, проводять резекційну хірургію печінки як радикальний метод лікування онкологічного захворювання.
13. Після радикального хірургічного видалення пухлини слід розглянути проведення ад’ювантної хімієтерапії; оптимальний режим – капецитабін впродовж шести місяців.
14. Щодо пацієнтів з ознаками локорегіонарного поширеного захворювання (ураженням лімфовузлів або іншими факторами високого ризику) необхідно розглянути проведення неоад’ювантної хімієтерапії для виключення швидкого прогресування й уникнення недоцільного хірургічного втручання. Рішення щодо призначення неоад’ювантної терапії ухвалюють індивідуально у кожному випадку після консультацій з лікарем хірургом-онкологом. Доцільна тривалість терапії – 2-6 місяців із повторним обстеженням через кожні 2-3 місяці.
15. Певних пацієнтів із первинно нерезектабельним захворюванням, які відповіли на системну або локорегіонарну терапію, можна розглянути щодо хірургічного втручання після повторної діагностики.
16. У разі нерезектабельності пухлини і наявності метастазів призначають проведення системної терапії.
Лікування ППХК
17. Пацієнтам із резектабельною пухлиною без вторинного ураження (за винятком лімфовузлів воріт печінки для перихілярної ППХК; воріт печінки і парапанкреатичних лімфовузлів для дистальної ППХК) за умови можливості досягнення хірургічного кліренсу (R0) та збереження достатнього об’єму майбутнього залишку печінки проводять резекційну хірургію як радикальний метод лікування онкологічного захворювання.
18. Рішення щодо дренування жовчних проток перед резекцією, за наявності механічної жовтяниці, ухвалюють після консультації лікаря-хірурга, лікаря хірурга-онколога. Якщо резекцію не заплановано, дренування жовчних проток можна виконати за допомогою черезшкірного дренування або ендобіліарного стентування.
19. У разі резектабельної перихілярної ППХК із наявністю холангіту призначають дренування жовчних проток при малому об’ємі печінкового залишку (< 50% або < 30%) або коли заплановане використання методики індукції гіпертрофії залишку.
20 У разі перихілярної ППХК обсяг резекції залежить від характеру ураження жовчних проток. При ІІ, ІІІа, ІІІb і IV типі за Бісмут – Корлетт необхідно виконати велику резекцію печінки з каудальною лобектомією і резекцією позапечінкових жовчних проток.
21. Після радикального хірургічного видалення пухлини слід розглянути проведення ад’ювантної хімієтерапії; оптимальний режим – капецитабін впродовж шести місяців.
22. При дистальній ППХК обсяг резекції зазвичай охоплює панкреатодуоденальну зону. Лімфодисекція має включати лімфовузли воріт печінки та вузли груп 8, 12, 13, 14, 17 (табл. 9). Рекомендоване експрес-дослідження замороженого зрізу проксимального краю резекції жовчної протоки.
23. У деяких випадках перихілярної ППХК (тип І за Бісмут – Корлетт) пухлини на межі визначення перихілярної і дистальної ППХК – пухлини середнього відділу жовчних проток.
24. Можлива ізольована резекція позапечінкових жовчних проток. У такому разі рекомендоване експрес-дослідження замороженого зрізу проксимального і дистального країв резекції жовчної протоки. Лімфодисекція має включати лімфовузли груп 8, 12, 13 (табл. 9).
25. У разі значного проксимального і дистального поширення пухлини проводять комбінацію широкої резекції печінки та панкреатодуоденальної резекції. Необхідно розраховувати суттєвий періопераційний ризик цих втручань.
26. Деяким пацієнтам із первинно нерезектабельним захворюванням, які відповіли на системну або локорегіонарну терапію, може бути проведене хірургічне втручання.
27. Пацієнтам із нерезектабельним, але трансплантабельним захворюванням призначають неоад’ювантну хімієпроменеву терапію.
28. Після радикального хірургічного видалення пухлини призначають ад’ювантну хімієтерапію, вибір схеми якої здійснює лікар-онколог, оптимальний режим – капецитабін впродовж шести місяців.
29. Після хірургічного видалення пухлини з низьким хірургічним кліренсом (R1) або позитивними регіонарними лімфовузлами рекомендоване призначення ад’ювантної хімієпроменевої терапії.
|
Таблиця 9. Номер станції та назви лімфатичних вузлів |
|
|
№ |
Назва |
|
5 |
Супрапілоричні лімфатичні вузли |
|
6 |
Інфрапілоричні лімфатичні вузли |
|
7 |
Лімфатичні вузли вздовж лівої шлункової артерії |
|
8а |
Лімфатичні вузли в передньоверхній групі вздовж загальної печінкової артерії |
|
8р |
Лімфатичні вузли в задній групі вздовж загальної печінкової артерії |
|
9 |
Лімфатичні вузли навколо черевного стовбура |
|
10 |
Лімфатичні вузли в межах воріт селезінки |
|
11р |
Лімфатичні вузли вздовж проксимального відділу селезінкової артерії |
|
11d |
Лімфатичні вузли вздовж дистального відділу селезінкової артерії |
|
12а |
Лімфатичні вузли вздовж власне печінкової артерії |
|
12p |
Лімфатичні вузли вздовж портальної вени |
|
12b |
Лімфатичні вузли вздовж жовчної протоки |
|
13 |
Лімфатичні вузли на задній поверхні голівки підшлункової залози |
|
14 |
Лімфатичні вузли навколо верхньобрижової артерії |
|
15 |
Лімфатичні вузли навколо середньої товстокишкової артерії |
|
16а, b |
Лімфатичні вузли навколо абдомінального відділу аорти |
|
17 |
Лімфатичні вузли на передній поверхні голівки підшлункової залози |
|
18 |
Лімфатичні вузли по нижньому краю підшлункової залози |
Лікування РЖМ
30. Пацієнтам із резектабельною пухлиною жовчного міхура без вторинного ураження (за винятком лімфовузлів воріт печінки), за умови можливості досягнення хірургічного кліренсу (R0), рекомендована резекційна хірургія як радикальний метод лікування. Стандартний обсяг операції передбачає видалення жовчного міхура одним блоком із прилеглою паренхімою (тут і далі – радикальна холецистектомія) та регіонарну лімфаденектомію груп 8, 12, 13 відповідно до класифікації станцій лімфатичних вузлів щодо печінки та підшлункової залози (табл. 9).
31. Для забезпечення достатнього хірургічного кліренсу може бути необхідна обширна резекція печінки та/або резекція позапечінкових жовчних проток.
32. Пацієнтам, у яких РЖМ діагностовано гістологічно після звичайної холецистектомії, за умови відсутності вторинного ураження (за винятком лімфовузлів воріт печінки), рекомендована резекційна хірургія. Перед радикальною резекцією необхідно провести повторну візуалізацію органів грудної клітки, черевної порожнини і таза. Якщо дослідження виконувалось перед холецистектомією – рекомендовано провести повторне.
33. Пацієнтам із несприятливим прогнозом (гістологічно підтверджене вторинне ураження регіонарних лімфовузлів, механічна жовтяниця) після розгляду мультидисциплінарною командою рекомендовано розглянути проведення неоад’ювантної терапії. Для її призначення необхідно провести морфологічну верифікацію.
34. Системну терапію проводять пацієнтам із нерезектабельним і метастатичним захворюванням при збереженому соматичному статусі або тим, що не є кандидатами на хірургічне втручання через стан здоров’я або супутнє захворювання. На початку системної терапії рекомендовано мати радіологічне дослідження (КТ/МРТ черевної порожнини та малого таза із внутрішньовенним контрастуванням, КТ органів грудної клітки з або без контрастування).
Бажані
35. Пацієнтам із нерезектабельним захворюванням або тим, що не є кандидатами на хірургічне втручання через стан здоров’я або супутнє захворювання, за необхідності розглядають проведення променевої терапії (в режимі 3D-КПТ, IMRT або SBRT), основні принципи якої наведені на панелі 3.
36. Якщо це можливо і доцільно, можуть бути застосовані малоінвазивні методики для хірургічного видалення у ЗОЗ, що надають спеціалізовану медичну допомогу.
37. За необхідності у пацієнтів із недостатнім майбутнім залишковим об’ємом печінки слід розглянути використання методик індукції гіпертрофії майбутнього залишку (портовенозна емболізація, комбінація портовенозної емболізації та емболізації печінкових вен).
38. Резекція і реконструкція ворітної вени та/або печінкової артерії можуть бути необхідними в разі пухлинної інвазії; їх потрібно виконувати у ЗОЗ, що надають спеціалізовану медичну допомогу. Реконструкцію жовчних проток переважно виконують за допомогою гепатикоєюностомії за методом Roux-en-Y.
39. Трансплантацію печінки можна розглянути в деяких пацієнтів із нерезектабельною пухлиною із радіальним діаметром ≤ 3 см без ураження регіонарних лімфовузлів. Слід розглянути неоад’ювантну хімієпроменеву терапію у пацієнтів, що є потенційними кандидатами на трансплантацію.
Панель 3
Принципи променевої терапії
Загальні принципи
Променева терапія (ПТ) під візуальним контролем (IGRT) рекомендована в разі застосування ПТ, ПТ із модуляцією інтенсивності (IMRT) або об’ємно-модульованої дугової терапії (VMAT) і стереотаксичної ПТ (SBRT) для підвищення точності лікування і зниження токсичності, пов’язаної з лікуванням.
Ад’ювантна ПТ
Післяопераційна ПТ із застосуванням 3D-конформної ПТ (3D-КПТ) або IMRT є одним із варіантів терапії після резекції позапечінкової ХК та РЖМ. При ВПХК можна розглянути ПТ після резекції з низьким хірургічним кліренсом (R1) або при позитивних регіонарних лімфовузлах.
Під час планування потрібно враховувати дренуючі регіонарні лімфатичні вузли: у воротах печінки, черевні, верхні брижові, шлунково-печінкові та парааортальні. Доза опромінення ложа пухлини має становити до 45 Гр фракціями по 1,8 Гр/фракцію та 50-60 Гр фракціями по 1,8-2 Гр/фракцію залежно від наявності пухлинних клітин у краї резекції.
Нерезектабельний рак
У разі усіх пухлин, незалежно від локалізації, можна проводити ПТ із застосуванням 3D-КПТ, IMRT або SBRT.
Променева терапія в режимі стандартного фракціонування з одночасною хімієтерапією на основі фторпіримідину у стандартній чи високій дозі є прийнятним варіантом при внутрішньопечінкових і позапечінкових пухлинах.
Гіпофракціоноване опромінення фотонами є прийнятним варіантом у разі внутрішньопечінкових пухлин, але проводити лікування рекомендовано в центрах із відповідним досвідом та обладнанням з наявністю систем контролю дихання пацієнта та КТ конусним пучком, cone beam CT.
Паліативну ПТ призначають для контролю симптомів та/або запобігання ускладненням метастатичних уражень, наприклад, уражень кісток або головного мозку.
Дозування ПТ – залежно від можливості дотримуватися граничних доз для здорового органа та з урахуванням основних функцій печінки:
Стандартне фракціонування (післяопераційне або при нерезектабельних пухлинах):
- початкові дози – до 45 Гр по 1,8 Гр/фракцію;
- буст – до 50-60 Гр по 1,8-2 Гр/фракцію.
Гіпофракціонування (при нерезектабельних пухлинах): 58-67,5 Гр у 15 фракціях для отримання середньої біологічно еквівалентної дози 80,5 Гр.
SBRT (для нерезектабельних пухлин):
- 30-50 Гр (зазвичай у 3-5 фракціях).
Розділ ІV. Подальше спостереження пацієнтів із карциномами гепатобіліарного тракту та раком жовчного міхура
Положення СМД. Спостереження пацієнтів із КГТ, які завершили курс радикального лікування і не мають ознак продовження хвороби, здійснює лікар загальної практики – сімейний лікар, лікар-онколог. Подальше спостереження пацієнтів, які мають ризик рецидиву після оперативного втручання та отримують ад’ювантну терапію, здійснюється виключно у ЗОЗ, що надають спеціалізовану медичну допомогу онкологічним хворим.
Обґрунтування. Регулярні огляди відповідно до плану спостереження сприяють ранньому виявленню рецидиву захворювання та/або метастазів. Процедури, показані під час контрольних візитів, проводять залежно від клінічної ситуації. Під час кожного наступного візиту обов’язково враховують історію хвороби включно із психологічними аспектами, ознаками прогресування захворювання й ускладненнями, пов’язаними з лікуванням. Подальше спостереження відбувається за клінічними показаннями.
Критерії якості медичної допомоги
Обов’язкові
- Подальше спостереження за пацієнтами, яким було проведено обширну холецистектомію через РЖМ, має включати проведення візуалізаційних досліджень (КТ/МРТ черевної порожнини і таза із внутрішньовенним контрастом, КТ органів грудної клітки з або без контрасту) кожні 3-6 місяців впродовж двох років, а потім щороку впродовж п’яти років або за клінічними показаннями.
- У разі рецидиву або прогресування захворювання необхідно розглянути доцільність повторної діагностики за схемою початкового обстеження.
- За необхідності розглянути доцільність визначення рівнів РЕА та CA 19-9 за клінічними показаннями.
- У разі прогресування/рецидиву захворювання лікування пацієнта здійснюють відповідно до алгоритму лікування нерезектабельного або метастатичного захворювання.
- Пацієнти, у яких РЖМ був виявлений випадково за результатами патоморфологічного дослідження, що мають стадію T1a (пухлини без інвазії в м’язовий шар), за умови негативних країв резекції можуть переходити під спостереження.
- Для визначення резектабельності під час діагностики ППХК використовують стандартизований протокол радіологічного звіту (панель 4).
Панель 4
Стандартизований протокол радіологічного звіту під час діагностики ППХК для визначення резектабельності
1. Рівень ураження жовчних проток (за класифікацією Бісмут –Корлетт):
- пухлина локалізована в загальній чи печінковій жовчній протоці;
- наявність поширення пухлини на праву або ліву дольові протоки;
- наявність поширення пухлини на гілки другого порядку і бік ураження.
2. Пухлина щодо ворітної вени: прилежання/охоплення пухлиною головної/правої/лівої гілок ворітної вени і ступінь залучення.
3. Пухлина щодо печінкової артерії:
- залучення загальної печінкової артерії/власної печінкової артерії та ступінь залучення;
- залучення правої/лівої печінкової артерії та ступінь залучення;
- наявний варіант артеріальної анатомії.
4. Лімфатичні вузли: збільшені регіонарні (N1/2) або віддалені (M1).
5. Оцінювання віддалених метастазів.
Під час проведення системної терапії рекомендовано періодично виконувати контрольне радіологічне дослідження (КТ/МРТ кожні два або три місяці терапії, на розсуд клінічного онколога) для оцінювання відповіді захворювання на лікування.
Гістологічні варіанти, визнані ВООЗ
1. Аденокарцинома біліарного типу (~ 75%):
- схожа на аденокарциному підшлункової залози;
- включає аденокарциному, NOS (найчастіше), папілярну, мікропапілярну;
- складається з канальців (встелених клітинами кубічної або стовпчастої форми), вбудованих у десмопластичну строму;
- помірно диференційований тип є більш поширеним, але має широкий гістологічний спектр, від оманливо м’якого до низькодиференційованого.
2. Аденокарцинома кишкового типу: тубули, вистелені стовпчастими клітинами з подовженими гіперхроматичними ядрами, дуже схожі на аденокарциноми товстої кишки.
3. Муцинозна карцинома: складається з > 50% позаклітинного муцину.
4. Світлоклітинний рак: прозорі клітини в альвеолярному розташуванні, розділені кровоносними судинами, подібні за зовнішнім виглядом до метастатичного світлоклітинного раку нирки.
5. Каблучкоподібна карцинома: компонент, що переважає або є винятковим, – каблучкоподібні клітини.
6. Гепатоїдна карцинома: 50% із великою кількістю еозинофільної цитоплазми, збільшеними ядрами та помітними ядерцями, розташованими у формі трабекули.
7. Саркоматоїдна карцинома (карциносаркома): переважна морфологія веретеноподібних клітин із гетерологічною диференціацією або без неї (наприклад, скелетні м’язи, кістки та хрящі).
Затверджено наказом Міністерства охорони здоров’я України від 01.04.2025 р. № 565
Перегляд стандарту медичної допомоги заплановано на 2029 р.
Текст адаптовано і уніфіковано відповідно до стандартів Тематичного випуску Медичної газети «Здоров’я України».
Друкується скорочено. Повний текст за посиланням: https://www.dec.gov.ua/wp-content/uploads/2025/04/dn_565_01042025_dod.pdf
Тематичний номер «Онкологія. Гематологія. Хімієтерапія» № 4 (97) 2025 р.