30 грудня, 2021
Сучасні підходи до лікування хворих на доброякісну гіперплазію передміхурової залози
 Лікування захворювань передміхурової залози залишається одним із пріоритетних напрямків сучасної медицини. Понад 50% усіх пацієнтів урологічного профілю в нашій країні становлять хворі на доброякісну гіперплазію передміхурової залози.
Лікування захворювань передміхурової залози залишається одним із пріоритетних напрямків сучасної медицини. Понад 50% усіх пацієнтів урологічного профілю в нашій країні становлять хворі на доброякісну гіперплазію передміхурової залози.
Ключові слова: доброякісна гіперплазія передміхурової залози, тамсулозин, фінастерид, дутастерид, соліфенацин.
Доброякісна гіперплазія передміхурової залози (ДГПЗ) – одне з найпоширеніших хронічних захворювань у чоловіків, яке призводить до збільшення передміхурової залози (ПЗ) доброякісного генезу, простатичної обструкції та виникнення симптомів нижніх сечових шляхів (СНСШ). Поширеність цієї патології зростає з віком. Вікова залежність розвитку захворювання, за даними гістологічних досліджень, коливається від 20% у чоловіків 41-50 років до 50% у віці 51-60 років і перевищує 90% у чоловіків віком від 80 років (Novara G. et al., 2006). В Україні станом на 2016 рік захворюваність на ДГПЗ дорівнювала 281,5 випадку на 100 тис. чоловічого населення. СНСШ включають симптоми накопичення (збільшення частоти сечовипускання, нічна полакіурія, імперативні позиви та імперативне нетримання сечі) та симптоми, що виникають під час та після сечовипускання (утруднене сечовипускання, ослаблення струменя сечі, сечовипускання краплями, відчуття неповного спорожнення сечового міхура). У більшості літніх чоловіків виявляється, як правило, декілька симптомів (Sociеtе Internationale d’Urologie, 2013), однак у більшості випадків вони легкі або помірно виражені й не значно турбують пацієнта (De Ridder D. et al., 2015). СНСШ можуть прогресувати динамічно: у деяких людей вони зберігаються і посилюються протягом тривалого періоду часу, а в інших минають.
Відповідно до настанов Американської урологічної асоціації (AUA) та Європейської асоціації урології (EAU), сучасна класифікація ДГПЗ ґрунтується на наступних критеріях:
- тяжкість СНСШ за Міжнародною шкалою оцінки простатичних симптомів (IPSS): слабко виражені (0-7 балів); помірні (8-19 балів); тяжкі (20-35 балів);
- наявність залишкової сечі: відсутня, <200 мл, >200 мл;
- розміри ПЗ: <30 мл, 31-80 мл, >80 мл;
- показники урофлоуметрії: максимальна швидкість потоку сечі (Qmax) не порушена; Qmax <15 мл/с; Qmax <10 мл/с;
- наявність/відсутність ретенційних змін у верхніх сечових шляхах: уродинаміка не порушена, наявність уретерогідронефрозу;
- наявність/відсутність епізодів гострої затримки сечі (ГЗС);
- наявність/відсутність порушень функції нирок, таких як хронічна ниркова недостатність (ХНН);
- наявність/відсутність супутніх ускладнень (ГЗС, ішемічна хвороба серця, гематурія, інфекційно-запальні процеси сечовивідних шляхів, ХНН, камінь у сечовому міхурі, гідронефроз та ін.).
Відповідно до сучасних настанов (EAU, 2021) лікувальна тактика хворих на ДГПЗ передбачає консервативне (динамічне спостереження, модифікація способу життя, дієта, фармакологічні засоби) та хірургічне лікування. Динамічне спостереження показано пацієнтам із неускладненими СНСШ легкої та помірної вираженості, які бажають відкласти призначення лікування. Модифікація способу життя з/без медикаментозного лікування зазвичай є методом першого вибору.
Хірургічне лікування проводиться у пацієнтів із вираженою симптоматикою, із залученням у процес верхніх сечовивідних шляхів, коли є підстави припускати, що консервативне лікування буде неефективним.
Медикаментозна терапія може бути показана пацієнтам із помірно вираженими СНСШ, за відсутності показань або за наявності протипоказань до хірургічного лікування. Ця найбільша група пацієнтів становить 60-70%. Успішність фармакологічного лікування й задоволеність пацієнта напряму залежать від правильно обраної тактики в кожному конкретному випадку. Персоніфіковане медикаментозне лікування хворих, які страждають від СНСШ, визначається за результатами проведених діагностичних обстежень, з урахуванням переважання певних симптомів та особистих вподобань пацієнтів.
Алгоритм лікування чоловіків зі СНСШ відповідно до даних доказової медицини та профілів пацієнтів представлений на рисунку.
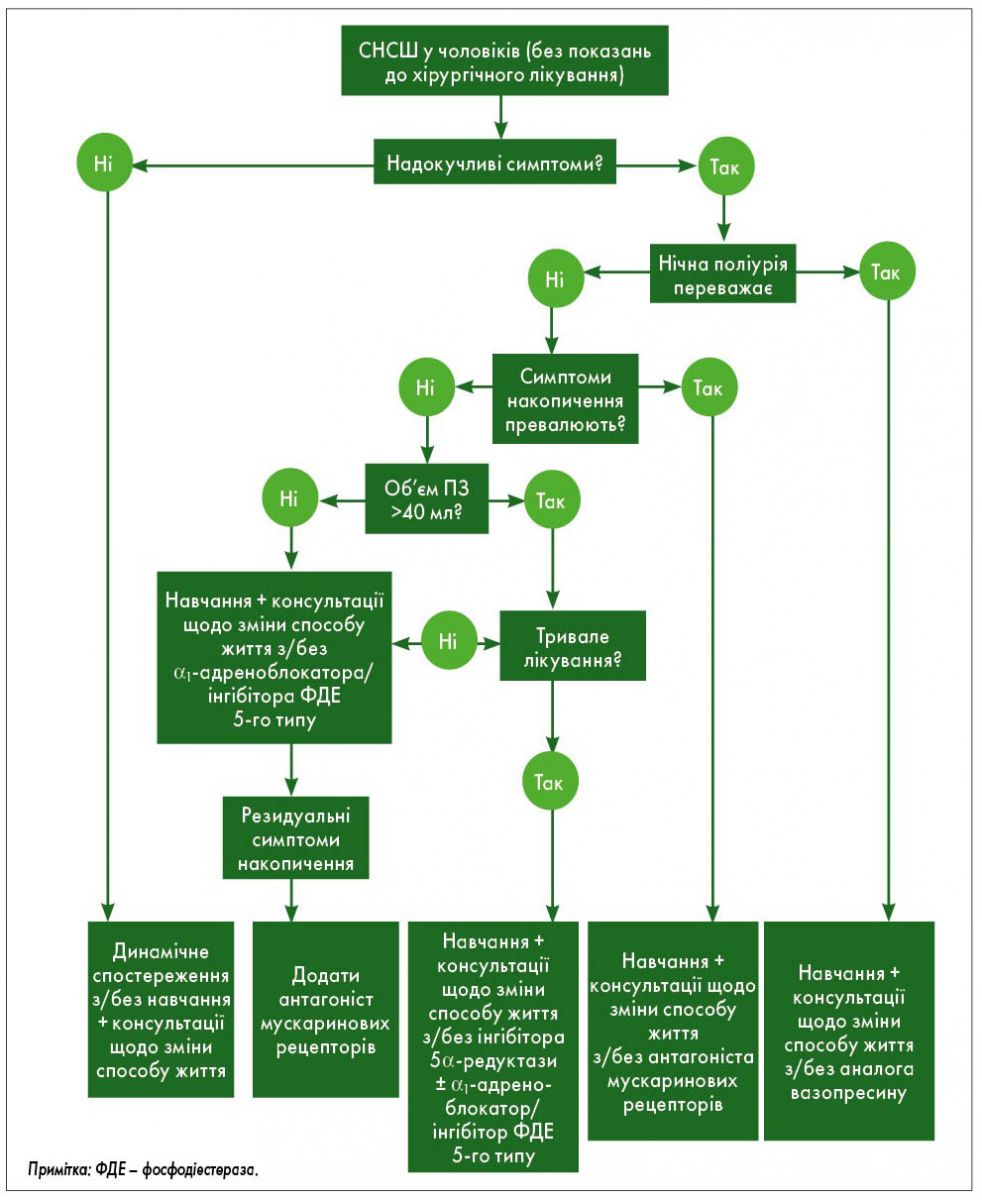 Рис. Алгоритм медикаментозного й/або консервативного лікування СНСШ у чоловіків
Рис. Алгоритм медикаментозного й/або консервативного лікування СНСШ у чоловіків
Альфа-адреноблокатори
Основна мета медикаментозної терапії у хворих на ДГПЗ полягає в усуненні СНСШ у короткі терміни, зведенні до мінімуму побічних ефектів лікування, запобіганні розвитку ускладнень та підтриманні якості життя пацієнтів на високому рівні. На сьогодні застосування α1-адреноблокаторів є засобом першого вибору при консервативній терапії хворих на ДГПЗ завдяки швидкому початку дії, хорошій ефективність, низькій частоті та тяжкості побічних ефектів (EAU, 2021). Блокування α-адренорецепторів, розташованих у гладком’язових волокнах шийки сечового міхура та ПЗ, викликає релаксацію гладкої мускулатури, внаслідок чого відбувається швидке зменшення вираженості СНСШ й підвищення якості життя пацієнта.
Зазвичай ця група препаратів показана хворим із помірними та тяжкими СНСШ. Відповідно до результатів дослідження P. Dahm et al. (2017), при застосуванні α1-адреноблокаторів відбувається зменшення бала за IPSS на 30-40% від початкового рівня та збільшення Qmax приблизно на 20-25%. Хоча остаточне поліпшення стану може спостерігатися через кілька тижнів, виражена дія препаратів порівняно із плацебо проявляється вже у період від кількох годин до декількох днів. Ці препарати здатні покращувати як симптоми накопичення, так і спорожнення, але їх ефективність вища у пацієнтів із невеликим об’ємом ПЗ. Хоча, за даними досліджень із тривалістю спостережень менше року, ефективність α1-блокаторів не залежить від розміру ПЗ, при більш тривалому терміні лікування їх ефективність була вищою у пацієнтів із об’ємом ПЗ <40 мл (Boyle P. et al., 2001; Roehrborn C.G. et al., 2008, 2010). Ефективність α1-адреноблокаторів не залежить від віку. Також вони не зменшують розмір ПЗ.
Із використовуваних сьогодні у клінічній практиці α1-адреноблокаторів найкраще співвідношення ефективності та переносимості має тамсулозин, тому він призначається частіше за інші препарати даної групи (Djavan B., 2004). Популярність препарату зумовлена поєднанням позитивної дії на симптоми ДГПЗ, мінімального негативного впливу на серцево-судинну систему та відсутності взаємодії з антигіпертензивними засобами (Chapple C.R.M. et al., 1996; Lowe F.C., 1997; Narayan P. et al., 2005). Остання властивість зумовлена високою селективністю тамсулозину до адренергічних рецепторів підтипу α1A. Це перший препарат, що був розроблений спеціально для лікування СНCШ, спричинених ДГПЗ.
Серед лікарських засобів урологічної групи тамсулозин представлений препаратом Фокусин (виробництво компанії «Зентіва»).
Інгібітори 5α-редуктази
Пацієнтам із помірними або сильно вираженими СНСШ та збільшеною ПЗ (>40 мл) або підвищеним рівнем простат-специфічного антигена (ПСА >1,4-1,6 нг/мл) показаний прийом інгібіторів 5α-редуктази (5-АРІ) (EAU, 2021). Їх застосування може запобігати прогресуванню захворювання, знижувати ризик виникнення ГЗС та зменшувати ризик хірургічного втручання.
Такі ефекти пов’язані з інгібуючим впливом на 5α-редуктазу, ключовий у перетворенні тестостерону на дигідротестостерон фермент, який стимулює активність ДНК у ядрах клітин ПЗ та їх ріст, а також пригнічує апоптоз. При блокуванні цього ферменту пригнічуються проліферативні процеси, індукується апоптоз, а об’єм ПЗ зменшується (Неймарк А.И., 2020).
За умови нормальної переносимості ці препарати необхідно приймати тривало або довічно, оскільки ефект від їх застосування починає проявлятися не раніше ніж через 6-12 міс від початку лікування. Необхідно попереджати пацієнтів, що застосування коротких курсів 5-АРІ є недоцільним. Це єдина група препаратів, здатних зменшити об’єм ПЗ на 18-28%, що запобігає подальшому прогресуванню ДГПЗ. На фоні терапії 5-АРІ відбувається зменшення суми балів за IPSS на 15-30% та збільшення Qmax на 1,5-2 мл/с (EAU, 2021).
Для клінічного застосування доступні два препарати 5-АРІ: дутастерид та фінастерид.
Найбільш значущі результати стосовно ефективності й безпечності фінастериду отримані в дослідженнях PLESS (McConnell J.D. et al., 1998) та MTOPS (McConnell J.D. et al., 2003). Метою подвійного сліпого рандомізованого плацебо-контрольованого дослідження MTOPS, у якому взяли участь 3047 пацієнтів, було вивчення впливу медикаментозної терапії на прогресування ДГПЗ. Учасники були розподілені на чотири групи: прийом доксазозину (4-8 мг/добу), фінастериду (5 мг/добу), комбінації даних препаратів та плацебо. Період спостереження склав п’ять років. Вчені зіставляли вираженість симптомів за шкалою IPSS, об’єм ПЗ, а також динаміку клінічного прогресування захворювання. Останнє визначалося як збільшення суми балів за шкалою IPSS, виникнення ГЗС, гострої ниркової недостатності, пов’язаної із ДГПЗ, рецидивуючих інфекцій сечових шляхів, нетримання сечі. Відповідно до результатів дослідження, фінастерид знижував відносний ризик ГЗС на 68% і необхідність операції на 64%. Найбільш виражене зменшення об’єму ПЗ (-16%) було відзначено у групі фінастериду. Крім того, нещодавніми дослідженнями було встановлено, що прийом фінастериду може зменувашити втрату крові під час трансуретрального хірургічного втручання на ПЗ, ймовірно, через його вплив на васкуляризацію залози (Khwaja M.A. et al., 2016).
На українському ринку якісний препарат фінастериду представлений під торговою назвою Пенестер (виробництво компанії «Зентіва»).
Комбінація: альфа-адреноблокатор + інгібітёор 5α-редуктази
Пацієнтам із надокучливими помірними або тяжкими СНСШ, збільшеною ПЗ (>40 мл) та ризиком її подальшого збільшення призначають комбінацію α1-адреноблокатора та 5-АРІ (EAU, 2021).
Різні та комплементарні механізми дії 5-АРІ та α-адреноблокаторів є потужним, раціональним обґрунтуванням для комбінованої терапії. Така терапія перевершує монотерапію при тривалих термінах спостереження, демонструючи хороші результати щодо ефективності та безпеки у пацієнтів зі збільшеним розміром ПЗ та високим ризиком прогресування ДГПЗ. Застосування α-адреноблокатора дає ефект зниження симптомів аденоми ПЗ уже через кілька днів, розслаблюючи гладкі м’язи залози, хоча й не зменшуючи її розмір. Натомість 5-АРІ протягом кількох місяців лікування призводить до зменшення ПЗ у розмірах.
До найбільших досліджень, у яких було підтвердено переваги комбінованої терапії, відносяться MTOPS та CombAT. У дослідженні CombAT взяли участь 4844 пацієнти старше 50 років, які методом рандомізації були розподілені на три групи (Roehrborn C.G. et al., 2008, 2010):
- комбінована терапія (дутастерид 0,5 мг/добу + тамсулозин 0,4 мг/добу, n=1610);
- монотерапія дутастеридом (0,5 мг/добу, n=1623);
- монотерапія тамсулозином (0,4 мг/добу, n=1611).
Було проведено порівняльний аналіз можливостей комбінованої терапії та монотерапії 5-АРІ та α1-адреноблокатором щодо віддалених результатів захворювання (ГЗС, необхідність хірургічного лікування) у пацієнтів із високим ризиком прогресування ДГПЗ. Лікування проводилося протягом 48 міс. Дослідження CombAT продемонструвало ефективність довгострокової комбінованої терапії як щодо суб’єктивних даних, так й об’єктивних параметрів оцінки сечовипускання. Одночасний прийом дутастериду і тамсулозину виявився ефективнішим у поліпшенні симптомів, що проявилося статистично значущим зниженням сумарного бала за IPSS порівняно з кожним із варіантів монотерапії (p<0,001). Було показано, що порівняно з монотерапією тамсулозином через 4 роки комбінована терапія дутастеридом/тамсулозином знижувала відносний ризик ГЗС на 68%, хірургічного втручання із приводу ДГПЗ – на 71% та прогресування симптомів – на 41%.
Необхідність постійного тривалого прийому препаратів зумовлює актуальність питання вартості лікування. Зазвичай висока ціна обмежує застосування оригінальних препаратів. У такому випадку альтернативою є генерики, що виготовляються за стандартами Належної виробничої практики (GMP).
Саме таким препаратом є комбінація дутастериду/тамсулозину, який має назву Дутастерид Т (виробництво компанії «Зентіва»).
Антагоністи мускаринових рецепторів
У пацієнтів із помірними та тяжкими СНСШ, серед яких переважають симптоми накопичення, доцільним є призначення антагоністів мускаринових рецепторів. Холіноблокатори у таких хворих із наявними проявами гіперактивного сечового міхура (ГАСМ) зменшують ургентніть, ургентне нетримання сечі та частоту сечовипускань у денний час, що значно покращує якість життя (EAU, 2021).
Антагоністи мускаринових рецепторів вже понад 20 років є препаратами вибору в лікуванні ГАСМ, проте раніше їх застосування переважно вивчали у жінок. Це зумовлено існуючою думкою про те, що генез СНСШ у чоловіків викликаний виключно захворюваннями ПЗ, і, відповідно, лікувати їх пропонувалося лише простатоспецифічними препаратами. Проте наукових даних на користь такого припущення немає (Chapple C.R. et al., 2006). При додатковому аналізі досліджень із відкритим прийомом, до яких входили пацієнти із симптомами ГАСМ, було показано, що на ургентність, частоту сечовипускання або імперативне нетримання сечі впливає вік, а не стать пацієнтів (Veenboer P.W. et al., 2014).
Препарати з антимускариновою активністю дозволяють впливати на скорочувальну здатність сечового міхура та зменшувати вираженість спонтанних скорочень детрузора, що спостерігаються при ГАСМ. При їх призначенні відзначається позитивна динаміка щодо ноктурії, частоти денних сечовипускань та вираженості ургентності. Відзначено також деяке зменшення сумарного бала за IPSS. Основний принцип дії препаратів цієї фармакотерапевтичної групи – блокування провідності по волокнах парасимпатичної нервової системи. Їх застосування потребує ультразвукового моніторингу кількості залишкової сечі. М-холіноблокатори, або «медикаментозні засоби з антихолінергічною активністю», можуть призначатися як терапія першої лінії у пацієнтів із вираженими розладами сечовипускання фази накопичення за відсутності або мінімальної вираженості розладів фази спорожнення. У великому рандомізованому клінічному дослідженні було показано, що соліфенацин значно покращує середні показники відчуття стану сечового міхура, середні оцінки за опитувальником щодо ГАСМ та загальне сприйняття порушень з боку сечового міхура (Kaplan S.A. et al., 2010).
Ще одним показанням для призначення антагоністів мускаринових рецепторів є СНСШ, що зберігаються після місяця безперервної терапії α1-адреноблокаторами в активному терапевтичному дозуванні. Так, у метааналізі 16 досліджень пацієнтів із ДГПЗ/ГАСМ (n=3548) показано, що первинна комбінована терапія α1-адреноблокатором і холіноблокатором перевершує за ефективністю монотерапію α1-адреноблокатором щодо симптомів накопичення та якості життя, не викликаючи при цьому порушень функції сечовипускання (Kim H.J. et al., 2017).
Серед лікарських засобів урологічної групи виробництва компанії «Зентіва» соліфенацин представлений препаратом Солецист.
Запорукою успішного лікування і тривалого ефекту медикаментозної терапії хворих на ДГПЗ є довготривалість і комплаєнтність. Значну роль в останньому відіграє баланс між якістю та доступністю ліків, коли покращення стану здоров’я й якості життя пацієнта напряму залежить від ефективності, безпечності та доступності лікарських засобів. На сьогодні фармацевтичний ринок України поповнився цілим рядом високоякісних генериків, що входять в основний перелік препаратів, рекомендованих для лікування хворих на ДГПЗ. Це значно розширює вибір і доступність лікарських засобів належної якості для максимальної кількості пацієнтів, що їх потребують.
Тематичний номер «Урологія. Нефрологія. Андрологія» № 4 (25), 2021 р.



