17 квітня, 2025
Простамол® Уно: доведені переваги стандартизованого спиртового екстракту Serenoa repens у лікуванні ДГПЗ
Доброякісна гіперплазія передміхурової залози (ДГПЗ) – це збільшення об’єму передміхурової залози (ПЗ) доброякісного генезу, яке відбувається за рахунок розростання її періуретральної залозистої зони, що може спричиняти простатичну обструкцію та симптоми нижніх сечових шляхів (СНСШ). Фітотерапія для лікування симптомів, пов’язаних із ДГПЗ, є поширеною практикою в усьому світі. Екстракт ягід американської пальми пилкоподібної, або карликової пальми, Serenoa repens зарекомендував себе як дієвий засіб для полегшення проявів ДГПЗ та запобігання її прогресуванню. Належний контроль виробництва та відповідність вимогам Європейського агентства лікарських засобів щодо стандартизації рослинних екстрактів грають вирішальну роль щодо очікуваної ефективності та доброї переносимості фітопрепаратів на основі Serenoa repens.
Ключові слова: доброякісна гіперплазія передміхурової залози, симптоми нижніх сечових шляхів, фітотерапія, стандартизований спиртовий екстракт Serenoa repens, Простамол® Уно.
ДГПЗ: сучасні підходи до лікування
Перебіг ДГПЗ характеризується повільним прогресуванням симптомів, що в разі неадекватного лікування може призводити до серйозних наслідків, таких як гостра затримка сечі або інфекційно-запальні процеси сечовивідних шляхів. ДГПЗ негативно впливає на здоров’я чоловічої популяції в цілому, зокрема на фізичний та емоційний стан чоловіка, суттєво погіршуючи якість життя [1]. За статистикою, у Європі 30% чоловіків старше 50 років (близько 26 млн осіб) страждають від докучливих СНСШ, включаючи симптоми накопичення (часте сечовипускання, ургентні позиви та ніктурія) і симптоми спорожнення (утруднене сечовипускання, слабкий струмінь сечі, напруження до сечовипускання та тривалий акт сечовипускання) [2].
Лікування пацієнтів з СНСШ внаслідок ДГПЗ передбачає урахування наявних симптомів, їх ступеня вираженості та впливу на якість життя пацієнта. Початкова терапія включає консервативні (зміна способу життя), фітотерапевтичні (Serenoa repens) та фармакологічні (a-блокатори та інгібітори 5a-редуктази) опції [3]. Якщо пацієнт не відповідає на це лікування та в разі виникнення ускладнень, зокрема гострої затримки сечі, рецидивуючої інфекції сечовивідних шляхів, каменів у сечовому міхурі або дивертикулів, гематурії або ниркової недостатності, розглядаються варіанти хірургічного втручання [4].
Згідно з актуальними настановами, фітотерапія (Serenoa repens) є рекомендованим підходом у випадках, коли пацієнти хочуть уникнути побічних ефектів інших методів лікування, тому вони мають бути чітко проінформовані про корисні властивості та переваги використання Serenoa repens [2].
Існує близько 30 фітотерапевтичних сполук, доступних для лікування ДГПЗ, але одним із найбільш широко використовуваних та добре вивчених є екстракт плодів американської карликової пальми Serenoa repens, яка також відома під своєю ботанічною назвою Sabal serrulatum.
Лікувальні властивості екстракту Serenoa repens
Основним діючим компонентом екстракту Serenoa repens є поліненасичені жирні кислоти. Механізм їхньої дії є комплексним і включає антиандрогенний, антипроліферативний, протизапальний та протинабряковий ефекти. Активність різних екстрактів може відрізнятися, ймовірно, залежно від вмісту жирних кислот. Антиандрогенний ефект екстракту Serenoa repens був продемонстрований у дослідженні in vitro, де він дозозалежно інгібував внутрішньоклітинне зв’язування дигідротестостерону з цитозольними та ядерними рецепторами в культурі клітин із крайньої плоті [5]. Bayne et al. (1999) довели, що Serenoa repens значною мірою інгібує обидва ізомери 5a-редуктази I і II типів і не впливає на секрецію простат-специфічного антигена епітеліальними клітинами, навіть після стимуляції тестостероном [6]. Було виявлено, що морфологія клітин, які зазнали дії фітопрепарату на основі екстракту Serenoa repens, помітно відрізняється від такої в контрольних зразках. У таких клітинах учені виявили значне накопичення ліпідів у цитоплазмі та поширене пошкодження внутрішньоклітинних мембран, включаючи мітохондріальні та ядерні.
Dedhia et al. (2008) встановили, що Serenoa repens пригнічує перетворення тестостерону на дигідротестостерон [7] і сприяє дозозалежному інгібуванню 5a-редуктази у стромі та епітелії ПЗ [8]. Так, середній інгібуючий ефект етанольного екстракту в концентрації 500 мкг/мл складав приблизно 29% в епітелії та 45% у стромі. Інгібування 5a-редуктази (антиандрогенний ефект) відбувається за рахунок основного діючого компонента Serenoa repens – поліненасичених жирних кислот (рис. 1).
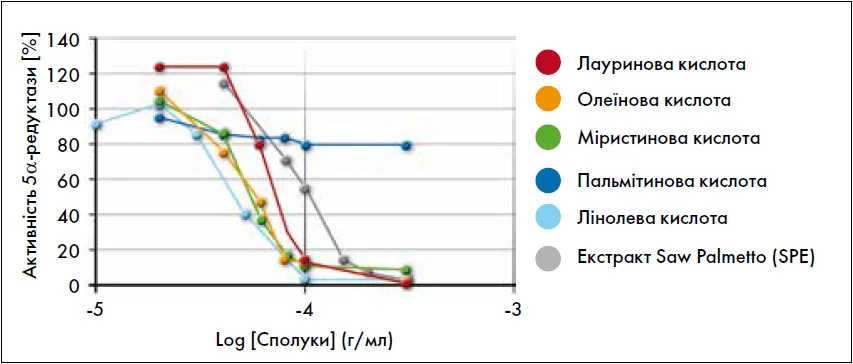 Рис. 1. Інгібування активності 5a-редуктази під впливом вільних жирних кислот та екстракту Serenoa repens (адапт. за Abe et al., 2009)
Рис. 1. Інгібування активності 5a-редуктази під впливом вільних жирних кислот та екстракту Serenoa repens (адапт. за Abe et al., 2009)
Ступінь пригнічення 5a-редуктази відрізняється залежно від екстракту (гексан, етанол, CO2): за висновками Koch et al. (1995), показник інгібування спиртового екстракту був вищим, ніж гексанового (71 та 59 мкг/мл відповідно).
Протизапальний і протинабряковий ефекти екстракту Serenoa repens зумовлені його здатністю інгібувати ферменти арахідонового каскаду в клітинах ПЗ: фосфоліпазу А2, циклооксигеназу та ліпооксигеназу [9, 10]. Згідно з висновками Di Silverio et al. (1993), екстракт Serenoa repens здатний знижувати вміст доступного глобуліну, що зв’язує статеві гормони [11]. Ще один механізм дії екстракту Serenoa repens – це вплив на апоптоз за допомогою фактора росту. Vacherot et al. (2000) довели, що в чоловіків зі здоровою ПЗ не було виявлено істотної різниці між показниками апоптозу та проліферації, натомість у хворих на ДГПЗ кількість клітин і показники проліферації були вищими порівняно зі здоровою ПЗ. Учені встановили, що екстракт Serenoa repens, значно пригнічував проліферацію та індукував загибель клітин як в епітелії, так і в стромі [12], а отже, індукція апоптозу та інгібування проліферації клітин, ймовірно, є основою клінічної ефективності Serenoa repens.
Ще однією важливою властивістю Serenoa repens є розслаблення гладкої мускулатури детрузора сечового міхура та ПЗ через a1‑адренергічні рецептори [13].
Чи всі екстракти Serenoa repens однаково ефективні та безпечні?
Відповідь на це питання залежить від процесу виробництва фітопрепаратів. Препарати на рослинній основі, зокрема на основі екстракту Serenoa repens, не втрачають своєї актуальності у сучасній клінічній практиці завдяки доведеній ефективності, високій біодоступності й кращій переносимості у терапевтичних дозах, а також широкому діапазону лікувальних властивостей та меншій кількості побічних ефектів порівняно зі стандартною фармакологічною терапією. Крім того, для фітопрепаратів менш характерні обмеження щодо тривалості застосування та вікової групи. Однак екстракція, тобто вилучення біологічно активних компонентів (БАК) із рослинної сировини, що лежить в основі створення фітопрепаратів, є надзвичайно складним процесом, який має певні ризики. Так, кожен етап екстракції БАК пов’язаний із суттєвим ризиком повної або часткової втрати компонентів через їхню нестабільність і залежність від зовнішніх фізичних та хімічних чинників [14]. Екстракти однієї й тієї ж рослини можуть суттєво різнитися за своїми біологічно активними властивостями через особливості рослинної сировини (географічне походження, умови вирощування) і технологію екстрагування. Повнота та швидкість екстракції значною мірою залежать від тривалості процесу (надмірна тривалість призводить до забруднення витяжок супутніми високомолекулярними сполуками, що може викликати небажані наслідки), в’язкості екстрагента, температурного режиму (спиртова або ефірна екстракція здійснюється при кімнатній температурі, оскільки більш високі показники спричиняють більші втрати екстрагентів), вибору екстрагента, ступеня подрібнення сировини тощо.
Щоб бути впевненим в ефективності та безпеці призначеного фітопрепарату, рослинна лікарська речовина має бути стандартизована відповідно до всіх фармацевтичних вимог до контролю. Стандартизовані екстракти містять певну фіксовану частку активної речовини, чого вдається досягти шляхом високоефективної рідинної та газової хроматографії. Порівняно зі звичайними екстрактами стандартизовані фітопрепарати мають низку абсолютних переваг, зокрема [14]:
- гарантія незмінної якості;
- більш висока концентрація БАК завдяки видаленню баластових речовин;
- здатність зберігатися протягом тривалого періоду;
- більш високий рівень біоактивності;
- легше засвоєння організмом.
Екстракти Serenoa repens – це складні суміші, що складаються переважно з вільних (85%) або етерифікованих (приблизно 2% метилетилових ефірів і 5-6% тригліцеридів) жирних кислот і стандартизуються саме за їх вмістом. Основними вільними жирними кислотами є лауринова (30%), олеїнова (30%), міристинова (10%) і пальмітинова (10%) кислоти. Крім вільних або етерифікованих жирних кислот в екстрактах Serenoa repens також були виявлені тритерпени (1%) і жирні спирти (0,8-1,1%). Разом із тим були описані інші, другорядні компоненти, такі як поліпреноли, каротиноїди, токофероли, вуглеводні та леткі сполуки (1%) [15, 16]. Booker et al. (2014) спостерігали значну гетерогенність у вмісті вільних жирних кислот між різними розчинниками, що значно вплинуло на фінальний продукт [17]. Найвища концентрація моно-, тригліцеридів та вільних жирних кислот була зафіксована в етанольному екстракті, зокрема у Простамол® Уно [18].
Відповідно до Європейської фармакопеї, стандартизованим вважається екстракт Serenoa repens, у якому:
- вміст жирних кислот (загалом) – більше 80% (у тому числі лауринової – більше 23%)
- вміст фітостеринів (загалом) – більше 0,2% (у тому числі b-ситостерину – більше 0,1%).
Експерти Комітету з лікарських засобів рослинного походження (HMPC) встановили, що етанольний екстракт Serenoa repens сприяє полегшенню СНСШ, пов’язаних із ДГПЗ. Традиційне застосування спиртового екстракту Serenoa repens при ДГПЗ обґрунтоване ефективністю та доказами його безпечного використання протягом щонайменше 30 років (включаючи щонайменше 15 років у межах Європейського Союзу). Крім того, використання препарату за показаннями не потребує медичного контролю [19].
В Україні оригінальний стандартизований спиртовий екстракт плодів пальми пилкоподібної Serenoa repens представлений фітопрепаратом Простамол® Уно (виробництво «Берлін-Хемі АГ», Німеччина).
Склад екстракту Serenoa repens та якість фінального продукту значною мірою залежать від дотримання технології виробництва. Простамол® Уно за своїми характеристиками повністю відповідає вимогам Європейського агентства з лікарських засобів (EMA) та HMPC. Завдяки високому контролю якості сировини до процесу екстракції допускається лише 20% зібраних ягід із подальшим негайним початком висушування з метою максимального збереження фітостеролів і жирних кислот, що визначає ефективність фітопрепарату.
Клінічно доведені переваги спиртового екстракту Serenoa repens
Ефективність етанолового екстракту Serenoa repens підтверджена в багатьох контрольованих клінічних дослідженнях. За повідомленням Saidi et al. (2017), у пацієнтів, які приймали спиртовий екстракт Serenoa repens, спостерігалося статистично значуще збільшення середніх значень максимальної та середньої швидкості потоку сечі зі зменшенням об’єму залишкової сечі порівняно з контрольною групою (p<0,05). Автори також відмітили достовірні відмінності в об’ємі ПЗ та оцінці за Міжнародною шкалою оцінки простатичних симптомів (IPSS), які свідчать на користь застосування Serenoa repens [20].
Спиртовий екстракт Serenoa repens довів високий профіль безпеки навіть при трикратному перевищенні клінічної дози: між групами пацієнтів, які приймали 320, 640 і 960 мг препарату щодня або плацебо з інтервалом у 6 міс протягом 18 міс, не було зареєстровано статистично значущих відмінностей у частоті серйозних або незначних побічних ефектів [21].
Широкомасштабний огляд, який включав дані 21 рандомізованого дослідження тривалістю до 48 тижнів за участю понад 3 тис. пацієнтів із ДГПЗ, показав, що застосування Serenoa repens сприяло покращенню оцінки за шкалою IPSS і збільшенню максимального потоку сечі. Побічні ефекти, пов’язані із застосуванням Serenoa repens, були легкими та нечастими, що свідчить про високий профіль безпеки препарату [22] (рис. 2).
![Рис. 2. Результати лікування ДГПЗ екстрактом Serenoa repens за даними Кокранівського огляду [22] Рис. 2. Результати лікування ДГПЗ екстрактом Serenoa repens за даними Кокранівського огляду [22]](/multimedia/userfiles/images/2025/Uro_1_2025/Uro_1_2025_st3_pic2.webp) Рис. 2. Результати лікування ДГПЗ екстрактом Serenoa repens за даними Кокранівського огляду [22]
Рис. 2. Результати лікування ДГПЗ екстрактом Serenoa repens за даними Кокранівського огляду [22]
Важливою перевагою спиртового екстракту Serenoa repens (Простамол® Уно) є відсутність системних побічних ефектів завдяки тропності виключно до клітин ПЗ. Дослідження, проведене у 30 урологічних відділеннях Словаччини, показало, що прийом Простамол® Уно протягом одного року сприяв збільшенню максимального потоку сечі (різниця – 2,31 мл/с до та після лікування), зменшенню об’єму залишкової сечі (різниця – 53,6% до та після лікування) і суттєво полегшував СНСШ [23]. Слід зазначити, що прийом Простамолу Уно не викликав жодних серйозних побічних ефектів і жоден із пацієнтів не припинив лікування через небажані явища.
За результатами 10‑річного обсерваційного дослідження, терапія Простамолом Уно запобігла прогресуванню проявів ДГПЗ як за суб’єктивними (IPSS, шкала якості життя QoL), так і за об’єктивними (розміри ПЗ, швидкість сечовипускання, об’єм залишкової сечі) критеріями. Крім того, побічних ефектів, безпосередньо пов’язаних із застосуванням препарату, у пацієнтів не спостерігалося [24].
Згідно з висновками Aliaev et al. (2009), Простамол® Уно в дозі 320 мг/добу ефективно зменшував прогресування симптомів ДГПЗ, покращуючи якість життя чоловіків. Як повідомили автори, препарат добре переносився й не викликав серйозних побічних ефектів, які змусили б пацієнтів припинити лікування [25].
У трирічному клінічному дослідженні було встановлено, що терапія Простамолом Уно суттєво зменшувала СНСШ, оцінені за шкалою IPSS, поліпшувала якість життя хворих і призупиняла прогресування ДГПЗ, не спричинивши побічних ефектів [26]. Препарат продемонстрував ефективність у купіруванні докучливих СНСШ, зокрема обструктивних, характерних для ДГПЗ у поєднанні з хронічним абактеріальним простатитом [27]. Ефект аналізували за даними анамнезу захворювання, скаргами пацієнтів, результатами пальцевого ректального дослідження ПЗ, оцінкою за шкалами IPSS, QoL, індексу симптомів хронічного простатиту Національного інституту охорони здоров’я США (опитувальник NIH-CPSI), бактеріологічними дослідженнями сечі та секрету ПЗ, а також за показниками урофлоуметрії, ультразвукового дослідження сечового міхура/ПЗ і трансректальної енергетичної доплерографії ПЗ. У ході дослідження було встановлено значне зменшення кількості балів за шкалою IPSS (з 14 до 6,8) та індексу шкали NIH-CPSI (з 18,4 до 12,3), покращення QoL (з 3,9 до 1,9) та підвищення максимального потоку сечі (з 12,4 до 18,2 мл/с). Спектральна доплерографія виявила поліпшення кровотоку ПЗ у 53,3% пацієнтів. При цьому суттєвих побічних реакцій під час застосування препарату зареєстровано не було.
Покращення якості життя та запобігання прогресуванню симптомів за мінімального ризику побічних ефектів – це головні цілі ефективної терапії ДГПЗ. Дієвість і високий профіль безпеки фітопрепарату Простамол® Уно були продемонстровані в багатьох клінічних дослідженнях. Належний контроль виробництва та відповідність вимогам EMA/HMPC щодо стандартизації рослинних екстрактів гарантує якість фітопрепарату Простамол® Уно, забезпечуючи таким чином високу ефективність, добру переносимість і безпечність за відсутності системного впливу.
Література
- Kozminski M.A., Wei J. T., Nelson J., Kent D. M. Baseline characteristics predict risk of progression and response to combined medical therapy for benign prostatic hyperplasia (BPH). BJU Int. 2015 Feb;115(2):308-16. doi: 10.1111/bju.12802. Epub 2014 Aug 13. PMID: 24825577; PMCID: PMC4231026.
- Franco J.V., Trivisonno L., Sgarbossa N. J., Alvez G. A., Fieiras C., Escobar Liquitay C. M., Jung J. H. Serenoa repens for the treatment of lower urinary tract symptoms due to benign prostatic enlargement. Cochrane Database Syst Rev. 2023 Jun 22;6(6): CD001423. doi: 10.1002/14651858.CD001423.pub4. PMID: 37345871; PMCID: PMC10286776.
- Gravas S., Cornu J. N., Gacci M., Gratzke C., Herrmann T. R.W., Mamoulakis C. et al. EAU Guidelines on Management of Non-Neurogenic Male Lower Urinary Tract Symptoms (LUTS), incl. Benign Prostatic Obstruction (BPO). European Association of Urology. Available at: https://uroweb.org/guidelines/management-of-non-neurogenic-male-luts (Accessed 7 June 2023) 2022.
- Lerner L.B., McVary K.T., Barry M.J., Bixler B.R., Dahm P., Das A.K. et al. Management of Lower Urinary Tract Symptoms Attributed to Benign Prostatic Hyperplasia: AUA GUIDELINE PART I-Initial Work-up and Medical Management. Journal of Urology 2021;206(4):806–817. [DOI: 10.1097/JU.0000000000002183].
- Sultan C., Terraza A., Devillier C. et al. Inhibition of androgen metabolism and binding by a liposterolic extract of Serenoa repens B in human foreskin fibroblasts // J. Steroid. Biochem. 1984. Vol. 20. No 1. P. 515-519.
- Bayne C.W., Donnelly F., Ross M., Habib F.K. Serenoa repens (Permixon): a 5alpha-reductase types I and II inhibitor-new evidence in a coculture model of BPH. Prostate. 1999 Sep 1;40(4):232-41. doi: 10.1002/(sici)1097-0045(19990901)40:4<232:aid-pros4>3.0.co;2-0. PMID: 10420151.
- Dedhia R.C., McVary K.T. Phytotherapy for lower urinary tract symptoms secondary to benign prostatic hyperplasia. The Journal of Urology 2008;179:2119-25
- Weisser H., Tunn S., Behnke B., Krieg M. Effects of the sabal serrulata extract IDS 89 and its subfractions on 5 alpha-reductase activity in human benign prostatic hyperplasia. The Prostate 1996;28:300.
- Breu W., Hagenlocher M., Redl K. et al. Anti-inўammatory activity of sabal fruit extracts prepared with supercritical carbon dioxide. In vitro antagonists of cyclooxygenase and 5‑lipoxygenase metabolism // Arzneimittelforschung. 1992. Vol. 42. No 4. P. 547-551.
- Paubert-Braquet M., Mencia Huerta J.M., Cousse H., Braquet P. Effect of the lipidic lipidosterolic extract of Serenoa repens (Permixon) on the ionophore A23187‑stimulated production of leukotriene B4 (LTB4) from human polymorphonuclear neutrophils // Prostaglandins Leukot Essent Fatty Acids. 1997. Vol. 57. No 3. P. 299-304.
- Di Silverio F., Flammia G.P., Sciarra A., Caponera M., Mauro M., Buscarini M., Tavani M., D’Eramo G. Plant extracts in BPH. Minerva Urol Nefrol. 1993 Dec;45(4):143-9. PMID: 7517582.
- Vacherot F., Azzouz M., Gil-Diez-De-Medina S., Colombel M., De La Taille A., Lefrиre Belda M.A., Abbou C.C., Raynaud J.P., Chopin D.K. Induction of apoptosis and inhibition of cell proliferation by the lipido-sterolic extract of Serenoa repens (LSESr, Permixon in benign prostatic hyperplasia. Prostate. 2000 Nov 1;45(3):259-66.
- Roehrborn C.G. Chapter 103: Benign prostatic hyperplasia: etiology, pathophysiology, epidemiology, and natural history. In: Partin AW, Peters CA, Kavoussi LR, Dmochowski RR, Wein AJ, editors(s). Campbell Walsh Wein Urology. 13th edition. Elsevier, 2020.
- https://acosm.ru/obuchenie/statyi/4772.
- Abe M., ItoY., Suzuki A., Onoue S., Noguchi H., Yamada S. Isolation and pharmacological characterization of fatty acids from Saw palmetto extract. Anal. Sci. 2009,25, 553-557.
- Bedner M., Schantz M.M., Sander L.C., Sharpless K.E. Development of liquid chromatographic methods for the determination of phytosterols in standard reference materials containing Saw palmetto. J. Chromatogr. A2008,1192, 74-80.
- Booker A., Suter A., Krnjic A., Strassel B., Zloh M., Said M., Heinrich M. A phytochemical comparison of Saw palmetto products using gas chromatography and 1H nuclear magnetic resonance spectroscopy metabolomic profiling: Saw palmetto – Metabolomic profiling. J. Pharm. Pharmacol. 2014, 811-822.
- Marti Guillaume & Joulia, Philippe & Amiel, Aurйlien & Fabre, Bernard & David, Bruno & Fabre, Nicolas & Fiorini-Puybaret, Christel. (2019). Comparison of the Phytochemical Composition of Serenoa repens Extracts by a Multiplexed Metabolomic Approach. Molecules. 24. 2208. 10.3390/molecules24122208.
- Sabalis serrulatae fructus – herbal medicinal product / European Medicines Agency (EMA). Saw palmetto fruit: summary for the public. 5 April 2016 EMA/823974/2015.
- Saidi S., Stavridis S., Stankov O., Dohcev S., Panov S. Effects of Serenoa repens Alcohol Extract on Benign Prostate Hyperplasia. Pril (Makedon Akad Nauk Umet Odd Med Nauki). 2017 Sep 1;38(2):123-129.
doi: 10.1515/prilozi‑2017-0030. PMID: 28991765. - Avins A.L., Lee J.Y., Meyers C.M., Barry M.J. Safety and Toxicity of Saw Palmetto in the CAMUS Trial, The Journal of Urology, Volume 189, Issue 4, 2013, Pages 1415-1420, ISSN 0022-5347, https://
doi.org/10.1016/j.juro.2012.10.002. - Wilt T., Ishani A., MacDonald R. Serenoa repens for benign prostatic hyperplasia. Cochrane Database of Systematic Reviews 2002, Issue 3. Art. No.: CD001423. doi: 10.1002/14651858.CD001423.
- Breza J. & Kliment Jan & Valansky Ladislav & Capova Gertruda. (2005). Prostamol uno (alcohol extract of the fruits of Serenoa repens) in the treatment of symptomatic benign prostatic hyperplasia. Lekarsky Obzor. 54. 139-144.
- Aliaev Iu.G., Vinarov A.Z., Demidko Iu.L., Spivak L.G. [The results of the 10‑year study of efficacy and safety of Serenoa repens extract in patients at risk of progression of benign prostatic hyperplasia]. Urologiia. 2013 Jul-Aug;(4):32-6. Russian. PMID: 24159762.
- Aliaev Iu. & Apolikhin O. & Mazo E.B. & Vinarov A. & Lokshin K.L. & Medvedev A.A. & Permiakova O.V. & Spivak L. & Shkol’nikov M.E. (2009). Efficacy and safety of prostamol-UNO in the treatment of patients with initial symptoms of prostatic adenoma and risk of progression: 2 years of investigations. Urologii͡a, 1999. 36-40.
- Vinarov A.Z., Aliaev Iu.G., Apolikhin O.I., Mazo E.B., Darenkov S.P., Demidko Iu.L., Lokshin K.L., Medvedev A.A., Permiakova O.V., Spivak L.G., Shkol’nikov M.E. [Results of three-year clinical study of prostamol uno efficacy and safety in patients with initial symptoms of prostatic adenoma and risk of its progression]. Urologiia. 2010 Nov-Dec;(6):3-10. Russian. PMID: 21433319
- Trapeznikova M.F., Dutov V.V., Dolgovq A.G., Urenkov S.B. [Prostamol-Uno treatment in patients with prostatic adenoma and chronic non-infectious prostatitis]. Urologiia. 2008 Sep-Oct;(5):39-42. PMID: 19069494.
Підготувала Дарина Чернікова
Тематичний номер «Урологія. Нефрологія. Андрологія» № 1 (36), 2025 р.




