12 серпня, 2022
Вітчизняний досвід використання едаравону в пацієнтів із гострим коронарним синдромом
 Незважаючи на сучасні методи відновлення коронарного кровотоку, показники смертності після перенесеного гострого коронарного синдрому (ГКС) залишаються досить високими, що пов’язують з ушкодженням міокарда під час реперфузії. Відповідно до сучасних уявлень, провідною причиною цього явища є ішемічний каскад, який може запускати процеси загибелі кардіоміоцитів і бути відповідальним за 50% кінцевого розміру зони некрозу при ГКС, виникнення реперфузійних аритмій, систолічної мікросудинної дисфункції. Саме тому адекватне блокування ішемічного каскаду, спрямоване на елімінацію активних форм кисню, активацію антиоксидантів, на сьогодні вважається важливою складовою менеджменту пацієнтів із ГКС. Одним із найдієвіших блокаторів ішемічного каскаду, що довів свою ефективність у клінічній практиці, є едаравон. Цей препарат внесено до низки клінічних рекомендацій з лікування багатьох захворювань, патогенез яких пов’язаний з ішемічним каскадом.
Незважаючи на сучасні методи відновлення коронарного кровотоку, показники смертності після перенесеного гострого коронарного синдрому (ГКС) залишаються досить високими, що пов’язують з ушкодженням міокарда під час реперфузії. Відповідно до сучасних уявлень, провідною причиною цього явища є ішемічний каскад, який може запускати процеси загибелі кардіоміоцитів і бути відповідальним за 50% кінцевого розміру зони некрозу при ГКС, виникнення реперфузійних аритмій, систолічної мікросудинної дисфункції. Саме тому адекватне блокування ішемічного каскаду, спрямоване на елімінацію активних форм кисню, активацію антиоксидантів, на сьогодні вважається важливою складовою менеджменту пацієнтів із ГКС. Одним із найдієвіших блокаторів ішемічного каскаду, що довів свою ефективність у клінічній практиці, є едаравон. Цей препарат внесено до низки клінічних рекомендацій з лікування багатьох захворювань, патогенез яких пов’язаний з ішемічним каскадом.
Ішемічний каскад у розрізі гострої серцево-судинної патології
Внаслідок різкого розвитку ішемії та припинення надходження до клітини кисню і поживних речовин для енергетичного забезпечення клітин міокарда виникає ціла низка патологічних процесів, об’єднаних спільною назвою «ішемічний каскад». При цьому один процес тягне за собою інший.
Для розуміння шляхів подолання ішемічного пошкодження міокарда необхідно враховувати його механізми, які тісно взаємопов’язані. На сьогодні основними вважаються такі процеси:
- внутрішньоклітинне та мітохондріальне перевантаження Ca2+ – «кальцієвий парадокс» із набряком і некрозом клітин;
- зменшення оксиду азоту (NO) з ендотеліальною дисфункцією та порушенням регіонарного кровотоку;
- відкриття перехідної пори проникності мітохондрій (mPTP);
- активація запальної відповіді.
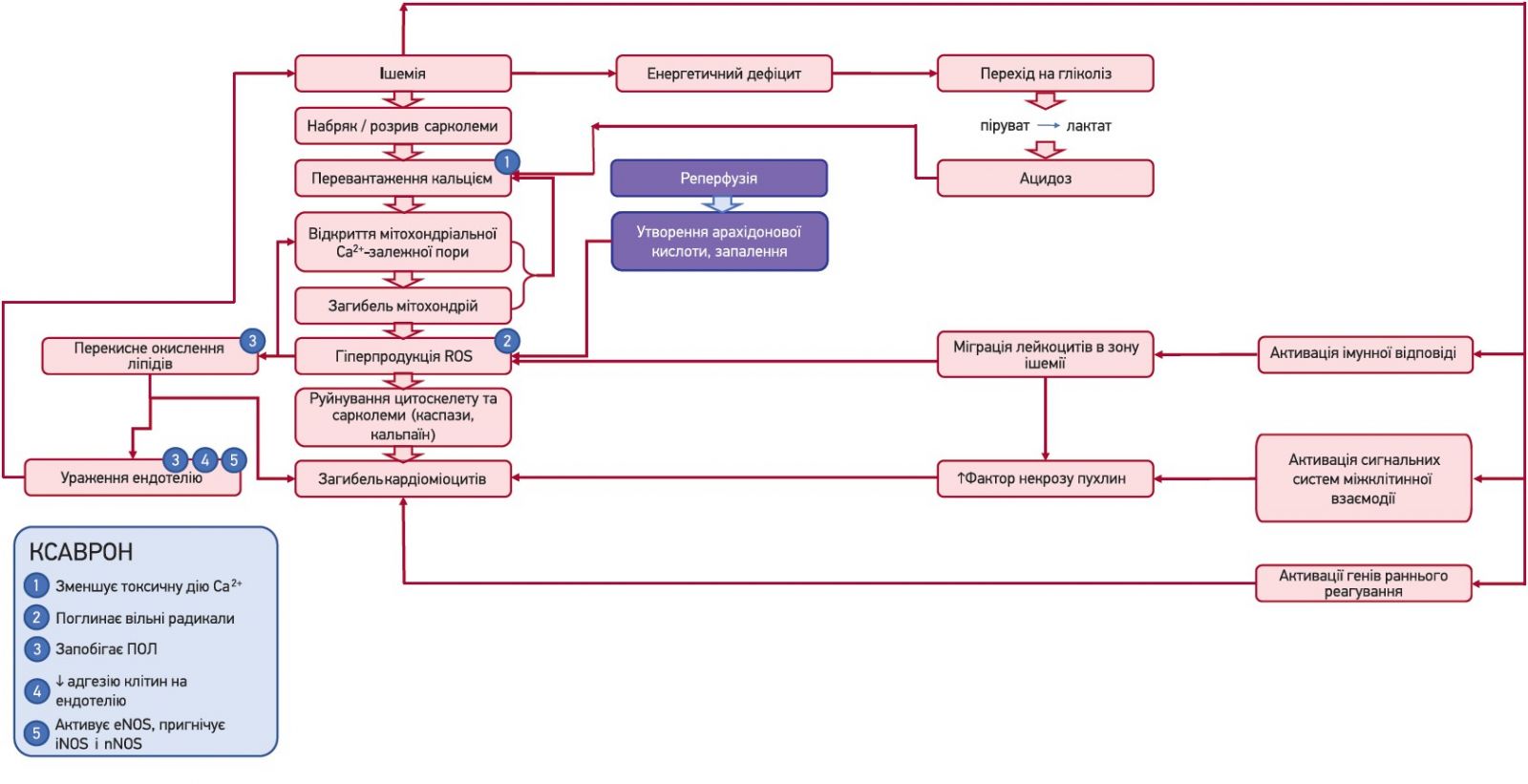
Разом із пошкодженням зовнішніх та внутрішніх мембран клітини Ca2+-перевантаження та відкриття mPTP призводять до масивного набряку, лізису органел, фрагментації та некрозу клітин, що запускає гостру запальну відповідь, наслідки якої також роблять свій внесок у загибель кардіоміоцитів. Через кілька годин після початку реперфузії в зону інфаркту активно мігрують нейтрофіли у відповідь на вивільнення хемоатрактантів (АФК, цитокінів та активованого комплементу). Масивне накопичення нейтрофілів сприяє вивільненню NF‑κB, інших сигнальних молекул і факторів транскрипції, посиленій експресії молекул клітинної адгезії, що веде до подальшої лейкоцитарної інфільтрації, закупорки судин та феномену no-reflow, посилюючи пошкодження тканин (рис.).
Рис. Ішемічний каскад при ГКС
Примітка: ПОЛ – перекисне окислення ліпідів.
Особливе значення ішемічний каскад має у пацієнтів із ГКС, яким виконують медикаментозну реперфузію або перкутанне коронарне втручання, у зв’язку з утворенням арахідонової кислоти та гіперпродукцією активних форм кисню. На перший погляд, швидке відновлення коронарного кровотоку в ішемізованій ділянці міокарда має забезпечувати покращення як безпосередніх, так і віддалених наслідків ГКС. Утім, успіх такого лікування може затьмаритися реперфузійним ушкодженням міокарда (РУМ), патогенез якого пов’язаний передусім з надмірним утворенням АФК та оксидативним стресом. До найпоширеніших проявів РУМ відносять електрофізіологічну нестабільність із розвитком реперфузійних аритмій, систолічну дисфункцію, ендотеліальну та мікросудинну дисфункцію, незворотне ушкодження міокарда. Таким чином, реперфузійне ушкодження призводить до загибелі тих кардіоміоцитів, які ще були життєздатними безпосередньо перед реперфузією міокарда.
Перспективи профілактики ішемічних пошкоджень за допомогою едаравону
Зменшити прояви описаних ушкоджень здатен едаравон, який сприяє блокаді ішемічного каскаду. Препарат має низьку молекулярну масу, є водорозчинним і ліпофільним, що дозволяє йому легко потрапляти всередину клітини.
Крім того, едаравон чинить різноманітний вплив на ланки патогенезу ішемічного каскаду. Сьогодні детально вивчено два основні ефекти препарату: здатність віддавати електрон різним формам АФК (насамперед пероксильному радикалу) та підвищувати синтез оксиду азоту, відновлюючи функцію ендотелію в умовах ішемії (Subcommittee U. P. et al., 2020).
Також слід нагадати, що едаравон здатен забезпечувати стабілізувальний вплив як на самі мітохондрії, так і на перехідну пору мітохондріальної проникності (mPTP), що може захистити клітину від перевантаження Са2+ при РУМ. Саме mPTP вважається перспективною терапевтичною мішенню, оскільки відповідає за реалізацію мітохондріального сигнального шляху апоптозу (Zhang G. M. et al., 2013). Отже, застосування едаравону може захищати клітини різних тканин і від надмірного апоптозу.
Важлива складова ефекту препарату – активація природних антиоксидантних систем у тканинах. Так, в експериментальній роботі з моделюванням ішемії міокарда на пацюках попереднє введення едаравону спричиняло суттєве підвищення активності супероксиддисмутази, глутатіонпероксидази та каталази. Крім того, на тлі введення едаравону значно знижується рівень каспази‑3 (бере участь в активації апоптозу), а також спостерігається нижчий рівень креатинфосфокінази-МВ (КФК-МВ) порівняно з контролем, що є додатковим свідченням його кардіопротекторного ефекту (Hassan M. Q. et al., 2016).
Едаравон продемонстрував свої позитивні ефекти щодо запобігання фероптозу, який є механізмом загибелі клітин і фінальною стадією ішемічного каскаду. Зокрема, було показано, що застосування препарату зменшує рівень Fe2+ та ліпідних і гідроксильних радикалів (Homma T. et al., 2019); це відбувається шляхом прямої донації електронів та нейтралізації вільних радикалів, а також шляхом активації сигнального білка Nrf2, який запускає процеси ядерної транскрипції з синтезом ферментів глутатіонпероксидази (Gpx4), гемоксигенази‑1, що руйнують АФК і пригнічують фероптоз (Zhang G. W. et al., 2016).
На експериментальній моделі атеросклерозу едаравон виявив здатність пригнічувати активацію фактора NF‑κB та iNOS і зменшувати надмірну міграцію макрофагів до зони бляшки, що разом із прямою його антиоксидантною активністю та позитивним впливом на дисфункцію ендотелію сприяє зменшенню атеросклеротичного ураження аорти (Onogi H. et al., 2006).
Отже, едаравон – це блокатор ішемічного каскаду, який також має властивості універсального антиоксиданта та забезпечує цитопротекторний ефект (запобігає апоптозу, фероптозу), протизапальну дію, а також позитивно впливає на судинну стінку. Зазначені ефекти мають важливе значення в лікуванні захворювань, патогенез яких пов’язаний з ішемічним каскадом і синдромом системної запальної відповіді, куди відноситься й ГКС.
Експериментальне застосування едаравону на моделях гострої ішемії міокарда підтвердило його захисні властивості. Введення препарату супроводжувалося зменшенням кількості ушкоджених кардіоміоцитів із фрагментованими органелами та фатальним набряком, апоптотичних клітин (Li Q. et al., 2019). У результаті спостерігалося зменшення розміру зони некрозу при ішемії/реперфузії, частоти фатальних шлуночкових тахіаритмій, подальшого розвитку чи прогресування серцевої недостатності. Зазначені захисні ефекти відзначалися за умови введення едаравону до або одразу після (не пізніше 5 хв) початку реперфузії (González-Montero J. et al., 2018).
Доказова база ефективності едаравону в пацієнтів із ГКС
Пілотне рандомізоване клінічне дослідження, присвячене вивченню короткострокових ефектів едаравону, було проведено у 2004 році японськими науковцями за участю 80 пацієнтів із ГКС. Препарат вводили в дозі 30 мг за 10 хв до початку перкутанного втручання. Тоді вперше підтвердили ефективність превентивного застосування едаравону саме для профілактики реперфузійних аритмій під час інтервенційного лікування ГКС (ризик розвитку реперфузійних аритмій протягом 30 хв після реперфузії зменшувався у 8 разів). Також було показано, що застосування препарату до реперфузійних процедур супроводжується достовірним зменшенням зони некрозу зі зниженням рівня маркерів ушкодження міокарда, зменшенням «оглушення» міокарда зі швидким відновленням його скоротливості (Tsujita K. et al., 2004).
У наступному дослідженні цих же авторів із більшою вибіркою пацієнтів із ГКС (n=101) оцінювали як коротко-, так і довгострокові ефекти застосування едаравону. Було продемонстровано, що на тлі застосування едаравону (протягом 14 днів у гострому періоді) спостерігається суттєве зменшення ризику подальших кардіальних ускладнень у віддаленому періоді (415±32 дні) порівняно із плацебо. Зокрема, знижувалася частота повторного нефатального інфаркту, ішемічного інсульту, рефрактерної стенокардії. Крім того, едаравон у разі його застосування до проведення реперфузії сприяв зменшенню зони інфаркту та ризику реперфузійних аритмій. Автори вважають, що відсутність призначення едаравону є незалежним предиктором розвитку кардіоваскулярних подій після інфаркту міокарда (рефрактерна стенокардія, повторний нефатальний інфаркт міокарда, ішемічний інсульт) протягом 415±32 дні.
У дослідженні Y. Nakamura та співавт. (2009) введення едаравону пацієнтам із ГКС зумовлювало зменшення зони некрозу, запобігало патологічному ремоделюванню міокарда, а також розвитку серцевої недостатності.
Пізніше в декількох клінічних дослідженнях включення едаравону до схеми лікування хворих з інфарктом міокарда в поєднанні з тромболітичною терапією сприяло зменшенню зони некрозу, покращувало фракцію викиду лівого шлуночка, зменшувало ризик фатальних тахіаритмій, а також запобігало повторній госпіталізації у зв’язку з декомпенсацією серцевої недостатності (Cui Y. G., Lu X. N., 2011; Hou H., 2013).
Едаравон виявився ефективним не лише як супровідна терапія тромболізису. Згідно з даними J. Oyama та співавт. (2010), введення препарату пацієнтам зі значимим стенозом коронарних артерій супроводжувалося достовірним покращенням коронарного кровотоку (за даними коронарографії), суттєвим зниженням рівня малональдегіду (маркера перекисного окиснення ліпідів).
У 2015 році C. Zheng і співавт. провели метааналіз 9 однорідних рандомізованих плацебо-контрольованих досліджень (загалом 380 пацієнтів) стосовно клінічного застосування едаравону при гострій ішемії міокарда. Препарат застосовували в дозі 60 мг/добу в хворих із ГКС, котрим проводили перкутанне втручання. Тоді було встановлено, що у групах едаравону спостерігалося достовірне зниження рівня маркерів некрозу міокарда КФК-МВ і тропоніну І через 6 год після реперфузії (3 дослідження) та через 24 год після реперфузії (4 дослідження) порівняно із плацебо. Під час аналізу маркерів окисного стресу виявилося, що на тлі застосування едаравону рівень супероксиддисмутази зростав, а концентрація малональдегіду зменшувалася. Проведений метааналіз доводить антиоксидантні ефекти едаравону та його кардіопротекторні властивості, пов’язані з запобіганням РУМ.
Вітчизняний досвід застосування блокатора ішемічного каскаду едаравону в пацієнтів із ГКС
Українські кардіологи провели клінічну апробацію едаравону в пацієнтів із ГКС. З огляду на те що едаравон сприяє покращенню коронарного кровотоку, про що йшлося в одному із вищезазначених досліджень, препарат призначали як перед реперфузійною терапією ГКС, так і без її проведення. Згодом лікарі описували динаміку електрокардіограми (ЕКГ) та інших параметрів на тлі застосування едаравону, а також свої враження від його призначення.
Визначена форма для внесення результатів застосування препарату едаравон (Ксаврон®) у пацієнтів із ГКС містила такі дані: демографічна частина; діагноз при госпіталізації; діагноз заключний; призначення Ксаврону; тривалість курсу лікування Ксавроном; час від появи симптомів до реперфузії; метод реперфузії; час від введення першої дози Ксаврону до реперфузії; лабораторні дані, інструментальні дослідження; супутнє лікуваня; результати терапії; загальні враження від терапії Ксавроном.
Застосування Ксаврону здійснювали за такою схемою:
- у випадку виконання реперфузії – першу дозу препарату (30 мг/1 ампула) вводили перед реперфузією внутрішньовенно струйно, а в подальшому – по 1 ампулі препарату, розведеного в 100 мл 0,9% хлориду натрію внутрішньовенно крапельно двічі на день (курс 10 днів);
- якщо реперфузію не проводили – по 1 ампулі препарту, розведеного в 100 мл 0,9% хлориду натрію внутрішньовенно крапельно двічі на день, починаючи з 1-го дня госпіталізації (курс 10 днів).
Далі подано серію клінічних випадків, котрі описують практичний досвід ведення пацієнтів із ГКС, до схеми лікування яких було включено препарат Ксаврон®.
Клінічний випадок № 1 (С.С. Кошарська, завідувачка відділення кардіології Київської міської клінічної лікарні № 7)
Жінка 58 років госпіталізована до кардіологічного відділення 15.11.2021.
Діагноз при госпіталізації: ІХС: ГКС з елевацією сегмента ST, Q‑позитивний передньо-перетинково-верхівково-боковий інфаркт міокарда (ІМ).
Діагноз заключний: Q‑позитивний передньо-перетинково-верхівково-боковий ІМ.
Тривалість лікування препаратом Ксаврон®: 10 днів. Реперфузійна терапія не проводилася.
Лабораторні дані: МВ-КФК при госпіталізації (15.11.2021) – 65 од/л. МВ-КФК повторно (29.11.2021) – 30 од/л.
Інструментальні дослідження: зміни на ЕКГ при госпіталізації (15.11.2021) – ритм синусовий, неправильний, елевація сегмента ST на 7 мм у відведеннях V2-V5. Зміни на ЕКГ повторно (30.11.2021) – ритм синусовий, регулярний, частота серцевих скорочень (ЧСС) 78 уд./хв, зберігається негативна елевація сегмента ST у відведеннях V2-V5.
Ультразвукове дослідження (УЗД) серця: при госпіталізації (15.11. 2021) – аорта 3,2 см; аортальний, мітральний і трикуспідальний клапани без структурно-функціональних змін; фракція викиду лівого шлуночка (ФВ ЛШ) 51%; правий шлуночок 2,0 см; середній тиск у легеневій артерії 20 мм рт. ст. Повторно (30.11.2021) – зниження ФВ ЛШ до 41%, потовщення частин перикарда. Функціональні параметри серця відповідають даним ехокардіографії (ЕхоКГ) від 15.11.2021.
Супутня терапія: тикагрелор, гепарин 5000 ОД, Біблок®, езомепразол, розувастатин.
Результати терапії: у пацієнта відмічено відсутність реперфузійних аритмій, відновлення синусового ритму та відсутність ускладнень у гострому періоді інфаркту міокарда.
Клінічний випадок № 2 (Д. М. Жорніченко, лікар-кардіолог Київської міської клінічної лікарні № 12)
Жінка 58 років госпіталізована до кардіологічного відділення 09.11.2021.
Діагноз при госпіталізації: ІХС: ГКС з елевацією сегмента ST.
Діагноз заключний: ІХС, ГІМ із Q передньо-перетинковим зубцем.
Тривалість лікування препаратом Ксаврон®: 10 днів.
Лабораторні дані: МВ-КФК при госпіталізації (9.11.2021) 54,31 од/л. МВ-КФК повторно (20.11.2021) 24,44 од/л.
Інструментальні дослідження: зміни на ЕКГ при госпіталізації (9.11.2021) – ритм неправильний; ЧСС 99 уд./хв, елевація сегмента ST на 10 мм у відведеннях V2-V5, часта суправентрикулярна екстрасистолія. Зміни на ЕКГ повторно (19.11.2021) – ритм синусовий, правильний; синусова брадикардія зберігається; елевація сегмента ST 1-2 мм у відведеннях V2–V6 з негативізацією зубця Т.
УЗД серця: при госпіталізації (9.11.2021) – ФВ ЛШ 39%; гостра аневризма міжшлуночкової перетинки.
Коронарографія: при госпіталізації (9.11.2021) – правий тип коронарного кровообігу. ПКА с/3 (2), стеноз С, стенозування 100%, ТІМІ 0.
Супутня терапія: АСК, клопідогрель, допамін, аміодарон, торасемід, ізосорбіду динітрат.
Результати терапії: відсутність реперфузійних аритмій, відновлено синусовий ритм, відсутні ускладнення в гострому періоді, відмічено позитивну динаміку маркера ураження міокарда (МВ-КФК), зменшення елевації сегмента ST на ЕКГ. Пацієнтка виписана в руховому режимі.
Клінічний випадок № 3 (А. В. Татарчук, кардіолог відділення інтенсивної терапії Черкаської обласної лікарні)
Жінка 70 років госпіталізована до відділення інтенсивної терапії 27.11.2021.
Діагноз при госпіталізації: гострий трансмуральний інфаркт нижньої стінки міокарда.
Діагноз заключний: ІХС: гострий Q ІМ нижньої стінки ЛШ.
Тривалість лікування препаратом Ксаврон®: 5 днів (причина зменшення тривалості курсу – лікування було припинене передчасно у зв’язку з випискою пацієнтки зі стаціонару). Час від появи симптомів до реперфузії – 4,5 год. Метод реперфузії – стентування. Час від введення першої дози Ксаврону до реперфузії – 15 хв.
Лабораторні дані: МВ-КФК при госпіталізації (27.11.2021) 78 ОД/л; МВ-КФК повторно (30.11.2021) 29 ОД/л. Тропонін Т при госпіталізації (27.11.21) 287 нг/л. Тропонін І при госпіталізації (27.11.2021) 10 нг/л.
Зміни на ЕКГ: при госпіталізації (27.11.2021) – ритм синусовий правильний; елевація ST в області задньої стінки ЛШ із реципрокними змінами; maxSTE: 2 мм; ∑maxST Е/D2,5 мм*. При виписці (30.11.21) – ритм синусовий, правильний; зберігається елевація ST із реципрокними змінами; maxSTE0.4 мм; ∑maxST Е/D1 мм.
* Визначення максимальної елевації сегмента ST (maxSTE): найбільше за абсолютною величиною зміщення сегмента ST над ізолінією в одному відведенні в зоні, яка відповідала локалізації ІМ.
Сума максимальних елевації та депресії сегмента ST – ∑maxST Е/D:
• елевацію у випадку передньої локалізації ІМ визначали у відведеннях V1-V6, I, aVL;
у випадку задньої локалізації ІМ –
у відведеннях II, III, aVF, V5, V6;
• депресію у випадку передньої локалізації ІМ визначали у відведеннях II, III, aVF;
у випадку задньої локалізації ІМ –
у відведеннях V1-V6, I, aVL.
Ізолінією вважали сегмент PR.
УЗД серця: при госпіталізації (27.11.2021) – КСР 40 мм; КДР 54 мм; КСО 70 мл; КДО 141,3 мл; МШП 11 мм; ЗС 10 мм; ФВ 50.4%; ЛП 39 мм; КДР (ПШ) 26 мм; аорта 33 мм. Висновок: фіброз, недостатність аортального клапана І ст., недостатність мітрального клапана ІІ ст. Гіпокінез нижньо-бокового сегмента лівого шлуночка. Помірне зниження скорочувальної здатності міокарда.
Коронарографія: правий тип коронарного кровообігу; ПКА с/3 (2), стеноз С, стенозування 100%, ТІМІ 0.
Супутня терапія: тикагрелор, аторвастатин, гепарин, карведілол, периндоприл, ізосорбіду динітрат, ацетилсаліцилова кислота, метоклопрамід, корвітин, тіазотна кислота.
Результати терапії: ПКА с/3 TIMI 3; позитивна динаміка ЕКГ; значне покращення загального стану пацієнтки, приступи ангінозних болей не реєструвалися. Загальні враження від лікування Ксавроном – відсутність реперфузійних аритміій, незважаючи на обтяжений анамнез і підвищений ризик їх виникнення. Суб’єктивно кращий психоемоційний стан пацієнтки. Побічних явищ не спостерігалося.
Клінічний випадок № 4 (О. Я. Сорока, завідувачка кардіологічного відділення № 1 КНП ЛОР «Львівський обласний клінічний лікувально-діагностичний кардіологічний центр»)
Жінка 65 років госпіталізована 10.01.2022.
Діагноз при госпіталізації: ІХС: прогресуюча стенокардія.
Діагноз заключний: ІХС: гострий інфаркт міокарда.
Тривалість лікування препаратом Ксаврон®: 8 днів (причина зменшення тривалості курсу – в пацієнтки було діагностовано COVID-19, тому для продовження лікування її було переведено до іншого медичного закладу). Час від появи симптомів до реперфузії – 10 год. Метод реперфузії – коронарна ангіографія. Час від введення першої дози Ксаврону до реперфузії – 1 год.
Лабораторні дані: тропонін Т при госпіталізації 10.01.2022 (+); повторно 11.01.2022 (+).
Інструментальні дослідження: зміни на ЕКГ при госпіталізації (10.01.2022) – підйом сегмента ST на 4 мм; через 90 хв після реперфузії – зниження сегмента ST на 2 мм; 11.01.2022 – подальше зниження сегмента ST; 18.01.2022 – сегмент ST на ізолінії.
УЗД серця: при госпіталізації (10.01.2022) – недостатність мітрального клапана ІІ ст.
Супутня терапія: молсидомін, небіволол, розувастатин, клопідогрель.
Результати терапії: позитивна динаміка ЕКГ, відсутність скарг пацієнтки на біль у грудній клітці.
Клінічний випадок № 5 (О. Я. Сорока, завідувачка кардіологічного відділення № 1 КНП ЛОР «Львівський обласний клінічний лікувально-діагностичний кардіологічний центр»)
Жінка 75 років госпіталізована 24.01.2022.
Діагноз при госпіталізації: ІХС: гострий інфаркт міокарда.
Діагноз заключний: ІХС: гострий інфаркт міокарда.
Тривалість лікування препаратом Ксаврон®: 10 днів. Час від появи симптомів до реперфузії – 6 год. Метод реперфузії – коронарна ангіографія. Час від введення першої дози Ксаврону до реперфузії – 2 год.
Лабораторні дані: тропонін Т при госпіталізації 24.01.22 (+); повторно, якісний тест 24.01.2022 (+).
Інструментальні дослідження: зміни на ЕКГ при госпіталізації (24.01.2022) – підйом сегмента ST на 4 мм у відведеннях ІІ, ІІІ, aVF, V4-V6. Через 90 хв після реперфузії – зниження сегмента ST у відведеннях ІІ, ІІІ, aVF, V4-V6 на 1-2 мм. Повторно (31.01.2022) – ST на ізолінії. Повторно (7.07.2022) – ST на ізолінії.
Супутня терапія: ізособіду динітрат, клопідогрель, ацетилсаліцилова кислота, небіволол, периндоприл.
Результати терапії: покращення стану пацієнтки, позитивна динаміка показників ЕКГ, відсутність реперфузійноих аритмій та ускладнень в гострому періоді інфаркту міокарда.
Отже, ішемічний каскад фактично є відображенням патогенезу ГКС. Застосування блокатора ішемічного каскаду Ксаврон® – це напрям покращення результатів лікування ГКС, зокрема зменшення РУМ. При додаванні препарату Ксаврон® до стандартної терапії ГКС відзначалося покращення клініко-лабораторних показників, а саме загального стану пацієнта, зменшення порушень ритму серця, зменшення елевації сегмента ST на ЕКГ, зниження рівнів маркерів ураження міокарда (МВ-КФК, тропонін).