24 вересня, 2022
«Квартет» прямих пероральних антикоагулянтів у пацієнтів із неклапанною фібриляцією передсердь. Практичні аспекти застосування едоксабану
 Терапія пацієнтів із неклапанною фібриляцією передсердь (ФП) згідно з рекомендаціями Європейського товариства кардіологів (ESC, 2020) відповідає керівним принципам ABC [1]. Трансформуючи англійську абревіатуру в конкретні настанови, маємо чіткі вказівки щодо ведення пацієнтів із різними формами ФП.
Терапія пацієнтів із неклапанною фібриляцією передсердь (ФП) згідно з рекомендаціями Європейського товариства кардіологів (ESC, 2020) відповідає керівним принципам ABC [1]. Трансформуючи англійську абревіатуру в конкретні настанови, маємо чіткі вказівки щодо ведення пацієнтів із різними формами ФП.
- А (anticoagulation / avoid stroke): застосування препаратів антикоагулянтної терапії з метою профілактики розвитку ішемічного інсульту / системної емболії (ІІ/СЕ) згідно з критеріями ризику тромбоемболічних ускладнень за шкалою CHA2DS2-VASc. Якщо бал ризику ІІ/СЕ за шкалою CHA2DS2-VASc у чоловіків ≥1, у жінок ≥2, то призначення антикоагулянтної терапії є беззаперечним незалежно від форми ФП. Препаратами для профілактики ІІ/СЕ є прямі оральні антикоагулянти (ПОАК) або антагоністи вітаміну К (АВК) за умови добре керованої лабораторної оцінки їхньої ефективності відповідно до показника TTR – відсотка днів у терапевтичному вікні при цільовому значенні міжнародного нормалізованого відношення (МНВ) 2,0-3,0. Ефективною вважається терапія при TTR >70%. Також потрібно оцінити ризик кровотечі за шкалою HAS-BLED [1], змінювані чинники ризику кровотечі мають бути усунені.
- B (better symptom control): оцінка симптомів у пацієнта з ФП та визначення стратегії контролю серцевого ритму (кардіоверсія, протиаритмічна терапія або абляція).
- С (comorbidities / cardiovascular risk factor management): коморбідність / управління чинниками ризику серцево-судинних захворювань – корекція/терапія супутніх серцево-судинних захворювань і чинників ризику (зміна способу життя: боротьба з ожирінням, регулярні фізичні вправи, зменшення вживання алкоголю тощо).
Для реалізації першого положення ведення пацієнтів із ФП насамперед слід розглядати ПОАК як препарати з доведеною ефективністю та добрим профілем безпеки. Є чотири ПОАК, досліджені в рандомізованих клінічних випробуваннях, які показали принаймні не меншу ефективність порівняно з варфарином за комбінованою точкою інсульт/СЕ [1].
У коагуляційному каскаді основними мішенями для ПОАК є тромбін і фактор Xa, котрий разом із фактором Va розщеплює протромбін (фактор II), який формує тромбін (фактор IIa). Ривароксабан, апіксабан, едоксабан і бетриксабан – це прямі інгібітори фактора Xa. Дабігатрану етексилат і AZD0837 – прямі інгібітори тромбіну. Коагуляційний каскад у підсумку призводить до перетворення розчинного фібриногену на нерозчинний фібрин, що зумовлює формування тромбу. Каталізатором такого перетворення є тромбін (фактор IIa) [2].
Одним із представників ПОАК є едоксабан, зареєстрований 2015 року в Європі та США для профілактики тромбоемболічних ускладнень у пацієнтів із неклапанною ФП.
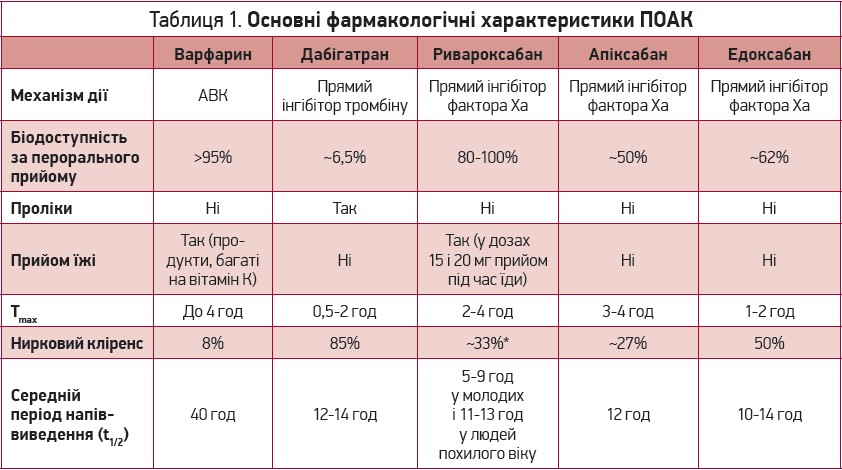
Вибір щодо застосування ПОАК у реальній клінічній практиці насамперед має ґрунтуватися на особливостях фармакокінетики та фармакодинаміки препарату [3-5]. Зокрема, для едоксабану характерним є швидкий початок дії – 1-2 год після прийому їжі (табл. 1).
При пероральному прийомі біодоступність едоксабану становить 62%, препарат призначається незалежно від прийому їжі, можливе його застосування в подрібненому вигляді, в тому числі через назогастральний зонд [3-5]. На всмоктуваність едоксабану суттєво не впливають інгібітори протонної помпи, Н2-блокатори, антациди, що містять алюміній і магній. Препарат має збалансовані шляхи елімінації: в печінці метаболізується не більш як 10%, інша його частина виводиться в незмінному вигляді нирками (50%) і шляхом біліарної секреції (40%) [6]. Період напіввиведення препарату становить 10-14 год [3-5].
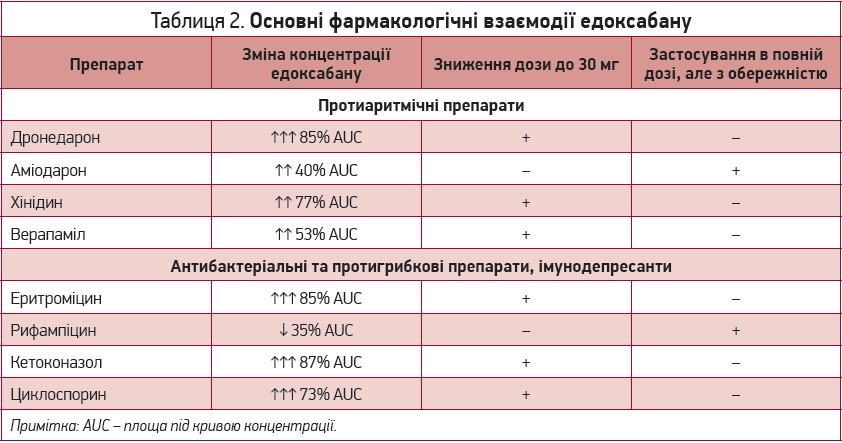
Едоксабан характеризується мінімальним спектром фармакологічної взаємодії, оскільки лише 4% препарату метаболізується за участю ферменту CYP3A4. Водночас потрібно враховувати, що в усмоктуванні препарату в кишечнику активну участь бере глікопротеїн Р, тому сумісне застосування зазначеного антикоагулянту з іншими субстратами цієї транспортної молекули може мати значний вплив на концентрацію едоксабану [1, 7-9]. Дані щодо фармакологічної взаємодії едоксабану наведено в таблиці 2. Інформацію щодо зниження дози едоксабану на тлі прийому верапамілу та хінідину наведено відповідно до рекомендацій ESC (2020) [1].
У європейській інструкції із застосування препарату вказано, що прийом верапамілу та хінідину не потребує зниження дози едоксабану. В анотації застосування едоксабану, яка діє на території США, зазначається, що не рекомендовано його сумісний прийом із рифампіцином. Також потенційно можливою є взаємодія едоксабану з кларитроміцином, іншими азоловими антимікотиками (крім кетоконазолу), ВІЛ‑специфічними противірусними препаратами.
Реєстраційним дослідженням, у якому едоксабан у дозі 60/30 мг/добу порівнювався з варфарином, є ENGAGE AF-TIMI 48 (Effective Anticoagulation with Factor Xa Next Generation in Atrial Fibrillation – Trombolysis in Myocardial Infarction 48). Наразі це багатоцентрове міжнародне рандомізоване подвійне сліпе дослідження ІІІ фази є наймасштабнішим випробуванням, у якому порівнюються ПОАК і варфарин у пацієнтів із ФП, як за кількістю включених осіб (n=21 105), так і за тривалістю спостереження (в середньому 2,8 року) [10, 11].
Випадкові групи пацієнтів були збалансовані за основними клінічними характеристиками та супутньою терапією. Середній вік пацієнтів становив 72 роки, 62% включених у дослідження були чоловіки, середній бал за оцінкою CHADS2 дорівнював 2,8 бала [10, 11]. У пацієнтів групи варфарину показник TTR становив 64,9%, що зіставно з показниками в реальній клінічній практиці згідно з даними міжнародних реєстрів [10, 11]. У цьому дослідженні первинною кінцевою точкою ефективності була частота інсульту та системних тромбоемболічних ускладнень. Основна кінцева точка безпеки – частота великих кровотеч (відповідно до критеріїв ISTH).
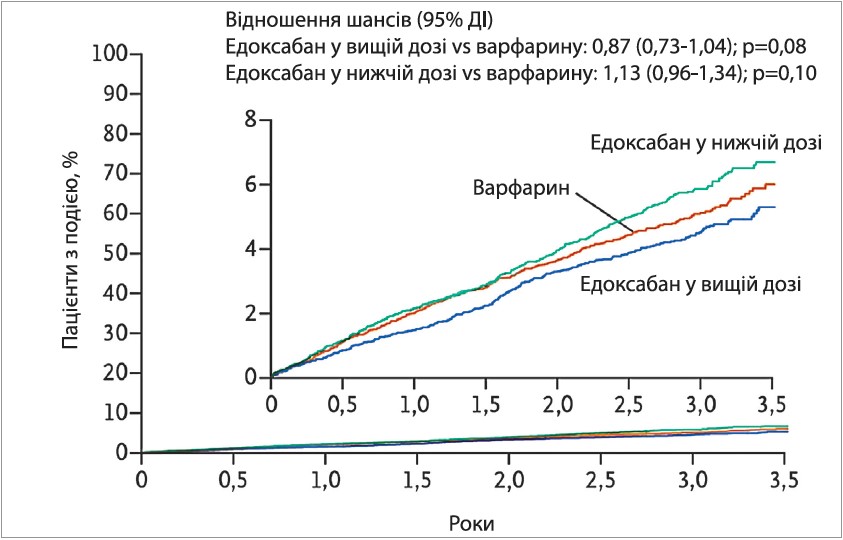
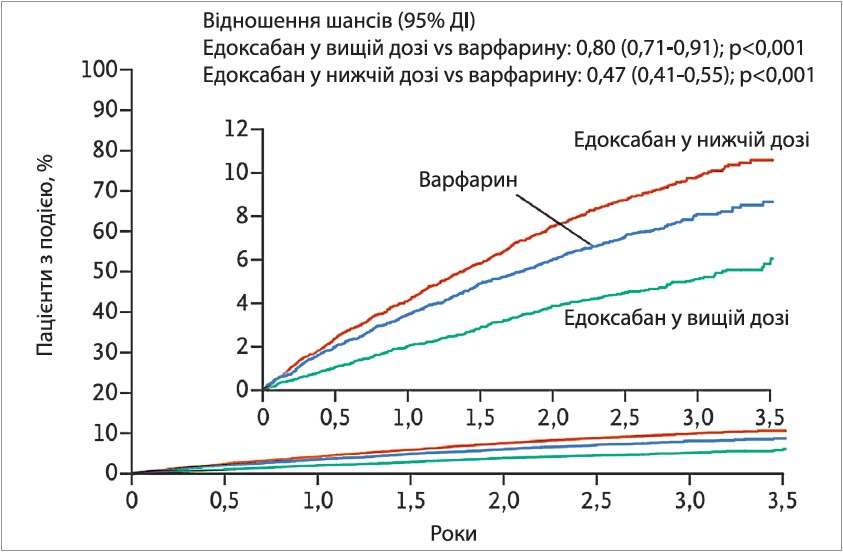
У групі застосування едоксабану в дозі 60 мг спостерігали нижчу частоту інсульту та СЕ на 13% порівняно з варфарином, але різниця була статистично незначущою (рис. 1). Крім того, відзначено на 20% менше випадків великих кровотеч для дози едоксабану 60 мг і на 53% менше – для дози 30 мг (рис. 2). Частота геморагічного інсульту в пацієнтів, які отримували едоксабан у дозах 60 або 30 мг, була відповідно на 46 і 67% нижчою порівняно з групою варфарину (р<0,001 для обох порівнянь). Частота ішемічного інсульту не відрізнялася в групах варфарину й едоксабану 60 мг, але була на 41% вищою в групі едоксабану 30 мг (р<0,001).
Рис. 1. Інсульт або системна емболія
Рис. 2. Великі кровотечі
Майже третина (28%) учасників ENGAGE AF-TIMI 48 мали в анамнезі ІІ або транзиторну ішемічну атаку. У таких пацієнтів очікувано вищим є ризик ішемічних ускладнень і кровотеч, аніж у когорті загалом, але всі виявлені тенденції зберігалися: прийом едоксабану в дозі 60/30 мг асоціювався з меншою частотою великих кровотеч і нижчим на 43% ризиком розвитку геморагічного інсульту (p=0,02), а також відзначено тенденцію до зменшення (на 14%, статистично незначущо) частоти ІІ/СЕ порівняно з варфарином [10, 11].
Ще одна когорта включених у дослідження ENGAGE AF-TIMI 48 – це пацієнти із супутньою ішемічною хворобою серця – ІХС (n=4510; 21,4%). У ході проведення субаналізу в цій групі спостереження виявлено тенденцію до переваг едоксабану 60/30 мг проти варфарину порівняно з пацієнтами без ІХС. Зокрема, в підгрупі з супутньою ІХС зареєстровано на 35% менше випадків розвитку інсульту/СЕ порівняно з пацієнтами без ІХС (p=0,062). У групі едоксабану зареєстровано на 31% менше випадків інфаркту міокарда в пацієнтів з ІХС порівняно з пацієнтами без ІХС (р=0,017). Переваги едоксабану в нижчій дозі над варфарином щодо частоти великих кровотеч не залежали від супутньої ІХС.
У більш як половини (58%) включених у дослідження ENGAGE AF-TIMI 48 пацієнтів діагностовано серцеву недостатність (СН). Хворі на СН характеризуються значним несприятливим профілем чинників ризику, що виражається в більшій частоті випадків серцево-судинної смерті. Проте навіть у пацієнтів із хронічною СН ІІІ-ІV функціонального класу прийом едоксабану асоціювався з меншою частотою геморагічних інсультів [12].
За показника кліренсу креатиніну (КлКр) 15-49 мл/хв потрібно зниження дози едоксабану до 30 мг/добу. У дослідженні ENGAGE було включено 4074 пацієнти (19% від загальної кількості) з КлКр 30-50 мл/хв. Аналіз post hoc показав, що при зменшенні КлКр <50 мл/хв ступінь зниження частоти великих кровотеч є більшим (ВШ 0,76; 0,58-0,98; р=0,036), аніж у пацієнтів із КлКр >50-95 мл/хв (ВШ 0,89; 0,75-1,04; р=0,15) [13].
У випробування ENGAGE AF-TIMI 48, як і в інші реєстраційні дослідження основних ПОАК, не включалися пацієнти з КлКр <30 мл/хв. Однак і експертні спільноти, й регуляторні органи допускають застосування едоксабану в зниженій дозі в пацієнтів із КлКр 15-29 мл/хв. У пацієнтів зі збільшеним КлКр (>95 мл/хв) згідно з даними аналізу рost hoc відзначається тенденція до збільшення числа ІІ/СЕ на тлі прийому едоксабану 60/30 мг порівняно з варфарином [13]. Оскільки едоксабан на 50% виводиться нирками, посилення ниркової функції теоретично може призводити до підвищеної екскреції препарату та зниження його концентрації в плазмі. Отримані дані стали обґрунтуванням для настанов Управління з контролю якості продуктів харчування та лікарських засобів США (FDA), згідно з якими прийом едоксабану не рекомендовано пацієнтам із ФП та КлКр >50 мл/хв. На думку ж експертів ESC, отримані в аналізі рost hoc результати не є такими, що обумовлюють подібні обмеження.
Відповідно до клінічної характеристики пацієнтів із ФП та моніторингового спостереження, близько 15% із них потребують черезшкірних коронарних втручань (ЧКВ) [14]. Однак поєднання антикоагулянтів із подвійною антитромбоцитарною терапією асоціюється з істотним збільшенням ризику геморагічних ускладнень. Водночас стратегія скасування ацетилсаліцилової кислоти та проведення подвійної антитромботичної терапії з ПОАК продемонструвала переваги щодо частоти виникнення кровотеч [15-17]. Ефективність і безпека едоксабану при подвійній антитромботичній терапії в пацієнтів із ФП та ЧКВ визначалася в дослідженні ENTRUST-AF PCI. Всього в дослідження було включено 1506 пацієнтів, порівнювалися дві тактики лікування: 1) едоксабан 60 мг/добу + інгібітор рецепторів P2Y12; 2) варфарин + інгібітор P2Y12 + ацетилсаліцилова кислота 100 мг (призначалася на розгляд лікаря на період від 1 до 12 міс, медіана потрійної терапії становила 66 днів) [18]. ЧКВ виконувалося в пацієнтів як зі стабільною ІХС, так і внаслідок гострого коронарного синдрому (52% випадків). У дослідженні ENTUST-AF PCI 92% пацієнтів отримували клопідогрель, 8% – тикагрелор або прасугрель. Рандомізація проводилася через 4-5 днів від моменту ЧКВ. Дозу едоксабану корегували за тими самими принципами, що й у дослідженні ENGAGE AF-TIMI 48. Тривалість спостереження становила 12 міс. З огляду на результати ENTUST-AF PCI, як і досліджень з іншими ПОАК (RE-DUAL PCI, PIONЕER AF-PCI й AUGUSTUS [15-18]), експерти ESC рекомендували дотримуватися такої тактики: після ЧКВ пацієнти з гострим коронарним синдромом повинні отримувати терапію антикоагулянтом (перевагу віддають ПОАК) і клопідогрелем протягом 12 міс, після планового ЧКВ – протягом 6 міс.
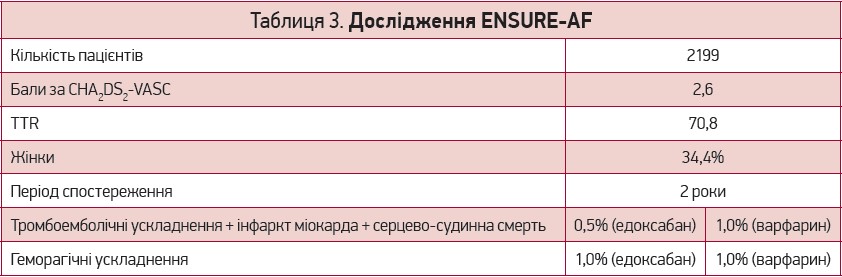
Високий ризик тромбоемболічних ускладнень мають кардіоверсія та катетерна абляція, котрі застосовуються для усунення ФП. Тому клінічні дослідження, в яких порівнювали едоксабан і варфарин у цих клінічних ситуаціях, становлять великий інтерес. ENSURE-AF – найбільше дослідження, в якому проводилося клінічне порівняння ПОАК (едоксабан 60/30 мг) та еноксапарину/варфарину в пацієнтів, яким виконували кардіоверсію [19]. Включено 2199 пацієнтів (середній вік – 64 роки, середнє значення CHA2DS2-VASc – 2,6 бала). Кардіоверсія після черезстравохідної ехокардіографії (ЧстЕхоКГ) проведена в трохи більш як половини пацієнтів. ЧстЕхоКГ та кардіоверсія виконувалися протягом 3 діб від моменту рандомізації. У групі едоксабану пацієнт отримував препарат щонайменше за 2 год до кардіоверсії. Тактика в групі варфарину/еноксапарину залежала від МНВ: за показника >2,0 ініціація еноксапарину була не потрібна, виконувалася кардіоверсія; за показника <2,0 одночасно з варфарином призначався еноксапарин, який скасовували при досягненні цільових значень МНВ. У пацієнтів другої страти ЧстЕхоКГ не проводили, кардіоверсію виконували через 3 тиж терапії едоксабаном або варфарином (МНВ протягом усіх 3 тиж мало перебувати в цільовому діапазоні). Після кардіоверсії пацієнти отримували антикоагулянт упродовж не менш як 4 тиж. Частота тромбоемболічних ускладнень була низькою в усіх групах (табл. 3).
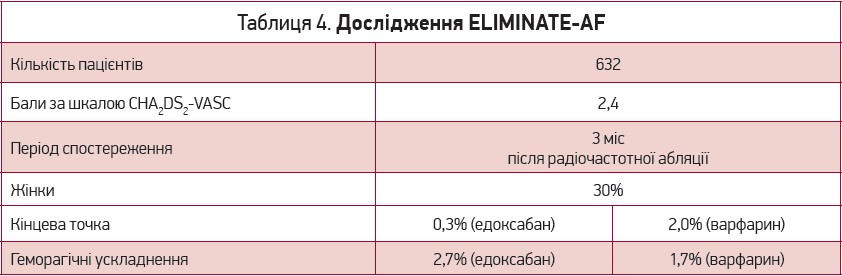
У рамках дослідження ELIMINATE-AF оцінювалася безпека проведення катетерної абляції з приводу ФП без скасування едоксабану 60/30 мг (група порівняння – прийом варфарину без скасування) [20]. Дослідження було порівняно невеликим (n=632). Абляція проводилася найбільше через 18 год після прийому останньої дози едоксабану, наступний прийом – не пізніше 6 год після завершення втручання. У групі варфарину абляція проводилася при значеннях останнього показника МНВ від 1,5 до 3,5.
Частота первинної кінцевої точки (серцево-судинна смерть, ІІ/СЕ) за 3 міс післяопераційного спостереження була незначною (табл. 4).
Певна тенденція до більшого відсотка геморагічних ускладнень у групі едоксабану зумовлена вищою дозою гепарину, котра була використана перипроцедурально. Частота небажаних подій у разі прийому едоксабану зіставна з такою за прийому дабігатрану в дозі 150 мг двічі на добу в дослідженні RE-CIRCUIT (1,6%) й апіксабану 5 мг двічі на добу в дослідженні AFAXA (3,1%), тоді як частота ускладнень у групі варфарину була нижче очікуваної (для порівняння: в дослідженні RE-CIRCUIT вона становила 6,9%, в AFAXA – 4,4%) [21, 22].
Отже, едоксабан є однією з можливих опцій антикоагулянтної терапії пацієнтів, яким проводиться катетерна абляція з приводу ФП. У рекомендаціях ESC (2020) підкреслено, що це втручання має виконуватися без скасування ПОАК [1].
Підбиваючи підсумки щодо аналізу практичних аспектів застосування едоксабану в пацієнтів із неклапанною ФП, слід зазначити, що цей ПОАК має низку переваг, які зумовлюють його вибір для лікування певних категорій пацієнтів. Насамперед едоксабан демонструє оптимальний профіль безпеки в пацієнтів із хронічною хворобою нирок помірного ступеня тяжкості. У пацієнтів з ІХС прийом едоксабану асоціюється зі зниженням частоти інфарктів міокарда, а також інсультів та епізодів системної тромбоемболії порівняно з варфарином. Мала кількість фармакологічної взаємодії гарантує безпеку й ефективність його призначення поліморбідним пацієнтам, які отримують значну кількість лікарських препаратів.
На фармацевтичному ринку України едоксабан представлено препаратом Едоксакорд 60/30 мг виробництва АТ «Київський вітамінний завод». Його біоеквівалентність препарату Lixiana німецького виробництва доведено в клінічному випробуванні в умовах одноразового перорального прийому здоровими добровольцями.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 9 (526), 2022 р.