31 березня, 2023
Ефективність та безпека неоад’ювантно-ад’ювантної або ад’ювантної терапії пембролізумабом при прогресуючій меланомі
Пембролізумаб (Кітруда®) – препарат гуманізованих моноклональних антитіл, що блокує взаємодію між рецептором білка програмованої клітинної смерті 1 (PD-1) та його лігандами PD-L1 і PD-L2. Пембролізумаб є першим протипухлинним препаратом, схваленим Управлінням з контролю якості харчових продуктів і лікарських препаратів США (FDA) для лікування пацієнтів з нерезектабельними і метастатичними солідними пухлинами (незалежно від їх локалізації чи гістологічного типу) з певними генетичними аномаліями. Результати сучасних досліджень продемонстрували, що пембролізумаб є ефективним при лікуванні пацієнтів з меланомою III або IV стадії після хірургічного втручання. Застосування цього препарату покращує прогноз і якість життя пацієнтів, а також знижує ризик розвитку рецидивів.
Пацієнти з меланомою III або IV стадії, які перенесли хірургічне лікування, залишаються у групі високого ризику виникнення рецидиву захворювання. Результати трьох раніше проведених рандомізованих досліджень засвідчили, що ці пацієнти отримали користь від ад’ювантної терапії препаратами моноклональних антитіл (ніволумаб або пембролізумаб) порівняно з відсутністю лікування чи попередньою стандартною ад’ювантною терапією (інтерферон-α2b або іпілімумаб) [1-3].
Клінічні переваги застосування анти-PD-1 в ад’ювантній терапії ґрунтуються на тому, що блокування PD-1 викликає системну протипухлинну відповідь, це призводить до елімінації мікрометастазів меланоми протипухлинними Т-клітинами. Відомо, що зв’язування PD-L1 і PD-L2 із рецептором PD-1, який міститься у T-клітинах, інгібує проліферацію Т-клітин і продукцію цитокінів [4]. У пухлині відбувається активізація PD-L1 та PD-L2, і передача сигналів цим шляхом може сприяти гальмуванню активного Т-лімфоцитарного контролю пухлин. Відповідно анти-PD-1 (пембролізумаб) зв’язує рецептори PD-1 і блокує їх взаємодію з PD-L1 і PD-L2, запускаючи інгібування імунної відповіді, опосередкованої PD-1, зокрема й протипухлинної [5-6].
Для того щоб імунотерапія спрацювала, пухлина має бути імуногенною та доступною для розпізнавання: вона повинна представляти на своїй поверхні змінені власні антигени, які можуть бути розпізнані Т-лімфоцитами як чужі. Зважаючи на такий механізм дії, резекція основної маси пухлини разом з лімфоцитами, що її інфільтрують, найімовірніше, забере значну частину потенційних протипухлинних Т-клітин, які могли б проліферувати після блокади PD-1. Введення антитіл, які блокують PD-1 перед операцією – неоад’ювантна терапія – стало підґрунтям для перевірки гіпотези, що неоад’ювантна терапія може активувати більше протипухлинних Т-клітин і поліпшити клінічні результати, ніж введення тієї ж кількості препарату після хірургічного втручання [7, 8]. Імовірно, що підсилення експозиції Т-клітин на пухлинні антигени також може відігравати певну роль. Щоб перевірити, чи забезпечить анти-PD-1 терапія до і після операції кращі результати, ніж введення препарату лише після операції, було розроблено дослідження Південно-західної онкологічної групи (SWOG) з вивчення раку S1801 за участю пацієнтів з клінічно верифікованою меланомою III або IV стадії. Основними кінцевими точками представленого рандомізованого клінічного дослідження ІІ фази були безрецидивна виживаність, виживаність з подіями, що включали постхірургічний рецидив, а також прогресування захворювання та токсичні ефекти до початку ад’ювантної терапії.
Методи
З лютого 2019 по травень 2022 року в дослідження було включено пацієнтів віком від 18 років, які мали гістологічно підтверджену шкірну, акральну або мукозальну меланому, клінічно виявлену та виміряну згідно з критеріями оцінки відповіді для солідних пухлин (RECIST) [9]; меланому IIID стадії або олігометастатичну резектабельну меланому IV стадії (M1a, M1b і M1c). Не включали пацієнтів з локальними рецидивами в хірургічному рубці від первинної меланоми. Локалізація мала бути підтверджена гістологічно за допомогою неексцизійної біопсії. Тип і ступінь хірургічного втручання були попередньо визначені для всіх пацієнтів. Хірургічне втручання призначали пацієнтам, які були рандомізовані в групу неоад’ювантно-ад’ювантного лікування, незалежно від відповіді на неоад’ювантну терапію за даними рентгенографії.
Пацієнти могли отримувати попередню ад’ювантну терапію (крім імунотерапії) або променеву терапію. Візуалізаційні обстеження були проведені протягом 42 днів до рандомізації з метою документації стану меланоми пацієнта при зарахуванні у дослідження. Пацієнти з наявністю вірусу імунодефіциту людини (ВІЛ) мали право на участь у дослідженні за умови стабільного й адекватного рівня CD4 (≥350 клітин на мм3) та вірусного навантаження ВІЛ у сироватці крові <25 000 МО/мл незалежно від того, чи отримували вони противірусну терапію. Основними критеріями виключення були попередня імунотерапія меланоми, активна автоімунна хвороба пацієнтів, які отримували системне лікування протягом 2 років до включення в дослідження, увеальна меланома та будь-які метастази в мозку в анамнезі.
Оцінка рецидиву дослідником базувалася на методах візуалізації або фізикальному обстеженні, а при можливості підтверджувалася біопсією. Клінічну оцінку та візуалізацію всього тіла проводили через кожні 3 місяці протягом перших 2 років, потім – через кожні 6 місяців. Візуалізацію мозку виконували щорічно протягом 5 років, але статус без рецидиву захворювання та загальну виживаність необхідно моніторити до 10 років. Побічні реакції оцінювали з використанням загальних термінологічних критеріїв NCI щодо побічних явищ (версія 5.0). У групі неоад’ювантно-ад’ювантного лікування використовували критерії RECIST (версія 1.1.9) для клінічної оцінки протипухлинної активності трьох доз пембролізумабу в неоад’ювантному режимі.
Результати
Загалом до дослідження було включено 313 пацієнтів, з яких 154 були розподілені до групи неоад’ювантно-ад’ювантної терапії та 159 – ад’ювантної терапії. Безпеку оцінювали у пацієнтів, які згідно з протоколом отримали хоча б одну дозу досліджуваного препарату. Характеристики пацієнтів при рандомізації були подібними в обох групах як за статтю, так і расовою й етнічною належністю. Серед усіх включених у дослідження пацієнтів 2 із групи неоад’ювантно-ад’ювантної терапії і 7 із групи ад’ювантної терапії не отримали жодного призначеного лікування через відкликання згоди.
Медіана тривалості спостереження становила 14,7 місяця в обох групах. Відмічено 105 подій (38 в групі неоад’ювантно-ад’ювантної терапії і 67 – ад’ювантного лікування). Виживаність без рецидиву була вірогідно довшою у групі неоад’ювантно-ад’ювантної терапії, ніж у групі ад’ювантного лікування (р=0,004 за логранговим критерієм). За даними знакового аналізу дворічна безрецидивна виживаність становила 72% (95% довірчий інтервал 64-80) у групі неоад’ювантно-ад’ювантної терапії та 49% (95% довірчий інтервал 41-59) у групі ад’ювантного лікування (рис.). На момент отримання проміжних даних було зареєстровано 36 випадків смерті (14 у групі неоад’ювантно-ад’ювантного лікування та 22 у групі ад’ювантної терапії). Така кількість летальних випадків унеможливлює остаточне порівняння груп відносно загальної виживаності.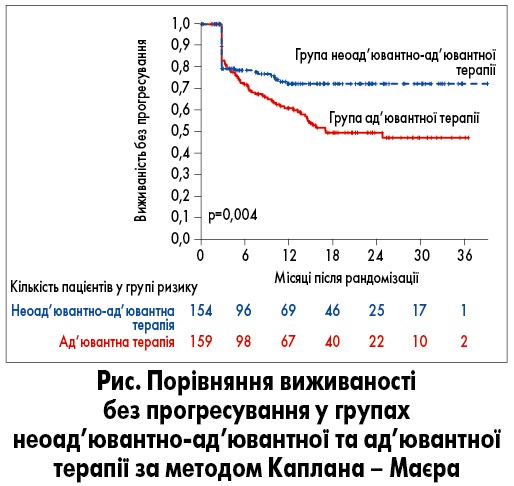
Міжгрупові відмінності щодо безрецидивної виживаності були послідовними в підгрупах відповідно до базових характеристик. Користь неоад’ювантного застосування пембролізумабу відзначали у всіх підгрупах пацієнтів, однак розміри вибірки в деяких окремих підгрупах були занадто малі, щоб робити висновки. Серед усіх рандомізованих пацієнтів на момент проведення цього аналізу 10 все ще отримували пембролізумаб у неоад’ювантному режимі. Решті 127 (88%) пацієнтів із 144 в групі неоад’ювантно-ад’ювантної терапії та 151 (95%) із 159 осіб у групі ад’ювантної терапії виконано хірургічне втручання. Причинами відміни операції в групі неоад’ювантно-ад’ювантного лікування були відкликання згоди після рандомізації (2 пацієнти), токсичні ефекти (1 пацієнт), прогресування захворювання (12 пацієнтів) та супутні стани (1 пацієнт). Крім того, 1 пацієнт із повною клінічною відповіддю відмовився від хірургічного втручання і продовжував спостереження через 31,5 місяця без ознак захворювання. Пацієнт групи неоад’ювантно-ад’ювантної терапії, який відмовився від операції через токсичні ефекти, не мав рецидиву під час спостереження протягом 65 днів. У групі, що отримувала лише ад’ювантне лікування, 8 пацієнтів відкликали згоду.
У групі неоад’ювантно-ад’ювантної терапії 14 (11%) зі 127 пацієнтів після хірургічного втручання не отримували ад’ювантної терапії з різних причин, включаючи «неоад’ювантні» токсичні ефекти у 3 пацієнтів (коліт, пневмоніт і ревмополіміалгія), прогресування захворювання, виявлене при візуалізації після операції (9 пацієнтів), залишкову хворобу (1 пацієнт), припинення участі через COVID-19 (1 пацієнт), занепокоєння щодо контакту з хворим на COVID-19 (1 пацієнт), а також інше захворювання, виявлене під час операції (2 пацієнти). У групі ад’ювантної терапії 21 (14%) із 151 пацієнта її не отримували. Двоє пацієнтів відмовилися від прийому ад’ювантної терапії. Іншими причинами були прогресування захворювання, виявлене при візуалізації після операції (16 пацієнтів), залишкова хвороба (2 пацієнти) та затримки, пов’язані з променевою терапією (1 пацієнт). Застосування ад’ювантної променевої терапії перед ад’ювантним введенням пембролізумабу було подібним в обох групах (2 пацієнти в групі неоад’ювантно-ад’ювантної та 1 пацієнт у групі ад’ювантної терапії). На момент проведення аналізу рецидив захворювання мали 9 пацієнтів у групі неоад’ювантно-ад’ювантного лікування та 41 пацієнт із групи ад’ювантного лікування. У групі неоад’ювантно-ад’ювантної терапії 50 пацієнтів завершили всі цикли ад’ювантного лікування, жоден з них не мав подальшого рецидиву захворювання. У групі ад’ювантної терапії 38 пацієнтів завершили всі її цикли, а у 4 (11%) згодом виник рецидив захворювання.
У групі неоад’ювантно-ад’ювантної терапії після завершення неоад’ювантного лікування оцінювали відповідь методами візуалізації. Зі 142 охарактеризованих пацієнтів 9 (6%) мали повну відповідь за даними візуалізаційних методів, а 58 (41%) – часткову відповідь. Огляд патофізіологічних звітів після неоад’ювантної терапії показав, що 28 (21%) зі 132 пацієнтів мали повну відповідь (відсутність життєздатної пухлини). Один пацієнт із повною відповіддю за даними візуалізаційних методів відмовився від операції і не мав рецидиву після 31 місяця спостереження.
Зі 152 пацієнтів у групі неоад’ювантно-ад’ювантної терапії, які отримали принаймні одну дозу пембролізумабу і для яких були доступні дані про несприятливі події, 11 (7%) мали принаймні одну побічну реакцію (ПР) 3 або 4 ступеня, котру дослідники пов’язували із введенням пембролізумабу. Із 127 пацієнтів, яким виконали визначену протоколом операцію після неоад’ювантної терапії і для яких були доступні дані про несприятливі події, 9 (7%) мали принаймні одну ПР 3 або 4 ступеня, котру дослідники пов’язували з хірургічним втручанням. З-поміж 141 пацієнта в групі ад’ювантної терапії після проведеної протокольної резекції, для яких були доступні дані про несприятливі події, 5 (4%) мали принаймні одну ПР 3 ступеня, що була визнана дослідниками як пов’язана з хірургічним втручанням. Не було відзначено ПР 4 ступеня, пов’язаних із хірургічним втручанням. Частота ПР 3 ступеня або вище під час ад’ювантної терапії була подібною в обох групах: 12% у групі неоад’ювантно-ад’ювантної терапії і 14% – ад’ювантної. В обох групах не зафіксовано жодних нових токсичних ефектів, спричинених введенням пембролізумабу, а також летальних випадків, які дослідники пов’язували із застосуванням препарату.
Висновки
У представленому рандомізованому дослідженні ІІ фази за участю пацієнтів з резектабельною меланомою III або IV стадії частка пацієнтів з дворічною безрецидивною виживаністю була на 23% більша у групі, що отримувала пембролізумаб у неоад’ювантному й ад’ювантному режимах, ніж у групі ад’ювантної терапії. У групі неоад’ювантно-ад’ювантного лікування прогресування захворювання або токсичні ефекти, що унеможливлювали хірургічне втручання, виявлені у менш ніж 10% пацієнтів, а загальна частота токсичних ефектів 3 або 4 ступеня була нижчою, ніж у дослідженнях, присвячених неоад’ювантному використанню інгібітора контрольних точок імунної відповіді анти-PD-1 та антигену 4 цитотоксичних Т-лімфоцитів (CTLA-4) [8, 10].
Дані представленого дослідження демонструють, що терміни введення інгібітора контрольних точок імунної відповіді відносно хірургічного втручання можуть мати великий вплив на результати лікування, навіть якщо в обох досліджуваних групах проведена однакова системна терапія [10, 11]. Отримані результати в поєднанні з розумінням механізму дії блокатора PD-1 підтверджують, що неоад’ювантне введення функціонально інгібує контрольну точку імунної відповіді до того, як протипухлинні Т-клітини будуть видалені хірургічно. Таким чином, отримані дані розширюють масив знань про використання неоад’ювантної терапії в онкології, коли серед пацієнтів з резектабельною меланомою III та IV стадії ті, хто отримував пембролізумаб як неоад’ювантну терапію з подальшою ад’ювантною терапією, мали довшу безрецидивну виживаність, ніж особи, які отримували препарат лише в ад’ювантному режимі.
Реферативний огляд Patel S.P., Othus M., Chen Y. et al. Neoadjuvant-Adjuvant or Adjuvant-Only Pembrolizumab in Advanced Melanoma. N Engl J Med. 2023; 388: 813-23. Doi: 10.1056/NEJMoa2211437.
Підготувала Валентина Момот
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 1 (80) 2023 р.



