9 червня, 2023
Аналіз підходів до лікування антикоагулянтами у пацієнтів із фібриляцією передсердь в умовах реальної клінічної практики
Терапія пероральними антикоагулянтами для запобігання інсульту та системній емболії є наріжним каменем у схемі лікування пацієнтів із фібриляцією передсердь (ФП). Однак пул інформації щодо стратегій такої профілактики є досить обмеженим. Метою проспективного багатоцентрового обсерваційного дослідження ROTA, учасниками якого стали амбулаторні пацієнти з ФП, було отримання даних про схеми лікування антикоагулянтами в умовах реальної клінічної практики в Туреччині. Пропонуємо до вашої уваги огляд результатів цього дослідження, викладених у публікації U. Kocabas et al. «Evaluation of anticoagulant treatment patterns in patients with atrial fibrillation: data from multicenter ROTA study» видання Turk Kardiyol Dern Ars (2023 Mar; 51 (2): 88‑96).
Фібриляція передсердь належить до найпоширеніших стійкиї порушень серцевого ритму в клінічній практиці, глобальна частота якої становить 2‑4% і пов’язана з п’ятиразовим підвищенням ризику інсульту та системної емболії.
Антикоагулянтна терапія, зокрема антагоністами вітаміну К (АВК) і пероральними антикоагулянтами прямої дії (ПАПД), є важливою частиною схеми лікування пацієнтів із ФП, спрямованою на запобігання інсульту та системній емболії (Kocabaş et al., 2016; Hindricks et al., 2020).
Для профілактики інсульту та системної емболії АВК застосовують в осіб із ФП >50 років, але використання їх у повсякденній практиці лишається складним через вузький терапевтичний діапазон, необхідність ретельного моніторингу стану пацієнтів, відстрочені початок дії та припинення антикоагуляції, а також низку харчових і лікарських взаємодій (Kocabaş et al., 2016). Ще важливішим є те, що безпека та ефективність АВК здебільшого залежать від так званого «терапевтичного вікна» (time in therapeutic range [TTR] – часу дотримання міжнародного нормалізованого відношення [МНВ] у цільовому діапазоні), яке визначає якість антикоагуляції. Хоча в поточних настановах для пацієнтів, які отримують АВК, рекомендовано показник TTR >70%, дані обсерваційних досліджень засвідчили, що в рутинній клінічній практиці у багатьох країнах він не відповідає цій умові (Rose et al., 2010; Turk et al., 2015; Hindricks et al., 2020).
ПАПД було розроблено для подолання обмежень, притаманних АВК. У чотирьох ключових рандомізованих контрольованих дослідженнях (РКД) продемонстровано не меншу ефективність та/або перевагу дабігатрану, ривароксабану, апіксабану та едоксабану порівняно з варфарином щодо профілактики інсульту та системної емболії (Connolly et al., 2009; Patel et al., 2011; Granger et al., 2011; Giugliano et al., 2013).
На підставі результатів цих РКД III фази, у яких доведено, що досліджувані препарати не поступаються за ефективністю препарату порівняння, застосування всіх чотирьох ПАПД схвалене відповідними регулювальними органами для запобігання інсульту й системній емболії у пацієнтів із ФП та принаймні одним чинником ризику інсульту.
У нещодавно опублікованих настановах щодо лікування ФП рекомендовано надавати перевагу ПАПД перед АВК, за винятком пацієнтів із механічними серцевими клапанами або помірним / тяжким мітральним стенозом (Hindricks et al., 2020; Andrade et al., 2020).
U. Kocabaş et al. зазначають, що вперше дабігатран був призначений у Туреччині 2013 року. Відтоді підхід до лікування для запобігання інсульту та системній емболії в осіб із ФП було змінено, і частка пацієнтів, які отримували терапію ПАПД, постійно зростала, сягнувши 37% 2016 року (Başaran et al., 2010).
Дослідники також наголошують, що реєстрація поточних даних, отриманих в умовах реальної клінічної практики, є вирішальною для розуміння фактичних стратегій профілактики інсульту та системної емболії у пацієнтів із ФП.
Тож основною метою дослідження ROTA було отримати реальні дані про схеми лікування антикоагулянтами у пацієнтів із ФП та описати демографічні й клінічні характеристики цих пацієнтів.
Матеріали та методи дослідження
Учасниками національного проспективного багатоцентрового обсерваційного дослідження ROTA стали пацієнти із ФП віком від 18 років (загалом 2597), які отримували лікування в кардіологічних амбулаторних клініках у семи географічних регіонах Туреччини із січня до травня 2021 року.
Під час першого візиту було зібрано демографічні, клінічні та лабораторні дані: вік, стать, індекс маси тіла (ІМТ), тип ФП, анамнез та супутні захворювання, показники функції нирок (рівень креатиніну в сироватці крові та кліренс креатиніну), анамнез кровотеч та лікування антикоагулянтами. Для визначення ризику тромбозу та кровотечі для кожного пацієнта розраховували показники за шкалою оцінювання ризику інсульту та системної тромбоемболії у пацієнтів із ФП (CHA2DS2-VASc). Така оцінка охоплює: застійну серцеву недостатність або дисфункції лівого шлуночка, артеріальної гіпертензії; вік (>75 років або 65‑74 років); цукровий діабет (ЦД); інсульт та/або системну емболію в анамнезі; захворювання судин; стать пацієнта. До уваги брали показники за шкалою оцінювання ризику кровотеч за миготливої аритмії (HAS-BLED) на підставі: наявності артеріальної гіпертензії, ниркової та/або печінкової недостатності; анамнезу інсульту та кровотеч; лабільного показника МНВ; віку пацієнта (до чи >65 років); даних щодо приймання препаратів, які призводять до кровотеч, та/або надмірного вживання алкоголю.
Для пацієнтів, які отримували АВК, для оцінювання якості антикоагуляції розраховували TTR за методом Розендаля. Велику кровотечу визначали як таку, що призвела до смерті, та/або симптоматичну кровотечу в критичній ділянці або органі (внутрішньочерепна, внутрішньоспинномозкова, внутрішньоочна, заочеревинна, внутрішньосуглобова, перикардіальна або внутрішньом’язова з компартмент-синдромом) та/або кровотеча, що зумовила зниження рівня гемоглобіну щонайменше на 2,0 г/л або спричинила потребу в переливанні ≥2 ОД суспензії еритроцитів. Клінічно значущу невелику кровотечу визначали як така, що потребувала медичної допомоги. Незначними вважали інші явні кровотечі, які не відповідали критеріям великої або клінічно значущої.
Статистичний аналіз
Отримані дані представлено або як середнє значення (± стандартна похибка), або як медіану (міжквартильний розмах) відповідно до нормального розподілу безперервних змінних, перевіреного за допомогою критерію Колмогорова–Смірнова для однієї вибірки. Зокрема, для категоріальних змінних частоти подано у відсотках. Для порівняння медіанних значень віку, ІМТ, балів за CHA2DS2-VASc і HAS-BLED, вмісту креатиніну в сироватці крові та кліренсу креатиніну (для всіх показників нормальний розподіл було відхилено) серед пацієнтів, що отримували різні типи лікування антикоагулянтами, застосовували тест Крускала–Волліса (ретроспективне тестування з використанням непарних U-тестів Манна–Уїтні зі скоригованим за Бонферроні рівнем значущості; p<0,01).
Частоти категоріальних змінних порівнювали за допомогою критерію χ2 Пірсона або точного критерію Фішера, коли це було доцільно. Усі статистичні аналізи виконували за допомогою пакета програм SPSS версії 23 для Windows. Значущою вважали величину р<0,05.
Результати дослідження
Середній вік пацієнтів становив 72 роки (діапазон: 22‑98 років); 57,4% – жінки. Постійну форму ФП мали 51,5% пацієнтів, пароксизмальну – 30,1%, персистувальну або тривало персистувальну – 13,9%. Найпоширенішими супутніми захворюваннями були артеріальна гіпертензія (АГ), застійна серцева недостатність, ішемічна хвороба серця (ІХС) та ЦД (табл. 1).
|
Таблиця 1. Вихідні характеристики досліджуваної популяції (загалом 2597 учасників) |
|
|
Демографічні показники |
Кількість пацієнтів (%) |
|
Середній вік (МКР), роки |
72 (13) |
|
Вікові групи |
|
|
• <65 років |
589 (22,7) |
|
• 65-74 років |
984 (37,9) |
|
• ≥75 років |
1024 (39,4) |
|
Жінки |
1491 (57,4) |
|
Індекс маси тіла, середнє значення (МКР), кг/м2 |
28,04 (5,86) |
|
Низька маса тіла (≤60 кг) |
242 (9,3) |
|
Систолічний АТ, середній показник (МКР), мм рт. ст. |
130 (20) |
|
Діастолічний АТ, середній показник (МКР), мм рт. ст. |
80 (15) |
|
Частота серцевих скорочень, середній показник (МКР), уд./хв |
84 (26) |
|
Лабораторні показники |
|
|
Креатинін сироватки крові, середній показник (МКР), ммоль/л |
0,081 (0,033) |
|
Кліренс креатиніну, середній показник (МКР), мл/хв |
71,09 (34,9) |
|
Гемоглобін, середній показник ± стандартна похибка, г/л |
130±20 |
|
Анамнез |
|
|
• Інсульт і/або ТІА |
382 (14,7) |
|
• Інфаркт міокарда |
463 (17,8) |
|
• Ішемічна хвороба серця |
842 (32,4) |
|
• Застійна серцева недостатність |
984 (37,9) |
|
• Артеріальна гіпертензія |
1994 (76,8) |
|
• Цукровий діабет |
743 (28,6) |
|
• Дисліпідемія |
710 (27,3) |
|
• Захворювання периферичних артерій |
102 (3,9) |
|
• СОАС |
99 (3,8) |
|
• Анемія |
513 (9,8) |
|
• Хронічне захворювання печінки |
26 (1) |
|
• Тютюнокуріння на поточний час |
433 (16,7) |
|
• Кардіоверсія |
221 (8,5) |
|
• Абляція ФП |
80 (3,1) |
|
Анамнез щодо кровотеч |
|
|
• Велика кровотеча |
88 (3,4) |
|
• Клінічно значуща невелика кровотеча |
130 (5) |
|
• Незначна кровотеча |
622 (24) |
|
Примітки: МКР – міжквартильний розмах; СОАС – синдром обструктивного апное уві сні; ТІА – транзиторна ішемічна атака; ФП – фібриляція передсердь Адаптовано за U. Kocabas et al. Evaluation of anticoagulant treatment patterns in patients with atrial fibrillation: data from multicenter ROTA study. Turk Kardiyol Dern Ars. 2023 Mar. Vol. 51, № 2. Р. 88-96. |
|
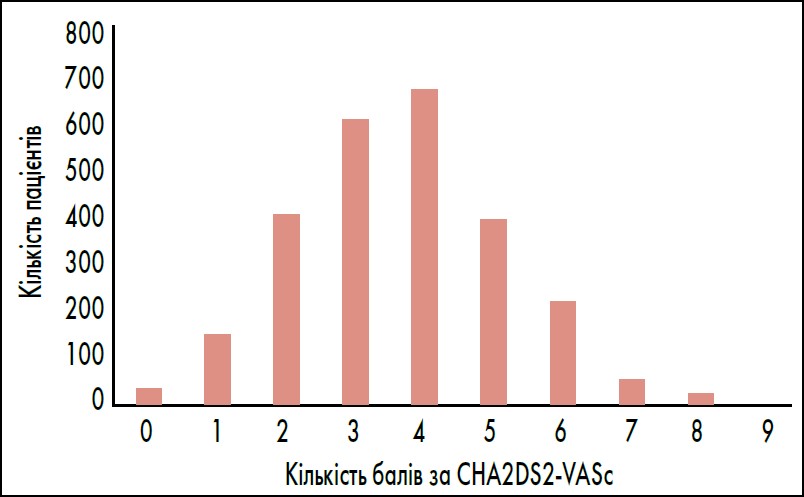
Середній показник за CHA2DS2-VASc становив 4 бали (діапазон: 0‑9 балів), 85,6% пацієнтів мали високий ризик інсульту (показник за CHA2DS2-VASc ≥2 балів для чоловіків і ≥3 балів для жінок) (рис. 1). Середній показник за HAS-BLED становив 1 бал (діапазон 0‑6 балів), 85,9% пацієнтів мали ризик кровотечі (показник за HAS-BLED <3 балів). Показник TTR був розрахований для 408 із 412 пацієнтів із ФП, які отримували терапію АВК; його середнє значення сягало 52,9% і для 76% пацієнтів було неадекватним (TTR <70%) (табл. 2).
|
Таблиця 2. Показники ризику інсульту та кровотечі і TTR (n=2597) |
|
|
Показник |
Кількість пацієнтів (%) |
|
Медіана показників за CHA2DS2-VASc (МКР), бали |
4 (2) |
|
Категорії показників за CHA2DS2-VASc, кількість пацієнтів (%) |
|
|
• Низький (0 балів для чоловіків, 1 бал для жінок) |
71 (2,7) |
|
• Середній (1 бал для чоловіків, 2 бали для жінок) |
303 (11,7) |
|
• Високий (≥2 балів для чоловіків, ≥3 балів для жінок) |
2223 (85,6) |
|
Медіана показників за HAS-BLED (МКР), бали |
1 (1) |
|
Категорії показників за HAS-BLED, кількість пацієнтів (%) |
|
|
• Низький (<3 балів) |
2230 (85,9) |
|
• Високий (≥3 балів) |
366 (14,1) |
|
• Немає даних |
1 (<0,1) |
|
TTR, середній показник ± стандартна похибка, %* |
52,9±21,3 |
|
Категорії показників TTR, кількість пацієнтів (%)* |
|
|
• Відповідає вимогам настанов (TTR ≥70%) |
98 (24) |
|
• Не відповідає вимогам настанов (TTR <70%) |
310 (76) |
|
Примітки: TTR – час дотримання міжнародного нормалізованого відношення у цільовому діапазоні; МКР – міжквартильний розмах. Адаптовано за U. Kocabas et al. Evaluation of anticoagulant treatment patterns in patients with atrial fibrillation: data from multicenter ROTA study. Turk Kardiyol Dern Ars. 2023 Mar. Vol. 51, № 2. Р. 88-96. |
|
Рис. 1. Розподіл пацієнтів (загалом 2597) згідно з показником за шкалою CHA2DS2-VASc
Адаптовано за U. Kocabas et al. Evaluation of anticoagulant treatment patterns in patients with atrial fibrillation: data from multicenter ROTA study. Turk Kardiyol Dern Ars. 2023 Mar. Vol. 51, № 2. Р. 88‑96.
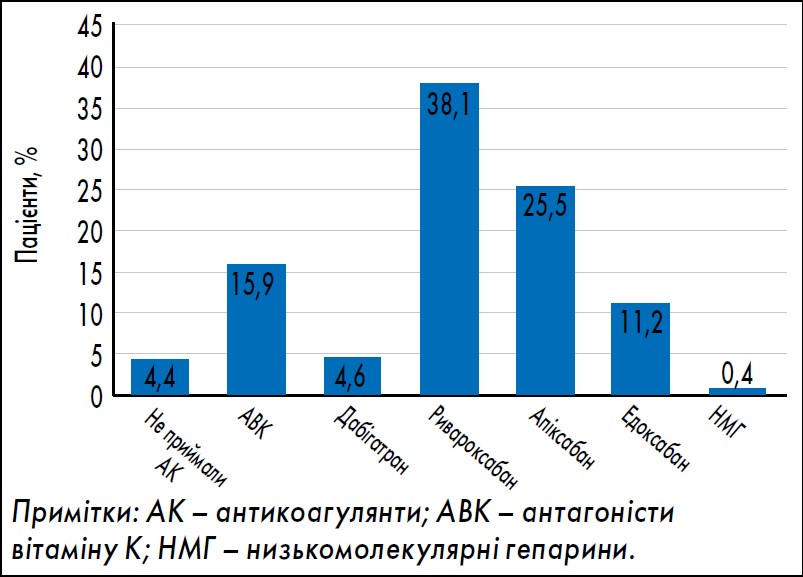
Загалом 2484 пацієнти з ФП (95,6%) отримували антикоагулянтну терапію для профілактики інсульту та системної емболії: 412 – АВК, 2062 – ПАПД (15,9 і 79,4% відповідно). Найчастіше призначуваними ПАПД були ривароксабан (38,1%) та апіксабан (25,5%) (табл. 3 і рис. 2).
|
Таблиця 3. Антикоагулянти та інші препарати, які приймали пацієнти досліджуваної популяції (n=2597) |
|
|
Терапія |
Кількість пацієнтів (%) |
|
Антикоагулянти |
|
|
АВК |
412 (15,9) |
|
ПАПД |
2062 (79,4) |
|
• Дабігатран (загалом) |
121 (4,6) |
|
Дабігатран (150 мг) |
61 (2,3) |
|
Дабігатран (110 мг) |
60 (2,3) |
|
• Ривароксабан (загалом) |
988 (38,1) |
|
Ривароксабан (20 мг) |
701 (27) |
|
Ривароксабан (15 мг) |
287 (11,1) |
|
• Апіксабан (загалом) |
661 (25,5) |
|
Апіксабан (5 мг) |
495 (19,1) |
|
Апіксабан (2,5 мг) |
166 (6,4) |
|
• Едоксабан (загалом) |
292 (11,2) |
|
Едоксабан (60 мг) |
229 (8,8) |
|
Едоксабан (30 мг) |
63 (2,4) |
|
НМГ |
10 (0,4) |
|
Не приймали антикоагулянтну терапію |
113 (4,4) |
|
Антиагрегантні препарати |
|
|
• АСК |
252 (9,7) |
|
134 (5,2) |
|
|
• Тікагрелор |
5 (0,2) |
|
• Прасугрель |
3 (0,1) |
|
Препарати для контролю ЧСС та/або серцевого ритму |
|
|
• β-Адреноблокатори |
1936 (74,5) |
|
• Верапаміл |
31 (1,2) |
|
• Дилтіазем |
289 (11,1) |
|
• Дигоксин |
383 (14,7) |
|
• Аміодарон |
123 (4,7) |
|
• Пропафенон |
106 (4,1) |
|
• Соталол |
14 (0,5) |
|
Інші види терапії |
|
|
• Інгібітори АПФ або БРА |
1515 (58,3) |
|
• ІРАН |
55 (2.1) |
|
• АМКР |
473 (18,2) |
|
• Діуретики |
1301 (50,1) |
|
• ДГП-БКК |
488 (18,8) |
|
• α-Блокатори |
73 (2,8) |
|
• Статини |
521 (20,1) |
|
• ІПП |
1276 (49,1) |
|
• НПЗП |
273 (10,5) |
|
• Стероїди |
32 (1,2) |
|
Примітки: АВК – антагоністи вітаміну К; ПАПД – пероральні антикоагулянти прямої дії; ЧСС – частота серцевих скорочень; АПФ – ангіотензинперетворювальний фермент; БРА – блокатори рецепторів ангіотензину; ІРАН – інгібітори рецептора ангіотензину-неприлізину; ДГП-БКК – дигідропіридин – блокатори кальцієвих каналів; НМГ – низькомолекулярні гепарини; АМКР – антагоністи мінералокортикоїдних рецепторів; НПЗП – нестероїдні протизапальні засоби; ІПП – інгібітори протонної помпи. Адаптовано за U. Kocabas et al. Evaluation of anticoagulant treatment patterns in patients with atrial fibrillation: data from multicenter ROTA study. Turk Kardiyol Dern Ars. 2023 Mar. Vol. 51, № 2. Р. 88-96. |
|
Рис. 2. Частота застосування антикоагулянтної терапії в досліджуваній популяції
Адаптовано за U. Kocabaş et al. Evaluation of anticoagulant treatment patterns in patients with atrial fibrillation: data from multicenter ROTA study. Turk Kardiyol Dern Ars. 2023 Mar. Vol. 51, № 2. Р. 88-96.
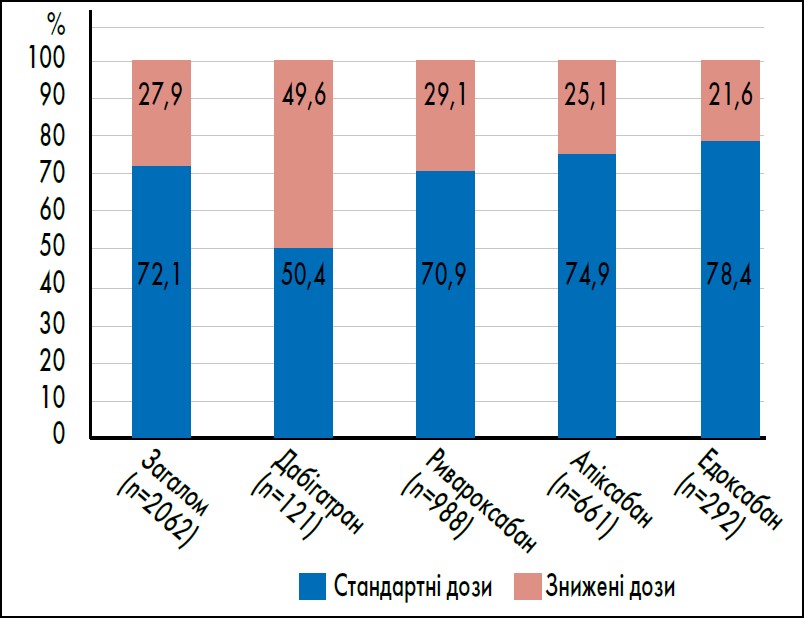
Стандартну дозу ПАПД призначали 1486 пацієнтам (57,7%), зменшену – 576 пацієнтам (22,2%). Частка пацієнтів, які приймали стандартні та знижені дози кожного ПАПД, становила 50,4 проти 49,6% для дабігатрану; 70,9 проти 29,1% для ривароксабану; 74,9 проти 25,1% для апіксабану та 78,4 проти 21,6% для едоксабану (табл. 3).
На рисунку 3 і в таблиці 3 наведено розподіл призначень ПАПД у стандартних (1486 пацієнтів, 57,7%) та знижених дозах (576 пацієнтів, 22,2%). Частки пацієнтів, які отримували стандартні та знижені дози кожного ПАПД, становили: 50,4 проти 49,6% для дабігатрану; 70,9 проти 29,1% для ривароксабану; 74,9 проти 25,1% для апіксабану та 78,4 проти 21,6% для едоксабану.
Рис. 3. Розподіл призначень ПАПД у стандартних та знижених дозах
Адаптовано за U. Kocabas et al. Evaluation of anticoagulant treatment patterns in patients with atrial fibrillation: data from multicenter ROTA study. Turk Kardiyol Dern Ars. 2023 Mar. Vol. 51, № 2. Р. 88‑96.
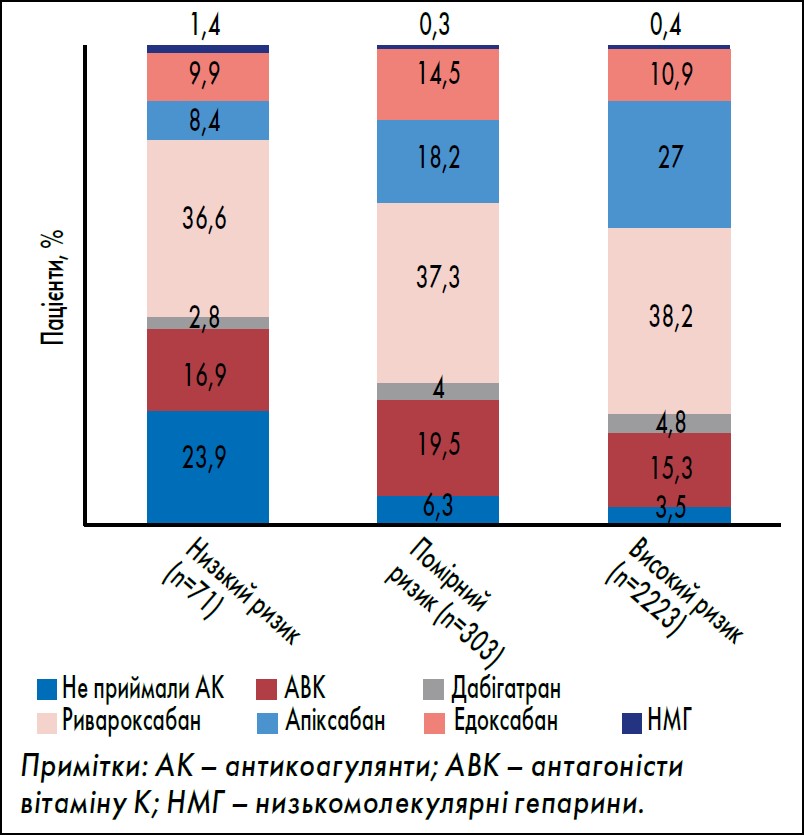
Оцінювання схем лікування антикоагулянтами відповідно до ризику інсульту засвідчило, що серед пацієнтів із низьким ризиком (показник за CHA2DS2-VASc 0 балів для чоловіків і 1 бал для жінок) 23,9% (n=17) не отримували терапії антикоагулянтами та 76,1% (n=54) отримували АВК, ПАПД або низькомолекулярний гепарин (НМГ).
Серед пацієнтів із високим ризиком інсульту (показник за CHA2DS2-VASc ≥2 балів для чоловіків і ≥3 балів для жінок) 3,5% (n=78) не приймали антикоагулянти, а 96,5% (n=2145) приймали АВК, ПАПД або НМГ. Дані щодо патернів лікування антикоагулянтами відповідно до ризику інсульту представлено на рисунку 4.
Рис. 4. Патерни лікування антикоагулянтами згідно з профілями ризику інсульту
Адаптовано за U. Kocabas et al. Evaluation of anticoagulant treatment patterns in patients with atrial fibrillation: data from multicenter ROTA study. Turk Kardiyol Dern Ars. 2023 Mar. Vol. 51, № 2. Р. 88-96.
Загалом 394 пацієнти (15,2%) отримували антиагрегантну терапію, зокрема ацетилсаліциловою кислотою (АСК), клопідогрелем, тікагрелором і прасугрелем (найчастіше призначали АСК – 9,7% пацієнтів і клопідогрель – 5,2% учасників).
Основними препаратами для контролю частоти серцевих скорочень були β-адреноблокатори, дигоксин і дилтіазем (74,5; 14,7 і 11,1% відповідно), а для контролю серцевого ритму – аміодарон і пропафенон (4,7 і 4,1% відповідно) (табл. 3). Пацієнти, які приймали АВК, були молодшими за осіб, які отримували ПАПД. Серед тих, хто лікувався ПАПД, пацієнти, які приймали апіксабан, були старшими, ніж за терапії ривароксабаном / едоксабаном. Крім того, середній показник за CHA2DS2-VASc був значно вищим у пацієнтів, які отримували апіксабан, ніж у тих, хто приймав АВК або ривароксабан / едоксабан. Середній показник за HAS-BLED був нижчим у тих, хто лікувався ривароксабаном / едоксабаном, ніж в учасників за терапії апіксабаном. Кліренс креатиніну був нижчим у пацієнтів, які отримували апіксабан, ніж у тих, хто приймав ривароксабан / едоксабан.
Частки пацієнтів із великою та/або клінічно значущою невеликою кровотечею, та/або шлунково-кишковою кровотечею в анамнезі були подібними в групах лікування. Антиагрегантну терапію одночасно з антикоагулянтною частіше застосовували пацієнти, які отримували лікування АВК, порівняно з тими, хто приймав ПАПД (табл. 4).
|
Таблиця 4. Порівняння демографічних і клінічних характеристик пацієнтів, які отримували пероральні антикоагулянти |
|||||||
|
Показник |
АВК |
Дабігатран |
Ривароксабан |
Апіксабан |
Едоксабан |
p |
Метод статистики |
|
Вік, середній показник ± SD, роки |
68,9±10,3 |
72,1±8,9 |
70,9±10,0 |
73,0±9,8 |
70,9±11,1 |
<0,001* |
47179а |
|
ІМТ, середнє значення ± SD, кг/м2 |
28,6±4,4 |
29,4±4,7 |
28,6±4,8 |
28,7±5,0 |
28,5±4,8 |
0,383 |
4177а |
|
Показник за CHA2DS2-VASC, середнє значення ± SD |
3,4±1,4 |
3,7±1,5 |
3,5±1,5 |
3,9±1,4 |
3,5±1,5 |
<0,001** |
32 |
|
Показник за HAS-BLED, середнє значення ± SD |
1,16±0,94 |
1,5±0,9 |
1,4±0,8 |
1,6±0,9 |
1,4±0,9 |
<0,001*** |
21775а |
|
Креатинін сироватки, середній вміст ± SD, ммоль/л |
0,103±0,083 |
0,086±0,027 |
0,087±0,031 |
0,091±0,035 |
0,085±0,027 |
0,074 |
8539а |
|
Кліренс креатиніну, середній показник ± SD, мл/хв |
71±28 |
72±25 |
72±24 |
69±25 |
74±23 |
0,014**** |
12516а |
|
Велика та/або клінічно значуща невелика кровотеча в анамнезі, кількість (%) |
29 (7) |
11 (9,1) |
68 (6,9) |
60 (9,1) |
26 (8,9) |
0,443 |
3739b |
|
ШК кровотеча в анамнезі, кількість (%) |
22 (5,6) |
7 (5,8) |
45 (4,6) |
45 (7) |
12 (4,3) |
0,297 |
4902b |
|
Супутня антиагрегантна терапія, n (%) |
60 (15,2) |
8 (6,6) |
123 (12,5) |
69 (10,5) |
29 (10,1) |
0,046***** |
9701b |
|
Примітки: SD – стандартна похибка; ІМТ – індекс маси тіла; a тест Крускала–Волліса; b критерій χ2 Пірсона; * значуще для АВК порівняно з дабігатраном, АВК порівняно з ривароксабаном, АВК порівняно з апіксабаном, АВК порівняно з едоксабаном, ривароксабану порівняно з апіксабаном, апіксабану порівняно з едоксабаном; ** значуще для АВК порівняно з апіксабаном, ривароксабану порівняно з апіксабаном, апіксабану порівняно з едоксабаном; *** значуще для АВК порівняно з ривароксабаном, ривароксабану порівняно з апіксабаном; **** значуще для ривароксабану порівняно з апіксабаном, апіксабану порівняно з едоксабаном; ***** значуще для АВК порівняно з іншими ПАПД. Адаптовано за U. Kocabas et al. Evaluation of anticoagulant treatment patterns in patients with atrial fibrillation: data from multicenter ROTA study. Turk Kardiyol Dern Ars. 2023 Mar. Vol. 51, № 2. Р. 88‑96. |
|||||||
Обговорення
U. Kocabaş et al. наголошують на тому, що завдяки дослідженню ROTA отримано важливу інформацію про демографічні, клінічні характеристики та схеми лікування пацієнтів із ФП в умовах реальної практики в Туреччині. За опублікованими раніше реєстрами, що уміщували дані пацієнтів із країн Заходу, середній вік пацієнтів із ФП становив ≥70 років (Huisman et al., 2015; Ruiz Ortiz et al., 2018; Piccini et al., 2019).
Натомість кілька досліджень, виконаних у Туреччині, продемонстрували, що він коливається в межах 64‑70 років (Başaran et al., 2010; Yavuz et al., 2017; Altay et al., 2017; Sayin et al., 2019). Згідно з Глобальним реєстром антикоагулянтів у FIELD-Atrial Fibrillation (GARFIELD-AF), частка зареєстрованих літніх пацієнтів (віком >75 років) з інших країн була значно вищою, ніж частка таких пацієнтів із Туреччини (37,2 проти 26,3% відповідно; p=0,001) (Sayin et al., 2019).
Середній вік (72 роки) учасників цього дослідження подібний до такого в опублікованих результатах, отриманих у західноєвропейських країнах або Північній Америці, і є вищим, ніж за даними попередніх реєстрів, створених у Туреччині, оприлюднених до 2017 року (Huisman et al., 2015; Ruiz Ortiz et al., 2018; Piccini et al., 2019; Sayin et al., 2019).
Така значуща різниця між результатами дослідження ROTA та даними попередніх турецьких реєстрів, на думку U. Kocabaş et al., може бути зумовлена багатьма причинами, як-от зміною демографічної картини пацієнтів із ФП, збільшенням популяції осіб похилого віку в Туреччині та вибором пацієнтів / центрів для цього дослідження. Ще одна важлива демографічна відмінність, яка спостерігається в дослідженні ROTA, полягає в переважанні пацієнтів жіночої статі. Попри те, що понад 55% учасників, залучених до РКД ефективності ПАПД III фази та попередніх звітів західних систем охорони здоров’я були чоловіками, у випробуванні ROTA 57,4% досліджуваної популяції становили жінки (Kakkar et al., 2012; Steinberg et al., 2014; Huisman et al., 2015).
Отримані результати відповідають даним досліджень, виконаних у Туреччині раніше. Зокрема, випробування TRAF засвідчило, що 57,1% суб’єктів були жінками (Yavuz et al., 2017). Це може бути пов’язано з високою поширеністю метаболічного синдрому, ожиріння, сидячого способу життя, серцево-судинних чинників ризику та/або захворювань серед турецьких жінок порівняно з європейською популяцією (Timmis et al., 2020). Середній показник за CHA2DS2-VASc коливається від 3,2 до 4 балів, а за HAS-BLED – між 1 і 1,6 бала у дослідженнях в умовах реальної практики. Популяційне когортне дослідження, виконане в Туреччині за участю 507 тис. 136 осіб, продемонструвало, що середній показник за CHA2DS2-VASc становив 4 бали, а реєстр із даними щодо турецьких пацієнтів свідчить, що середній показник за HAS-BLED – 1 бал, що подібно до результатів дослідження ROTA (Yavuz et al., 2017; Piccini et al., 2019; Sayin et al., 2019.
Результати дослідження ROTA підтверджують зміну схеми лікування антикоагулянтами у пацієнтів із ФП. До початку застосування ПАПД у Туреччині рівень призначення АВК становив лише 40%, а антиагрегантної терапії без АВК – 42% (Ertas et al., 2013). Уперше 2016 року настанова Європейського товариства кардіологів (ESC) щодо лікування ФП обмежила використання антиагрегантної терапії для запобігання інсульту та системній емболії; рекомендовано надавати перевагу ПАПД перед АВК для пацієнтів із ФП із помірним / високим ризиком інсульту (Kirchhof et al., 2016). До публікації цієї настанови глобальні реєстри продемонстрували, що пероральні антикоагулянти не застосовують відповідно до показань запобігання ризику інсульту й недостатньо використовують у пацієнтів із високим ризиком інсульту.
За даними реєстру GARFIELD, 38% пацієнтів із показником за шкалою оцінювання ризику інсульту (CHADS2) ≥2 балів не отримували антикоагулянтну терапію (Kakkar et al., 2013). Відповідно до європейського реєстру даних обсерваційних досліджень за участю пацієнтів із ФП (EORP-AF), частота призначення ПАПД становила лише 8,4% (Lip et al., 2014).
Після схвалення застосування ПАПД та публікації настанов, основаних на даних доказової медицини, обсерваційні дослідження засвідчили, що використання цих препаратів збільшилося, а застосування АВК для пацієнтів із ФП із часом зменшилася (Altay et al., 2017). У Європі протягом 2012‑2016 рр. частка призначень ПАПД зросла з 53,4 до 75,8%, а частка призначень АВК, навпаки, зменшилася з 35,5 до 16,8% (Camm et al., 2017).
U. Kocabaş et al. зазначають, що, згідно з їхнім аналізом, частота призначень пероральних антикоагулянтів є значною, і лише 3,5% пацієнтів із високим ризиком інсульту не отримували їх в умовах реальної практики. Інше важливе спостереження в межах дослідження ROTA полягає в тому, що протягом останніх п’яти років у Туреччині значно поліпшилося дотримання рекомендацій щодо лікування пацієнтів із ФП. У дослідженні RAMSES (2016), показники використання ПАПД та АВК в популяції амбулаторних пацієнтів із ФП становили 37 і 35% відповідно (Başaran et al., 2016). В іншому дослідженні частота застосування ПАПД та АВК у пацієнтів із ФП становила 42,4 і 23,2% відповідно, тоді як у межах випробування ROTA ті самі показники становили 79,4 і 15,9% відповідно.
Хоча поточні настанови не рекомендують терапію пероральними антикоагулянтами у пацієнтів із низьким ризиком інсульту, результати досліджень у реальних умовах продемонстрували, що частота надмірного використання АВК та ПАПД у цій популяції є високою (Kirchhof, 2015). Зокрема, у Туреччині поширеність надмірного застосування терапії цими препаратами пацієнтами з низьким ризиком інсульту коливається від 45 до 72% (Başaran et al., 2016; Sayın et al., 2019). У дослідженні ROTA понад 75% таких хворих отримували терапію пероральними антикоагулянтами. Подібне надмірне використання антикоагулянтної терапії пов’язане з підвищеним ризиком кровотечі без суттєвого зменшення частоти інсультів і системної емболії (Hindricks et al., 2020; Andrade et al., 2020).
U. Kocabaş et al. переконані, що необхідно підвищувати обізнаність лікарів щодо класифікації ризику інсульту у пацієнтів із ФП. Це допоможе уникати застосування пероральних антикоагулянтів у пацієнтів із ФП та низьким ризиком інсульту.
Ефективність і безпеку застосування ПАПД у знижених дозах вивчали у невеликої частини пацієнтів у базових дослідженнях. Близько 21% досліджуваної популяції отримували знижену дозу ривароксабану в дослідженні з порівняння ефективності цього інгібітора фактора Xa та АВК для запобігання інсульту та емболії при ФП (ROCKET-AF), і лише 4,7% пацієнтів приймали знижену дозу апіксабану в дослідженні ARISTOTLE (Patel et al., 2011; Granger et al., 2011).
Як зазначають U. Kocabaş et al., результати обсерваційних досліджень у реальних умовах, за якими поширеність застосування знижених доз антикоагулянтів коливається від 29 до 56%, не узгоджуються з результатами згаданих вище базових випробувань (Altay et al., 2017; Nielsen et al., 2017; Ruiz Ortiz et al., 2018; Miyazaki et al., 2020).
За результатами дослідження ROTA, частка пацієнтів, які отримували знижені дози ПАПД, становить приблизно 28%. Це більше, ніж у базових дослідженнях, і збігається з даними інших обсерваційних досліджень. Отримані в дослідженні ROTA результати підтвердили, що зниження дози є поширенішим явищем у щоденній клінічній практиці, ніж у межах РКД.
Невідповідне призначення ПАПД, а саме зниження дози без належного показання асоційоване зі збільшенням частоти інсульту й системної емболії та/або кровотечі. Така значуща різниця щодо призначення знижених доз ПАПД між реальною практикою та РКД може бути зумовлена численними причинами, зокрема чинниками, пов’язаними з пацієнтом (як-от старший вік, стареча астенія, наявність декількох супутніх захворювань) або з лікарем (як-от недостатня обізнаність щодо лікування антикоагулянтами у відповідних дозах і побоювання щодо побічних ефектів), а також немедичними чинниками, як-от вартість ліків, законодавство про реімбурсацію та обмеження доступу до медичних послуг.
На думку U. Kocabaş et al., слід підвищувати обізнаність лікарів щодо рекомендацій, основаних на даних доказової медицини, і заохочувати їх до призначання відповідних дозувань ПАПД пацієнтам із ФП.
Безпека та ефективність АВК, як правило, залежать від показника TTR, який відображає якість антикоагуляції. Невідповідна антикоагуляція, оцінена за цим показником, пов’язана з несприятливими наслідками, як-от кровотечі, інсульт і смерть (Rose et al., 2010).
За поточними настановами рекомендовано дотримуватися показника TTR >70% для пацієнтів, які отримують терапію АВК (Hindricks et al., 2020).
У базових дослідженнях ефективності ПАПД цей показник становив 64% (RELY), 62% (ARISTOTLE), 55% (ROCKET-AF) та 68% (ENGAGE-AF TIMI‑48) (Connolly et al., 2009; Patel et al., 2011; Granger et al., 2011; Giugliano et al., 2013).
Проте у пацієнтів, які приймали АВК в умовах реальної медичної практики та в межах обсерваційних досліджень, не вдалося досягти оптимального часу в терапевтичному діапазоні – показники TTR були нижчими, ніж за результатами РКД. За даними досліджень, виконаних у Туреччині, середнє значення показника TTR коливається від 40 до 54% у пацієнтів, які приймають АВК (Ertas et al., 2013; Basaran et al., 2016; Ḉelik et al., 2016).
Систематичний метааналіз результатів 11 досліджень із залученням загалом 10 тис. 501 пацієнта засвідчив, що показник TTR у середньому становить 49,8% (Topcuoglu and Arsava, 2021).
Як встановлено у дослідженні ROTA, середній показник часу в терапевтичному діапазоні був 52,9%, а 76% пацієнтів, які отримували терапію АВК, мали неадекватні значення TTR (<70%). Зокрема, продемонстровано низьку ефективність терапії антикоагулянтами в разі застосування АВК пацієнтами в медичних закладах Туреччини, а також, що, відповідно до поточних рекомендацій, понад три чверті осіб із ФП за терапії АВК потребують скерування до лікування ПАПД (Hindricks et al., 2020).
U. Kocabaş et al. упевнені, що основною причиною використання АВК замість ПАПД є критерії реімбурсації установ соціального забезпечення в Туреччині. Згідно з ними, «якщо за результатами принаймні трьох з останніх п’яти вимірювань, виконаних з інтервалами щонайменше впродовж тижня, цільове МНВ не може підтримуватися в межах від 2,0 до 3,0 за допомогою варфарину, можна припинити лікування варфарином і призначити дабігатран чи ривароксабан, або розпочати терапію апіксабаном чи едоксабаном» (Topcuoglu and Arsava, 2021).
На думку авторів, недостатня якість антикоагуляції та низький показник TTR за терапії варфарином, за результатами дослідження ROTA, свідчать, що рекомендації поточних настанов щодо дотримання показника часу в терапевтичному діапазоні понад 70% та критерії відшкодування вартості препаратів установ соціального забезпечення в Туреччині є нереалістичними для умов реальної медичної практики. Отже, призначення антикоагулянтної терапії АВК або ПАПД для лікування інсульту та профілактики системної емболії у пацієнтів із ФП має бути рішенням лікаря-практика, яке він прийматиме на власний розсуд і без будь-яких обмежень (Topcuoglu and Arsava, 2021).
З іншого боку, результати дослідження ROTA вказують на потребу в швидких і організованих діях для поліпшення показників TTR, як-от навчання пацієнтів або родичів, надання консультацій, забезпечення самоконтролю згаданого параметра пацієнтами, які приймають АВК.
Досі не виконано прямого РКД, присвяченого порівнянню ефективності й безпеки різних ПАПД. Результати досліджень IV фази та метааналізу даних обсерваційних досліджень свідчать, що, хоча ПАПД мають подібний вплив на ризик ішемічного інсульту та системної емболії, терапія апіксабаном асоціюється з меншим ризиком великих і клінічно значущих невеликих кровотеч проти інших ПАПД (Ntaios et al., 2017; Douros et al., 2019; Li et al., 2019).
За даними дослідження ROTA, пацієнти, які отримували терапію апіксабаном, були старшими, мали вищі показники за CHA2DS2-VASc і HAS-BLED і нижчий кліренс креатиніну, ніж ті, хто приймав інші ПАПД. Як зазначають U. Kocabaş et al., як і в ROTA, за даними попередніх досліджень в умовах реальної практики, пацієнти, які отримували апіксабан, теж були старшими та страждали на більшу кількість супутніх захворювань, ніж ті, хто приймав інші ПАПД (Born et al., 2017; Gedikli et al., 2021; Pham and Brown, 2019).
Вчені пояснюють це наявністю в пацієнтів старечої астенії, ниркової недостатності, функціональних порушень та інших супутніх захворювань. До того ж кардіологи, які брали участь у дослідженні ROTA, через занепокоєння щодо ризику кровотеч, можливо, призначали апіксабан пацієнтам, у яких цей ризик був високим, завдяки сприятливому профілю безпеки цього препарату.
U. Kocabaş et al. зауважують, що дослідження ROTA мало певні обмеження. Власне, це спостережний дизайн, який міг призвести до упередженості у відборі пацієнтів та/або оцінюванні їхнього стану. Досліджувану популяцію відбирали з кардіологічних амбулаторних клінік, і вона не охоплювала тих, хто звертався до амбулаторних клінік сімейної медицини та терапевтичних відділень медзакладів.
Отже, учасники дослідження не повною мірою представляють пацієнтів реальної клінічної практики. Можливо, що деякі географічні регіони Туреччини були представлені недостатньо. Зокрема, дослідження базувалося на документації щодо демографічних даних, історій хвороб та лікування, отриманій під час першого амбулаторного відвідування клініки, без результатів подальших спостережень щодо випадків інсультів, системної емболії, кровотеч і смертей у пацієнтів із ФП. Через ці обмеження автори вважають, що результати дослідження слід інтерпретувати з обережністю.
Висновки
На думку U. Kocabaş et al., дослідження ROTA підтвердило, що ситуація з призначенням пероральних антикоагулянтів для профілактики інсульту в пацієнтів із ФП значно поліпшилося протягом останніх п’яти років. За даними аналізу результатів цього дослідження, понад 90% пацієнтів із ФП отримують лікування пероральними антикоагулянтами, зокрема АВК і ПАПД. Упровадження останніх у клінічну практику змінило схеми лікування антикоагулянтами, і їх призначають частіше, ніж АВК.
Попри те, що показники використання пероральних антикоагулянтів були загалом задовільними, виявлено, що частота надмірного застосування АВК і ПАПД пацієнтами з низьким ризиком інсульту лишається високою.
Застосування ПАПД у знижених дозуваннях є доволі поширеним явищем у реальній клінічній практиці, ніж у межах РКД. Так, результати дослідження ROTA чітко продемонстрували низьку якість антикоагуляції за використання АВК.
Отже, основними висновками дослідження ROTA є:
- Рівень призначення пероральних антикоагулянтів у Туреччині є високим, причому ПАПД застосовують загалом частіше, ніж АВК.
- Частота надмірного використання ПАПД та АВК у пацієнтів із низьким ризиком інсульту є значною.
- Понад чверть пацієнтів із ФП за терапії ПАПД отримують препарати у знижених дозах.
- Лише чверть пацієнтів із ФП за терапії АВК мають адекватний показник часу в терапевтичному діапазоні.
- Пацієнти, які отримували терапію апіксабаном, були старшими та мали вищі показники за шкалами CHA2DS2-VASc і HAS-BLED, а також нижчий кліренс креатиніну, ніж ті, хто отримував інші ПАПД.
Підготувала Наталія Купко