21 червня, 2023
Бемпедоєва кислота: ефективність і безпека в лікуванні пацієнтів із гіперхолестеринемією та цукровим діабетом 2 типу
 Пацієнти із цукровим діабетом (ЦД) і діабетичною (атерогенною) дисліпопротеїнемією (ДЛП) мають високу схильність до розвитку серцево‑судинних захворювань (ССЗ). Низкою настанов і рекомендацій щодо атеросклеротичних ССЗ (АССЗ) підтверджено належність хворих на ЦД до категорії високого та дуже високого кардіоваскулярного ризику, а також переваги холестеринознижувальної терапії, а саме досягнення відповідного цільового значення холестерину (ХС) ліпопротеїнів низької щільності (ЛПНЩ) із метою профілактики АССЗ у цих пацієнтів. Проте пацієнти з дуже високим ризиком розвитку ССЗ частіше не досягають своєї терапевтичної мети, особливо це стосується хворих на ЦД.
Пацієнти із цукровим діабетом (ЦД) і діабетичною (атерогенною) дисліпопротеїнемією (ДЛП) мають високу схильність до розвитку серцево‑судинних захворювань (ССЗ). Низкою настанов і рекомендацій щодо атеросклеротичних ССЗ (АССЗ) підтверджено належність хворих на ЦД до категорії високого та дуже високого кардіоваскулярного ризику, а також переваги холестеринознижувальної терапії, а саме досягнення відповідного цільового значення холестерину (ХС) ліпопротеїнів низької щільності (ЛПНЩ) із метою профілактики АССЗ у цих пацієнтів. Проте пацієнти з дуже високим ризиком розвитку ССЗ частіше не досягають своєї терапевтичної мети, особливо це стосується хворих на ЦД.
Усі сучасні міжнародні настанови розглядають статини як медикаментозну терапію першої лінії для первинної та вторинної профілактики АССЗ, однак їхнє призначення може супроводжуватися розвитком низки побічних ефектів, у т. ч. на додаток до діабетогенних, з боку опорно-рухового апарату й печінки. Ліпідознижувальна терапія (а саме використання статинів) пов’язана з довгостроковими патофізіологічними змінами гомеостазу глюкози та розвитком ЦД 2 типу. З огляду на важливість проведення гіполіпідемічної терапії для хворих із діабетичною (атерогенною) ДЛП здійснюється інтенсивний пошук нових лікарських засобів (ЛЗ). Актуальні дослідження зосереджені на пошуку нових нестатинових ліпідомодифікувальних ЛЗ.
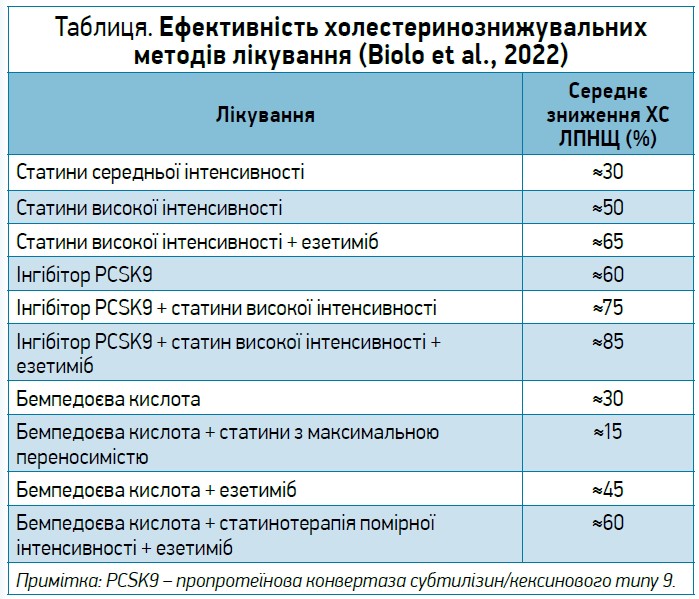
У таблиці наведено також ефективність холестеринознижувальних методів лікування (Biolo et al., 2022).
Бемпедоєва кислота (8-hydroxy-2,2,14,14-tetramethyl pentadecanedioic acid, ETC-1002) є невеликою молекулою з унікальним механізмом впливу на шляхи метаболізму ХС, жирних кислот (ЖК) і вуглеводів. Бемпедоєва кислота належить до нестатинових гіполіпідемічних засобів, що знижують рівень ХС ЛПНЩ. Бемпедоєва кислота (Nexletol® у США, Nilemdo® в Європейському Союзі (ЄС), Daiichi Sankyo; Esperion) (ETC-1002; ESP55016) є першою в своєму класі невеликою молекулою, яка знижує рівень ХС ЛПНЩ. Використання бемпедоєвої кислоти схвалено Управлінням з контролю за якістю продуктів харчування та лікарських засобів США (FDA), Європейським агентством з лікарських засобів (EMA) у 2020 році. Згідно з рекомендаціями FDA, лікарський препарат застосовують перорально 1 р/добу в дозі 180 мг як доповнення до статинів із максимальною переносимістю в дорослих із гетерозиготною сімейною гіперхолестеринемією (ГХС) або діагностованим АССЗ, які потребують додаткового зниження рівня ХС ЛПНЩ. У ЄС ліцензовані показання дещо відрізняються, зокрема, бемпедоєва кислота використовується в дорослих із первинною ГХС (сімейною/несімейною) чи комбінованою (змішаною) ДЛП у поєднанні зі статином та іншими гіполіпідемічними методами лікування або без них у пацієнтів, які не можуть досягти цільових показників ХС ЛПНЩ за допомогою монотерапії максимально переносимими дозами статинів чи в поєднанні з іншими гіполіпідемічними методами лікування; за непереносимості та/або протипоказань до призначення інгібіторів 3-гідроксил-3-метилглутарил-коферменту А-редуктази (ГМГ-КоА-редуктази).
Механізми дії бемпедоєвої кислоти
Сприятливий вплив бемпедоєвої кислоти на метаболізм і запальні процеси тісно пов’язаний із модуляцією двох ключових ферментів, які регулюють ліпідний, вуглеводний та енергетичний обміни. По-перше, бемпедоєва кислота пригнічує активність аденозинтрифосфат-цитратліази (ACLY) в печінці – фермента, який регулює надходження позамітохондріального цитрату для синтезу ліпідів. По-друге, бемпедоєва кислота активує аденозинмонофосфат (AMP)-активовану протеїнкіназу (AMPK) – ключову кіназу, яка контролює енергетичний гомеостаз і запальні процеси на рівні всього організму. Поєднання цих двох молекулярних ефектів призводить до виразного впливу на синтез ХС ЛПНЩ і процеси системного запалення, що є особливо актуальним при метаболічному синдромі та ЦД.
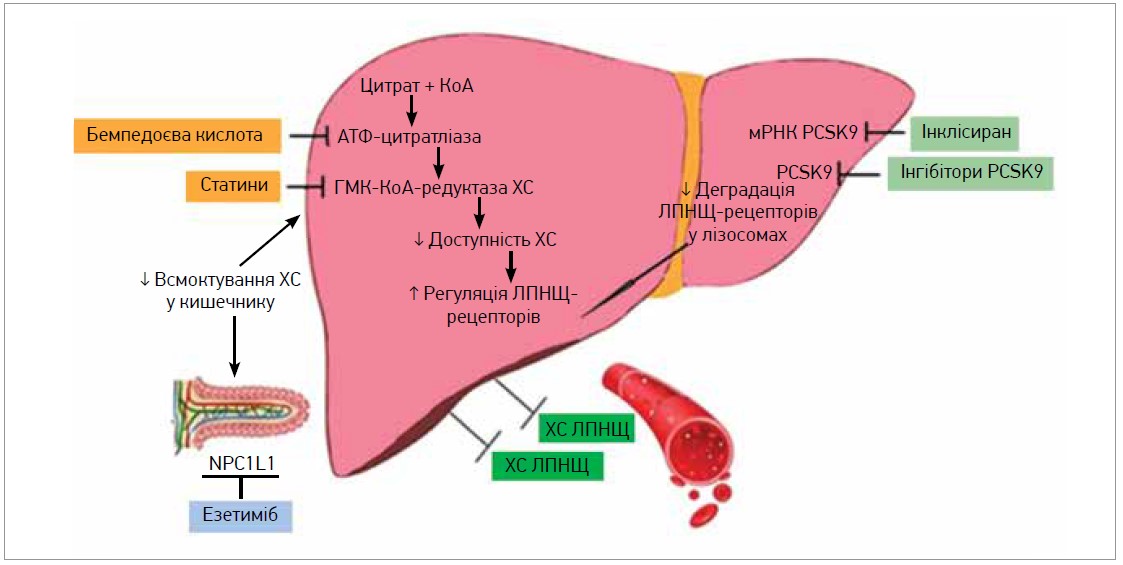
На рисунку наведено механізм дії основних нестатинових гіполіпідемічних препаратів, що використовуються в лікуванні ГХС (Bardolia et al., 2021).
Рис. Механізм дії основних нестатинових гіполіпідемічних препаратів (Bardolia et al., 2021)
Примітки: мРНК PCSK9 – матрична рибонуклеїнова кислота PCSK9; NPC1L1 – білок Nieman-Pick C1-Like 1.
Пригнічення регуляції ACLY. Бемпедоєва кислота є проліками, перетворюється в печінці на активну форму – бемпедоїл-КоА; це відбувається за участю дуже довголанцюгової ацил-КоА-синтетази-1 (ACSVL1) – фермента, локалізованого в гепатоцитах, але повністю відсутнього в посмугованих м’язах. Активна речовина ETC-1002 пригнічує активність ACLY, яка знаходиться на перетині шляхів метаболізму глюкози та ліпідів, регулюючи процеси глюконеогенезу і ліпогенезу. Бемпедоїл-КоА завдяки прямому інгібуванню ACLY пригнічує синтез стеролів і ЖК de novo. Цитоплазматична ACLY сприяє перетворенню цитрату – продукту мітохондріального циклу Кребса – в оксалоацетат і ацетил-КоА (попередник ліпогенезу та синтезу стеролів), а зменшення доступності оксалоацетату знижує процеси глюконеогенезу, продукцію глюкози в печінці. Ліпогенез досягається шляхом утворення малоніл-КоА за допомогою ацетил-КоА-карбоксилази (ACC) і подальшого синтезу ЖК і тригліцеридів (ТГ). Синтез ХС відбувається утворенням 3-гідрокси-3-метилглутарил-КоА (ГМГ-КоА) і мевалонової кислоти за допомогою ГМГ-КоА-редуктази, яка є мішенню для статинів. Ефекти бемпедоєвої кислоти на синтез ХС схожі на такі статинів, однак виявляються на вищому рівні щодо впливу на метаболічний синтетичний шлях. Інгібування цитоплазматичною ACLY бемпедоїл-КоА зумовлює гальмування синтезу ХС і компенсаторне збільшення кількості ЛПНЩ-рецепторів на мембранах гепатоцитів, що призводить до підвищення кліренсу циркулювальних ЛПНЩ. ACSVL1 не експресується в посмугованих м’язах, що перешкоджає перетворенню ETC-1002 на її активну форму, тому в скелетних м’язах бемпедоєва кислота не має спричиняти м’язових розладів, пов’язаних із пригніченням синтезу ХС.
Посилення регуляції активності АМРK. Бемпедоєва кислота (на додаток до пригнічення ACLY в печінці бемпедоїл-КоА) безпосередньо активує AMPK – основний регулятор рівня глюкози й енергетичного гомеостазу в організмі. Активація AMPK знижує швидкість ключових ферментів глюконеогенезу, як-от глюкозо-6-фосфатаза та фосфоенолпіруваткарбоксикіназа. Крім того, пригнічення ACLY сприяє зниженню продукції глюкози шляхом зменшення доступності оксалоацетату для глюконеогенезу. Крім впливу на метаболізм глюкози, AMPK інгібує ферменти, що обмежують швидкість синтезу ЖК і ХС, а саме ACC і ГМГ-КоА-редуктази відповідно. Отже, бемпедоєва кислота впливає на два різні шляхи зниження синтезу ЖК і ХС у печінці. На додаток до метаболічної дії бемпедоєва кислота завдяки виразним системним протизапальним ефектам значно знижує уміст циркулювального високочутливого С-реактивного білка (hs-CRP) in vivo. Додавання бемпедоєвої кислоти до дієти з високим умістом жирів у мишей LDLR-/- (ЛПНЩ-рецептор, моделі для вивчення сімейної ГХС) зменшувало ступінь підвищення вмісту ліпідів у плазмі крові та тканинах, послаблювало експресію прозапальних генів, пригнічувало накопичення ефірів ХС у стінці аорти, отже, сприяло запобіганню розвитку атеросклеротичних бляшок. In vitro продемонстровано, що ETC-1002 регулює запальну відповідь активованих моноцитів активацією протизапального шляху AMPK та інгібування прозапального шляху мітогенактивованої протеїнкінази, що призводить до зниження вивільнення прозапальних цитокінів і хемокінів. На мишачій моделі ожиріння та ДЛП, спричиненої дієтою з високим умістом жиру, ETC-1002 відновлювала активність AMPK, зменшувала запалення та знижувала синтез інтерлейкіну-6 у жировій тканині. Крім того, пригнічення ACLY бемпедоєвою кислотою зменшувало продукцію простагландину E2 та сприяло зменшенню запальної відповіді.
Генетична варіативність
У дослідженнях із використанням методу менделівської рандомізації генетичні варіанти, які імітують ефект інгібування ACLY, були пов’язані зі зниженням сироваткових біомаркерів серцево-судинного (СС) ризику, як-от ТГ і ХС ЛПНЩ, неалкогольною жировою хворобою печінки, ожирінням, ЦД 2 типу. Ці результати узгоджуються з відповідною міжіндивідуальною варіативністю експресії ACLY, яка може впливати на активність процесів глюконеогенезу та ефективність бемпедоєвої кислоти.
Ference та співавт. (2016) використовували генетичні оцінки, що складаються з незалежно успадкованих варіантів генів, які кодують PCSK9 і ГМГ-КоА-редуктазу (мішень статинів), як інструменти для випадкового розподілу 112 772 учасників із 14 проспективних когортних випробувань або досліджень «випадок – контроль» (14 120 із СС-подіями і 10 635 випадків ЦД). Мета – розподіл на групи відповідно до кількості успадкованих ними алелей, що знижують рівень ХС ЛПНЩ для проведення порівняльного аналізу впливу зменшення ХС ЛПНЩ, опосередкованого варіантами PCSK9, ГМГ-КоА-редуктази або обох, на ризик СС-подій і ЦД. Установлено, що варіанти PCSK9 і ГМГ-КоА-редуктази пов’язані з майже ідентичним захисним ефектом щодо ризику СС подій, а також ризику ЦД при зниженні рівня ХС ЛПНЩ на 0,26 ммоль/л. Підвищений ризик ЦД обмежувався особами з порушенням глікемії натще для обох показників і був нижчим за величиною, ніж захисний кардіопротекторний ефект. Поєднання ефектів варіантів PCSK9 і ГМГ-КоА-редуктази сприяло додатковому позитивному впливу на зменшення ризику СС подій і ЦД, причому їхні ефекти були незалежними й адитивними. Цей висновок підтверджено в дослідженнях із використанням методу менделівської рандомізації; зокрема, особи з мутаціями в генах, що кодують мішені ліпідознижувальних препаратів, мали нижчий рівень ХС ЛПНЩ і ймовірність розвитку ССЗ. Отримані результати демонструють суттєвіше зниження СС ризику (50‑55%) на 1 ммоль/л, зменшення ХС ЛПНЩ, що пов’язано з кумулятивним зниженням впливу ХС ЛПНЩ протягом усього життя. Подальші дослідження цього самого автора були присвячені генетичній оцінці незалежно успадкованих варіантів у генах, які кодують ACLY і ГМГ-КоА-редуктазу. Мета роботи – створити імітаційну модель механізмів впливу інгібіторів ACLY й інгібіторів ГМГ-КоА-редуктази та порівняти результати цих генетичних досліджень з рівнями ліпідів і ліпопротеїнів у плазмі крові, а також ризиком СС-подій, онкологічних захворювань. Загалом до дослідження залучили 654 783 учасників, у т. ч. 105 429 осіб із серйозними СС-подіями. Встановлено, що ACLY та ГМГ-КоА-редуктаза пов’язані зі схожими моделями змін рівнів ліпідів і ліпопротеїнів у плазмі, а також впливом на ризик СС подій і зниження рівня ХС ЛПНЩ на 10 мг/дл. Отже, моделювання генетичних варіантів, які імітують дію інгібіторів ACLY й інгібіторів статинів, продемонструвало, що останні знижують уміст ХС ЛПНЩ у плазмі крові за однаковим механізмом дії та асоціюються зі схожим впливом на ризик ССЗ на одиницю зниження рівня ХС ЛПНЩ. Фармакогенетика інгібіторів ACLY може бути потенційним сценарієм персоналізованої медицини.
Рандомізовані клінічні дослідження
Аналіз результатів рандомізованих клінічних досліджень (РКД) ІІ фази показує, що застосування бемпедоєвої кислоти в стандартній дозі 180 мг/добу в пацієнтів із ГХС, котрі не переносять терапію статинами, сприяє зниженню рівня ХС ЛПНЩ на ≈30%. Ефект бемпедоєвої кислоти на зменшення концентрації ХС ЛПНЩ зазвичай є вираженішим у хворих на ЦД 2 типу. Ефекти введення бемпедоєвої кислоти в комбінації з езетимібом, інгібітором кишкового всмоктування ХС є адитивними, що призводить до зниження ХС ЛПНЩ на 45%.
Бемпедоєва кислота та статини діють на два різні ферменти одного шляху синтезу ХС. Інгібування ACLY бемпедоєвою кислотою знижує доступність попередника для ГМГ-КоА-редуктази та синтезу ХС. Отже, ми не очікуємо адитивних ефектів комбінованої терапії двома препаратами. Насправді введення бемпедоєвої кислоти посилює дію високоінтенсивної терапії статинами на зниження рівня ХС лише на ≈15% порівняно з одним статином. Комбінація бемпедоєвої кислоти 180 мг, езетимібу 10 мг і аторвастатину 20 мг у пацієнтів із ГХС знижувала рівень ХС ЛПНЩ на≈60%. Адитивний ефект бемпедоєвої кислоти на зниження ХС ЛПНЩ також спостерігався в пацієнтів, які отримували терапію інгібітором PCSK9. Бемпедоєва кислота (180 мг 1 р/день), додана до фонової терапії еволокумабом (420 мг 1 р/міс), значно знизила рівень ХС ЛПНЩ на ≈30%. Відомо, що інгібітори синтезу ХС, як-от статини та бемпедоєва кислота, спричиняють збільшення експресії PCSK9 – білка, який підвищує рівень циркулювального ХС ЛПНЩ шляхом посилення деградації ХС ЛПНЩ-рецепторів. У випадках комбінування бемпедоєвої кислоти, статинів та інгібіторів PCSK9 інгібування PCSK9 посилює вплив інгібіторів синтезу ХС на надмірну експресію ЛПНЩ-рецепторів, що призводить до синергічної дії щодо зниження ХС ЛПНЩ. На додаток до зменшення рівня ХС ЛПНЩ ефект пригнічення синтезу ЖК спричиняє зниження показників вільних ЖК і ТГ у плазмі крові. Метааналіз РКД II і III фаз підтвердив, що бемпедоєва кислота суттєво знижує рівень ТГ на 15% та ХС ЛПВЩ на 6%.
Із 7 РКД III фази, під час яких оцінювали ефективність і безпеку бемпедоєвої кислоти, 4 завершено й опубліковано: Cholesterol Lowering via Bempedoic Acid, an ACL-Inhibiting Regimen (CLEAR) Harmony (NCT02666664), CLEAR Wisdom (NCT02991118), CLEAR Tranquillity (NCT03001076) і CLEAR Serenity (NCT02988115). Усі доступні дані досліджень демонструють значне зниження рівня ХС ЛПНЩ.
Метою багатоцентрового рандомізованого подвійного сліпого плацебо-контрольованого дослідження ІІІ фази CLEAR Tranquility (2018) було оцінити ефективність і безпеку бемпедоєвої кислоти за комбінування з основною ліпідознижувальною терапією в 269 пацієнтів із непереносимістю статинів в анамнезі та рівнем ХС ЛПНЩ ≥100 мг/дл (≥2,6 ммоль/л). Після 4-тижневого періоду призначення езетимібу в дозі 10 мг/добу пацієнти були рандомізовані 2:1 для лікування бемпедоєвою кислотою в дозі 180 мг/добу чи плацебо/добу в поєднанні з 10 мг/добу езетимібу протягом 12 тиж. Первинна кінцева точка – відсоткова зміна ХС ЛПНЩ від вихідного рівня до 12-го тиж, вторинна – зміни вмісту ліпідів, ліпопротеїнів і біомаркерів. Продемонстровано, що комбінування бемпедоєвої кислоти з езетимібом сприяло значному зниженню рівня ХС ЛПНЩ (>28,5%), ХС ліпопротеїнів невисокої щільності (ХС неЛПВЩ) (-23,6%), загального ХС (ЗХС) (-18,0%), аполіпопротеїну В (АпоВ) (-19,3%) і hs-CRP (-31,0%) порівняно із плацебо. Бемпедоєва кислота добре переносилася; частота побічних ефектів, пов’язаних із лікуванням (а також його припиненням), виявилася схожою в групах бемпедоєвої кислоти та плацебо. Отже, як вважають автори, бемпедоєва кислота може бути терапевтичним варіантом, який доповнює езетиміб у пацієнтів із непереносимістю статинів і необхідністю додаткового зниження рівня ХС ЛПНЩ.
Дослідження CLEAR Harmony Clinical (2019) присвячене визначенню ефективності бемпедоєвої кислоти в 2230 пацієнтів з АССЗ та/або гетерозиготною сімейною ГХС. Основні критерії включення: рівень ХС ЛПНЩ ≥70 м/дл (≥1,8 ммоль/л) на тлі максимально переносимої терапії статинами з або без додаткової ліпідознижувальної терапії. Первинна кінцева точка – безпека, основна вторинна (основна кінцева точка ефективності) – відсоткові зміни рівня ХС ЛПНЩ на 12-му із 52 тиж. На 12-му тиж бемпедоєва кислота статистично значуще знизила середній рівень ХС ЛПНЩ на -16,5% від початкового. Отже, в цьому 52-тижневому РКД установлено, що призначення бемпедоєвої кислоти, доданої до максимально переносимої терапії статинами, не призвело до вищої частоти загальних побічних ефектів, ніж плацебо, а також сприяло значному (статистично значущому) зниженню рівня ХС ЛПНЩ.
Мета випробування CLEAR Wisdom Randomized Clinical (2019) – оцінка ефективності бемпедоєвої кислоти порівняно із плацебо в пацієнтів із високим СС ризиком, які отримували максимально переносиму гіполіпідемічну терапію. Загалом рандомізовано 779 пацієнтів з АССЗ та/або гетерозиготною сімейною ГХС і рівнем ХС ЛПНЩ ≥70 мг/дл (1,8 ммоль/л), які знаходилися на максимально переносимій ліпідознижувальній терапії. Хворих рандомізували 2:1 для лікування бемпедоєвою кислотою (180 мг) або плацебо 1 р/добу протягом 52 тиж. Первинна кінцева точка – відсоткова зміна рівня ХС ЛПНЩ на 12-му тиж від вихідного рівня, вторинна – зміни вмісту ліпідів, ліпопротеїнів і біомаркерів. Результати, отримані на 12-му тиж лікування, продемонстрували, що бемпедоєва кислота значно більше знижувала рівень ХС ЛПНЩ (різниця -17,4%, 95% довірчий інтервал (ДІ) від -21,0 до -13,9%; р<0,001), ХС неЛПВЩ (р<0,001), ЗХС (р<0,001), АпоВ (р<0,001) і hs-CRP (р=0,04).
У CLEAR (Serenity study) – подвійному сліпому плацебо-контрольованому РКД III фази – рандомізовано 345 хворих із ГХС і непереносимістю щонайменше двох статинів. Бемпедоєва кислота 180 мг або плацебо призначалися 1 р/день протягом 24 тиж. Первинна кінцева точка – середня відсоткова зміна ХС ЛПНЩ від вихідного рівня до 12 тиж. Установлено, що лікування бемпедоєвою кислотою порівняно із плацебо суттєво знизило рівень ХС ЛПНЩ (-21,4%, 95% ДІ від -25,1 до -17,7%; р<0,001), ХС неЛПВЩ (-17,9%), ЗХС (-14,8%), АпоВ (-15,0%) і hs-CRP (-14,8%). Бемпедоєва кислота була безпечною та добре переносилася; зокрема, міалгія спостерігалася лише в 4,7 і 7,2% пацієнтів, які отримували бемпедоєву кислоту чи плацебо відповідно. Автори вважають, що бемпедоєва кислота є безпечним і ефективним терапевтичним варіантом для зниження ліпідів у пацієнтів із непереносимістю статинів.
Bays і співавт. (2020) проаналізували результати 4 рандомізованих плацебо-контрольованих подвійних сліпих клінічних досліджень III фази в пацієнтів із ГХС, які на тлі використання максимально переносимої ліпідознижувальної терапії потребували додаткового зниження ХС ЛПНЩ. Хворі отримували 180 мг бемпедоєвої кислоти (n=2424) або плацебо (n=1197) 1 р/день протягом 12-52 тиж. Мета дослідження – описати профіль безпеки бемпедоєвої кислоти, зокрема побічних явищ і клінічних лабораторних тестів. Продемонстровано, що призначення бемпедоєвої кислоти супроводжувалося розвитком випадків міалгії та м’язової слабкості, однак частота яких була зіставною із плацебо. Використання ЛЗ асоціювалося з незначним підвищенням азоту сечовини, креатиніну та сечової кислоти, а також зниженням гемоглобіну в крові на 4-му тиж лікування, які були стабільними протягом тривалого часу й зворотними після припинення вживання препарату. Автори констатують, що бемпедоєва кислота загалом є безпечною та добре переноситься пацієнтами із ГХС, котрі потребують додаткової ліпідознижувальної терапії. Комбінацію із фіксованою дозою (КФД) бемпедоєвої кислоти й езетимібу (180 та 10 мг відповідно) порівнювали з ефективністю бемпедоєвої кислоти, езетимібу чи плацебо в пацієнтів із високим СС ризиком і ГХС (ХС ЛПНЩ 149,8 мг/дл, незважаючи на використання максимально переносимої терапії статинами). На 12-му тиж КФД бемпедоєвої кислоти + езетимібу була ефективнішою в зниженні рівня ХС ЛПНЩ, ніж монотерапія, причому в більшого відсотка пацієнтів рівень ХС ЛПНЩ виявився нижчим за 70 мг/дл. КФД сприяла зниженню рівня hs-CRP (-35,1 порівняно з -8,2% у групі езетимібу). Водночас жодної різниці не спостерігалося, якщо порівнювати лише бемпедоєву кислоту (-35,1 проти -31,9% відповідно). Ця КФД також мала сприятливий профіль безпеки при додаванні до фонової терапії статинами. Отже, на підставі наявних і очікуваних результатів РКД застосування бемпедоєвої кислоти є ефективнішим для лікування ГХС як окремо, так і в комбінації з езетимібом.
Cicero та співавт. (2020) провели систематичний огляд і метааналіз ІІ і ІІІ фази 10 РДК щодо оцінки впливу бемпедоєвої кислоти на вміст ліпідів, а також hs-CRP у плазмі крові людини та безпеки її використання в лікуванні ГХС. Установлено, що призначення бемпедоєвої кислоти значно знижувало рівень ЗХС, ХС неЛПВЩ, ХС ЛПНЩ (середня різниця (СР) -22,94%; 95% ДІ від -26,63 до -19,25%; p<0,001), часточок ЛПНЩ, АпоВ, ХС ліпопротеїнів високої щільності (ЛПВЩ), часточок ЛПВЩ і hs-CRP. Водночас використання бемпедоєвої кислоти не виявляло істотного впливу на рівень ТГ, часточок ліпопротеїнів дуже низької щільності й АпоА-1. Проаналізовано фактичні дані щодо динаміки відсоткової зміни вмісту ХС ЛПНЩ від базового рівня до відповідних кінцевих точок 9 РКД за участю 3957 пацієнтів. Об’єднані результати показали, що застосування бемпедоєвої кислоти сприяло зниженню рівня ХС ЛПНЩ порівняно із плацебо із СР 22,9% (95% ДІ від -27,35 до -18,47%); індекс кількісної оцінки ступеня гетерогенності в метааналізі (тест неоднорідності, I2) дорівнював 99%. У 7 дослідженнях, які включали 3555 учасників, повідомлялося про відсоткові зміни показників концентрації hs-CRP. Об’єднані результати виявили, що бемпедоєва кислота знижувала рівень hs-CRP порівняно із плацебо із СР 24,70% (95% ДІ від -32,10 до -17,30%; I2 дорівнював 53%). Аналіз результатів даних щодо серйозних несприятливих СС-подій (MACE) у 3008 учасників РКД, зокрема зведений підрахунок випадків смерті внаслідок ССЗ, гострого коронарного синдрому (ГКС), нефатального інсульту, госпіталізації щодо нестабільної стенокардії та коронарної реваскуляризації, виявив, що застосування бемпедоєвої кислоти асоціювалося зі зниженням загального СС-ризику (коефіцієнт ризику (КР) 0,75, 95% ДІ від 0,56 до 0,99; I2 дорівнював 0%).
Бемпедоєва кислота та ЦД
Метааналіз РКД показав значно нижчу частоту появи чи загострення ЦД 2 типу при застосуванні бемпедоєвої кислоти (КР 0,68; p=0,02). Leiter і співавт. (2022) провели аналіз результатів 4 рандомізованих подвійних сліпих плацебо-контрольованих досліджень впливу бемпедоєвої кислоти на показники глікемії та ліпідів у пацієнтів із ГХС, які отримували статини з максимальною переносимістю. Хворі (n=3621) були рандомізовані 2:1 для перорального прийому бемпедоєвої кислоти 180 мг або плацебо 1 р/добу протягом 12-52 тиж з аналізом результатів за вихідним глікемічним статусом (ЦД, предіабет або нормоглікемія). Встановлено, що бемпедоєва кислота в пацієнтів із ЦД або переддіабетом статистично значуще знижувала рівень HbA1c і не погіршувала вмісту глюкози натще порівняно із плацебо. Використання бемпедоєвої кислоти незалежно від початкового глікемічного статусу сприяло суттєвому та стабільному зменшенню вмісту ХС ЛПНЩ. Окрім того, не спостерігалося збільшення частоти нових випадків ЦД порівняно із плацебо протягом середнього періоду спостереження в 1 рік.
Результати одноцентрового подвійного сліпого плацебо-контрольованого дослідження ефективності ETC-1002 у хворих на ЦД 2 типу та підвищеним рівнем ХС ЛПНЩ продемонстрували, що призначення 80 мг ETC-1002 на добу протягом 2 тиж із подальшим вживанням 120 мг протягом 2 тиж сприяло статистично значущому зменшенню рівня ХС ЛПНЩ на 43±2,6%, ХС неЛПВЩ, ЗХС, умісту hs-CRP. Окрім того, жодних клінічно значущих результатів, пов’язаних із безпекою лікування, не спостерігалося. Результати CLEAR Wisdom показали, що в хворих на ЦД, які отримували бемпедоєву кислоту, рівень HbA1c знизився на 0,08% від вихідного, а в когорті плацебо він підвищився на 0,13%.
Аналіз результатів 4 РКД виявив задокументовану 161 подію щодо нових випадків ЦД або декомпенсації захворювання (92/2424 (3,7%) для бемпедоєвої кислоти та 69/1197 (5,7%) для плацебо). Однак загалом застосування бемпедоєвої кислоти асоціювалося зі зниженням частоти нових випадків ЦД або загострення його перебігу (КР 0,65, 95% ДІ від 0,44 до 0,96; І2 дорівнював 23%). Результати доклінічних, клінічних і менделівських рандомізованих досліджень свідчать, що пригнічення ACLY не впливає негативно на контроль глікемії та може сприяти зменшенню ризику розвитку ЦД. Leiter і співавт. (2022) повідомляють, що лікування ЛЗ не супроводжувалося негативним впливом на контроль глікемії у пацієнтів із ЦД, а також збільшенням його ризику. В хворих на ЦД і з предіабетом, яким призначали бемпедоєву кислоту, спостерігалося статистично значуще (однак помірне) зниження рівня HbA1c та маси тіла порівняно із плацебо. Крім того, за предіабету на тлі терапії бемпедоєвою кислотою зареєстровано незначне зниження ризику нових випадків ЦД порівняно з пацієнтами, які отримували плацебо. Ці дані узгоджуються з результатами одноцентрового плацебо-контрольованого подвійного сліпого клінічного дослідження ІІ фази, проведеного Gutierrez і співавт. (2014). Лікування ETC-1002 не спричинило погіршення стану глікемічного контролю. Незначне зниження всіх попередньо визначених глікемічних маркерів спостерігалося на 29-й день при лікуванні ETC-1002 порівняно із плацебо. Ці глікемічні маркери передбачали визначення динаміки концентрації глюкози (середня зміна порівняно із плацебо складала -8,5 мг/дл), інсуліну, фруктозаміну натще; 15-годинного середньозваженого рівня глюкози (-14,3 мг/дл) і площі ранкової постпрандіальної глюкози в плазмі крові під кривою концентрація – час (AUC0-4 год) після проведення стандартизованого перорального глюкозотолерантного тесту (-79,2 мг∙год/дл). Оцінка результатів безперервного 24-годинного моніторингу глюкози виявила незначну тенденцію до покращення глікемічного контролю, особливо пов’язану зі зниженням піків після прийому їжі порівняно із плацебо. Це узгоджується також із результатами метааналізу 10 РКД, який показав, що бемпедоєва кислота сприяє зниженню ризику виникнення ЦД та/або не асоціюється з погіршенням його перебігу.
У CLEAR Harmony продемонстровано, що частота вперше задокументованого ЦД або його декомпенсації була нижчою в групі лікування порівняно із плацебо (3,3 проти 5,4%). У CLEAR Tranquillity нові випадки ЦД зареєстровано в 2,3% пацієнтів у групі плацебо порівняно з 1,1% хворих, які отримували бемпедоєву кислоту. Аналогічно CLEAR Serenity продемонструвало, що вперше діагностований ЦД або декомпенсація захворювання зустрічалися рідше в групі лікування бемпедоєвою кислотою (2,1%) порівняно із плацебо (4,5%). Метааналіз, проведений Wang і співавт. (2020), об’єднав результати повідомлень про випадки вперше виявленого ЦД та/або його декомпенсації у цих 4 дослідженнях. Зокрема, повідомлялося про 3,7% випадків для бемпедоєвої кислоти та 5,7% для плацебо. Зниження ризику маніфестації та/або декомпенсації ЦД для бемпедоєвої кислоти становило 0,65 (95% ДІ від 0,44 до 0,96; І2 дорівнював 23%).
Безпека бемпедоєвої кислоти
Результати РКД свідчать про те, що бемпедоєва кислота добре переноситься. Найпоширеніші побічні ефекти – подагра, інфекції сечовивідних шляхів, назофарингіт і гіперурикемія. Призначення бемпедоєвої кислоти супроводжувалося підвищенням рівня сечової кислоти, однак не сприяло зниженню швидкості клубочкової фільтрації. Використання бемпедоєвої кислоти не асоціювалося зі збільшенням частоти будь-яких побічних явищ, MACE або небажаних явищ, пов’язаних із м’язами. Крім того, призначення бемпедоєвої кислоти не супроводжувалося підвищенням рівня креатиніну в крові, розвитком подагри, нейрокогнітивними розладами, частотою збільшення печінкових ферментів >3×верхню межу норми (ULN) або креатинкінази >5×ULN.
Висновки
На додаток до бемпедоєвої кислоти існує багато нових ЛЗ, які продемонстрували здатність зменшувати рівень ХС ЛПНЩ або додатково знижувати ризик MACE в хворих на ЦД і пацієнтів без нього. Ці ЛЗ характеризуються різноманітними механізмами дії; до них належать інгібітори PCSK9, інгібітори рецептора, що активується проліфераторами пероксисом, та інгібітори інтерлейкіну-1β. Багато нових терапевтичних засобів проходять клінічну оцінку; деякі з них уже схвалено FDA. Використання нестатинової терапії для первинної профілактики ДЛП у субпопуляціях пацієнтів із непереносимістю статинів залишається особливо актуальною, тому клініцистам слід керуватися чинними рекомендаціями з метою початкового фармакотерапевтичного вибору для хворих із гіперліпопротеїнеміями.
В рекомендаціях з оцінки технологій Національного інституту охорони здоров’я та вдосконаленого надання медичної допомоги Великої Британії (NICE) (TA694), опублікованих у 2021 році, пропонується застосування бемпедоєвої кислоти з езетимібом як варіант лікування первинної ГХС або змішаної ДЛП, якщо статини не переносяться або протипоказані; за неадекватності контролю ХС ЛПНЩ лише за допомогою езетимібу.
Крім того, для підтвердження отриманих результатів необхідні такі РКД, як CLEAR Outcomes (NCT02993406), тобто з більшою кількістю пацієнтів і тривалішим спостереженням. Метою CLEAR Outcomes було визначити ефективність лікування бемпедоєвою кислотою (Nexletol) порівняно із плацебо в зменшенні ризику MACE в пацієнтів із ССЗ або високим його ризиком і непереносимістю до статинів, рівнем ХС ЛПНЩ ≥100 мг/дл (≥2,6 ммоль/л). CLEAR Outcomes включало >14 000 пацієнтів у >1200 дослідницьких центрах 32 країн.
Основна кінцева точка випробування: смерть, пов’язана із ССЗ, нефатальним ГКС, нелетальним інсультом, або госпіталізація щодо нестабільної стенокардії (MACE-4). Мінімальна тривалість лікування становила 36 міс, а прогнозована середня загальна експозиція лікування – 42 міс. Компанія Esperion повідомила, що дослідження CLEAR Outcomes досягло своєї основної кінцевої точки, продемонструвавши статистично значуще зниження ризику MACE-4 в пацієнтів, які отримували 180 мг Nexletol® на день (порівняно із плацебо).
4-6 березня 2023 р. в Новому Орлеані (США) відбувся черговий конгрес Американської колегії кардіології, в рамках якого професор Steven Nissen і співавт. представили основні результати CLEAR Outcomes trial й одночасно опублікували статтю в The New England Journal of Medicine.
Основні результати CLEAR Outcomes trial:
- призначення бемпедоєвої кислоти впродовж 6 міс сприяло зменшенню рівня ХС ЛПНЩ на 21,7% і hs-CRP на 22,2%. У пацієнтів, які отримували плацебо протягом 6 міс, спостерігалося зниження ХС ЛПНЩ лише на 0,6% і підвищення hs-CRP на 2,2%;
- бемпедоєва кислота сприяла зменшенню показників первинної кінцевої точки MACE-4 на 13% (коефіцієнт ризику (HR) 0,87; 95% ДІ 0,79-0,96; р=0,004; абсолютне зниження ризику (ARR) 1,6%; кількість пацієнтів, які потребують лікування (NNT), – 63);
- спостерігалось також зниження параметрів перших 3 вторинних кінцевих точок: -15% для MACE-3 (HR 0,85; 95% ДІ 0,76-0,96; р=0,006; ARR 1,3%), -23% для летального або нефатального ГКС (HR 0,77; 95% ДІ 0,66-0,91; р=0,002; ARR 1,1%) і -19% для необхідності проведення коронарної реваскуляризації (HR 0,81; 95% ДІ 0,72-0,92; р=0,001; ARR 1,4%);
- не спостерігалось істотної різниці між показниками вторинних кінцевих точок летального або нефатального інсульту, серцево-судинної смерті та смерті від усіх причин у пацієнтів, які отримували бемпедоєву кислоту та плацебо;
- не виявлено суттєвих відмінностей у загальній частоті побічних явищ, серйозних побічних явищ і небажаних явищ, які призвели до припинення прийому препарату;
- однак частота подагри (3,1% проти 2,1%), жовчнокам’яної хвороби (2,2% проти 1,2%), ниркової недостатності (11,5% проти 8,6%), підвищення рівня печінкових ферментів (4,5% проти 3,0%) та гіперурикемії (10,9% проти 5,6%) були вищими в пацієнтів, які отримували бемпедоєву кислоту, порівняно з учасниками групи плацебо.
CLEAR Outcomes trial продемонструвало, що в пацієнтів із непереносимістю статинів, які отримували первинну та вторинну профілактику, бемпедоєва кислота знижувала ризик первинної комбінованої кінцевої точки нефатального ГКС, нефатального інсульту, коронарної реваскуляризації або серцево-судинної смерті.
Отже, бемпедоєва кислота стає першим інгібітором ACLY, який демонструє клінічно значущі результати в пацієнтів із непереносимістю статинів або хворих із діагностованими АССЗ.
Медична газета «Здоров’я України 21 сторіччя» № 9 (545), 2023 р.