28 червня, 2023
Блокатори кальцієвих каналів у лікуванні артеріальної гіпертензії: як зробити оптимальний вибір?
 Артеріальна гіпертензія (АГ) залишається однією з найактуальніших проблем сучасної медицини, що обумовлено її високою поширеністю, здатністю спричиняти ураження органів-мішеней (серця, нирок, судин), а також підвищувати частоту виникнення серйозних ускладнень, як-от інфаркт міокарда, інсульт, хронічна серцева недостатність, погіршення функції нирок, до розвитку термінальної ниркової недостатності. За ефективного лікування АГ ризик серцево-судинних ускладнень і смертності значно знижується, тобто досягається основна мета лікування. Під час обрання тактики ведення хворого необхідно враховувати рівень артеріального тиску (АТ), наявність і характер факторів ризику, коморбідної патології (ішемічна хвороба серця (ІХС), цукровий діабет (ЦД), захворювання нирок тощо), що передбачає персоніфікований підхід до вибору ефективного та безпечного антигіпертензивного препарату. Дигідропіридинові блокатори кальцієвих каналів (ДГП БКК) привабливі доведеними органопротекторними ефектами, метаболічною нейтральністю, мінімумом протипоказань, що робить їх препаратами першої лінії у хворих на АГ, особливо із супутньою ІХС, ЦД, хронічною хворобою нирок (ХХН).
Артеріальна гіпертензія (АГ) залишається однією з найактуальніших проблем сучасної медицини, що обумовлено її високою поширеністю, здатністю спричиняти ураження органів-мішеней (серця, нирок, судин), а також підвищувати частоту виникнення серйозних ускладнень, як-от інфаркт міокарда, інсульт, хронічна серцева недостатність, погіршення функції нирок, до розвитку термінальної ниркової недостатності. За ефективного лікування АГ ризик серцево-судинних ускладнень і смертності значно знижується, тобто досягається основна мета лікування. Під час обрання тактики ведення хворого необхідно враховувати рівень артеріального тиску (АТ), наявність і характер факторів ризику, коморбідної патології (ішемічна хвороба серця (ІХС), цукровий діабет (ЦД), захворювання нирок тощо), що передбачає персоніфікований підхід до вибору ефективного та безпечного антигіпертензивного препарату. Дигідропіридинові блокатори кальцієвих каналів (ДГП БКК) привабливі доведеними органопротекторними ефектами, метаболічною нейтральністю, мінімумом протипоказань, що робить їх препаратами першої лінії у хворих на АГ, особливо із супутньою ІХС, ЦД, хронічною хворобою нирок (ХХН).
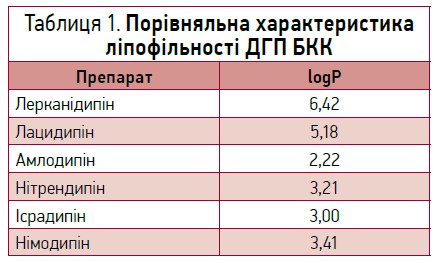
Лерканідипін – ДГП БКК ІІІ покоління, який конкурентно зв’язується з локусами кальцієвих каналів L-типу в гладком’язових клітинах кровоносних судин і кардіоміоцитах, пригнічує трансмембранний струм іонів кальцію, зумовлюючи розслаблення гладкої мускулатури. Лерканідипін – рацемічна суміш 2 оптичних ізомерів (R і S), антигіпертензивна активність яких обумовлена наявністю S-ізомера, що проявляє спорідненість до кальцієвих каналів L-типу в 100-200 разів вище порівняо з R-ізомером. Особливістю препарату є високий показник ліпофільності (logP-коефіцієнт розподілу октанол-вода), що становить 6,42, завдяки чому лерканідипін здатний накопичуватися в ліпідному шарі клітинних мембран клітин з утворенням депо, з якого повільно вивільняється (табл. 1). Виражена ліпофільність лерканідипіну визначає його високу зв’язаність з ліпідами мембран, пролонговану взаємодію з L-типом кальцієвих каналів і тривалішу дію порівняно з іншими ДГП БКК [1].
Ліпофільні властивості препарату обумовлюють короткий період напіврозпаду плазми та значну тривалість дії. Період напіввиведення лерканідипіну становить ≈2 год, що знижує навантаження на екскреторні органи та покращує переносимість. Поступове вивільнення і тривала дія – найважливіші характеристики лерканідипіну, необхідні для підтримки ефективної концентрації препарату та контролю АТ протягом доби за одноразового прийому. Лерканідипін метаболізується мікросомальними ферментами печінки до неактивних метаболітів і виводиться майже однаково нирками (44%) і через кишечник (56%). Подвійний шлях виведення створює переваги у виборі дози препарату для печінкової, а також легкої і помірної ниркової недостатності, оскільки корекція дози не потрібна. Прийом препарату 1 р/добу забезпечує його терапевтичну активність >24 год. Біодоступність лерканідипіну не змінюється з віком; у пацієнтів із цирозом печінки, а також у хворих із вираженою дисфункцією нирок спостерігається затримка виведення препарату. Препарат є метаболічно нейтральним, не змінює концентрації глюкози, сечової кислоти, креатиніну, основних електролітів, не має негативного впливу на тонус м’язів бронхів, травної системи, статеву функцію, що надає підстави для застосування цього препарату в пацієнтів з АГ і коморбідною патологією.
Дані досліджень свідчать про те, що в пацієнтів з АГ лікування лерканідипіном пов’язане з регресією мікросудинних структурних змін, що підтверджується оцінкою артеріолярної морфології сітківки. Співвідношення товщини стінки до просвіту артеріол сітківки було оцінено за допомогою сканувальної лазерної доплерівської флоуметрії для оцінки перфузії сітківки. Результати показали, що лерканідипін значно зменшує співвідношення стінки до просвіту, а також товщину стінки та площу поперечного перерізу стінок артерій сітківки. Цей ефект може бути пов’язаний з антиоксидантними та протизапальними властивостями лерканідипіну, які разом зі зниженням АТ мають високу клінічну значимість, ураховуючи роль ендотеліальної дисфункції, оксидативного стресу, запалення і жорсткості артерій у патогенезі атеросклерозу, ушкодженні органів-мішеней у разі тривалого серцево-судинного захворювання [2].
Лерканідипін має виражений нефропротекторний ефект, що було показано в дослідженнях на щурах зі спонтанною гіпертензією. Препарат може контролювати тиск у клубочкових капілярах, а також індукувати вазодилатацію аферентних і еферентних клубочкових артеріол у щурів після 12 тиж застосування. Крім того, лерканідипін має здатність пригнічувати гіпертрофію клубочків, а також покращувати морфологію звивистих канальців у щурів в експерименті. При спонтанній гіпертензії у щурів на тлі прийому лерканідипіну спостерігалася вазодилатація на різних ділянках ниркових артеріол. Препарат має здатність збільшувати просвіт артерій, пригнічувати потовщення туніки, зменшувати кількість сполучної тканини всередині адвентиції і зумовлювати зворотний розвиток ремоделювання ниркових артеріальних гілок у щурів зі спонтанною гіпертензією. На відміну від інших антагоністів дигідропіридину кальцієвих каналів (манідипіну та нікардипіну), лерканідипін стимулює вазодилатацію дрібних артерій діаметром <25 мкм. У судинних сегментах діаметром 50-150 мкм лерканідипін спричиняє зворотний розвиток ремоделювання набагато більшою мірою (р<0,05), ніж манідипін і нікардипін. У щурів зі спонтанною гіпертензією на тлі застосування лерканідипіну спостерігалося зниження концентрації альбуміну в сечі, а також знижувалася протеїнурія після субтотальної нефректомії. Однак ці ефекти ще не підтверджені в повному обсязі в клінічних дослідженнях за участю пацієнтів з АГ. Як і в разі випробування інших антагоністів кальцієвих каналів за терапії лерканідипіном не спостерігалося значного впливу на співвідношення альбумін/креатинін у пацієнтів з АГ та ЦД 2 типу, які приймали препарат протягом 16 тиж.
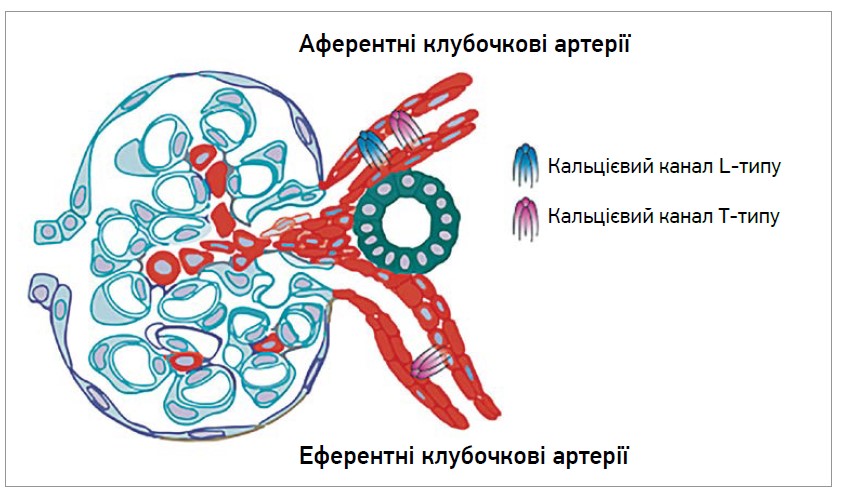
На нирковому рівні лерканідипін діє не так, як інші ДГП БКК І і ІІ поколінь. Він розширює як аферентні, так і еферентні клубочкові артерії, при цьому внутрішньогломерулярний капілярний тиск залишається незмінним (рис. 1).
Рис. 1. Вплив лерканідипіну на клубочкові артерії
Вважається, що ця здатність є наслідком інгібування як L-типу (прегломерулярного), так і Т-типу (постгломерулярного) кальцієвих каналів на нирковому рівні. Постгломерулярні артерії збагачені кальцієвими каналами Т-типу; доведено, що БКК ІІІ покоління інгібують канали Т-типу в постгломерулярних судинах. Окрім того, лерканідипін зменшує інтерстиціальний фіброз і мікроальбумінурію у щурів із гіпертензією, демонструючи нефропротекторний ефект, незалежний від зниження АТ. Позитивний вплив лікарського засобу був підтверджений у моделі подвійного трансгенного щура з надмірною експресією генів людського реніну й ангіотензиногену. Лікування лерканідипіном запобігало ушкодженню нирок і смертності, пов’язаній з ангіотензином II. У пролікованих тварин протеїнурія знижувалася, а рівень креатиніну в плазмі крові підтримувався в межах норми порівняно з нелікованими щурами. Крім того, в ниркових судинах спостерігалися зниження інфільтрації моноцитів, утворення позаклітинного матриксу, фіброзу. Ці ефекти можуть бути результатом пригнічення запалення тканин і поліпшення біодоступності оксиду азоту, а також були підтверджені в дослідженні, в якому ендотеліальна функція в 15 здорових осіб і 15 пацієнтів з АГ оцінювалася за ступенем вазодилатації у відповідь на інфузію брадикініну. Терапія лерканідипіном у дозі 10 мг/добу протягом 3 міс значно підвищувала реакцію плечової артерії на інфузію брадикініну. Знижувалася блокувальна дія інгібіторів оксиду азоту, а також плазмові концентрації малондегіду, ізопростаноїдів, підвищувалася антиоксидантна активність плазми крові. Отже, лерканідипін підвищує біодоступність оксиду азоту й ендотелій-залежну вазодилатацію в пацієнтів з АГ, зменшує маркери оксидативного стресу, пригнічує проліферацію судинних неоінтимальних і гладком’язових клітин, а також накопичення холестерину за рахунок зменшення клітинних реактивних видів кисню. Препарат зменшує рівень лейкоцитів, С-реактивного білка, Е-селектину, Р-селектину та внутрішньоклітинних молекул адгезії, що беруть участь у процесах тромбоутворення і ушкодження судин, а також тканин [3].
На відміну від інших представників ДГП БКК, лерканідипін знижує симпатичну активність, пов’язану з АГ. Під час хронічного лікування в разі зіставного зниження АТ концентрація норадреналіну в плазмі крові не модифікувалася лерканідипіном (10-20 мг/добу), а збільшувалася на тлі прийому ніфедипіну та фелодипіну. Крім того, м’язовий симпатичний нервовий рух, оцінений за допомогою мікронейрографії, був зменшений лерканідипіном і збільшений фелодипіном, а це свідчить про те, що лерканідипін як монотерапія або в поєднанні з еналаприлом під час хронічного введення не спричиняє симпатичної активації, вторинної до периферичної вазодилатації. Цей аспект має важливе клінічне значення, враховуючи те, що симпатична гіперактивність може бути пов’язана з розвитком і прогресуванням ураження органів-мішеней та серцево-судинних подій у пацієнтів з АГ [4].
В іншому дослідженні в 60 хворих на есенціальну гіпертензію було виявлено значне підвищення рівня норадреналіну в плазмі крові за прийому ніфедипіну в дозі 30-60 мг/добу (р<0,05), що не спостерігалося при прийомі лерканідипіну в дозі 10-20 мг/добу протягом 48 тиж лікування. Завдяки аналізу порівняльних клінічних досліджень засвідчено, що в пацієнтів з АГ різного ступеня під час лікування лерканідипіном (10 або 20 мг/добу протягом 2-16 тиж) істотних змін у параметрах електрокардіограми не спостерігалося. Загалом при лікуванні лерканідипіном жодного впливу препарату на частоту серцевих скорочень виявлено не було. Кількість пацієнтів, у яких спочатку були шлуночкові та/або надшлуночкові аритмії, також істотно не змінювалася після 2 тиж терапії лерканідипіном. На тлі відсутності активації симпатоадреналової системи з боку лерканідипіну препарат проявляє антиангінальну дію. У хворих зі стабільною стенокардією його призначення в дозі 10-20 мг протягом 2 тиж зумовило позитивні клінічні зміни: зменшилася кількість нападів стенокардії та необхідної дози нітрогліцерину, підвищилася толерантність до фізичних навантажень, за даними холтерівського моніторингу, зменшилися прояви ішемії міокарда, не змінилися частота серцевих скорочень, концентрація норадреналіну, адреналіну в плазмі крові.
Як й інші БКК лерканідипін має антиатерогенні властивості, безпосередньо не пов’язані з його гіпотензивною активністю. In vitro продемонстровано, що в концентраціях 10-50 мкмоль/л лерканідипін може пригнічувати проліферацію гладком’язових клітин артерій і знижувати ступінь атеросклеротичних уражень судин у кроликів із гіперхолестеринемією. Дослідження за участю пацієнтів з АГ і ЦД 2 типу чи без нього показали, що лерканідипін має антиоксидантну активність. За його прийому в дозі 10 мг/добу протягом 16 тиж було виявлено значне зниження інтенсивності окислення ЛПНЩ (р<0,001), зіставне з таким при терапії лозартаном у дозі 50 мг/добу. Останніми роками з’явилися експериментальні дослідження, що констатують антиатеросклеротичні властивості лерканідипіну. Антиатеросклеротичні ефекти ДГП БКК ІІІ покоління були продемонстровані в окремих рандомізованих клінічних випробуваннях. Установлено, що в малих дозах (10 мг) препарат значно знижує інтенсивність потовщення комплексу інтима-медіа сонних артерій. Механізм цього впливу обумовлений сприятливим впливом на ендотелій, зниженням швидкості відкладення атерогенних ліпопротеїнів до судинної стінки, однак вивчення можливих механізмів цієї властивості лерканідипіну потребує подальшої розробки й аналізу. Лерканідипін є метаболічно нейтральним препаратом. Як свідчать результати подвійних рандомізованих досліджень, лерканідипін у дозах 10-30 мг/добу протягом 24-48 тиж істотно не змінював показників ліпідного профілю, а в одному з них навіть спостерігалася тенденція до зниження рівня загального холестерину. Вплив лерканідипіну на вуглеводний обмін продемонстровано в дослідженні, де прийом препарату в дозі 10 або 20 мг/добу протягом 8 тиж спричиняв зниження глюкози в крові натще, HbA1c і фруктозаміну сироватки крові порівняно з початковими даними (p<0,001), а також покращував показники глюкозотолерантного тесту (p<0,001). У додаткових дослідженнях було встановлено, що застосування лерканідипіну в дозі 10 мг/добу протягом 16 тиж не впливало на рівень HbA1c, але через 6 міс терапії зумовлювало достовірне зниження рівня глюкози в крові (p<0,00005) [5]. За результатами багатьох досліджень установлено нейропротекторні властивості лерканідипіну. Так, при 10-хвилинній білатеральній оклюзії сонних артерій лерканідипін, на відміну від інших антигіпертензивних препаратів (валсартан, нікардипін, лізиноприл), запобігав пізній (через 1 тиж після ішемії) загибелі нейронів гіпокампа, рівною мірою знижуючи АТ порівняно з іншими досліджуваними лікарськими засобами. Результати випробування дозволили передбачити клінічні можливості лерканідипіну в зниженні ризику розвитку деменції, спричиненої ішемічними мікроінсультатами. Роботи вітчизняних науковців засвідчили, що лерканідипін у дозі 10 мг покращує церебральну гемодинаміку за рахунок судинного та нейрогенного механізму дії. Лерканідипін у хворих на АГ 2 ступеня та дисциркуляторну енцефалопатію 2 ступеня чинить гармонізувальну дію на біоелектричну активність головного мозку; характеризується зниженням потужності повільних ритмів на тлі підвищеної потужності в діапазоні альфа-ритму в двох півкулях, особливо в лобових ділянках. Препарат збільшує лінійну швидкість кровотоку в двох вертеброцеребральних артеріях, що дозволяє дійти висновку про вазоактивну та метаболічну дію на функціональний стан головного мозку в пацієнтів з АГ [6].
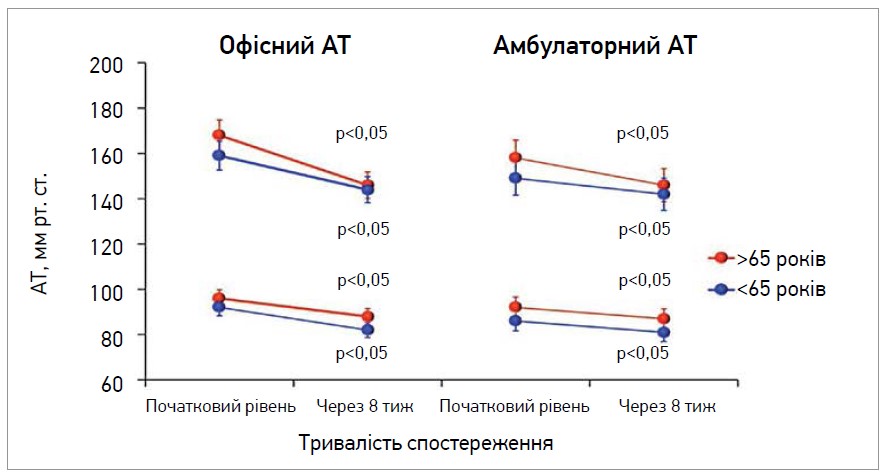
Терапевтична ефективність лерканідипіну була оцінена в подвійних сліпих рандомізованих порівняльних дослідженнях і великих обсерваційних аналізах у пацієнтів з АГ різного ступеня, ізольованою систолічною гіпертензією, АГ, ЦД, ХХН, множинними серцево-судинними факторами ризику, а також у людей похилого віку. Для лікування АГ лерканідипін зазвичай призначається в дозі 10-20 мг 1 р/добу. Такий режим прийому є зручним для хворих і створює передумови для високої прихильності до лікування. Антигіпертензивна ефективність лерканідипіну є добре вивченою. Серед хворих з АГ 1 та 2 ступенів відсоток пацієнтів, які мали хорошу терапевтичну відповідь на лікування лерканідипіном у дозі 10-20 мг/добу, становив ≈68%. Лекарнідипін однаково добре контролює АТ як у молодих, так і в літніх хворих без потреби зниження дози у вікових пацієнтів. У дослідженні AGATE порівняли ефективність лерканідипіну в осіб віком <65 років, а також >65 років. Проаналізували результати лікування в 691 хворого: 375 осіб мали вік <65 років, 316 – >65 років. Лерканідипін призначався в дозі 10 мг; за потреби вона подвоювалася або додавали препарати інших груп (рис. 2). Наприкінці дослідження 507 хворих отримували монотерапію лерканідипіном (221 хворий – 10 мг/добу, 286 – 20 мг/добу) та 184 осіб – комбіновану терапію. Зниження АТ виявилося зіставним у хворих віком <65 років і >65 років – систолічний АТ (САТ) знизився на 17 і 21 мм рт. ст., діастолічний (ДАТ) – на 10 та 9 мм рт. ст. відповідно [7].
Рис. 2. Антигіпертензивна ефективність лерканідипіну в пацієнтів з АГ різних вікових груп
Цей висновок підтверджено в дослідженні, метою якого було дослідити ефективність і переносимість лерканідипіну у великій невідібраній популяції пацієнтів з АГ. Отримано схожі показники зниження САТ/ДАТ у пацієнтів віком <65 років і хворих >65 років (–24/14 мм рт. ст. та –29/13 мм рт. ст.), що супроводжувалося нормалізацією АТ у 65 й 60% пацієнтів відповідно. Крім того, антигіпертензивна ефективність препарату не залежала від гендерних відмінностей і дозволила досягти цільових значень АТ у 66% жінок та в 61% чоловіків.
У дослідженні ELYPSE вивчали антигіпертензивну ефективність лерканідипіну в дозі 10 мг/добу в 9059 пацієнтів з АГ 1-2 ступенів [8]. Після 1 міс спостерігалося зниження САТ на 13,5±11,5, ДАТ – на 9,4±7,7 мм рт. ст. Через 3 міс нарощувався антигіпертензивний ефект, а також (що є дуже важливим) досягнуто незначного, але достовірного (р<0,01) зменшення частоти серцевих скорочень порівняно з початковими показниками [8].
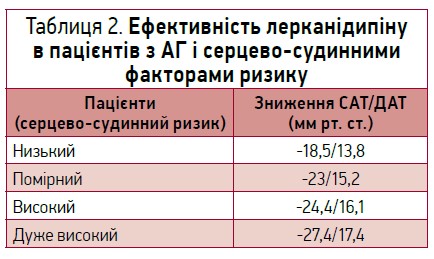
Особливу увагу привертають аспекти застосування лерканідипіну в пацієнтів з АГ і супутніми факторами серцево-судинного ризику. У 2004 році A. Marx і співавт. довели антигіпертензивну ефективність лерканідипіну в 6-тижневому обсерваційному дослідженні, яке включало 32 345 хворих з м’якою та помірною АГ і супутніми коморбідними станами: з ІХС, серцевою недостатністю, ЦД 2 типу, дисліпідемією. Важливим було те, що препарат є ефективним у пацієнтів з АГ у всіх групах серцево-судинного ризику, причому найкращий ефект спостерігався в хворих із дуже високим ризиком [9].
У багатоцентровому обсерваційному відкритому дослідженні LAURA, в якому взяло участь 3175 пацієнтів, оцінювалася ефективність лерканідипіну в пацієнтів з АГ і супутніми факторами ризику серцево-судинних захворювань, як-от дисліпідемія, куріння, сімейний анамнез серцево-судинних захворювань, ураження органів-мішеней. Після 6 міс лікування лерканідипіном зниження АТ спостерігалося в усіх групах пацієнтів, хоча найбільше зниження АТ отримано серед хворих дуже високого серцево-судинного ризику (табл. 2). Контролю АТ вдалося досягти в 55% пацієнтів, котрі отримували лерканідипін у дозі 10 мг/добу, а також у 82% хворих, яким підвищили дозу препарату до 20 мг/добу [10].
У дослідженні LERZAMIG взяли участь 2793 пацієнти з таким фактором ризику, як ожиріння або надлишкова маса тіла. Мета цього випробування – оцінити, чи впливають на ефективність і переносимість лерканідипіну в хворих з АГ показники індексу маси тіла (ІМТ) або відсоток жиру в організмі. Загалом у багатоцентровому проспективному відкритому дослідженні взяли участь 2793 амбулаторні пацієнти (середній вік складав 59,8 року) з легкою та помірною гіпертензією. Всі хворі протягом 12 тиж отримували лікування лерканідипіном у дозі 10 мг, яку титрували до 20 мг, якщо контролю АТ не було досягнуто. На початку дослідження АТ становив 159,4/94,5 мм рт. ст. Через 3 міс лікування АТ знизився до 138/81 мм рт. ст. Доведено, що зниження АТ не залежало від початкового ІМТ і відсотка жиру в організмі, 42% пацієнтів високого ризику потребували дози 20 мг, при цьому спостерігався низький відсоток виникнення побічних ефектів (5,5%) [11].
У хворих із ЦД застосування лерканідипіну може мати особливі переваги. Крім нормалізації АТ, продемонстровано відсутність негативного впливу на стан вуглеводного обміну. Дані, отримані в пацієнтів з АГ і ЦД 2 типу, показали, що антигіпертензивна ефективність лерканідипіну як монотерапії не була пов’язана з порушенням гомеостазу глюкози. На початковому етапі пацієнтів рандомізували для отримання 10 або 20 мг лерканідипіну. Дозу можна було збільшити через 4 тиж до 20 або 30 мг відповідно до клінічної відповіді. Наприкінці випробування в 55% пацієнтів спостерігалася ефективна антигіпертензивна відповідь на дозу 10 мг, а також у 95%, які приймали 20 мг лерканідипіну. В цих хворих рівень глюкози в крові натще значно знизився (зі 153 до 133 мг/дл), а також рівень глікозильованого гемоглобіну (із 5,8 до 5,5%), фруктозаміну (із 280 до 230 мг/дл), площі під кривою, отриманої під час перорального тесту на толерантність до глюкози, та практично не залежав від дози препарату.
ДГП БКК можуть здійснювати нефропротекторні ефекти під час тривалого лікування АГ, адже вони мають гетерогенний вплив на ниркову гемодинаміку. На відміну від інших представників цього класу лерканідипін спричиняє дилатацію як аферентних, так і еферентних клубочкових артерій, запобігаючи підвищенню внутрішньоклубочкового капілярного тиску та ураженню нирок у майбутньому. На думку дослідників, саме із цими властивостями пов’язана наявність у лерканідипіну нефропротекторної дії, яка була переконливо продемонстрована в дослідженнях DIAL і ZAFRA (ZAndip en Function Renal Alterada).
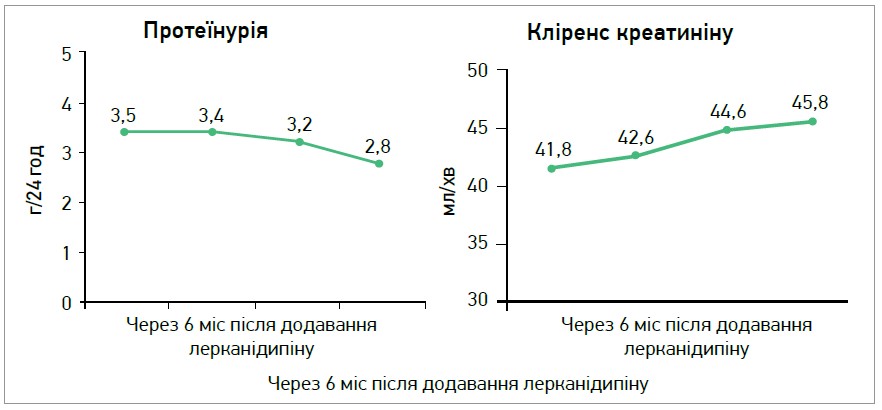
У випробуванні ZAFRA вивчалися антигіпертензивна ефективність, можливість покращення кліренсу креатиніну за рахунок додавання лерканідипіну в пацієнтів з АГ з або без ЦД 2 типу та із помірною ХНН, які приймали ІАПФ (63,4%) чи БРА (36,6%). У дослідженні взяли участь 203 пацієнти із ХНН, що розвинулася внаслідок різної патології (гіпертензивна нефропатія, інтерстиціальна нефропатія / пієлонефрит, діабетична нефропатія, гломерулонефрит тощо). Початкова концентрація креатиніну плазми склала >1,4 мг/дл у чоловіків, >1,2 мг/дл – у жінок. У всіх пацієнтів рівень АТ виявився вищим за рекомендований при ХНН (>130/85 мм рт. ст.). Лерканідипін додавали до терапії у дозі 10 мг/добу протягом 6 міс із метою досягнення цільових цифр АТ. Статистично достовірне зниження рівня АТ спостерігали вже через 1 міс лікування комбінованою терапією, до якої входив лерканідипін. Протягом 6-місячного періоду спостереження додавання лерканідипіну до терапії блокаторами РАС виявилося безпечним і ефективним, дозволило ще більше знизити САТ від 162 до 132 мм рт. ст., ДАТ від 93 до 78 мм рт. ст., а в 58,1% хворих досягти цільового рівня АТ. На тлі комбінованої антигіпертензивної терапії відзначили покращення функції нирок, що асоціювалося зі збільшенням кліренсу креатиніну зі 41,8 до 45,8 мл/хв (р=0,019), а також зниженням добової протеїнурії з 3,5 до 2,8 г (р=0,015). Під час дослідження рівня загального холестерину в плазмі крові виявили достовірне зниження із 221 до 211 мг/дл (р=0,001). Частота небажаних ефектів становила 3,4% (рис. 3). Результати дослідження засвідчили високу антигіпертензивну ефективність лерканідипіну в пацієнтів із супутнім захворюванням нирок, а також підтвердили припущення про уповільнення прогресування ХНН у разі застосування ДГП БКК у комбінації з інгібітором АПФ чи БРА [12].
Рис. 3. Застосування лерканідипіну в хворих із ХНН
Ці дані є зіставними з результатами дослідження Diabete Ipertensione Albuminuria Lercanidipina, в якому оцінювалася ефективність монотерапії лерканідипіном (10-20 мг/д) порівняно з раміприлом (5-10 мг/д) у пацієнтів із легкою та помірною гіпертензією, ЦД 2 типу та стійкою мікроальбумінурією. Результати цієї роботи засвідчили зниження мікроальбумінурії на >50% у 34,2 та 22,2% хворих, котрі отримували лікування лерканідипіном і раміприлом відповідно [13].
Нефропротекторний та антиальбумінурійний ефекти лерканідипіну можуть бути наслідком його протекторного впливу на клубочкову гемодинаміку, інгібування проліферації мезангіальних клітин, пригнічення ендотеліально-опосередкованих ниркових ефектів, підвищення активності синтезу оксиду азоту, що зумовлює розвиток антиоксидантних ефектів. Зниження окислювального стресу на тлі прийому лерканідипіну може бути пов’язано з інгібуванням судинної неоінтими та проліферації гладком’язових клітин і накопичення холестерину.
Вплив лерканідипіну на протеїнурію виявився дозозалежним і не корелював з антигіпертензивною ефективністю. Протекцію нирок зі значним зниженням мікроальбумінурії, а також оптимізацією кліренсу креатиніну продемонстровано в пацієнтів із ЦД і порушенням функції нирок. Отже, можна стверджувати, що лерканідипін завдяки своїм унікальним нефропротекторним властивостям займає особливе місце серед ДГП БКК у лікуванні діабетичної нефропатії та недіабетичних захворювань нирок, у т. ч. у пацієнтів із ХНН.
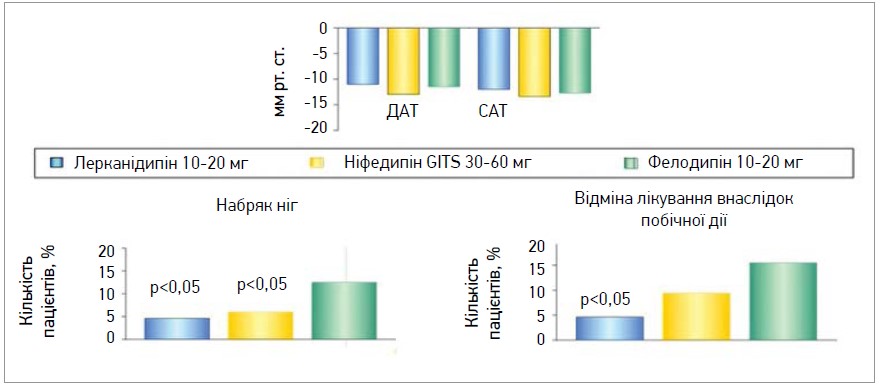
Слід зазначити про хорошу переносимість лерканідипіну, частота розвитку побічних реакцій якого є зіставною із плацебо. Результати порівняльного аналізу антигіпертензивного ефекту лерканідипіну з іншими ДГП БКК (амлодипін, ніфедипін, фелодипін, лацидипін, ретардні лікарські форми) й ІАПФ свідчать про певні його переваги. Так, у дослідженні LEAD проведено порівняльний аналіз впливу терапії протягом 8 тиж лерканідипіном (10 мг/д), ніфедипіном (30 мг/д), фелодипіном (10 мг/д) на АТ, частоту серцевих скорочень, частоту виникнення побічних реакцій, прихильність до лікування в 325 хворих з м’якою / помірною АГ. Антигіпертензивний ефект виявився зіставним у всіх групах, але профіль безпеки та прихильність пацієнтів до лікування лерканідипіном перевершували ці показники в групах порівняння. Розвиток побічної реакції (набряк ніг) у групі лерканідипіну спостерігався лише в 5,5% хворих, ніфедипіну – в 6,6%, фелодипіну – в 13% (р<0,05). Відзначався достовірно менший відсоток пацієнтів, які припинили прийом лерканідипіну (<5%) порівняно із хворими, котрі приймали інші ДГП БКК (р<0,05). Лерканідипін ефективно знижував АТ, практично не впливав на частоту серцевих скорочень як у стані спокою, так і під час проведення різних психологічних тестів. Слід зазначити, що прийом лерканідипіну навіть у дозі 40 мг/добу не супроводжувався підвищенням частоти серцевих скорочень (рис. 4). Прийом лерканідипіну протягом 48 тиж не впливав на рівень норадреналіну в плазмі в хворих на АГ. Відсутність ознак симпатоадреналової активації у лерканідипіну є надзвичайно важливою властивістю, особливо для хворих, яким потрібна постійна антигіпертензивна терапія [14].
Рис. 4. Результати порівняльного аналізу антигіпертензивного ефекту лерканідипіну з іншими ДГП БКК
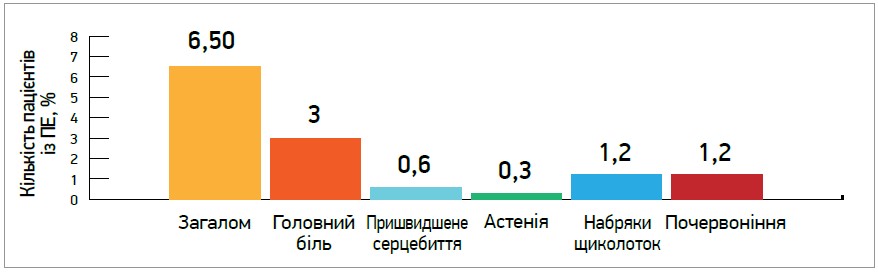
Найчастіші побічні явища на тлі прийому ДГП БКК: набряк гомілковостопного суглоба, запаморочення, головний біль, припливи, пришвидшене серцебиття. Численні дослідження показали, що лікування лерканідипіном асоціюється з дуже низькою частотою побічних ефектів і відмовою від продовження терапії. Навіть якщо відсотки виникнення побічних ефектів дещо відрізняються між собою в різних дослідження і становлять загалом у 11,5-11,8% пацієнтів, характерна для всіх ознака – дуже низький відсоток (1-2%) припинення лікування лерканідипіном через побічні ефекти. В дослідженні ELYPSE, до якого залучили 9000 хворих, побічні ефекти реєструвалися в 6,5% випадків (рис. 5). Порівняно з іншими ДГП БКК (амлодипіном, фелодипіном, лацидипіном, ніфедипіном, нітрендипіном) переносимість лерканідипіну була кращою протягом тривалої терапії [15].
Рис. 5. Частота побічних ефектів на тлі лікування лерканідипіном
Примітка: ПЕ – побічний ефект.
Вищезазначене підтверджується отриманими результатами в клінічних випробуваннях, зокрема в 2 метааналізах досліджень. Порівняно з наданими об’єднаними даними для амлодипіну, ніфедипіну, фелодипіну, лікування лерканідипіном асоціюється зі значно меншим відсотком пацієнтів із периферичним набряком (7,0 проти 14,0%; p<0,001), зниженням відносного ризику на 56%. Це може бути пов’язано з тим, що ліпофільні ДГП БКК асоціюються зі зниженням ризику розвитку набряку щиколотки на 57% порівняно з гідрофільними ДГП БКК. Низька частота виникнення набряків щиколоток на лерканідипіні не залежить від віку, статі, етнічної групи, наявності супутніх серцево-судинних захворювань або зниження АТ.
Отже, лерканідипін – ДГП БКК ІІІ покоління, що характеризується високою вазоселективністю, вираженим і довготривалим антигіпертензивним ефектом; має органопротекторні властивості, є метаболічно нейтральним, чудово переноситься, може успішно застосовуватися як у монотерапії, так і в комбінації з будь-якими іншими класами антигіпертензивних препаратів як у чоловіків, так і в жінок. Застосування лерканідипіну може сприяти нейро-, нефро- й ангіопротекції. Хороша переносимість, низький ризик розвитку побічних ефектів, а також зручний режим прийому створюють передумови для високої прихильності хворих до лікування цим препаратом.
Висновки
Фармакологічна характеристика. Лерканідипін – ліпофільний ДГП БКК ІІІ покоління. Завдяки високій ліпофільності він легко проникає, має значну концентрацію та стійкість у подвійному шарі фосфоліпідів мембран гладком’язових клітин, звідки поступово вивільняється, досягаючи кальцієвих каналів, тому, незважаючи на відносно короткий період напіввиведення, фармакологічна активність лерканідипіну пролонгується.
Антигіпертензивна ефективність. Загалом антигіпертензивна ефективність лерканідипіну не поступається такій інших препаратів; у деяких дослідженнях він навіть перевершував ефективність інших ДГП БКК або інші класи антигіпертензивних препаратів. Дозування лерканідипіну в різних дослідженнях становило 10-20 мг/добу. Антигіпертензивна ефективність лерканідипіну була продемонстрована в пацієнтів із легкою та помірною гіпертензією, а також у хворих із ЦД 2 типу, захворюваннями нирок, ізольованою систолічною гіпертензією, декількома супутніми факторами ризику серцево-судинних захворювань.
Вплив на нирки. Дослідження за участю пацієнтів з АГ і ЦД або порушенням функції нирок показали, що лерканідипін має нефропротекторну дію, оскільки розширює аферентні й еферентні клубочкові артерії, зберігаючи внутрішньоклубочковий тиск. На відміну від інших БКК було також продемонстровано, що лерканідипін зменшує альбумінурію, визнаний фактор ризику серцево-судинних подій у пацієнтів з АГ.
Переносимість. Лерканідипін має сприятливий профіль переносимості з меншою частотою виникнення побічних ефектів, особливо периферичних набряків, а також відміни прийому через них порівняно з амлодипіном, ніфедипіном, фелодипіном. Окрім того, прихильність хворих до терапії лерканідипіном є вищою, ніж до БКК І та ІІ поколінь. Ці докази мають велике значення для повсякденної клінічної практики та можуть допомогти лікарям краще адаптувати лікування відповідно до потреб пацієнтів і терапевтичної відповіді.
Отже, під час обрання препарату для лікування пацієнтів з АГ, у т. ч. із тяжкою коморбідною патологією, можна стверджувати, що серед ДГП БКК перевагу слід віддавати лерканідипіну. Антигіпертензивний ефект препарату обумовлює його застосування для лікування хворих на легку та тяжку резистентну АГ, ізольовану систолічну АГ, а наявність антиангінального ефекту визначає його перспективне застосування в лікуванні ІХС. Важлива властивість лерканідипіну – нефропротекція (зниження внутрішньоклубочкового тиску, швидкості виведення альбуміну, збільшення кліренсу креатиніну) в хворих на гіпертонічну та діабетичну нефропатію, пієлонефрит і гломерулонефрит, унаслідок чого сповільнюється прогресування ХНН. Велике значення в лікуванні пацієнтів із порушенням мозкового кровотоку, в т. ч. у гострому періоді мозкового інсульту, мають нейропротекторні властивості лерканідипіну.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 10 (546), 2023 р.