31 жовтня, 2023
Комплексний підхід до лікування дітей і підлітків зі спадковим ангіоневротичним набряком
 Спадковий ангіоневротичний набряк (САН) є рідкісним аутосомно-домінантним захворюванням, яке характеризується рецидивними епізодами ангіоневротичного набряку (АН). САН є серйозною глобальною проблемою, яка суттєво впливає на якість життя (ЯЖ) не тільки самих пацієнтів, а й членів їхніх сімей. Напади АН можуть спотворювати обличчя, призводити до інвалідності, викликати біль і навіть загрожувати життю, якщо виникає набряк гортані. Симптоми САН зазвичай проявляються в дитинстві. Для лікування цієї патології у дітей доступні та схвалені ефективні ліки, однак доказова база щодо застосування цих препаратів у педіатричній клінічній практиці обмежена. У цій статті представлений огляд принципів менеджменту САН, якими медичні працівники можуть керуватися при лікуванні педіатричних пацієнтів.
Спадковий ангіоневротичний набряк (САН) є рідкісним аутосомно-домінантним захворюванням, яке характеризується рецидивними епізодами ангіоневротичного набряку (АН). САН є серйозною глобальною проблемою, яка суттєво впливає на якість життя (ЯЖ) не тільки самих пацієнтів, а й членів їхніх сімей. Напади АН можуть спотворювати обличчя, призводити до інвалідності, викликати біль і навіть загрожувати життю, якщо виникає набряк гортані. Симптоми САН зазвичай проявляються в дитинстві. Для лікування цієї патології у дітей доступні та схвалені ефективні ліки, однак доказова база щодо застосування цих препаратів у педіатричній клінічній практиці обмежена. У цій статті представлений огляд принципів менеджменту САН, якими медичні працівники можуть керуватися при лікуванні педіатричних пацієнтів.
Більшість випадків САН пов’язана з мутаціями в гені SERPING 1, який кодує С1-INH [1]. Визначають 2 типи САН, пов’язані з дисфункцією C1-INH у плазмі крові. САН 1 типу, на який припадає близько 85% випадків, характеризується низьким рівнем C1-INH у плазмі крові. САН 2 типу, на який припадає близько 15% випадків, характеризується нормальним рівнем білка C1-INH, який є дисфункціональним [2]. САН характеризується непередбачуваними, гострими, рецидивуючими епізодами АН без свербежу [3, 4]. Набряки зазвичай виникають у шкірі й підшкірній клітковині або слизових оболонках верхніх дихальних шляхів (ВДШ), шлунково-кишкового тракту (ШКТ) та сечовивідних шляхів [3, 4]. Напади можуть бути спотворюючими, інвалідизуючими, болючими і навіть нести небезпеку для життя, якщо розвинувся АН гортані [3-5]. Епізоди САН можуть виникати спонтанно або у відповідь на такі фактори, як травма, психологічний стрес чи інфекції [3, 4]. Патофізіологія розвитку АН при САН пов’язана з тим, що дефіцит С1-INH призводить до надлишкової продукції брадикініну й активації рецептора брадикініну В2. Все це викликає збільшення проникності судин і, відповідно, просочування рідини в навколишні тканини, що і спричиняє АН [6, 7].
Симптоми САН, як правило, проявляються в дитинстві, причому вік появи симптомів коливається від 4,4 до 18 років [4, 8]. Хоча в рідкісних випадках напади можуть виникати на першому році життя, існує єдиний задокументований випадок, коли напад САН стався внутрішньоутробно у дитини, у матері якої напад стався під час активних пологів [9, 10]. Середній вік першого епізоду САН становить 10 років, а приблизно 40% пацієнтів мають перший епізод у віці до 5 років [3, 4, 8].
Поява клінічних симптомів у ранньому віці асоціюється з більш тяжким перебігом захворювання, включаючи більшу кількість епізодів САН на рік та більшу кількість госпіталізацій з приводу симптомів, пов’язаних із САН [10]. Частота епізодів САН зростає в період статевого дозрівання [11]. Як ранній початок САН, так і частота нападів пов’язані з більш негативним впливом на ЯЖ і настрій дитини [11-13]. Окрім того, саме по собі захворювання і напади САН впливають на ЯЖ, включаючи фізичну, емоційну та психосоціальну сфери [14]. Хоча жодне дослідження спеціально не оцінювало психологічний вплив САН у дітей і підлітків, численні дослідження задокументували негативний вплив хронічного захворювання на їх психологічний стан [15].
Середній час від появи симптомів до встановлення діагнозу САН становить 8,5 років. Діагноз часто встановлюється із запізненням, навіть пацієнтам з обтяженим сімейним анамнезом щодо САН [16]. Затримка діагностики цієї патології у дітей може бути пов’язана з тим, що САН є рідкісним захворюванням і більшість симптомів можуть імітувати симптоми більш поширених захворювань. При цьому затримка з діагностикою може відтермінувати ефективне лікування і призвести до невідповідного лікування або непотрібних хірургічних втручань [16].
Для лікування дітей із САН доступні та схвалені ефективні лікарські засоби. Однак доказова база щодо застосування цих препаратів у дитячій клінічній практиці є обмеженою, оскільки клінічні дослідження цих препаратів були зосереджені переважно на дорослих і недостатньо охоплювали пацієнтів дитячого віку [1]. Важливо враховувати, що обрана стратегія лікування має вирішальне значення для оптимізації результатів лікування і повинна включати лікування, запобігання виникненню фатальних ускладнень, а також вирішення неклінічних аспектів САН, включаючи ЯЖ та психологічні проблеми педіатричних пацієнтів.
Діагноз
Рання діагностика САН має вирішальне значення для зниження смертності та захворюваності, а також розробки відповідної стратегії лікування. Першим епізодом САН може бути набряк гортані, який може призвести до летального результату [1, 5, 18]. Результати попереднього аналізу 70 пацієнтів із САН, які померли внаслідок набряку гортані, продемонстрував, що смертність була вищою у пацієнтів із недіагностованим САН (63 випадки), ніж у пацієнтів із діагностованим САН (7 випадків) [2, 5]. Набряк ВДШ також є більш вираженим у пацієнтів дитячого віку через менший діаметр дихальних шляхів, що підвищує ризик асфіксії [1].
Перешкодами для ранньої діагностики САН є погане розпізнавання симптомів медичними працівниками, відсутність належних інструментів скринінгу та доступу до простих лабораторних тестів, які допомагають встановити точний діагноз [16, 19-21]. Симптоми САН зазвичай проявляються в дитинстві, а затримка діагностики може призвести до невідповідного лікування і непотрібних медичних втручань [16].
Незважаючи на сімейний характер захворювання, багато членів сімей пацієнтів із САН не проходять необхідний скринінг [21]. Опитування показало, що лише 48% найближчих родичів і 26% членів сім’ї були протестовані на наявність захворювання [21]. З появою ефективних методів лікування все частіше наголошується на необхідності скринінгу членів сім’ї як способу зниження значної захворюваності та смертності, пов’язаної із САН [21]. Кожна дитина з обтяженим сімейним анамнезом (мати або батько мають підтверджений САН) має 50% ймовірність успадкувати цей розлад, тому всіх немовлят із сімейним анамнезом САН потрібно розглядатися як таких, що мають цей розлад, доки діагноз не буде виключений [1, 21].
Клінічна презентація
 Клінічний перебіг та прояви САН доволі різноманітні. Однак характерними симптомами усіх форм САН є рецидивуючий АН, що спричиняє набряк шкіри, абдомінальні симптоми внаслідок АН ШКТ та респіраторні симптоми, зумовлені ураженням дихальних шляхів [1]. У дітей найчастішими початковими симптомами є набряк стінок кишечнику з болем у животі та набряк кінцівок [1, 22]. САН не асоціюється з кропив’янкою чи свербежем, але у пацієнтів може спостерігатися крайова еритема (erythema marginatum) [1]. На відміну від гістамін-індукованого АН, набряк, спричинений САН, є тривалим; при відсутності терапії симптоми САН можуть зберігатися від 3 до 5 днів. Затяжні епізоди пов’язані зі значною захворюваністю та смертністю, якщо їх не лікувати ефективними медикаментозними засобами [1]. У таблиці наведені ознаки та симптоми, які можуть дати лікарям підстави запідозрити САН. На рисунку представлений алгоритм обстеження пацієнтів із підозрою на САН [20].
Клінічний перебіг та прояви САН доволі різноманітні. Однак характерними симптомами усіх форм САН є рецидивуючий АН, що спричиняє набряк шкіри, абдомінальні симптоми внаслідок АН ШКТ та респіраторні симптоми, зумовлені ураженням дихальних шляхів [1]. У дітей найчастішими початковими симптомами є набряк стінок кишечнику з болем у животі та набряк кінцівок [1, 22]. САН не асоціюється з кропив’янкою чи свербежем, але у пацієнтів може спостерігатися крайова еритема (erythema marginatum) [1]. На відміну від гістамін-індукованого АН, набряк, спричинений САН, є тривалим; при відсутності терапії симптоми САН можуть зберігатися від 3 до 5 днів. Затяжні епізоди пов’язані зі значною захворюваністю та смертністю, якщо їх не лікувати ефективними медикаментозними засобами [1]. У таблиці наведені ознаки та симптоми, які можуть дати лікарям підстави запідозрити САН. На рисунку представлений алгоритм обстеження пацієнтів із підозрою на САН [20].
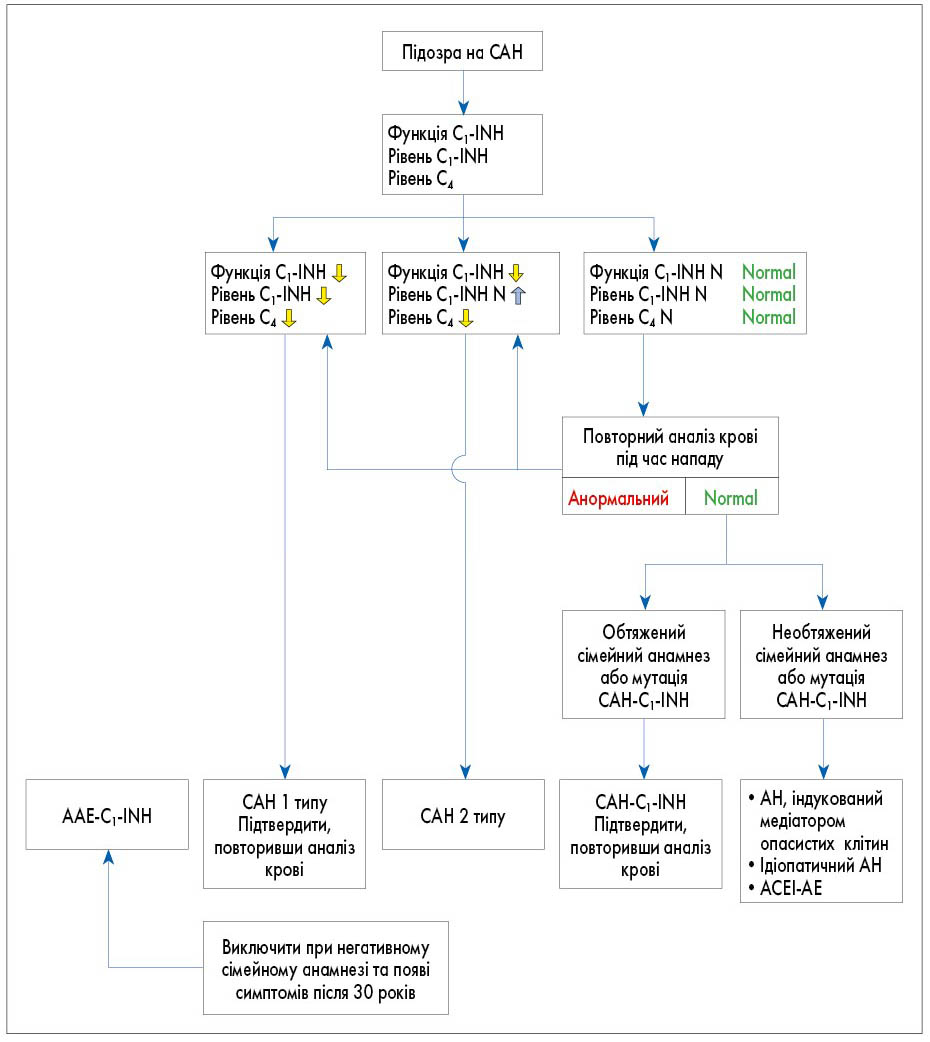 Рис. Алгоритм менеджменту пацієнтів із САН
Рис. Алгоритм менеджменту пацієнтів із САН
Примітки: С1-INH – інгібітор С1-естерази; С4 – білок комплементу 4; N – нормальні значення; AAE-C1-INH – форма САН, не асоційована з генетичними мутаціями; ACEI-AE – ангіоневротичний набряк, що виникає під час терапії інгібіторами АПФ.
Аналіз крові
Вимірювання антигенного та функціонального рівнів C1-INH необхідне для виявлення або виключення САН [1]. Вимірювання кількісної (антигенної) і функціональної активності C1-INH і плазмового білка комплементу 4 (C4), як правило, достатньо для встановлення діагнозу [2]. Хоча низькі функціональні рівні C4 та C1-INH є клінічно достатніми для встановлення діагнозу САН, аналіз генетичних мутацій є остаточним етапом підтвердження діагнозу; однак цей останній етап зазвичай дороговартісний [1]. Рівні білків С4 і C1-INH у крові є низькими при народженні, тому тестування на ці маркери рекомендується проводити після 1 року [1].
Генетичне тестування
Генетичне тестування може бути необхідним у певних клінічних ситуаціях, включаючи диференціацію генетичного від набутого дефіциту С1-INH, пренатальне тестування на вимогу сім’ї або в ситуаціях, коли результати повторних біохімічних тестів на С1-INH є неоднозначними [1]. У пацієнтів із відомою сімейною мутацією для швидкого встановлення діагнозу достатньо аналізу ДНК пуповинної або периферичної крові. Навіть якщо сімейна мутація невідома, більшість дітей матимуть таку ж генетичну аномалію, як батьки. Тому слід одночасно досліджувати гени обох батьків і дитини [2]. Якщо тестування на основі антитіл не підтверджує функціональну недостатність C1, але діагноз під підозрою, хромогенний функціональний аналіз C1-INH є більш чутливим, ніж імуноферментний, і може допомогти встановити остаточний діагноз [1].
Варіанти лікування дітей
Принципи, що визначають фармакологічне лікування САН:
- доступність ефективної невідкладної терапії на вимогу для усіх пацієнтів;
- раннє лікування для запобігання прогресуванню нападу;
- лікування нападів незалежно від локалізації набряку;
- впровадження довгострокової профілактики на основі спільного прийняття рішень.
Діти із САН повинні мати доступ до ≥2 стандартних доз лікарських засобів, схвалених Управлінням з контролю за продуктами та лікарськими засобами США (FDA) для лікування непередбачуваних епізодів АН [2]. У той час як для деяких пацієнтів може бути достатнім лише лікування за потребою, іншим показана профілактична терапія першої лінії разом з лікуванням нападів за потребою [2]. Наразі FDA схвалено 7 препаратів для використання в педіатричній практиці: 3 призначені для лікування гострих нападів САН (лікування за потребою), 4 – для профілактики.
Лікування на вимогу
Метою невідкладної терапії САН є мінімізація захворюваності та запобігання смертності від набряку [1]. Хоча лікування за потребою запобігає прогресуванню набряку, до його зникнення може пройти від 30 хвилин до 2 годин після введення ліків [1]. Дуже важливо пояснити батькам, що раннє лікування призводить до кращого контролю симптомів [1]. Повторна доза зазвичай не потрібна, якщо набряк не збільшується [1].
Інгібітори С1-естерази
Наразі доступні 3 концентрати C1-INH (pdC1-INH), отримані з людської плазми: Berrehert (CSLT, Inc: Berinert) схвалений для лікування дітей за потребою [32]; Haegarda (CSL Behring, LLC) схвалений для профілактики у дітей [33] і Cinryze H (Takeda) схвалений для профілактики у дорослих і підлітків [34] і вивчається для лікування гострих епізодів у дітей. Рекомбінантна форма C1-INH (rhC1-INH) Ruconest (Pharming N.V.) схвалена для лікування гострих епізодів у підлітків і дорослих [35].
Інгібітор калікреїну
Інгібітор калікреїну екаллантид (Kalbitor, Takeda) ліцензований тільки в США для лікування на вимогу всіх типів САН-1/2 у пацієнтів віком ≥12 років [36]. Аналіз об’єднаних даних свідчить про те, що екаллантид є ефективним для лікування епізодів САН у молодших пацієнтів і має прийнятний профіль безпеки [2, 37]. Екаллантид асоціюється з реакціями гіперчутливості у невеликої кількості (3-4%) реципієнтів, тому має застереження, яке вказує, що його слід застосовувати під наглядом медичного працівника [2].
Профілактика
Профілактичну терапію можна розглядати як для короткострокового, так і довгострокового лікування. Метою короткострокової профілактики є зниження ризику розвитку набряків у дитини, яка зазнає впливу стресових чинників (наприклад, стоматологічні або хірургічні маніпуляції), що може спровокувати АН. Довгострокова профілактика має на меті зменшити загальну частоту та тяжкість епізодів АН [1].
Профілактична терапія повинна бути індивідуалізована і розглядатися для всіх пацієнтів з тяжким перебігом САН. Слід враховувати тяжкість захворювання, частоту нападів, ЯЖ, доступність ресурсів охорони здоров’я та нездатність досягти адекватного контролю за допомогою відповідної терапії на вимогу.
Для профілактики у дітей схвалені pdC1-INH (Cinryze та Haegarda), а також інгібітори калікреїну (Takhzyro, Dyax Corp та Orladeyo, Biocryst Pharmaceuticals, Inc.) [38, 39]. Варіанти профілактичного лікування відрізняються за способом введення, потенційними побічними ефектами та ефективністю. Тому досвід пацієнта та його вподобання є важливими факторами при прийнятті рішення про те, яка терапія є найбільш підходящою конкретному пацієнту [1].
Для рутинної профілактики у дітей із САН доступні внутрішньовенні та підшкірні форми pdC1-INH [10]. Внутрішньовенне введення pdC1-INH для довгострокової профілактики вимагає багаторазового венозного доступу, що може бути важко підтримувати протягом тривалого часу і може призвести до місцевих та системних ускладнень [10, 40]. На противагу цьому, підшкірне введення pdC1-INH для профілактичної терапії може стати зручною альтернативою внутрішньовенному для пацієнтів молодшого віку й осіб, які за ними доглядають [10, 41].
Відповідно до міжнародних рекомендацій Всесвітньої організації алергії (WAO), pdC1-INH, отриманий з плазми крові, є варіантом вибору для довгострокової профілактики у дітей із САН [20]. Консенсусні рекомендації Міжнародної робочої групи зі спадкового АН (The Hereditary Angioedema International Working Group) також вказують плазмовий pdC1-INH як найбезпечніший варіант довготривалої профілактики у дітей, тоді як андрогени й антифібринолітичні препарати не рекомендовані до застосування у цій групі [10].
Переосмислення педіатричної допомоги при САН: комплексний підхід
Як зазначено у вступі, діти із САН мають справу з тяжким захворюванням. Як напади САН, так і саме захворювання впливають на ЯЖ у кількох сферах, включаючи фізичну, емоційну та психосоціальну [14]. Непередбачуваний характер нападів САН частково сприяє зниженню ЯЖ, тому надання ефективного профілактичного лікування та зменшення частоти нападів САН є важливим кроком до покращення життя пацієнтів дитячого віку [14, 42]. Плануючи лікування, лікарі повинні враховувати загальний вплив ефективного лікування на ЯЖ дитини.
Профілактична терапія може зменшити тягар захворювання, пов’язаного зі САН [39]. Потреба в профілактичному лікуванні не залежить від віку; для педіатричних пацієнтів, які відповідають критеріям прийнятності, необхідність профілактики повинна розглядатися та оцінюватися так само, як і для дорослих. На додаток до забезпечення ефективної довготривалої профілактики клініцисти також повинні розглянути інтегративний цілісний підхід до САН, який пропонує можливості для вирішення психологічних та емоційних потреб дітей із САН. Емоційний стрес є відомим тригером для епізодів САН, і діти можуть страждати від значного емоційного стресу через напади САН, що знижує якість життя. Тривога і депресія також поширені серед пацієнтів із САН, а ЯЖ знижується, коли тривога і депресія стають більш вираженими [43].
Хоча стандартна медикаментозна терапія спрямована на біологічні аспекти САН, додаткові види інтегративної терапії (наприклад, музична, гіпнотерапія) можуть підтримати медичні підходи і вирішити психосоціальні аспекти САН, щоб покращити загальний досвід пацієнта і його ЯЖ.
Висновок
САН – хронічне захворювання, яке не піддається повному виліковуванню, але призначення ефективної терапії може значно полегшити тягар хвороби і покращити ЯЖ пацієнтів, особливо дітей. Наразі у доробку клініцистів наявний значний арсенал медикаментів, рекомендованих як для купірування, так і профілактичного лікування САН. Застосування ефективної медикаментозної терапії є критично важливим, особливо з урахуванням високого ризику летальних випадків.
Реферативний огляд статті R. Tachdjian, A.P. Kaplan. A comprehensive management approach in pediatric and adolescent patients with hereditary angioedema. Clin Pediatr (Phila). 2023 Oct; 62 (9): 973-980. doi: 10.1177/00099228231155703.
Підготувала Анна Хиць
Тематичний номер «Педіатрія» № 4 (70) 2023 р.



