14 листопада, 2023
Холецистектомія та метаболічний синдром: патогенетичний взаємозв’язок
 Сьогодні з’являється все більше даних про зв’язок холецистектомії (XЕ) з надмірним ризиком розвитку метаболічного синдрому (МС) та його ускладнень – цукрового діабету 2 типу (ЦД2), атеросклеротичних судинних захворювань та неалкогольної жирової хвороби печінки (НАЖХП). ХЕ може спричинити аномальні метаболічні наслідки, такі як зміни рівня глюкози, інсуліну (а також індексу інсулінорезистентності – HOMA-IR), рівнів ліпідів (підвищення тригліцеридів та ліпопротеїнів дуже низької щільності – ЛПДНЩ), розвиток стеатозу печінки та МС [3, 6, 10].
Сьогодні з’являється все більше даних про зв’язок холецистектомії (XЕ) з надмірним ризиком розвитку метаболічного синдрому (МС) та його ускладнень – цукрового діабету 2 типу (ЦД2), атеросклеротичних судинних захворювань та неалкогольної жирової хвороби печінки (НАЖХП). ХЕ може спричинити аномальні метаболічні наслідки, такі як зміни рівня глюкози, інсуліну (а також індексу інсулінорезистентності – HOMA-IR), рівнів ліпідів (підвищення тригліцеридів та ліпопротеїнів дуже низької щільності – ЛПДНЩ), розвиток стеатозу печінки та МС [3, 6, 10].
Когортне дослідження в США, засноване на NHANES III (National Health and Nutrition Examination Survey III – Американська національна програма соціального дослідження, яку проводить Національний центр статистики охорони здоров’я США), показало, що НАЖХП як печінковий прояв МС була пов’язана з ХЕ, але не з камінням у жовчному міхурі (ЖМ), і цей зв’язок був сильнішим у чоловіків, ніж у жінок, оскільки у 68% чоловіків після ХЕ було виявлено НАЖХП. Відзначався також зв’язок між ХЕ та підвищеним рівнем печінкових ферментів (аланінамінотрансферази – АЛТ, аспартатамінотрансферази – АСТ, гама-глутамінтранспептидази – ГГТП), і ця тенденція була більш значущою, якщо ХЕ проводилася після 10-річного анамнезу жовчнокам’яної хвороби (ЖКХ) [4].
С. Ruhl та J. Everhart (2013) показали незалежний зв’язок НАЖХП із ХЕ у великому популяційному дослідженні в США. Серед 12 232 учасників поширеність ЖКХ становила 7,4%, ХЕ – 5,6% та НАЖХП – 20,0%. В учасників із ХЕ була більш висока скоригована за віком та статтю поширеність НАЖХП (48,4%), ніж у пацієнтів із ЖКХ (34,4%) або без неї (17,9%; р<0,01 в усіх порівняннях). Тобто багатоваріантний скоригований аналіз підтвердив зв’язок НАЖХП із ХЕ, але не з ЖКХ. Отже, ХЕ як така може бути чинником ризику розвитку НАЖХП [15].
МС також є серйозною проблемою громадської охорони здоров’я. Основними факторами ризику є атерогенна дисліпідемія, підвищений кров’яний тиск, підвищений рівень глюкози в плазмі, протромботичний та прозапальний стан.
Зв’язок ХЕ з різними компонентами МС відзначають багато авторів [3, 4, 6, 8, 10], що підтверджується збільшенням індексу маси тіла (ІМТ), рівня глюкози натще і високою поширеністю ЦД2, підвищеною концентрацією тригліцеридів, холестерину, ЛПДНЩ (що вказує на стеатогенний ефект у печінці) більшою мірою, ніж у цих пацієнтів до оперативного втручання щодо ЖКХ. Ці спостереження підтверджують досі невідому роль ЖМ у регуляції системного метаболізму ліпідів. Видалення ЖМ може призвести до порушення профілю ліпідів, стимулювати накопичення жиру в печінці (стеатоз) та посилювати метаболічний стрес.
Наведені вище дані переконливо свідчать про те, що ХЕ сама по собі є фактором ризику розвитку МС і може серйозно вплинути на загальне регулювання обміну речовин та стан здоров’я людини.
Основні патогенетичні механізми, за допомогою яких ХЕ може викликати МС, повністю не з’ясовані, проте привертають увагу такі положення:
- ЖМ, виконуючи резервуарну функцію, виступає фізіологічним водієм ритму ентерогепатичної циркуляції жовчних кислот (ЖК). Ця функція опосередкована різними механізмами нейрогормональної координації, які включають печінку та кишечник. Втрата множинних функцій ЖМ призводить до прискорення ентерогепатичної циркуляції як печінкових первинних кислот (холевої, хенодезоксихолевої), так і кишкових вторинних (дезоксихолевої, литохолевої) і третинних (урсодезоксихолевої – УДХК);
- у пацієнтів із ХЕ знижено пул первинних жовчних солей, холату та хенодезоксихолату, в той час як пул дезоксихолату залишається нормальних розмірів. У результаті цих змін загальний пул жовчних солей зменшується майже вдвічі порівняно з нормальним розміром, а дезоксихолат стає переважно жовчною сіллю [9];
- ХЕ впливає на ентерогепатичну циркуляцію жовчних солей та супутню передачу сигналів через рецептори жовчних солей, що беруть участь у метаболічному гомеостазі. Це може свідчити про те, що ХЕ є біомаркером метаболічних порушень через викликані ЖК зміни в ентерогепатичній циркуляції, а також біомаркером НАЖХП [8];
- через відсутність моторної та скорочувальної функції ЖМ, що виступає в ролі резервуара жовчі та скорочувальної помпи, порушується модулювання потоку ЖК в ентерогепатичній циркуляції, яка відповідає за регуляцію гомеостазу тригліцеридів, ЖК та холестерину в організмі;
- після ХЕ випадає концентраційна функція ЖМ, тому печінкова жовч концентрується сильніше в 4-5 разів через відсутність міхурової жовчі, при цьому збільшується пул ЖК і «перетравлювальна здатність» печінкової порції жовчі;
- після втраченої резервуарної функції ЖМ пул ЖК циркулює швидше, змінюючи ентерогепатичну циркуляцію. ХЕ може вплинути на гомеостаз глюкози і ліпідів і збільшити ризик високого кров’яного тиску та серцево-судинних захворювань [10];
- ХЕ може визначати порушення регуляції енергетичного гомеостазу всього організму шляхом значного скорочення часу рециркуляції ЖК, при цьому ЖК виробляють метаболічні сигнали, які діють без ритмічної функції ЖМ. ХЕ через викликані ЖК зміни ентерогепатичної циркуляції є фактором ризику розвитку метаболічних порушень і ще одним фактором ризику розвитку МС (рис. 1).
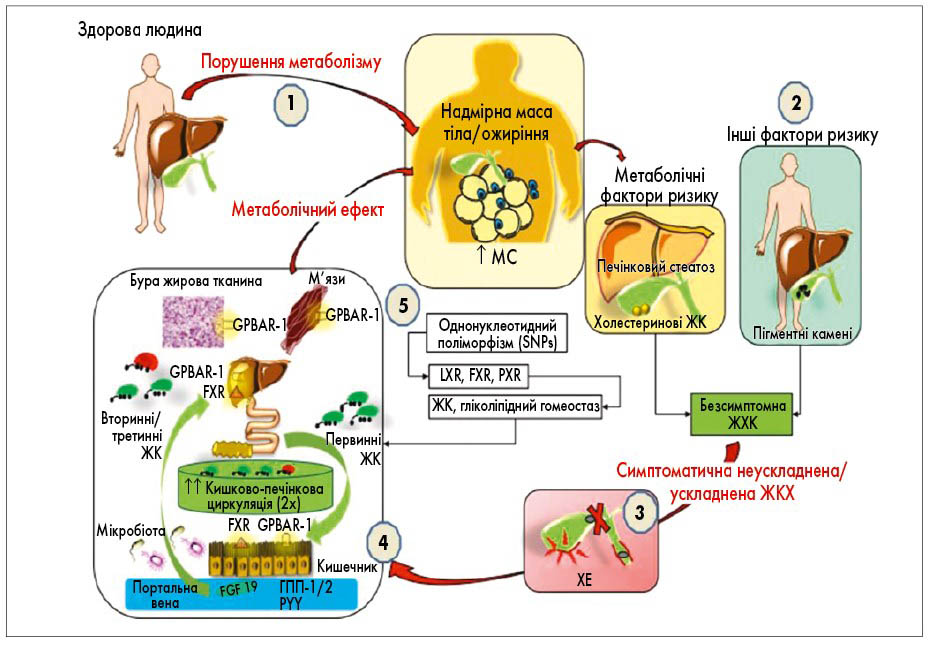 Рис. 1. Патогенетичні механізми зв’язку ХЕ та метаболічних порушень (за A. Di Ciaula et al., 2018)
Рис. 1. Патогенетичні механізми зв’язку ХЕ та метаболічних порушень (за A. Di Ciaula et al., 2018)
Примітки: ГПП – глюкагоноподібний пептид; PYY – пептид YY; GPBAR-1 – G-білок, пов’язаний із рецептором ЖК; FXR – фарнезоїдний рецептор; LXR, FXR, PXR – ядерні рецептори.
Втрата множинних функцій ЖМ призводить до прискорення ентерогепатичної циркуляції як печінкових первинних кислот (холевої, хенодезоксихолевої), так і кишкових вторинних (дезоксихолевої, литохолевої) і третинних (УДХК). У цих умовах зміни можуть відбуватися на рівні взаємодії:
- кишкових ЖК – фарнезоїдного Х-рецептора (FXR) та вивільнення фактора росту фібробластів 19 (FGF19);
- кишкові ЖК – рецептор ЖК-1, пов’язаний із G-білком (GPBAR-1, також відомий як TGR5), і вивільнення глюкагоноподібних пептидів-1 і 2 (GLP1/2) і пептиду YY (PYY) із важливими метаболічними впливами (на рівень глюкози, метаболізм інсуліну і апетит);
- ЖК сироватки та FXR гепатоцитів і клітин Купфера GPBAR-1 з інгібуванням синтезу ЖК, а також GPBAR-1 бурої жирової тканини та поперечно-смугастих м’язів із додатковими метаболічними ефектами. Виявляється також роль однонуклеотидних поліморфізмів (SNP) із впливом на механізми, опосередковані ядерними рецепторами, що призводять до розвитку МС та підвищення ризику у деяких осіб.
Нещодавно було виявлено, що слизова оболонка ЖМ є основною ентерогепатобіліарною ділянкою експресії фактора росту фібробластів 19 (FGF19), який у високих концентраціях секретується у жовч. FGF19 може функціонувати як ендокринний гормон та проявляти метаболічну дію в різних тканинах організму. FGF19 допомагає регулювати метаболізм ліпідів, глюкози та енергії під час їжі та натще, здатний пригнічувати індукований інсуліном синтез жирних кислот у печінці, що є ключовим процесом, який контролює толерантність до глюкози та накопичення триацилгліцеринів (ліпідів) у печінці, крові та жировій тканині [7].
Зниження рівнів циркулюючого FGF15/19, пов’язане з ХЕ, може викликати ряд метаболічних порушень: зміну гомеостазу глюкози, ЦД2, інсулінорезистентність (ІР), зміну вмісту ліпідів у печінці, що сприяє розвитку діабету та метаболічно-асоційованої неалкогольної жирової хвороби печінки (МАЖХП), а також шлунково-кишкових дисфункцій [4].
Фундаментальні дослідження, проведені за останні два десятиліття, виявили нові функції ЖК, такі як «гормональні» сигнальні молекули та метаболічні інтегратори [3].
Зміна гомеостазу ЖК впливає на метаболічний гомеостаз печінки, викликає запалення та сприяє патогенезу метаболічних захворювань, таких як МАЖХП, ЦД, ожиріння та запальні захворювання кишечнику (ЗЗК).
Метаболічна дія ЖК є результатом активації ними різних внутрішньоклітинних ліганд-активованих ядерних рецепторів, таких як фарнезоїдний X-рецептор (FXR), прегнановий X-рецептор (PXR), конститутивний андростановий рецептор (СAR) та рецептор вітаміну D (VDR), а також рецептори, пов’язані з G-білком на поверхні клітини (GPCR), такі як рецептор ЖК, пов’язаний із G-білком (TGR5 і Gpbar-1), і рецептор сфінгозин-1-фосфату-2 (S1PR2) у шлунково-кишковому тракті (ШКТ), що зумовлює появу системних сигнальних ефектів поза ентерогепатичними тканинами [11].
ЖК безпосередньо активують 3 ядерні рецептори: FXR, PXR і VDR, які високо експресуються в тканинах, що піддаються впливу ЖК, включаючи печінку та кишечник (рис. 2).
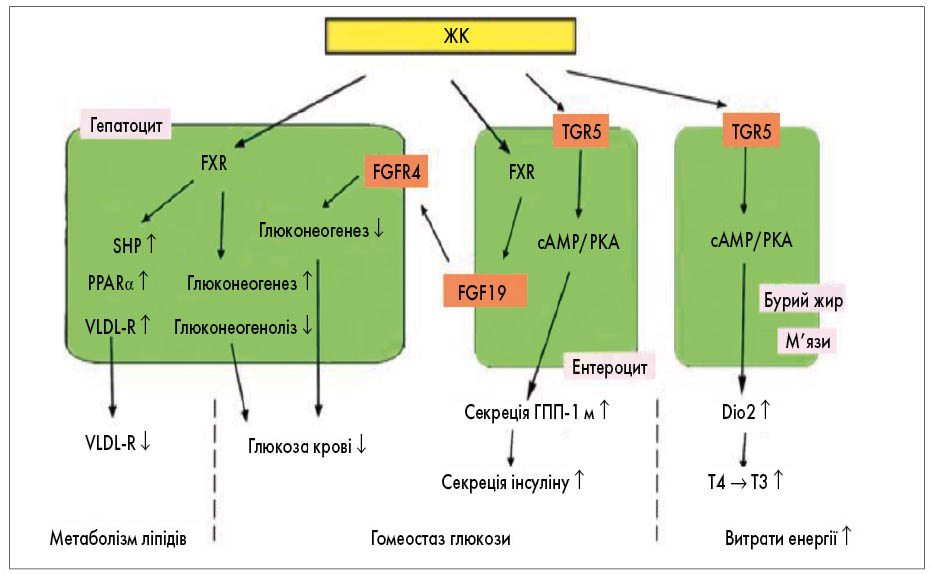 Рис. 2. Метаболічні ефекти ЖК (Y. Chen, S. Wu, Y. Tian, 2020)
Рис. 2. Метаболічні ефекти ЖК (Y. Chen, S. Wu, Y. Tian, 2020)
Примітки: Dio2 – йодтиронін-дейодиназа типу 2; FGFR4 – рецептор FGF4; FXR – фарнезоїдний рецептор; ГПП-1 – глюкагоноподібний пептид-1; PPARα – α-рецептор, що активується пероксисомними проліфераторами; SHP – малий гетеродимерний партнер; VLDL – ЛПДНЩ; VLDL-R – рецептор ЛПДНЩ; cAMP – циклічний аденозинмонофосфат; PKA – протеїнкіназа А; T4 – тироксин; Т3 – трийодтиронін.
ЖК активують сигнальні шляхи, опосередковані FXR і GPBAR1/TGR5. У гепатоцитах активація FXR ЖК може активувати SHP, PPAR і VLDL-R, що знижує ліпогенез і посилює ліполіз. У результаті рівень ЛПДНЩ у плазмі знижується. FXR також збільшує глікогенез та знижує глікогеноліз. В ентероцитах передача FXR-сигналів підвищує експресію FGF19. Потім FGF19 циркулює в печінці та інгібує глюконеогенез за допомогою зв’язування та активації FGFR4. Активація TGR5 РК стимулює секрецію GLP-1 ентероендокринними L-клітинами, що збільшує секрецію інсуліну з панкреатичних β-клітин та підвищує ІР. У клітинах бурого жиру та скелетних м’язів активація TGR5 призводить до підвищення внутрішньоклітинного рівня цАМФ і експресії Dio2. Dio2 перетворює неактивний тироксин (Т4) на активний 3,5,3'-трийодтиронін (Т3) для збільшення витрати енергії.
Активація FXR:
- координує біліарну секрецію ЖК, холестерину і фосфоліпідів, які утворюють змішані міцели в жовчі, тим самим запобігаючи утворенню жовчного каміння та пошкодженню ЖК епітелію жовчних проток;
- індукує печінкову експресію PPARγ (рецептор активації проліферації пероксисом), що спричинює накопичення жиру в печінці, яке призводить до стеатозу;
- бере участь у чутливості до інсуліну та регуляції рівня глюкози і ліпідів, відіграє протизапальну роль при пошкодженні печінки і ЗЗК;
- бере участь у передачі сигналів ядерного транскриптаційного фактора NF-κВ, що знижує продукцію прозапальних цитокінів у печінці;
- збільшує експресію печінкового переносника жирних кислот транслокази FAT/CD36 [6, 11].
Мембранний рецептор ЖК – TGR5 – має важливі метаболічні ефекти: активація TGR5 збільшує витрату енергії і запобігає накопиченню жиру в печінці. У тонкій кишці TGR5 позитивно регулює секрецію GLP1 L-ентероендокринними клітинами і, таким чином, сприятливо модулює чутливість до інсуліну та метаболізм глюкози [3].
Рецептори ЖК – PXR і CAR – також діють як регулятори метаболізму (так звані ендобіотичні рецептори) при фізіологічних та патологічних станах і можуть бути залучені в розвиток і лікування метаболічних захворювань.
Ці ядерні рецептори діють як датчики рівнів ЖК у гепатоцитах та ентероцитах і опосередковують плейотропні ефекти ЖК у регуляції метаболічного гомеостазу, що патогенетично пояснює доцільність застосування препаратів, які містять ЖК, зокрема, УДХК, у лікуванні МС, що розвинувся.
Планова ХЕ збільшує індекс вмісту жиру в печінці, HOMA-IR та концентрацію аполіпопротеїну В (ароВ) у сироватці крові. Ці результати підтверджують припущення, що ХЕ є чинником ризику розвитку НАЖХП та інших станів, асоційованих із ІР.
Проспективне дослідження типу «випадок – контроль» у пацієнтів латиноамериканського походження без ожиріння із ЖКХ, які перенесли планову ХЕ, показало, що, за даними магнітно-резонансної терапії, через 2 роки після операції спостерігалося значне збільшення рівня інсуліну в сироватці, індексу HOMA-IR, рівнів ароВ у сироватці та вмісту жиру в печінці. Підвищення рівнів ароВ свідчить про системну та печінкову ІР [17].
Останнім часом найбільший інтерес щодо ролі ХЕ у розвитку захворювань печінки пов’язаний із її прямим патогенетичним впливом на розвиток стеатотичного захворювання печінки, пов’язаного з метаболічною дисфункцією (MAСХП) [10, 16, 18].
Стеатотичне захворювання печінки, пов’язане з МАСХП, є всеосяжним терміном нової номенклатури захворювань печінки, про яку було оголошено Американською асоціацією з вивчення захворювань печінки (American Association for the Study of Liver Diseases – AASLD) у червні 2023 року, замість терміну МАЖХП. MAСХП включає пацієнтів зі стеатозом печінки та наявністю принаймні одного з п’яти кардіометаболічних факторів ризику. Стеатогепатит, пов’язаний з метаболічною дисфункцією (МАСГ), є терміном, що замінює НАСГ [10, 16].
Роттердамське дослідження (S. Latenstein, S. Carmen et al., 2020) повідомляє про проведений регресійний аналіз, що пов’язує ХЕ з МС та НАЖХП. Учасники дослідження пройшли ультразвукове дослідження (УЗД) печінки в період з 2009 по 2014 роки для оцінки стеатозу після ХЕ та поширеності МС і НАЖХП [8].
Дослідження у США показало сильніший зв’язок НАЖХП із ХЕ проти наявності лише каменів у ЖМ і передбачає, що ХЕ може бути чинником ризику розвитку самої НАЖХП [8].
Останні досягнення в розумінні передачі сигналів ЖК та їх ролі у регуляції метаболічного гомеостазу пояснюють необхідність застосування терапевтичних засобів на основі ЖК для лікування метаболічних захворювань. ЖК та їхні похідні є потенційними терапевтичними агентами для лікування метаболічних захворювань печінки.
Досвід застосування УДХК як лікарського засобу має багаторічну історію. За цей час показано досить високу її клінічну ефективність. Про патогенетично обґрунтоване застосування УДХК при МС та МАСХП повідомляють багато авторів [1, 9, 10]. Біологічні ефекти УДХК добре відомі, вона має широкий діапазон плейотропних властивостей. Встановлено, що УДХК виконує роль молекулярного шаперону, регулює гомеостаз ендоплазматичного ретикулуму, фолдинг і посттрансляційну модифікацію білків, покращує функції кишкового бар’єру і модулювання складу кишкової мікробіоти, взаємодіє з глюкокортикоїдним рецептором, позитивно впливає на цитокіновий статус, допомагає знизити рівень прозапальних цитокінів інтерлейкіну (IL)-6, Il-17, резервує клітинні структури гепатоцитів і стимулює антиапоптотичні шляхи, усуває мітохондріальну дисфункцію, має нейроцитопротекторну дію, покращує функціонування дофамінергічних нейронів, знижує нейротоксичність [10].
УДХК є агоністом та лігандом GPBAR (G protein-coupled bile acid receptor), усуває проатерогенний ліпідний профіль та зменшує стеатоз, тому її призначення терапевтично обґрунтоване при лікуванні запалення печінки (НАСГ) та товстої кишки.
Про патогенетично обґрунтоване застосування УДХК при МАСХП повідомляють багато авторів [1, 9, 10]. УДХК активує ліпопротеїнліпазу плазми крові – фермент, який гідролізує жири ліпопротеїдів, та холестерол-7α-гідроксилазу – фермент, який контролює синтез холестерину в печінці. Проведене дослідження високих доз УДХК послаблювало печінкову ІР, що підтверджують V. Rutzia та співавт. (2011), які провели 12-місячне рандомізоване подвійне сліпе плацебо-контрольоване багатоцентрове дослідження для оцінки ефективності й безпеки HD-УДХК (високодозова УДХК; 28-35 мг/кг/день) у 126 пацієнтів із підтвердженим за допомогою біопсії НАСГ та підвищеним рівнем АЛТ. HD-УДХК значно знизила середній рівень АЛТ на 28,3% від вихідного через 12 місяців порівняно з плацебо на 1,6% (p<0,001). Наприкінці дослідження рівні АЛТ нормалізувалися (≤35 МО/л) у 24,5% пацієнтів, які отримували HD-УДХК, і у 4,8% пацієнтів, які отримували плацебо (р=0,003). Обидва результати пояснюються змінами маси тіла під час дослідження. HD-УДХК значно знижувала маркер фіброзу сироватки FibroTest® (p<0,001) порівняно із плацебо. HD-УДХК також значно покращувала маркери глікемічного контролю та ІР. Проблем із безпекою у цій популяції не було.
Автори роблять висновок про те, що лікування HD-УДХК було безпечним, покращувало рівні амінотрансфераз, маркери сироваткового фіброзу та деякі метаболічні параметри. Дослідження з гістологічними кінцевими точками також були виправдані та достовірні [19].
Результати численних клінічних досліджень підтверджують, що патогенетично обґрунтованим способом профілактики і корекції МС та коморбідних патологій може бути застосування препарату УДХК – Урсофальк. Його призначення дозволяє скоригувати множинні клінічні прояви МС, що розвинувся після ХЕ: нормалізувати метаболізм глюкози, знизити ІР, зменшити атеросклеротичні ураження судин і вираженість стеатозу та МАСХП.
ЖК регулюють конфігурацію кишкового мікробіома, а мікробіом впливає на склад пулу ЖК та експресію генів, контрольованих рецептором FXR. Вісь «мікробіота – кишечник – печінка» грає вирішальну роль в обміні ліпідів, глюкози та енергетичному обміні всього організму.
Розуміння взаємодії ЖК та мікробіома дуже важливе для лікування і профілактики МС, МАСХП, ЗЗ ШКТ, ЦБ й ожиріння.
Для корекції МС і МАСХП, що розвинулися після ХЕ, патогенетично доцільним є призначення препаратів УДХК у комбінації з пре- та пробіотичними препаратами, які модулюють кишкову мікробіоту, зберігають її різноманіття, якісний склад: препаратами інуліну, масляної кислоти, які є колонопротекторами, енергетичними субстратами мікробіоти [1].
Сьогодні на фармацевтичному ринку України є новий високоефективний натуральний препарат-колонопротектор для лікування МС, патології печінки, дисбіозу кишечника і порушень мікробіоти та нейропротекції – Зафакол IQ.
Зафакол IQ містить метаболіт нормальної мікробіоти масляну кислоту 250 мг (у вигляді бутирату кальцію), вітамін холекальциферол D3 – 600 IU, пребіотик інулін 100 мг і пробіотик Lactоbacillus Helveticus LH060- LMG-P31392 – 3×109 CFU, Bifidobacterium Longum Synbalance BI072-DSM26197 – 3,18×108 CFU.
Зафакол IQ, враховуючи його склад, є колонопротектором, постбіотиком (метабіотиком). І вперше інноваційним є включення до препарату лактобактерії Lactоbacillus Helveticus 3×109 CF, що разом із Bifidobacterium Longum 3,18×108 CFU дозволило вважати Зафакол IQ психобіотиком.
T.G. Dinan та співавт. (2013) представили концепцію психобіотика, що визначається як пробіотик, який володіє нейроповедінковими або психіатричними перевагами [18].
Lactоbacillus Helveticus LH060-LMG-P31392 визнаний американською FDA безпечним мікроорганізмом (GRAS) та отримав у 2007 році статус безпеки (QPS) від Європейського агентства з безпеки харчових продуктів (EFSA), не має набутої стійкості до антибіотиків.
Вifidobacterium Longum Synbalance BI072-DSM 26197 – один із найпоширеніших з 32-х видів, присутніх у ШКТ людини, належить до роду Bifidobacterium – грампозитивна, каталазонегативна, паличкоподібна, анаеробна бактерія. Bifidobacterium Longum Synbalance BI072-DSM 26197 має один з найбільших бактеріальних геномів, що пояснює високу здатність до адгезії до кишкового епітелію та активної і пасивної колонізаційної резистентності, спрямованої на запобігання заселенню ШКТ умовно-патогенними та патогенними мікробами.
Lactobacillus Helvecii має властивості психобіотика – це пробіотик, що має характеристики модуляції функцій центральної нервової системи (ЦНС) або узгоджених дій осі «кишечник – мозок» (GBA) через нервові, гуморальні та метаболічні шляхи для поліпшення шлунково-кишкової активності, а також анксіолітичних і навіть антидепресивних функцій [20].
Ефекти Lactobacillus helveticus і Bifidobacterium longum як психобіотика полягають у зниженні депресії, тривожності, рівня стресу, підвищенні когнітивних функцій, ангедонії (втрати здатності відчувати задоволення), якості сну та життя.
Зростання даних показує, що депресія пов’язана з підвищеним ризиком розвитку МС, ЦД і серцево-судинних захворювань [5, 12, 17].
P. An та співавт. (2012) систематично проаналізували 29 поперечних досліджень за участю 155 333 суб’єктів та виявили зв’язок депресії (визначається або за симптомами, про які повідомляють самі пацієнти, або за психічним розладом) та МС. Результати аналізу вказують на двоспрямований зв’язок між депресією та МС і підтримують необхідність раннього виявлення й лікування депресії у пацієнтів із МС [14].
F.L. De Oliveira та співавт., використовуючи динамічну модель мікробіома, вперше показали (2023) позитивний вплив Lactobacillus helveticus R0052 і Bifidobacterium longum R0175 на мікробіоту кишечнику у людей із легкою тривожністю [12].
Пацієнти після ХЕ і розвиненого МС мають підвищений рівень тривожності й порушення когнітивних функцій, тому призначення препарату Зафакол IQ є патогенетичним і терапевтично правомочним, що дозволить зменшити поліпрагмазію у таких пацієнтів і зменшити негативний вплив фармакологічних засобів при розвиненій МАСХП на тлі МС та після ХЕ.
Мукофальк є натуральним пребіотиком для модуляції мікробіоти та усунення синдрому надлишкового бактеріального зросту (СНБЗ) у пацієнтів із МС після ХЕ. Діюча речовин – Ispaghula husk (лушпиння насіння подорожника Plantago ovata Forssk). Мукофальк створює умови для фізіологічної життєдіяльності нормальної мікрофлори товстої кишки та сприяє регенерації пошкоджених клітин кишкового епітелію. Літолітичний ефект засобу Мукофальк дозволяє використовувати його для запобігання формуванню біліарного сладжу в біліарному тракті після ХЕ. При його використанні у разі гіперхолестеринемії від легкого до помірного ступеня відзначається зниження холестерину ЛПНЩ приблизно на 7% [13].
При МС після ХЕ призначення засобу Мукофальк обґрунтовано його гіполіпідемічною, гіпохолестеринемічною, енергозберігаючою, пребіотичною діями. Препарат є природним регулятором і модулятором моторики кишечнику за рахунок вмісту природних баластових речовин, що скорочує транзиторний час у кишечнику.
У проведеному багатоцентровому рандомізованому проспективному дослідженні повідомляється про лікування 721 хворого віком від 19 до 91 року. Обґрунтовано застосування псиліуму (Мукофальк) у багатоцільовій терапії хворих з гіперліпідемією, МС та запором. Доведено гіполіпідемічну дію засобу Мукофальк в усіх групах хворих, продемонстровано можливість його одночасного призначення зі статинами для синергізму дії у групах хворих із високим та дуже високим ризиком розвитку серцево-судинних захворювань. При тривалому застосуванні засобу відмічається нормалізація випорожнень у більшості пацієнтів. Відміна препарату не знадобилася жодному пацієнту. На тлі 24-тижневого прийому засобу знизився ІМТ у середньому на 4,75-9,80% без суттєвих обмежень харчових звичок пацієнтів [7].
Група авторів опублікувала рекомендації щодо профілактики МАЖХП у пацієнтів із ЖКХ після лапароскопічної ХЕ. Автори провели лікування, що включало прийом засобів Урсофальк, Мукофальк і Хофітол. Урсофальк призначали по 10 мг/кг маси тіла на ніч протягом місяця. Курс профілактики повторюють через 3 місяці. Зазначена профілактична схема лікування дозволяє знизити частоту розвитку НАЖХП у пацієнтів із ЖКХ після лапароскопічної ХЕ [7].
Висновок
ХЕ може бути додатковим фактором ризику розвитку МС, незалежно від причин і механізмів виникнення конкрементів у ЖМ навіть за відсутності серйозних метаболічних порушень до операції. Це вимагає ретельного відбору пацієнтів на підставі наявних клінічних та епідеміологічних даних для виконання оперативного втручання, а також корекцію розвинених метаболічних порушень, щоб звести до мінімуму додаткові метаболічні ризики, визначити індивідуальні профілактичні і терапевтичні стратегії.
Для лікування МС після ХЕ слід використовувати як патогенетичну терапію препарати УДХК (Урсофальк), психобіотики (Зафакол IQ), природні модулятори моторики кишечнику з пребіотичним ефектом (Мукофальк), які є синергістами і потенціюють терапевтичні ефекти один одного – гіполіпідемічну, нейропротекторну, дезінтоксикаційну дії (за рахунок ентеросорбуючої дії псиліуму), що модулює кишкову мікробіоту.
Виконання «профілактичної» ХЕ за відсутності чітких показань може бути недоцільним, враховуючи ризик пізніх ускладнень МАСХП та прогресування МС із коморбідною патологією.
Зростання поширеності МС, особливо серед пацієнтів, які перенесли ХЕ, підкреслює необхідність вивчення фактичного причинно-наслідкового зв’язку в майбутніх проспективних епідеміологічних та інтервенційних дослідженнях. Дослідження метаболічної функції ЖМ можуть покращити наше розуміння механізмів взаємозв’язку між видаленням ЖМ і розвитком МС.
Повний список літератури знаходиться в редакції.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 3 (69) 2023 р.



