30 листопада, 2023
Сила 50: оптимальний рівень вітаміну D проти багатьох хвороб
Багато рецензованих дослідницьких статей переконливо демонструють, що низький рівень 25-гідроксивітаміну D (25(ОН)D) у крові значно підвищує ризик тяжких захворювань, довготривалих пошкоджень і смерті від інфекційних патологій, у тому числі від коронавірусної хвороби (COVID‑19). У цьому огляді висвітлено дослідження щодо залежності активності імунної системи від трьох сполук вітаміну D: вітаміну D3 (холекальциферолу), 25(ОН)D (кальцифедіолу) та 1,25-дигідроксивітаміну D (кальцитріолу).
Аналіз крові на вітамін D вимірює рівень 25(ОН)D, оскільки нирки й імунна система покладаються на нього як на джерело для своїх сигнальних функцій, які передбачають гідроксилювання до 1,25-дигідроксивітаміну D. 25(ОН)D утворюється переважно в печінці з вітаміну D3, який потрапляє в організм через шлунково-кишковий тракт або утворюється під дією короткохвильового високоенергетичного ультрафіолетового (УФ) випромінювання у шкірі. Важливо зазначити, що вітаміну D3 в їжі дуже мало, а УФ-випромінювання важко отримати, за винятком безхмарних днів із високим рівнем сонячного світла, яке завжди пошкоджує ДНК, а отже, підвищує ризик раку шкіри.
Розуміння передачі сигналів імунних клітин і ролі 25(ОН)D
Багато типів імунних клітин покладаються на досить високий рівень 25(ОН)D у кровотоку для підтримки інтракринної діяльності цих клітин і паракринних сигнальних систем. Інтракринна передача сигналів на основі 25(ОН)D необхідна для здатності різних імунних клітин реагувати на зміну обставин. Це було з’ясовано наприкінці 2000-х років Мартіном Х’юісоном і його колегами з Великої Британії, які працювали з макрофагами та дендритними клітинами.
У 2021 році Chauss і співавт. у журналі Nature Immunology опублікували результати великого дослідження, в якому вивчали особливості передачі сигналів на основі 25(ОН)D у регуляторних лімфоцитах Th1, що були виділені з легенів пацієнтів із COVID‑19. Учені дійшли висновку, що автокринна передача сигналів вітаміну D вимикає прозапальні програми клітин Th1.
Відомо, що багато інших типів клітин, особливо клітин імунної системи, які не беруть участі в кальцій-фосфатно-кістковому метаболізмі, значно змінюють експресію своїх генів у відповідь на активацію молекул рецепторів вітаміну D шляхом зв’язування з кальцитріолом. Можна припустити, що всі ці типи клітин також використовують інтракринні та/або паракринні сигнали на основі 25(ОН)D.
Ці клітини можуть повністю та швидко реагувати на зміну обставин, лише якщо достатня кількість 25(ОН)D дифундує всередину них, щоб підтримувати його перетворення на 1,25-гідроксивітамін D (який має дуже короткий період напіввиведення) під час внутрішньокринної сигналізації клітини.
Потреба в ≥50 нг/мл (125 нмоль/л) циркулювального 25(ОН)D
Внутрішньоклітинні рівні 25(ОН)D виміряти неможливо. Жодне дослідження клітинної біології на сьогодні не продемонструвало, що принаймні 50 нг/мл циркулювального 25(ОН)D необхідно для постачання цієї сполуки до клітин у достатній кількості. Проте можна зробити висновок про це через збільшення ступеня дисфункції імунної системи, яка виникає, що далі рівень циркулювального 25(ОН)D стає <50 нг/мл (одна частина з 20 млн за масою).
Цей зв’язок є очевидним у багатьох захворюваннях. Наприклад, А. Dror і співавт. (2022) виявили, що пацієнти з дефіцитом вітаміну D (<20 нг/мл) у 14 разів частіше страждають на тяжке або критичне захворювання, ніж пацієнти з рівнем ≥40 нг/мл (співвідношення шансів 14; 95% довірчий інтервал 4-51; p<0,001). У розвинених країнах державні рекомендації щодо додавання вітаміну D спрямовані на досягнення рівня 20 нг/мл незалежно від потреб організму (Kimball S.M., Holick M. F., 2019).
У 2008 році провідні дослідники вітаміну D закликали до того, щоб норма циркулювального 25(ОН)D становила 40-60 нг/мл. Від початку 2000-х років учені сперечалися з урядовими комітетами щодо настанов про необхідність підвищення рекомендованих норм вітаміну D3 у кількостях, які сприяють досягненню таких рівнів. У 2011 році спеціалісти з Товариства ендокринологів (Endocrine Society) рекомендували підвищити цільовий показник до 40 нг/мл (Holick M.F. et al., 2011). Вони зазначили, що токсичність у вигляді надмірного рівня кальцію та втрати мінеральної щільності кісткової тканини може виникнути, тільки якщо рівень 25(ОН)D буде вищим за 150 нг/мл, тому верхню межу «запасу безпеки» вони регламентують на рівні 100 нг/мл.
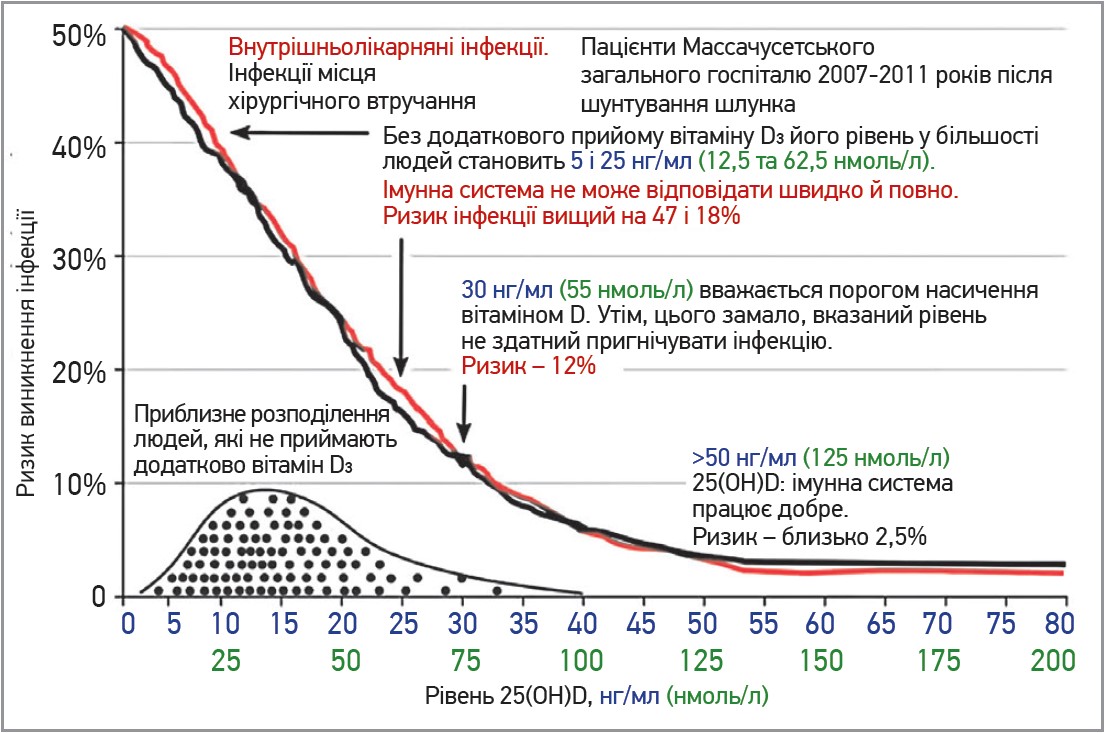
Доцільність підтримання концентрації 25(ОН)D на рівні ~50 нг/мл було підтверджено великою кількістю досліджень. У роботі 2014 року лікарі бостонської лікарні вивчали ризик виникнення внутрішньолікарняних інфекцій та інфекцій у місці хірургічного втручання залежно від рівня 25(ОН)D у 770 пацієнтів після шунтування шлунка (Quraishi S.A. et al.).
Як можна побачити на рисунку, для пацієнтів із рівнем циркулювального 25(ОН)D ≥50 нг/мл (що було досягнуто переважно або повністю за допомогою відповідних дієтичних добавок) ризик госпітальних інфекцій та інфекцій у місці хірургічного втручання окремо становив приблизно 2,5%. В учасників із рівнем 25(ОН)D 20 нг/мл (це абсолютно звичайний рівень для тих, хто не приймає окремо препарати з вітаміном D3 і хто нещодавно не піддавався сильному УФ-опроміненню шкіри) ризик інфекційних ускладнень становив 24%. Таке величезне зростання ризику розвитку інфекційних патологій пояснюється ослабленням уроджених і адаптивних реакцій на бактерії, які є основною причиною обох типів інфекції.
Рис. Ризик розвитку інфекційних ускладнень у пацієнтів після шунтування шлунка залежно від рівня 25(ОН)D
Низькі рівні 25(ОН)D, що послаблюють уроджені й адаптивні імунні реакції, пояснюють численні проблеми зі здоров’ям, від яких страждає багато людей сьогодні. Однак існує інший аспект імунної системи, який зазнає потенційно руйнівних наслідків, коли імунні клітини не можуть отримати достатню кількість 25(ОН)D, – надмірне запалення. Наприклад, у разі тяжкої форми COVID‑19 виснажливу та смертельну шкоду завдає імунна система, а не вірус, який на той час уже припиняє розмножуватися, на госпітальному етапі боротьба йде проти нерегульованих гіперзапальних імунних реакцій, а не проти реплікації вірусу.
Досягнення рівня 50 нг/мл 25(ОН)D
Їжа може забезпечити лише невелику частину вітаміну D3, потрібного для підтримки здоров’я. УФ-опромінення шкіри не є ані безпечним, ані легкодоступним методом генерації більшості або всього вітаміну D3, необхідного нашому організму. Прийом додаткових препаратів вітаміну D3 є єдиним способом для більшості людей досягти рівня 25(ОН)D, потрібного для належного функціонування їхньої імунної системи. Поточні рекомендації щодо додаткового прийому вітаміну D3 недостатні, адже вони спрямовані на досягнення рівня циркулювального 25(ОН)D лише на рівні 20 нг/мл, що зазвичай достатньо лише для функції нирок і здоров’я кісток. Ці рекомендації зазвичай визначають додаткові кількості залежно від вікової групи, часто з максимальним добовим споживанням від 0,1 до 0,25 мг (4000-10 000 МО).
У 2014 році канадські дослідники проаналізували довгострокові рівні 25(ОН)D відповідно до щоденного додаткового споживання для чотирьох морфологій тіла: недостатня вага, нормальна, надмірна вага й ожиріння (Ekwaru J.P. et al.). Вони зробили висновок: щоб досягти 50 нг/мл 25(ОН)D, людям, які страждають на ожиріння, потрібно приблизно на 43% більше вітаміну D, ніж людям із нормальною та недостатньою вагою.
Професор Wimalawansa адаптував цей висновок до щойно згаданих діапазонів співвідношень (табл.). Він також рекомендував прийом 70 МО вітаміну D3 на кг маси тіла на день для людей віком ≤18 років (без поправки на ожиріння) та менші співвідношення для дорослих із недостатньою вагою.
|
Таблиця. Рівні споживання вітаміну D3 залежно від ваги |
||||
|
|
МО вітаміну D3/день/кг |
Орієнтовна вага |
Орієнтовна доза вітаміну, МО/день |
Орієнтовна доза вітаміну, МО/тиж |
|
Недостатня, нормальна та надлишкова вага (ІМТ ≤29) |
70-90 |
30 кг |
2100-2700 |
15-19 |
|
70 кг |
4900-6300 |
35-44 |
||
|
90 кг |
6300-8100 |
44-57 |
||
|
Ожиріння 1 та 2 ступенів (ІМТ – |
90-130 |
60 кг |
5400-7800 |
38-55 |
|
90 кг |
8100-11 700 |
57-82 |
||
|
120 кг |
10 800-15 600 |
76-109 |
||
|
Ожиріння 3 ступеня (ІМТ ≥40) |
140-180 |
100 кг |
14 000-18 000 |
98-126 |
|
150 кг |
21 000-27 000 |
147-189 |
||
|
Примітки: ІМТ – індекс маси тіла. |
||||
Дотримуючись рекомендацій, заснованих на співвідношенні маси тіла, люди будь-якого віку, ваги та морфології тіла досягнуть щонайменше 50 нг/мл циркулювального 25(ОН)D протягом кількох місяців, при цьому рівні рідко перевищують 100 нг/мл, без необхідності аналізів крові чи медичного нагляду.
Вітамін D3 у лікувальній практиці
Вітамін D3 і кальцифедіол як раннє лікування COVID‑19
Рандомізовані контрольовані дослідження щодо лікування COVID‑19 вітаміном D дуже різноманітні з погляду тяжкості захворювання під час прийому, критеріїв успіху та протоколів лікування. Найзначнішою є робота іспанських дослідників (Castillo et al., 2020). Вони працювали із 76 пацієнтами з COVID‑19, госпіталізованими в Кордові, Іспанія, котрі отримували лікування гідроксихлорохіном і антибіотиком азитроміцином. 50 пацієнтів у групі лікування отримали одноразову пероральну дозу 0,532 мг кальцифедіолу відразу після госпіталізації, а потім дози 0,266 мг у дні 3, 7, 14, 21 тощо.
Позитивні результати були частково зумовлені недосконалою рандомізацією, яка призвела до того, що в контрольній групі було значно більше пацієнтів із супутніми захворюваннями. Результати, навіть з огляду на ці застереження, вражали: частка госпіталізацій у відділення інтенсивної терапії впала з 50 до 2%, а смертності з 8% до нуля.
Лікування сепсису
Сепсис – це патогенний стан, за якого неконтрольована вірусна, бактеріальна чи грибкова інфекція спричиняє екстремальну, саморуйнівну запальну реакцію, що пошкоджує органи та часто призводить до летального результату. Швидка діагностика є важливою, але складною, оскільки пацієнти можуть мати широкий спектр неспецифічних симптомів і їхній стан може швидко погіршуватися. Відомо, що у хворих на сепсис рівень 25(ОН)D навіть нижчий, аніж у загальній популяції. Тоді як інфекція та запалення можуть знизити цей рівень, низькі рівні перед зараженням значно підвищують ризик розвитку сепсису. Зважаючи на ці знання, стає зрозуміло, що рівень 25(ОН)D 50 нг/мл значно знизить ризик розвитку поширених інфекцій, які спричиняють сепсис, а також зменшить імовірність надмірної запальної реакції.
Хвороба Кавасакі, MIS-C, PIMS і COVID‑19
Хвороба Кавасакі – це гострий і потенційно смертельний запальний васкуліт, який уражає немовлят і переважно дітей молодшого віку. Інфекційний тригер зазвичай спостерігається за тижні або місяці до початку. Тяжкі випадки включають аневризми коронарних артерій, які можуть призвести до смерті пізніше.
У 2015 році італійські дослідники Stagi та співавт. опублікували статтю, яка змінила розуміння, принципи профілактики та лікування хвороби Кавасакі. У дослідженні взяли участь 21 дівчинка та 58 хлопчиків, середній вік яких становив 5,8 року. Середній рівень 25(ОН)D у них дорівнював 9,2 нг/мл, тоді як у контрольній групі відповідного віку в середньому він становив 23,3 нг/мл. Середній рівень у дітей, у яких виникли аномалії коронарних артерій, був іще нижчим – лише 4,9 нг/мл. Щонайбільше лише незначну частину цієї різниці можна пояснити тим, що хвороба виснажує рівень 25(ОН)D. Решта цієї сильної невідповідності є явною причиною, разом із генетичною схильністю й інфекціями, що провокують.
Хвороба Кавасакі також може бути спровокована COVID‑19, у тому числі безсимптомною, як це часто буває в дітей. У 2020 році з’явилися два діагнози, пов’язані з хворобою Кавасакі: MIS-C (мультисистемний запальний синдром у дітей) і PIMS (педіатричний запальний мультисистемний синдром). Хвороба Кавасакі, що виникає внаслідок COVID‑19, є частиною симптоматичного континууму з MIS-C/PIMS (Tsoukas Р., Yeung R.S.M., 2022). У немовлят і дітей молодшого віку частіше діагностують хворобу Кавасакі, тоді як у підлітків і молодих людей, найімовірніше, будуть діагностовані два інші захворювання, що передбачають менше васкуліту та більше пошкодження органів. Підвищення рівня 25(ОН)D за цих розладів також може бути важливим для припинення патологічного процесу.
Висновки
- Стан імунної системи певною мірою залежить від забезпеченості організму вітаміном D, а низький рівень 25(ОН)D у крові значно підвищує ризик тяжких захворювань, довготривалих пошкоджень і смерті від інфекційних патологій.
- 50 нг/мл циркулювального 25(ОН)D – достатній рівень для злагодженої роботи імунної системи та зниження ризику розвитку інфекцій. Адекватний рівень щоденного споживання вітаміну залежить від ваги людини.
- Добавки вітаміну D можна ефективно застосовувати для лікування таких інфекційних патологій, як коронавірусна інфекція, сепсис, хвороба Кавасакі та ін.
За матеріалами: 50 ng level of Vitamin D proven to fight many diseases – Whittle May 2023.
Довідка «ЗУ»
Одним із препаратів вітаміну D, що представлені на фармацевтичному ринку України, є Відеїн (АТ «Київський вітамінний завод»). Він виробляється у м’яких капсулах дозуванням 1000, 2000, 4000 та 20000 МО вітаміну. Відеїн 20000 – для щотижневого прийому, оскільки 1 капсула містить тижневий курс вітаміну D3. Залежно від дозування препарат призначається як для профілактики дефіциту вітаміну D в осіб різних вікових груп, так і для лікування клінічно підтверджених випадків дефіциту вітаміну D у дорослих, а також як доповнення до специфічної терапії остеопорозу.
Широка лінійка дозувань Відеїну дозволяє підібрати необхідний варіант для підтримання цільового рівня циркулюючого 25-гідроксивітаміну D 50 нг/мл. Варто зазначити,що профілактика й усунення гіповітамінозу D забезпечують не тільки гомеостаз кісток і мінеральних речовин, як вважалось раніше, а й позитивно впливають на імунну систему. Метаболіти вітаміну сприяють вродженій імунній відповіді, яка забезпечує першу лінію захисту від вірусних і бактеріальних інфекцій, одночасно обмежуючи адаптивну імунну відповідь, яка, якщо її не контролювати, спричиняє запальну реакцію, що призводить до розвитку гострого респіраторного дистрес-синдрому та незворотних подій.
Підготувала Юлія Котикович
Медична газета «Здоров’я України 21 сторіччя» № 19/1 (556), 2023 р