29 грудня, 2023
Оптимальна фармакологічна стратегія при синдромі подразненого кишечнику
Синдром подразненого кишечнику (СПК) є нагальною проблемою не тільки гастроентерології, а й системи охорони здоров’я в цілому, оскільки симптоми захворювання суттєво впливають на якість життя пацієнтів. Біль, здуття і дискомфорт у животі, які супроводжують пацієнтів із СПК, знижують працездатність і заважають щоденній діяльності. Спазмолітики наразі є найефективнішою стратегією усунення симптомів мультифакторних розладів осі «головний мозок – кишечник», які призводять до розвитку вісцеральної гіперчутливості, абдомінального болю і моторної дисфункції.
СПК та інші розлади, які виникають внаслідок порушення функціонування сигнальної системи між кишечником і головним мозком (disorders of gut brain interaction, DGBI), є поширеними хронічними захворюваннями, які вражають десятки мільйонів людей по всьому світу. Відповідно до статистичних даних, 4-10% населення світу страждають від СПК, тоді як симптоми, які спостерігаються у 40% населення, відповідають критеріям інших DGBI, раніше відомих як функціональні шлунково-кишкові розлади [1]. Незважаючи на те що СПК загалом вважається доброякісним станом, він пов’язаний зі значними витратами [2] і збільшеним навантаженням на систему охорону здоров’я [3], а також із погіршенням якості життя пацієнтів [4, 5] і зниженням працездатності [6]. Тому СПК та інші розлади, що характеризуються хронічним болем у животі, залишаються пріоритетом у системі охорони здоров’я.
Складна патофізіологія СПК: які фактори впливають на виникнення захворювання?
Згідно з даними метааналізу R.M. Lovell та співавт. (2012), СПК у 1,5-2 рази частіше зустрічається у жінок, ніж чоловіків. Крім того, більшість жінок із СПК скаржаться на біль у животі та запори, тоді як у чоловіків СПК частіше супроводжується діареєю [7].
Значну роль у виникненні СПК відіграє взаємодія факторів зовнішнього середовища (стресові фактори, харчова непереносимість, антибіотики, кишкові інфекції) та індивідуальних особливостей пацієнта [8]. Серед останніх виділяють, зокрема, порушення моторики кишечнику, вісцеральну гіперчутливість, знижену активність імунної системи, порушення бар’єрної функції кишечнику, мікрозапалення (low-grade) і зміни кишкової мікробіоти внаслідок порушення функціонування сигнальної системи між кишечником і головним мозком.
СПК поділяється на декілька субтипів: СПК із діареєю (СПК-Д) – 39%, запором (СПК-З) – 31%, змішаний – 6% і невизначений – 24%. Діагностика СПК ґрунтується на клінічній оцінці стійкої сукупності симптомів згідно з Римськими критеріями, які стосуються дистальних відділів кишечнику, виключенні симптомів тривоги, органічних захворювань, а також на необхідності повторного перегляду діагнозу після первинного курсу лікування.
Мета сучасної фармакологічної терапії СПК і препарати 1-ї лінії
Вибір оптимальної фармакологічної стратегії при СПК визначає якість життя пацієнтів, однак складна багатофакторна патофізіологія захворювання, гетерогенна популяція пацієнтів та їхні очікування щодо результату лікування вимагають більш ретельного підходу до призначення терапії.
Сучасна терапія СПК спрямована на полегшення симптомів, зокрема болю в животі і здуття, а також корекцію випорожнень. Препаратами вибору для пацієнтів із болем у животі є спазмолітики. Залежно від агента, механізм дії спазмолітиків зумовлений антихолінергічними властивостями і здатністю блокувати кальцієві канали, що призводить до розслаблення гладких м’язів кишечнику [9]. Пацієнти із СПК, особливо ті, в яких захворювання супроводжується діареєю, мають підвищений шлунково-товстокишковий рефлекс, частково опосередкований холінергічним шляхом (Chey et al., 2001). Таким чином, спазмолітики є найкращою опцією лікування пацієнтів зі спазмами в животі і зміненим випорожненням (діареєю чи запором).
Крок 1: комунікація з пацієнтом, рекомендації щодо корекції способу життя (виконання фізичних вправ, режим відпочинку), дієта (дієта FODMAP із низьким вмістом оліго-, ди-, моносахаридів і поліолів, що викликають бродіння, а також прийом пробіотиків).
Якщо після корекції способу життя і раціону харчування симптоми СПК зберігаються, рекомендоване фармакологічне лікування.
Крок 2: терапією 1-ої лінії при наявності абдомінального болю є спазмолітики і масло перцевої м’яти. При констипації варто розглянути застосування послаблюючих засобів із м’якою дією, а при діареї – лопераміду.
Якщо після такої терапії симптоми зберігаються, слід перейти до терапії 2-ої лінії.
Крок 3: на цьому етапі Національний інститут здоров’я і досконалості допомоги (NICE) рекомендує призначення центральних нейромодуляторів, таких як трициклічні антидепресанти або селективні інгібітори зворотного захоплення серотоніну (СІЗЗС). Використання цих препаратів обґрунтоване центральною роллю кишково-мозкової осі в патофізіології СПК. Терапією 2-ої лінії при запорі є секретагоги, які активують іонні канали в епітеліальних клітинах слизової кишечнику, збільшуючи вміст електролітів і рідини в його просвіті, розм’якшуючи калові маси і покращуючи шлунково-кишковий транзит. До препаратів цієї групи відносяться лубіпростон, лінаклотид, плеканатид і тенапанор. Додатковими лікувальними опціями у разі виникнення діареї у пацієнтів із СПК є антагоністи рецепторів 5-гідрокситриптаміну-3 (5-HT3), такі як алосетрон, рамосетрон, ондансетрон, що уповільнюють перистальтику кишечнику, або рифаксимін.
Крок 4: когнітивно-поведінкова терапія, гіпнотерапія.
Спазмолітики як ключові агенти у менеджменті симптомів СПК
Експерти зазначають, що звичайні аналгетики, такі як парацетамол, нестероїдні протизапальні препарати, опіати, навряд чи полегшать біль при СПК, а деякі навіть потенційно здатні посилити шлунково-кишкові симптоми. Натомість спазмолітичні препарати, включаючи олію м’яти перцевої, рекомендовані до застосування для полегшення болю і здуття живота. Їх використання обґрунтоване тим, що порушення моторики і кишковий спазм є основними причинами симптомів СПК, а спазмолітики безпосередньо діють на гладкі м’язи кишечнику, розслаблюючи їх. Наявні на сьогодні докази підтверджують провідну роль спазмолітиків у лікуванні СПК, тому NICE рекомендує лікарям розглянути призначення їх пацієнтам із СПК [10].
Метааналіз A.C. Ford та співавт. (2008) включав 22 дослідження, в яких порівнювали ефективність 12 різних спазмолітиків із плацебо у 1778 пацієнтів із СПК [11]. Кількість пацієнтів, які мали стійкі симптоми після проведеного лікування, була значно меншою серед тих, хто отримував спазмолітики, порівняно з тими, хто приймав плацебо (відносний ризик (ВР) =0,68; 95% довірчий інтервал 0,57-0,81). Метааналіз включав широкий спектр препаратів, у тому числі отилонію бромід, циметропію бромід і пінаверію бромід.
Отилонію бромід: доведена клінічна ефективність у лікуванні пацієнтів із СПК
Певні фармакологічні засоби, у тому числі отилонію бромід, здатні значно подовжити час до появи рецидиву симптомів СПК порівняно із плацебо. Спазмолітичні препарати використовуються впродовж багатьох років для контролю симптомів СПК. Отилонію бромід є спазмолітиком, який значно краще контролює симптоми СПК порівняно із плацебо. J. Triantafillidis та співавт. (2014) довели, що ефективність і переносимість отилонію броміду кращі у порівнянні як із плацебо, так і з іншими подібними препаратами. Крім того, препарат може ефективно використовуватися для тривалого лікування пацієнтів із СПК [12].
Отилонію бромід (в Україні зареєстрований як Спазмомен®) здатний ефективно проникати в стінки товстої кишки, що є визнаною мішенню для препаратів, орієнтованих на терапію СПК. Препарат відновлює фізіологічну моторику і підвищує больовий поріг до різноманітних кишкових подразників за допомогою поза- і внутрішньоклітинних механізмів. На позаклітинному рівні отилонію бромід блокує кальцієві канали L‑типу та інгібує вивільнення Са2+ у гладком’язових клітинах. На внутрішньоклітинному рівні препарат пригнічує вивільнення Са2+ із саркоплазматичного ретикулуму. Як антихолінергічний засіб, отилонію бромід пригнічує кальцієві сигнали, пов’язані з мускариновим М3-рецептором, та індуковану ацетилхоліном мобілізацію кальцію на рівні епітелію товстої кишки, демонструючи таким чином антисекреторний потенціал у пацієнтів із СПК-Д [13]. Крім того, отилонію бромід здатний блокувати тахікінінові рецептори (NK1-2) в епітеліальних, м’язових, нервових клітинах ШКТ і нейрокінінові рецептори (NK2), залучені до моторики кишки. Системне всмоктування отилонію броміду після перорального застосування є дуже низьким (3%), тому він екскретується в ШКТ майже у незміненому вигляді через жовчовивідні шляхи. Саме тому цей спазмолітик діє винятково місцево (в кишечнику) і не спричиняє системних побічних ефектів, а тому має високий профіль безпеки.
M. Glende та співавт. (2002) оцінювали ефективність отилонію броміду в лікуванні пацієнтів із СПК упродовж 15 тижнів. Результати рандомізованого дослідження продемонстрували, що кожного місяця частота відповіді на лікування в групі отилонію броміду була значно вищою порівняно з групою плацебо (ВР 37 проти 23%; р<0,05). Загальна місячна і щотижнева відповіді на окремі кінцеві точки (інтенсивність і частота болю й дискомфорту в животі, метеоризм/здуття, тяжкість діареї чи запору, а також наявність слизу в калі) значно частіше реєструвалися в групі отилонію броміду, ніж у групі плацебо [14]. Жодних побічних ефектів, пов’язаних із терапією, зареєстровано не було.
Відповідно до висновків подвійного сліпого плацебо-контрольованого дослідження P. Clavе та співавт. (2011), отилонію бромід має високий профіль безпеки, добре переноситься і перевершує плацебо щодо зменшення частоти епізодів абдомінального болю, тяжкості симптомів здуття живота, а також здатний захищати від рецидиву симптомів СПК. Ці результати додатково підтверджують, що отилонію бромід може покращувати стан пацієнтів як під час прийому препарату, так і після проведеного лікування [15].
Сукупний аналіз P. Clavе та співавт. (2017) показав, що отилонію бромід ефективніший за плацебо щодо полегшення симптомів СПК. При цьому значний терапевтичний ефект отилонію броміду щодо інтенсивності і частоти епізодів болю в животі спостерігався на 10-му і 15-му тижнях лікування 883 пацієнтів із СПК (доля пацієнтів, які відповіли на лікування, – 71,8% на 10-му тижні і 77,2% – на 15-му) і вираженості здуття живота (55% на 10-му тижні і 63,9% – на 15-му) [16].
Результати рандомізованого подвійного сліпого плацебо-контрольованого дослідження D. Chmielewska-Wilkon та співавт. (2014) з діапазоном доз демонструють, що отилонію бромід у дозах 40 і 80 мг може покращити індивідуальні і загальні клінічні симптоми СПК протягом 4-тижневого періоду. Автори зазначили, що всі дози препарату, в тому числі найвища доза 80 мг, добре переносилися пацієнтами, а частота побічних ефектів не була вищою за плацебо [17].
Наразі отилонію бромід (Спазмомен®) рекомендований до застосування як препарат 1-ої лінії для лікуванні пацієнтів із СПК. Отилонію бромід продемонстрував ефективність і високий профіль безпеки у численних рандомізованих клінічних дослідженнях. Препарат полегшує основні симптоми СПК – абдомінальний біль і здуття, а також попереджує рецидив симптомів захворювання після припинення терапії. Тривалість лікування залежить від перебігу захворювання, однак доведена безпека і добра переносимість разом із відсутністю системних побічних ефектів дозволяють призначати отилонію бромід як коротким курсом (від 2-3 тиж до 3 міс), так і тривало (до 2 років).
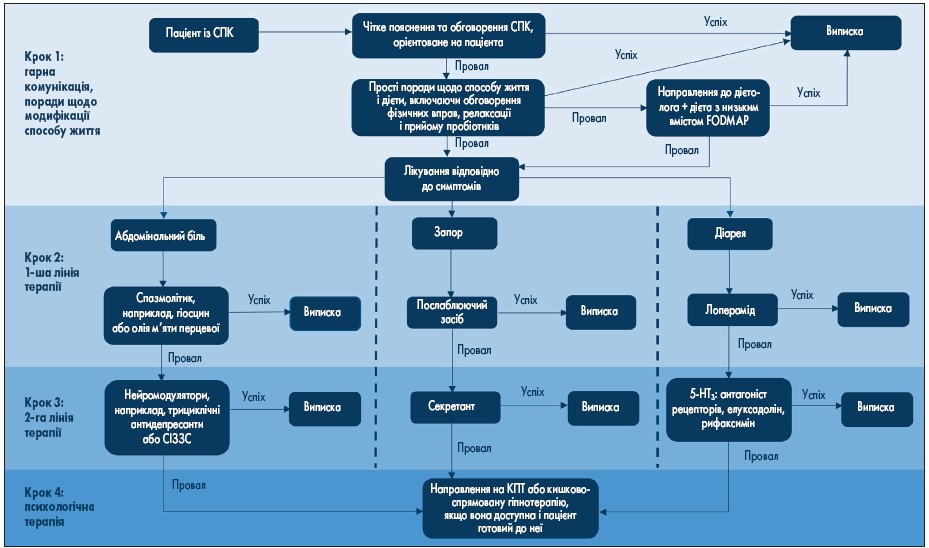 Рис. Алгоритм лікування пацієнтів із СПК
Рис. Алгоритм лікування пацієнтів із СПК
Примітки: FODMAP – ферментовані олігосахариди, дисахариди; КПТ – когнітивно-поведінкова терапія; 5-HT3 – 5-гідрокситриптамін-3; СІЗЗС – селективний інгібітор зворотного захоплення серотоніну
(C.J. Black, A.C. Ford. Best management of irritable bowel syndrome Frontline Gastroenterology. 2021; 12: 303-315).
Повний список літератури знаходиться в редакції.
Підготувала Дарина Чернікова
 Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 4 (70) 2023 р.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 4 (70) 2023 р.



