16 травня, 2024
Виклики та перспективи застосування протиепілептичних препаратів після черепно-мозкової травми
 Черепно-мозкова травма (ЧМТ) є однією з провідних причин смерті і втрати працездатності у всьому світі. За загальними статистичними даними, частота ЧМТ становить близько 200 випадків на 100 тис. населення в мирний час, а смертність від ЧМТ сягає 20 випадків на 100 тис. (Lee et al., 2022). Ці показники значно зростають під час військових конфліктів, тож проблема ЧМТ і зумовлених нею ускладнень нині є особливо актуальною в Україні.
Черепно-мозкова травма (ЧМТ) є однією з провідних причин смерті і втрати працездатності у всьому світі. За загальними статистичними даними, частота ЧМТ становить близько 200 випадків на 100 тис. населення в мирний час, а смертність від ЧМТ сягає 20 випадків на 100 тис. (Lee et al., 2022). Ці показники значно зростають під час військових конфліктів, тож проблема ЧМТ і зумовлених нею ускладнень нині є особливо актуальною в Україні.
Травматичне ушкодження головного мозку характеризується як «зміна функції мозку або інші ознаки патології головного мозку, що зумовлені зовнішньою силою». У світі на цей тяжкий інвалідизувальний неврологічний розлад страждає понад 57 млн осіб (Baiden, 2022). ЧМТ є однією з найпоширеніших причин захворюваності та смертності серед молодих осіб до 45 років. Внаслідок військових дій в Україні питання спостереження та лікування ЧМТ набуває значної актуальності.
Гострі симптоматичні епілептичні напади
ЧМТ – складна мультидисциплінарна проблема у системі охорони здоров’я, оскільки це одна з вагомих причин смертності та стійкої втрати працездатності. Щороку майже у 2,87 млн осіб, які мешкають у США, діагностують ЧМТ, серед них понад 280 тис. осіб потребують госпіталізації, а 56 тис. випадків закінчуються летально (Taylor et al., 2017).
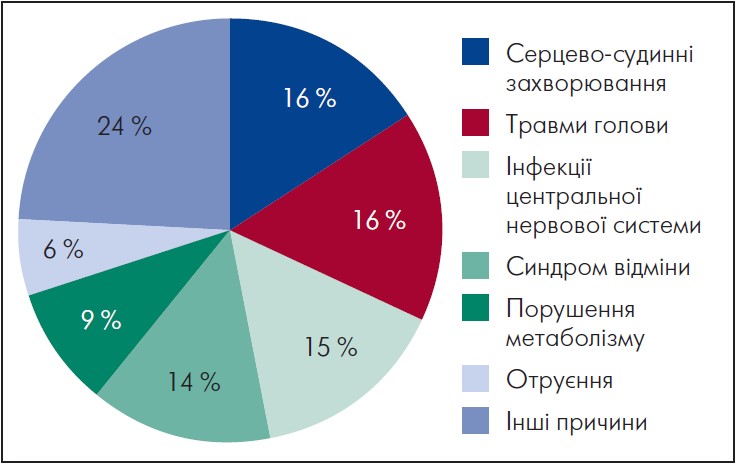
Епілептичні напади визнано одним із найчастіших тяжких ускладнень ЧМТ (Faul, 2010). Є багато причин зміни збудливості центральної нервової системи (ЦНС), що призводить до тимчасового зниження судомного порогу і виникнення епілептичних нападів (рис. 1).
Рис. 1. Причини гострих симптоматичних епілептичних нападів
Адаптовано за M. Mauritz et al. Acute symptomatic seizures: an educational, evidence-based review. Epileptic Disorders. 2022. Vol. 24, № 1. Р. 26‑49.
Як відомо, епілептичний напад – це тимчасова поява ознак та/або симптомів через аномальну надмірну або синхронну активність нейронів головного мозку. Для епілепсії характерні повторювані неспровоковані епілептичні напади. Проте епілептичний напад за гострого ушкодження головного мозку не завжди означає, що у хворого розвинулася епілепсія.
За практичним клінічним визначенням епілепсії, прийнятим Міжнародною протиепілептичною лігою (ILAE, 2014), епілепсія – захворювання головного мозку, що відповідає будь-якому з таких станів:
- Не менше двох неспровокованих (або рефлекторних) епілептичних нападів з інтервалом >24 год.
- Один неспровокований (або рефлекторний) епілептичний напад і ймовірність повторних нападів, що відповідає загальному ризику рецидиву (≥60%) після двох неспровокованих епілептичних нападів за наступні 10 років.
- Діагноз епілептичного синдрому.
Тобто епілептичні напади за перші сім діб після перенесеної ЧМТ не можна вважати епілепсією як самостійною хворобою, бо це гостра реакція організму на травматичне ушкодження – гострі симптоматичні напади.
За визначенням ILAE (2014), гострі симптоматичні напади відрізняються від неспровокованих судомних подій за кількома аспектами:
- На відміну від неспровокованих судом, завжди має бути чітко ідентифікований супутній гострий стан, що став їх причиною і виник близько до моменту нападу.
- Гострі симптоматичні судомні напади зазвичай не повторюються після усунення чинника або стану, що їх спровокував, і відновлення функціональної цілісності ЦНС. Отже, якщо після гострого симптоматичного нападу не спостерігається «стійкої схильності», то пацієнт не страждає на епілепсію.
Відмінність між гострими симптоматичними судомами та епілепсією є складнішою через деструктивні патології мозку, оскільки наявний підвищений ризик подальшого розвитку епілепсії. Саме до цих випадків і належить ЧМТ.
Відмінність гострих симптоматичних судомних нападів від епілепсії
Насамперед клініцист має визначити, чи наявні ознаки епілептичного нападу, чи це є одним із багатьох станів, що маскуються під напад (Fisher et al., 2017; ILAE / IBE, 2005, 2017). Часто на практиці лікарі послуговуються іншими термінами: «спровокований» або «реактивний» напад. За рекомендацією ILAE, ці терміни слід вважати синонімами «гострого симптоматичного нападу» та надалі використовувати лише останнє визначення (Beghi et al., 2010).
Основна проблема щодо визначення гострих симптоматичних нападів виникає через складність об’єднання в одному понятті нападів, зумовлених гострими структурними патологіями мозку і провокувальними чинниками. Різниця між «спровокованим» і «неспровокованим» нападами може бути доволі складною для визначення.
Так, на думку R. S. Fisher (2014), важко повністю виключити провокувальний чинник, навіть якщо судомний напад має ознаки неспровокованого. З іншого боку, наявність потенційно провокувального чинника не виключає основної схильності до виникнення епілептичних нападів. До 40% усіх нападів трапляються в осіб із гострим ураженням мозку, але без епілепсії (Hauser, 2008). На відміну від епілепсії, загальна концепція гострих симптоматичних нападів передбачає, що напади не повторюються після того як провокувальний чинник або стан було усунено. Однак на практиці підвищений ризик розвитку епілепсії зберігається після гострих симптоматичних нападів, спричинених структурними патологіями мозку. За часом є три критерії розвитку епілептичних нападів після ЧМТ:
- негайні епілептичні напади (оnset seizures) – розвиваються впродовж 24 год після ЧМТ;
- ранні епілептичні напади – виникають упродовж семи діб після ЧМТ;
- пізні напади – маніфестують через тиждень і більше.
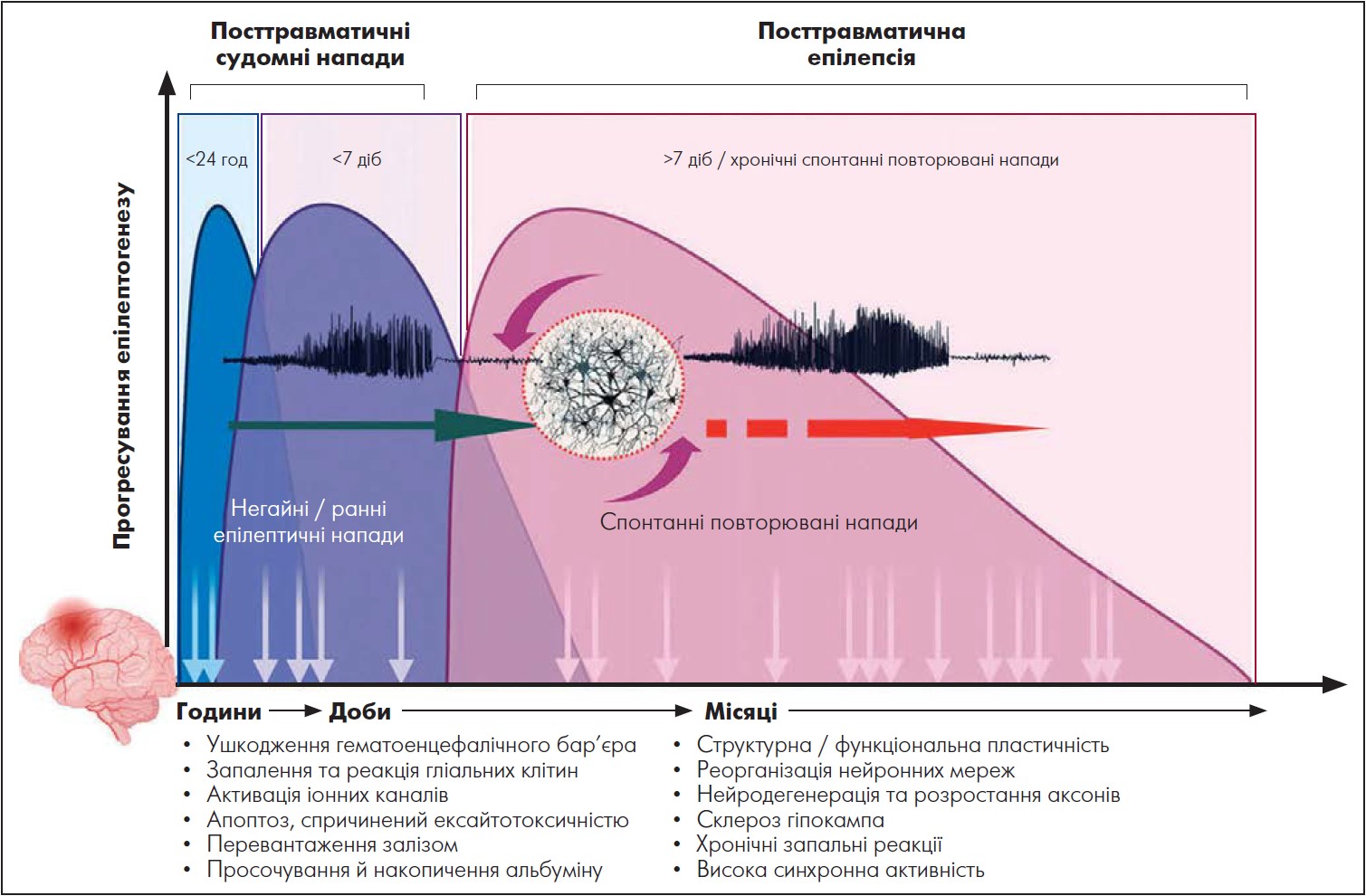
Епілептичні напади протягом першого тижня після ЧМТ є гострими симптоматичними (Beghi et al., 2010). Раніше їх називали ранніми посттравматичними судомами (Jennett et al., 1975). Тоді як епілептичні напади, що виникають пізніше сьомого дня після травми, спонтанно, внаслідок післятравматичних патологічних процесів у ЦНС, і є ознакою епілепсії, раніше їх називали пізніми посттравматичними судомами (Bergey et al., 2016). Після травми відбувається низка процесів, як-от некроз, мікрокрововиливи, ушкодження аксонів, апоптоз, демієлінізація, мікрогліоз, запалення та окиснювальний стрес. На пізніших фазах виникає нейродегенерація, реваскуляризація та ремоделювання, які можуть призводити до змін нейронних мереж і до розвитку епілепсії надалі (рис. 2).
Рис. 2. Хронологія прогресування негайних / ранніх і спонтанних епілептичних нападів після черепно-мозкової травми
Адаптовано за V. M. Golub and D. S. Reddy. Post-Traumatic Epilepsy and Comorbidities: Advanced Models, Molecular Mechanisms, Biomarkers, and Novel Therapeutic Interventions. Pharmacol Rev. 2022 Apr. Vol. 74, № 2. Р. 387‑438.
Посттравматична епілепсія
Сукупний ризик розвитку посттравматичної епілепсії (ПТЕ) коливається від 2 до 50% залежно від локалізації та тяжкості травми (Annegers, 1998; Chen, 2009; DVBIC, 2019; Tubi, 2019). Ранні посттравматичні судомні напади упродовж першого тижня підвищують імовірність розвитку епілепсії протягом перших двох років після ЧМТ (Haltiner, 1997; Christensen, 2009).
Раніше вважали, що ранні судомні напади виникають у 2,4% осіб із легкою травмою голови, що було визначено на підставі даних клінічних критеріїв оцінювання за шкалою коми Глазго (ШКГ) (Lee and Lui, 1992). Втім, за даними нейровізуалізації підтверджено значущі внутрішньочерепні кровотечі у значної частини цих пацієнтів, що призводили до зміни категоризації їхнього стану на тяжкий. Результати дослідження розширили знання про частоту ранніх нападів. Автори визначили чинники дворічного ризику в когорті всіх госпіталізованих пацієнтів віком від 18 років із ЧМТ на підставі даних із Національного банку даних США щодо травм. Із 360 тис. 863 госпіталізованих пацієнтів лише 0,4% (1559) мали ранні напади (Majidi, 2017).
Це порівняно небагато, але смертність у цій групі становила 7%, що відображає тяжчий стан пацієнтів, адже багато осіб із ЧМТ ніколи не госпіталізують. Ризик віддалених судомних нападів становив 0,38% у групі осіб із легкою ЧМТ (показник за ШКГ 13‑15 балів); 0,8% – у групі із помірною ЧМТ (показник за ШКГ 9‑12 балів) і 0,5% – у групі з тяжкою ЧМТ (показник за ШКГ <9 балів). Пацієнти з тяжкою ЧМТ і тривалою втратою свідомості мають значно вищий ризик розвитку епілептичних нападів.
В одному з ретроспективних досліджень протягом 50 років дослідники вивчали характеристики травм головного мозку, пов’язані з розвитком нападів. За результатами дослідження, тяжкість таких травми корелювала з інтервалом, протягом якого ризик судомних нападів був підвищеним, навіть за понад 20 років після травми.
ЧМТ було поділено на легкі, із менш ніж 30-хвилинною посттравматичною амнезією (ПТА) або втратою свідомості; помірно тяжкі – із ПТА або порушенням свідомості від 30 хв до 24 год та тяжкі – із більш тривалим порушенням свідомості та/або ушкодженнями кісток черепа, структурними ураженнями головного мозку, підтвердженими даними комп’ютерної томографії. Пацієнти з легкими ЧМТ не мали підвищеного ризику епілептичних нападів; із ЧМТ помірної тяжкості мали ризик розвитку нападів протягом 20 років приблизно 0,1%; із тяжкою ЧМТ – ризик розвитку нападів упродовж першого року після травми 5%, у період до 5 років – ще 5% та протягом 20 років після травми – 17% (Annegers, 1998).
Дослідники встановили, що впродовж перших трьох місяців після травми віддалені епілептичні напади виникали у 32% осіб із синдромом неспання / вегетативним станом (UWS/VS – наявністю збудження без ознак усвідомлення) та у 11% – у стані мінімальної свідомості (MCS – ознаки нерефлекторної кортикально-опосередкованої поведінки) (Bagnato et al., 2013).
В іншому дослідженні, що тривало 30 місяців, виявлено, що у когорті пацієнтів із розладами свідомості 26% осіб мали віддалені епілептичні напади та 47% – епілептиформну активність після травми головного мозку. Автори дійшли висновку, що немає суттєвої різниці між пацієнтами з UWS/VS та MCS щодо захворюваності на ПТЕ, а також будь-якого зв’язку ПТЕ зі смертністю, однак епілептичні напади (клінічні чи субклінічні) перешкоджали відновленню свідомості (Pascarella et al., 2016).
Європейське товариство інтенсивної терапії (ESICM) рекомендує використання безперервного моніторингу даних електроенцефалографії (ЕЕГ) у гострому періоді, особливо для пацієнтів, які перебувають у комі з нез’ясованими та стійкими порушеннями свідомості, для виявлення неконвульсивного нападу або несудомного епілептичного статусу, коли неврологічне обстеження є недостатнім для формування точного прогнозу (Claassen et al., 2013). Пацієнтам із порушенням свідомості рекомендовано виконувати повторну стандартну ЕЕГ для виявлення ризику розвитку епілептичних нападів, а також для диференціації UWS/VS від MCS (Pascarella et al., 2016; Estraneo et al., 2016).
За даними спостереження пацієнтів упродовж двох років від моменту травми, причини значної частки посттравматичних нападів, які виникли протягом першого місяця, ймовірно, були багатофакторними. Гострі провокувальні чинники охоплювали набряк мозку, періопераційні ускладнення та метаболічні чинники. Будь-який судомний напад, який виникає під час перебування в стаціонарі, зважаючи на супутні ускладнення, пов’язані з механічною вентиляцією легень, та іншими обтяжливими станами, що супроводжують помірну та тяжку ЧМТ, може являти собою спровокований гострий посттравматичний напад (Englander et al., 2003).
Щонайменше два неспровоковані віддаленні симптоматичні напади, які виникли з інтервалом >24 год у пацієнта з високим ризиком рецидиву, визначають як ПТЕ (Fisher et al., 2014). Після першого пізнього неспровокованого посттравматичного нападу ймовірність розвитку епілептичних нападів у майбутньому (через 2 роки) може сягати 86% (Haltineret al., 2012). Найбільший ризик мають ті, хто отримав проникні поранення головного мозку.
За даними дослідження за участю ветеранів війни у В’єтнамі, у понад половини осіб із проникними травмами голови розвинулася ПТЕ (Raymont, 2010). Хоча результати іншого дослідження засвідчили, що ПТЕ розвинулася у 10,6% осіб із переломами черепа, у 5,05 і 3,02% – із тяжкою та легкою ЧМТ відповідно (Yeh, 2013). Також ЧМТ асоціюється з дисоціативними нападами (раніше їх називали психогенними неепілептичними нападами). У 1990-х роках цей зв’язок було виявлено у дослідженнях в епілептичних центрах США, а пізніше підтверджено (Westbrook, 1998; Barry, 1998; Popkirov, 2018).
Дисоціативні події нагадують епілептичні судоми, і один із п’яти пацієнтів, скерованих до клініки з попереднім діагнозом ПТЕ, має такі напади (Alper, 1994; Benbadis, 2000). Якщо травма була легкою і ризик епілепсії дуже низький, посттравматичні судомні напади, найімовірніше, будуть дисоціативними, а не епілептичними. Більшість даних свідчить, що 81‑89% випадків дисоціативних нападів трапляються впродовж року після ЧМТ. Пацієнти з дисоціативними нападами не демонструють реакції на застосування протиепілептичних препаратів (ПЕП), що може сприйматися як «червоний прапорець» за встановлення діагнозу. Крім того, ПЕП погіршують результати у деяких пацієнтів із дисоціативними нападами (Alessi, 2014). Асоціація з посттравматичним стресовим розладом (ПТСР) та іншими супутніми психіатричними захворюваннями додатково розмежовує посттравматичні дисоціативні припадки та епілептичні напади. Наприклад, у США 57% ветеранів із посттравматичними дисоціативними нападами також мають ПТСР (Salinsky, 2011; Trivedi, 2015).
Підходи до лікування пацієнтів із судомними нападами внаслідок ЧМТ
Психотерапія є основою лікування пацієнтів із дисоціативними нападами, що допомагає досягти значного симптоматичного поліпшення. Втім, відносно небагато пацієнтів із дисоціативними нападами можуть розраховувати на те, що вони їх позбудуться (Reuber, 2003). Затримка діагностування посттравматичних дисоціативних нападів є більшою, ніж за епілепсії, і являє собою чинник, що може негативно позначитись на прогнозі (Reuber et al., 2002).
Відповідно до сучасної класифікації епілепсії, ПТЕ – це синдром із генералізованими та фокальними нападами і структурною причиною (Scheffer, 2016). Клінічні дослідження ПЕП у цій групі відбуваються без розрізнення етіології, тож нині бракує випробувань препаратів, призначених саме для пацієнтів із ПТЕ. Завданням клініцистів є досягнення контролю над судомними нападами, якщо це можливо, і уникнення специфічних супутніх захворювань, що можуть бути пов’язані із ЧМТ. Успіх терапії може бути визначений як досягнення стану без судомних нападів або зменшення їх частоти принаймні на 50%. Так, за пропозицією робочої групи Комісії з терапевтичних стратегій ILAE, можливість збільшити втричі найдовший інтервал між нападами може бути хорошим показником ефективності лікування (Kwan et al., 2010). Епілептичні напади після травми голови призводять до вторинного ураження мозку, що охоплює підвищення внутрішньочерепного тиску, збільшення метаболічних потреб мозку та надмірне вивільнення нейромедіаторів, зумовлюючи подальше ускладнення стану пацієнта. Основна мета застосування ПЕП – мінімізувати ушкодження мозку та його наслідки (Schierhout et al., 1998).
ПЕП також притаманний нейропротекторний ефект, який був продемонстрований на тваринних моделях. Дослідники припускають, що нейропротекторні властивості ПЕП пов’язані з блокуванням вольтажзалежних натрієвих каналів за гіпоксії, що зменшувало спричинену кальцієм нейротоксичність після гіпоксичного ушкодження мозку (Vartanian,1996; Tasker, 1992). Фенітоїн довгий час був засобом першої лінії для пацієнтів із ЧМТ, але ризик серйозних побічних ефектів (як-от аритмій, тяжкої реакції гіперчутливості шкіри), міжлікарської взаємодії і потреба в моніторингу сироваткового рівня препаратів сприяла переходу на леветирацетам (Temkin et al., 1990; Jones, 1989; Chaari, 2017; Levine, 1990, Richens, 1979; Kruer et al., 2013).
Відповідно до рекомендацій із лікування мінно-вибухової травми у військових та ведення пацієнтів за Об’єднаною системою травматологіїі (JTS CPG, 2017) препаратом вибору для лікування судомних нападів у пацієнтів із травматичним ураженням мозку леветирацетам (навантажувальна доза 1500 мг внутрішньовенно [в/в], надалі по 1000 мг внутрішньовенно двічі на добу).
Препаратом другої лінії є лакосамід (навантажувальна доза 400 мг в/в, надалі по 200 мг в/в що 12 год). Якщо є підозра на тяжку ЧМТ, профілактику судомних нападів слід виконувати за первинного оцінювання стану пацієнта та протягом 30 хв після прибуття пацієнта до стабілізаційного пункту. Лікування слід продовжувати до 7 діб і довше, якщо у пацієнта були клінічні ознаки судом (Dengler et al., 2023). Деякі автори припускають існування вікна можливостей приблизно впродовж години після ЧМТ. Протягом цього періоду лікування ПЕП може запобігти розвитку епілептичних нападів або призупинити їх (Ko et al., 2022). Хоча дослідження ефективності цього лікування тривають. За Настановою Національної служби охорони здоров’я Північного Бристоля (Guideline for North Bristol Trust, NHS, 2017) щодо лікування тяжкої ЧМТ рекомендовано застосовувати леветирацетам для пацієнтів, які не приймали ПЕП до травми та у яких після травми розвинувся судомний напад (Wigfield, 2017). Нині леветирацетам є ПЕП першої лінії при ЧМТ, замінивши фенітоїн. Дані проспективного рандомізованого порівняльного дослідження ефективності в/в леветирацетаму та фенітоїну для профілактики судомних нападів у відділенні інтенсивної терапії підтвердили, що леветирацетам є альтернативним засобом фенітоїну (Szaflarski, 2010).
За високого ризику розвитку епілепсії (чинники ризику судомних нападів після ЧМТ передбачають показник за ШКГ <10 балів, переломи черепа, проникні поранення, тривалу кому [>24 год]) у клініцистів є можливість розглянути запобігання нападам (Temkin et al., 2003).
Однак Кокранівський огляд профілактичного застосування ПЕП після ЧМТ визначає якість виконаних досліджень як низьку. Автори виявили, що профілактичне лікування може зменшити частоту ранніх посттравматичних нападів, але не чинить вплив на пізні напади або смертність після ЧМТ (Thompson et al., 2015). За даними метааналізу, нині бракує конкретного препарату, який би краще запобігав раннім нападам (Zafar, 2012).
Іншим антиконвульсантом, який викликає інтерес у клініцистів, є вальпроєва кислота. Її застосування пов’язане з можливим вищим рівнем смертності (Temkin et al., 1999). Це може бути пояснено спричиненою коагулопатією, яка може призводити до внутрішньочерепного крововиливу (Chang, 2003; LaRouche, 2007). Як зазначають клініцисти, вальпроєву кислоту застосовують у третині (35,4%) випадків. Ці дані, ймовірно, можна пояснити використанням вальпроєвої кислоти для лікування супутніх розладів поведінки у пацієнтів, які мали в анамнезі порушення свідомості або перебувають у стані сплутаності свідомості (Ganau, 2018; Williamson, 2019). Результати ретроспективного дослідження, у якому вивчали ефективність в/в введення вальпроату натрію для профілактики судомних нападів у дорослих і дітей із ЧМТ, засвідчили, що за терапії вальпроатом натрію у пацієнтів не виникло жодного епілептичного нападу, на відміну від тих, хто не отримував лікування цим препаратом (Ma, 2010). Також було підтверджено, що застосування вальпроату (480 мг/кг/добу протягом 7 діб) сприяло зниженню частоти і кумулятивної тривалості нападів (Eastman et al., 2011). ПТЕ пов’язана зі значною втратою працездатності, смертністю та розвитком резистентної до лікування епілепсії, тож нині продовжується пошук нових біомаркерів і потенційних антиепілептогенних методів лікування за ЧМТ (Vespa, 2019). На думку S. Hakimian et al. (2012), близько третини пацієнтів ПТЕ є резистентними до ліків. Для цієї групи можна розглянути застосування хірургічного втручання за епілепсії. За даними досліджень, це може бути успішним для осіб з уніфокальною або мультифокальною травмою (за останньої лише з наявністю тільки одного підтвердженого епілептогенного фокусу) (Hakimian et al., 2012). Дані ще одного масштабного дослідження підтвердили хороші показники нейрохірургічного лікування, яке, ймовірно, охоплювало значну кількість нетравматичних випадків (Gupta et al., 2014).
Висновки
Одним із найчастіших тяжких ускладнень ЧМТ є посттравматичні судомні напади, які можуть прогресувати до посттравматичної епілепсії. Підвищений ризик розвитку епілепсії зберігається після гострих симптоматичних нападів, зумовлених структурними патологіями мозку. Метою застосування протиепілептичних засобів, окрім протинападової дії, є мінімізація ураження мозку та забезпечення нейропротекторного ефекту. Нині препаратами першої лінії для лікування судомних нападів у пацієнтів із травматичним ураженням мозку є сучасні ефективні антиконвульсанти зі сприятливим профілем безпеки, передусім леветирацетам. Раннє застосування таких препаратів у пацієнтів із ЧМТ сприяє запобіганню розвитку епілептичних нападів.
UA-LEVI-PUB-032024-090
Тематичний номер «Неврологія. Психіатрія. Психотерапія» № 1 (68) 2024 р.