16 жовтня, 2024
Потенційні побічні ефекти протигрибкових препаратів, які застосовуються для лікування поверхневих грибкових інфекцій: аналіз американської системи FAERS
Поверхневі грибкові інфекції, як-от дерматомікози, оніхомікози, вульвовагінальний кандидоз (ВВК), є поширеною глобальною проблемою: щороку реєструють понад 1 млрд випадків, і велика кількість пацієнтів отримує топічні протигрибкові препарати, які зазвичай є першою лінією терапії в разі неускладненої інфекції. Попри загалом добру переносимість ці засоби, як і будь-які інші ліки, можуть спричиняти побічні ефекти, зокрема й такі, що не зазначені в інструкціях.
Цінним інструментом для вивчення нових або рідкісних побічних ефектів, які не завжди виявляються під час клінічних випробувань, є система FAERS (FDA Adverse Event Reporting System) – ключовий елемент фармаконагляду США, що допомагає контролювати безпеку ліків у реальному часі після їхнього виходу на ринок.
Є кілька прикладів, коли аналіз даних FAERS допоміг виявити нові побічні ефекти із суттєвими наслідками. Найвідомішим випадком є рофекоксиб, який у 2004 році відкликали з ринку після того, як аналіз FAERS разом із клінічними дослідженнями показали значне підвищення ризику серцево-судинних подій. На основі звітів FAERS було внесено зміни в інструкції із застосування розиглітазону (ризик розвитку серцевої недостатності й інфаркту міокарда), фторхінолонів (розриви сухожиль, периферична нейропатія), ліраглутиду (рак щитоподібної залози).
Як працює FAERS?
- Збір даних. Пацієнти, медичні працівники, фармацевтичні компанії через спеціальні онлайн-портали або форми можуть подавати звіти про побічні ефекти або проблеми, пов’язані з використанням ліків.
- Аналіз. Ці звіти потрапляють у базу даних FAERS, де експерти FDA аналізують їх на наявність нових або небезпечних побічних ефектів. Якщо спостерігаються незвичайна частота певних реакцій або серйозні небажані події, це може сигналізувати про проблему.
- Реакція. Якщо виявлено нові ризики або небезпеки, FDA може вживати заходів – приміром, вимагати оновлення інструкції із застосування препарату, запровадити попередження (black box warning – «застереження в чорній рамці»), обмежити використання ліків і навіть відкликати препарат з ринку.
Дослідження безпеки 4 імідазолів
Нещодавно в Scientific Reports – рецензованому науковому мегажурналі з відкритим доступом, який видає Nature Portfolio, – було опубліковано статтю, присвячену потенційним небажаним подіям (НП) при застосуванні імідазолових протигрибкових препаратів для лікування ВВК (Zhou T. et al., 2024). Автори використали дані системи FAERS за період з 2004 по 2022 рік для клотримазолу, еконазолу, кетоконазолу та міконазолу. Для дата-майнінгу скористалися такими показниками, як ROR (report odds ratio, коефіцієнт імовірності повідомлення [про НП]) та PRR (proportion report ratio, коефіцієнт пропорційності повідомлення). Що вищі ROR та PRR, то потужнішим є сигнал, що свідчить про сильніший статистичний взаємозв’язок між препаратом і НП.
Формула для обчислення ROR виглядає так:
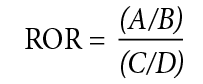
де:
А – кількість звітів про НП для конкретного препарату (Drug A + Reaction X),
B – кількість звітів про інші НП для цього ж препарату (Drug A + Not Reaction X),
C – кількість звітів про таку ж НП для інших препаратів (Not Drug A + Reaction X),
D – кількість звітів про інші НП для інших препаратів (Not Drug A + Not Reaction X).
Скажімо, ROR 2,5 означає, що небажана подія Х виникає в 2,5 рази частіше для препарату А, ніж для інших препаратів.
Загалом було знайдено 9985 сигналів НП, переважна більшість яких охоплювала 23 класи SOC (system organ class – клас відповідно до ураження органів і систем органів за термінологією медичного словника MedDRA). Сигнали SOC для 4 досліджуваних препаратів переважно включали порушення з боку судин, шкіри та підшкірної клітковини, дихальної системи, органів грудної клітки та середостіння, нирок та сечових шляхів; вагітність, післяпологовий період і перинатальні стани; психіатричні розлади і т. ін.
У межах топ‑10 класів SOC (рис.) для клотримазолу найпотужнішим сигналом (ROR 15,79) із найвищою частотою (40 випадків) була хронічна хвороба нирок, за якою йшли гостре ураження нирок (ROR 10,45) і ниркова недостатність (ROR 8,66).
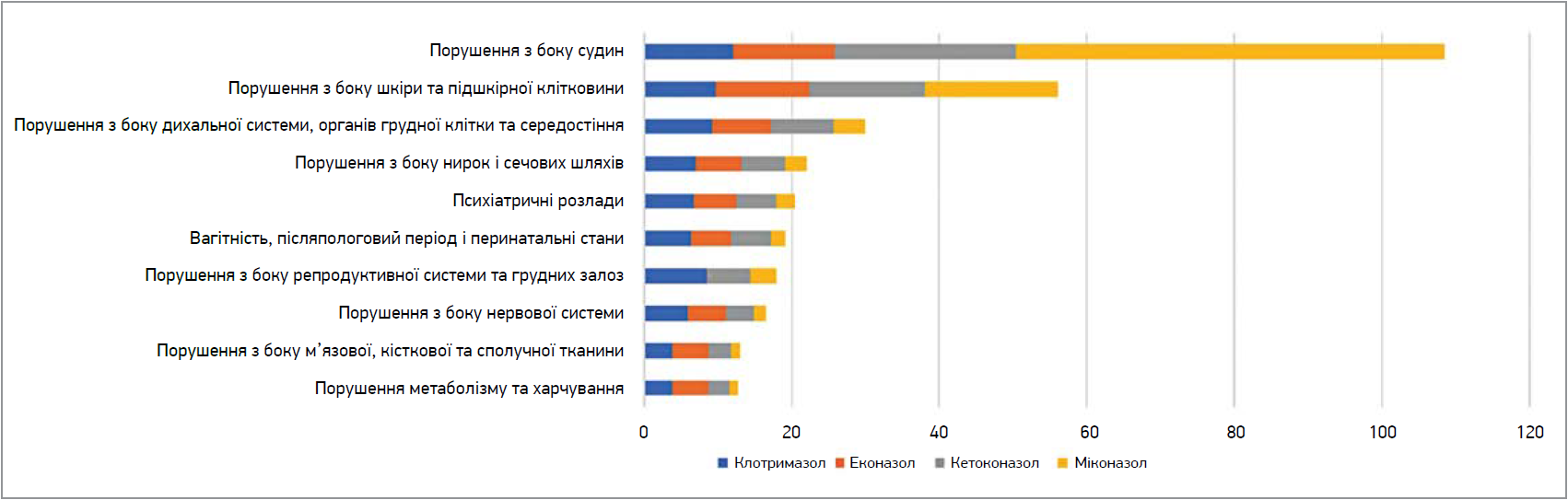 Рис. Розподіл сигналів небажаних подій відповідно до топ‑10 класів SOC для досліджених препаратів
Рис. Розподіл сигналів небажаних подій відповідно до топ‑10 класів SOC для досліджених препаратів
Для еконазолу спостерігали інтенсивний сигнал щодо порушень із боку шкіри та підшкірної клітковини, передусім скарлатиноподібного висипу (ROR 47 496) та ураження нігтів (ROR 3423). Найчастішою НП (9 випадків) був спонтанний аборт (ROR 19,62).
Для кетоконазолу НП з найвищою частотою були хронічна хвороба нирок (ROR 11,64) та алопеція (ROR 7,88).
Міконазол переважно спричиняв порушення з боку репродуктивної системи і грудних залоз, шкіри та підшкірної клітковини. Найтяжчим НП був набряк вульви (ROR 1043), найчастішим – вульвовагінальне печіння (ROR 842).
У дослідженні також проаналізували позитивні сигнали, не зазначені в інструкціях із застосування препаратів. Було встановлено, що клотримазол спричиняв неврологічні НП, наприклад синдром поствірусної втоми (ROR 2282), та порушення з боку імунної системи, як-от ендокринна офтальмопатія (ROR 464). Еконазол зумовлював ураження нігтів (ROR 3423) і недостатність надниркових залоз (ROR 166), міконазол – підвищення рівнів кортизолу (ROR 625), пригнічення гіпоталамо-гіпофізарно-надниркової осі (ROR 1012) і появу антифосфоліпідних антитіл (ROR 428), кетоконазол – позитивну реакцію Яриша – Герксгеймера (ROR 543).
Автори визначають, що їхній аналіз має низку обмежень. По-перше, FAERS – це пасивна і спонтанна база даних НП, яка наповнюється добровільно. Деякі дослідження свідчать, що в цю базу потрапляє тільки 5% усіх серйозних НП. По-друге, виявлені НП могли бути пов’язані з основним захворюванням, спричинені супутніми препаратами або іншими причинами. Зрештою для аналізу обрали лише 4 протигрибкові препарати – похідні імідазолу.
А як щодо сертаконазолу?
У США для лікування грибкових інфекцій шкіри, окрім досліджених імідазолів, застосовують сертаконазол – топічний протигрибковий препарат нового покоління. Ми провели пошук у системі FAERS за ключовими словами sertaconazole та sertaconazole nitrate за 19 років присутності на ринку (2004-2023 рр.). Протягом цього періоду в систему надійшло лише 69 повідомлень про НП (як порівняти з тисячами НП для 4 досліджених імідазолів), і переважна більшість цих НП були несерйозними (свербіж, почервоніння, відчуття печіння, сонливість і т. ін.). За такої малої кількості обчислювати ROR немає сенсу, оскільки результати будуть ненадійними. Утім, побічно це може свідчити про те, що сертаконазол насправді є безпечнішим протигрибковим препаратом.
Варто зазначити, що в США сертаконазол поки що застосовується не так широко, як 4 інші протигрибкові препарати, оскільки є рецептурним (приміром, клотримазол крем є безрецептурним), новішим і, відповідно, дорожчим. Крім того, сертаконазол на американському ринку представлений тільки у формі 2% крему (в Україні присутні сертаконазол 2% крем і сертаконазол 0,3 г овулі).
Щодо потенційно кращої безпеки сертаконазолу, то вона може пояснюватися особливостями молекули та вищою клінічною ефективністю. Так, на відміну від 4 досліджених препаратів, які є похідними імідазолу, сертаконазол є одночасно похідним імідазолу та бензотіофену.
За фунгістатичний ефект відповідає азольне кільце, яке порушує синтез ергостеролу – одного з основних компонентів клітинної мембрани грибів. Зменшення вмісту цієї сполуки в клітинній мембрані порушує її плинність і проникність.
Фунгіцидна дія сертаконазолу зумовлена бензотіофеном, структурно схожим на триптофан. Убудовуючись у клітинну мембрану гриба замість молекул триптофану, бензотіофен підвищує її проникність, що спричиняє втрату внутрішньоклітинної АТФ, руйнування цитоскелета та лізис клітинних органел. Цей механізм також перешкоджає утворенню гіф, запобігаючи їхній інвазії до тканин господаря. До того ж завдяки високій ліпофільності бензотіофену сертаконазол тривалий проміжок часу (близько 72 годин) утримується шкірою і не потрапляє до системної циркуляції.
Крім фунгістатичної та фунгіцидної дії, сертаконазол чинить протизапальний ефект (шляхом активації сигнального шляху p38-ЦОГ‑2-PGE2), а також забезпечує протисвербіжний вплив (завдяки індукції простагландину D2, який гальмує вивільнення гістаміну).
Подвійна протигрибкова дія та додаткові ефекти, імовірно, пояснюють вищу терапевтичну ефективність сертакозалу порівняно з іншими часто застосовуваними протигрибковими препаратами (Palacin C., 2001), що, своєю чергою, дозволяє уникнути рецидивів і повторних курсів лікування, а отже, зменшує експозицію препарату та, відповідно, покращує безпеку.
Практичні висновки
- Система FAERS – цінний інструмент для виявлення нових або рідкісних побічних ефектів у реальній клінічній практиці, які не завжди спостерігаються під час контрольованих досліджень.
- Аналіз FAERS показав, що під час лікування ВВК клотримазол переважно асоціюється з нефротоксичністю, еконазол – з ураженнями шкіри та репродуктивною токсичністю, кетоконазол – із нефротоксичністю й проблемами зі шкірою, міконазол – із порушеннями з боку репродуктивної системи і грудних залоз, шкіри та підшкірної клітковини. Ці результати подекуди узгоджуються з даними, отриманими в попередніх дослідженнях.
- За допомогою аналізу FAERS виявлені численні НП, які потенційно можуть асоціюватися із застосуванням 4 імідазольних похідних, але відсутні в актуальних інструкціях.
- У системі FAERS міститься дуже мала кількість НП для сертаконазолу (у формі 2% крему), що може побічно свідчити про його відносну безпеку. Цей результат слід інтерпретувати з обережністю через менший розмір вибірки та меншу тривалість присутності молекули на ринку.
- Потенційно краща безпека сертаконазолу може пояснюватися особливостями структури молекули та вищою терапевтичною ефективністю.
Результати дослідження T. Zhou та співавт. підкреслюють важливість рідкісних, але тяжких побічних ефектів препаратів, які використовуються в лікуванні поверхневих грибкових інфекцій. Хоча загальна частота НП може бути низькою, їхнє клінічне значення заслуговує на ретельний розгляд, особливо у вразливих категорій пацієнтів, як-от жінки репродуктивного віку, вагітні та пацієнти з нирковою дисфункцією.
Список літератури знаходиться в редакції.
Підготував Олексій Терещенко
Медична газета «Здоров’я України 21 сторіччя» № 17 (578), 2024 р



