2 грудня, 2021
Артеріальна гіпертензія із супутніми факторами ризику: як підвищити ефективність терапії?
За матеріалами ХХІІ Національного конгресу кардіологів України (21‑24 вересня 2021 року, м. Київ)
На сьогодні артеріальна гіпертензія (АГ) являє собою одну з найважливіших проблем населення світу. Підвищений артеріальний тиск (АТ) без належного контролю може призвести до інфаркту, інсульту, ниркової чи серцевої недостатності, погіршення зору та інших ускладнень, які є небезпечними для життя. Про те, як підвищити ефективність терапії АГ і контролювати супутні фактори ризику розповідають завідувач кафедри функціональної діагностики Національного університету охорони здоров’я України імені П.Л. Шупика (м. Київ), д. мед. н., професор Олег Йосипович Жарінов і д. мед. н., професор кафедри терапії та сімейної медицини післядипломної освіти Івано-Франківського національного медичного університету Сергій Валерійович Федоров.
Важливість контролю АГ
Нещодавно були опубліковані дані об’єднаного аналізу 1201 популяційного дослідження, що включало 104 млн учасників, в якому вивчали світові тенденції прогресу в лікуванні та контролі АГ із 1990 по 2019 рр. (NCD Risk Factor Collaboration, 2021). Ось кілька ключових висновків даної роботи:
- У 2019 р. вік-стандартизоване поширення АГ (серед осіб від 30 до 79 років) становило 32% у жінок та 34% у чоловіків, подібно до показників 1990 р. (32 і 32% відповідно).
- Відбулося зростання поширеності АГ у країнах із низьким рівнем економіки та зменшення – у розвинених країнах.
- Найнижча поширеність АГ у Канаді, Перу, Японії, Тайвані й Південній Кореї.
- Належний контроль АТ 2019 р. був у 23% жінок та 18% чоловіків.
- Найкращі показники контролю АТ і лікування АГ простежувалися у країнах, як-то Південна Корея, Канада, Ісландія (лікування >70%, контроль >50%), дещо менше – у США, Коста-Риці, Німеччині, Португалії, Тайвані.
АГ – один із основних модифікованих факторів ризику серцево-судинних захворювань (ССЗ) і причина 54% інсультів та 47% кардіоваскулярних подій, пов’язаних з ішемічною хворобою серця.
Відповідно до аналізу даних 1,25 млн дорослих осіб віком від 30 років без ССЗ (1997‑2010), взятих з електронної бази CALIBER, високий систолічний АТ (САТ) збільшує імовірність розвитку інсульту на 44%, субарахноїдальної кровотечі – на 43%, стабільної стенокардії – на 41%, інфаркту міокарда – на 29%, серцевої недостатності (СН) – на 27%, захворювання периферичних артерій – на 35%, аневризми черевної аорти – на 8%.
За словами професора Федорова, ключовими цілями у лікуванні АГ, які відображені у рекомендаціях Європейського товариства кардіологів (ESC, 2018) і настанові Міжнародного товариства з гіпертензії (ISH, 2020), є:
- досягнення та підтримка цільового рівня АТ;
- модифікація чинників ризику;
- ефективне лікування супутніх хвороб.
За даними двох метааналізів, зниження САТ на 10 мм рт. ст. чи діастолічного АТ на 5 мм рт. ст. зменшує імовірність серцево-судинних (СС) ускладнень на 20%, загальної смертності – на 10‑15%, інсульту – на ~35%, вінцевих подій – на 20% і СН – на ~40% (Dena Ettehad et al., 2016; Thomopoulos et al., 2014).
Антигіпертензивні засоби: аспекти вибору
ССЗ розвиваються на п’ять років швидше на тлі АГ, тому варто якомога раніше розпочати якісне лікування для запобігання ускладненням. Головні критерії вибору антигіпертензивних засобів: ефективне досягнення цільових значень АТ, сприятлива переносимість ліків, економічна прийнятність та просте вживання (фіксована комбінація).
Основними класами препаратів для терапії АГ є (ESC, 2018):
- блокатори ренін-ангіотензин-альдостеронової системи (РААС) – інгібітори ангіотензинперетворювального ферменту (іАПФ) та блокатори рецепторів ангіотензину ІІ (БРА);
- діуретики;
- блокатори кальцієвих каналів (БКК);
- β-блокатори.
Сергій Валерійович підкреслив, що для стартової терапії більшість хворих на АГ потребують щонайменше двох гіпотензивних засобів, бажано у фіксованій комбінації. Відомо, що поєднання блокаторів РААС із БКК або тіазидними діуретиками забезпечує хороший контроль АТ і позитивно впливає на прогноз.
На додачу, в лікуванні АГ препарати групи іАПФ мають низку таких переваг і показань для застосування, як АГ, СН, безсимптомна дисфункція лівого шлуночка (ЛШ), перенесений інфаркт міокарда, хронічна ішемічна хвороба серця, цукровий діабет, хронічна хвороба нирок (Herman et al., 2020).
Одним із представників іАПФ є периндоприл, серед особливостей якого – більша специфічність щодо органів-мішеней, потужніше гальмування тканинної та плазмової форм АПФ, тривала дія, відсутність потреби у титруванні для досягнення ефективної дози та менша ймовірність гіпотензії у разі приймання першої дози. Відомі також плейотропні ефекти цієї молекули, яка при зменшенні ендотеліальної дисфункції та хронічного запалення низької інтенсивності стримує прогресування атеросклерозу різних локалізацій.
З-поміж діуретиків, які застосовують у складі комбінованої гіпотензивної терапії (тіазидних і тіазидоподібних), доцільно відзначити індапамід. Як відомо, при порівнянні індапаміду з іншими препаратами цього класу він є найбільш метаболічно нейтральним. Важливо, що за рахунок високої біодоступності індапаміду (93%) спостерігається значно триваліший ефект.
У дослідженні G.C. Roush et al. (2015) автори дійшли таких висновків:
- Індапамід знижує САТ на 54% ефективніше, ніж гідрохлортіазид (ГХТЗ). Своєю чергою хлорталідон достовірно не перевищує ГХТЗ щодо антигіпертензивної ефективності.
- Індапамід зберігає антигіпертензивну ефективність протягом 32 год, тоді як ГХТЗ – менш ніж 24 год.
- На відміну від ГХТЗ, індапамід довів здатність зменшувати індекс маси міокарда ЛШ на 17%.
- Індапамід може зменшувати мікроальбумінурію, а про ГХТЗ таких даних немає.
Через місяць після оновлення настанов ESC (2018) щодо лікування АГ B. Williams et al. (2018) опублікували роботу, в якій представили низку критеріїв стосовно оптимального вибору фіксованих комбінацій гіпотензивних засобів. Приміром, якщо у пацієнта є прояви СН і діастолічної дисфункції ЛШ, для профілактики СН краще поєднувати діуретики із блокаторами РААС. В інших ситуаціях як прогнозмодифікувальні препарати переваги мають блокатори РААС і БКК.
COVID‑19 та АГ
Також спікер не оминув дуже важливу на сьогодні проблему – СOVID‑19 та АГ як часте фонове захворювання. За прогнозами американських епідеміологів, із цією хворобою лікарі стикатимуться в жорстких межах карантинних обмежень ще принаймні до кінця 2022 р. Потім, за прогнозами, COVID‑19 перейде у ранг сезонних інфекцій.
Проте відомо, що АГ, разом з іншими вагомими кардіометаболічними факторами ризику, негативно впливає на виживання хворих із середньотяжким чи тяжким перебігом COVID‑19. За даними дослідження, проведеного у Нью-Йорку, в якому взяли участь 5700 госпіталізованих із COVID‑19 хворих на АГ, наслідки коронавірусної інфекції були такими (Richardson et al., 2020):
- 21% померли;
- 14,2% проходили лікування у відділеннях інтенсивної терапії;
- 12,2% отримували штучну вентиляцію легень;
- 3,2% потребували діалізу.
Предикторами несприятливого прогнозу, крім АГ, були такі супутні патології, як цукровий діабет, ожиріння і хронічне обструктивне захворювання легень.
Ще один метааналіз показав, що серед 44 672 пацієнтів із COVID‑19 АГ виявлено у 12,8% осіб та 39,7% померлих (Wu, McGoogan, 2020).
Які можливі механізми впливу АГ на перебіг COVID‑19? Насамперед, це надекспресія АПФ2 та активація РААС у хворих на ССЗ. Важливу роль відіграє і дисрегуляція імунної системи при АГ, а саме дисфункції цитотоксичних Т-лімфоцитів і Т-кілерів, надпродукція прозапальних цитокінів, що так само простежується при COVID‑19. Інгібітори АПФ чи БРА шляхом кращого контролю АГ здатні відновити, щонайменше частково, дисрегуляцію імунітету при АГ (Guzic, 2020).
Важливим чинником погіршення прогнозу COVID‑19 в осіб із супутньою АГ є ендотеліальна дисфункція. Препарати для лікування АГ і контролю АТ, а саме іАПФ, БРА, статини тощо, стримують прогресування ендотеліальної дисфункції та, відповідно, покращують прогноз коронавірусної інфекції (Evans et al., 2020). Зокрема, застосування фіксованої комбінації препаратів периндоприл + індапамід асоційоване із поліпшенням функції ендотелію, зокрема ендотелійзалежної вазодилатації, незалежно від гіпотензивного ефекту (Ghiadoni et al., 2009).
О.Й. Жарінов підняв важливе питання – як зменшити кількість застосовуваних препаратів і зробити лікування зручнішим для пацієнта, і не лише при первинній профілактиці, коли перенесений ІМ, стенокардія та порушення мозкового кровообігу відсутні, але й при вторинній, за наявності серйозних СС-подій. У цьому контексті лектор звернув увагу на зміни, які відбулися в підходах до первинної профілактики у рекомендаціях ESC (2021). Так, у новій настанові особливий акцент зроблено на необхідності припинення куріння та зазначено, що відмова від цієї згубної звички забезпечує найсуттєвіше збільшення очікуваної тривалості життя у молодших пацієнтів.
Щодо контролю АГ, призначення лікування на ранніх етапах також збільшує очікувану тривалість життя (при зниженні САТ на 10 мм рт. ст.). Також це стосується зниження рівня холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ). Професор наголосив, що якщо мова йде про первинну профілактику і рішення щодо використання статинів, найбільш значущих переваг слід очікувати в тих пацієнтів, які почали приймати ліпідознижувальні та антигіпертензивні ліки у віці 40‑45 років, звісно, якщо є підстави для призначення медикаментозної профілактики.
За даними метааналізу, в який було включено 48 досліджень із загальною кількістю більш ніж 340 тис. учасників, ефективне зниження АТ достовірно зменшувало імовірність розвитку СС-подій (The Blood Pressure Lowering Treatment Trialists’ Collaboration, 2021). Так, при зниженні САТ лише на 5 мм рт. ст. ризик серйозних СС-ускладнень зменшувався приблизно на 10%, незалежно від попередніх діагнозів ССЗ і навіть за нормальних або високих нормальних значень АТ. Ці результати свідчать про те, що фіксований ступінь фармакологічного зниження АТ однаково ефективний для первинної та вторинної профілактики основних ССЗ, навіть при рівнях АТ, які на даний час не розглядаються як мішені лікування.
У випробуванні PROGRESS вивчали ефективність іАПФ периндоприлу щодо зниження АТ у хворих на АГ і без такої з інсультом або транзиторною ішемічною атакою в анамнезі та, відповідно, його вплив на вторинну профілактику інсульту (MacMahon et al., 2001). Загалом 6105 осіб зі 172 медичних центрів Азії, Австралії та Європи були випадковим чином рандомізовані на групи:
- активного лікування (n=3051), що передбачало гнучкий режим на основі периндоприлу (4 мг/добу) із додаванням діуретика індапаміду на розсуд лікарів;
- плацебо (n=3054).
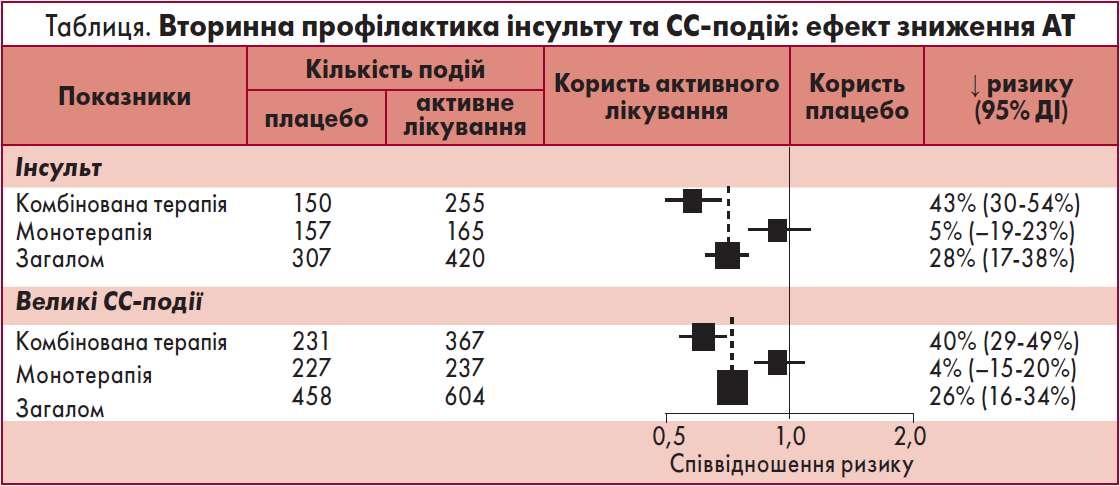
За чотири роки спостереження на тлі активного лікування (одним препаратом чи комбінацією) АТ знижувався на 9/4 мм рт. ст. Загалом 10% осіб, яким було призначено терапію, перенесли інсульт порівняно із 14% на тлі плацебо. У групі активного лікування на 26% знижувався ризик серйозних СС-подій, а також відзначалося подібне зменшення ймовірності інсульту в підгрупах з/без АГ.
При комбінованій терапії периндоприлом та індапамідом АТ знижувався на 12/5 мм рт. ст., ризик інсульту – на 43%. На тлі периндоприлу АТ знижувався на 5/3 мм рт. ст. і не привів до помітного зменшення ймовірності інсульту (таблиця).
Таким чином, було отримане ще одне свідчення суттєвих переваг фіксованої комбінації периндоприлу та індапаміду на початку антигіпертензивної терапії у пацієнтів із високим ризиком ССЗ.
Чи слід призначати статини у комплексному лікуванні АГ?
Статини являють собою потужну гіполіпідемічну терапію та впливають на ендотеліальну дисфункцію (Sever et al., 2003). У настанові ESC (2019) щодо менеджменту дорослих пацієнтів із дисліпідеміями рекомендовано призначати статини як частину комплексної стратегії первинної профілактики для хворих із підвищеним рівнем ХС ЛПНЩ та високим кумулятивним 10-річним СС-ризиком за шкалою SCORE. Варто відзначити, що первинна профілактика препаратами цієї групи приводить до значного зниження СС-захворюваності у короткостроковій та довгостроковій перспективах. Найпотужнішим із наявних на сьогодні статинів є розувастатин.
У дослідженні HOPE‑3 (2016) застосування 10 мг розувастатину сприяло зменшенню ХС ЛПНЩ на 26,5%, що супроводжувалося зниженням частоти інфаркту міокарда на 35% (р=0,02) та мозкового інсульту на 30% (р=0,02) порівняно із плацебо у пацієнтів без наявних ССЗ із двома факторами СС-ризику. Крім того, приймання статинів асоційоване з покращенням прогнозу при COVІD‑19, що є важливим для осіб із наявними чинниками СС-ризику (Kow et al., 2020).
На даний час в арсеналі лікаря наявний комбінований препарат Роксипер, до складу якого входять розувастатин, периндоприл та індапамід. Роксипер – це сучасне та просте лікування АГ і гіперліпідемії як основних факторів ризику ССЗ. Поєднання в одній таблетці трьох молекул дозволяє підвищити прихильність пацієнтів до терапії.
Отже, при дотриманні основних принципів профілактики СС-ускладнень, як-от зниження АТ і корекція резидуальних ризиків, застосування статинів дозволяє підвищити якість та тривалість життя більшості хворих.
Підготувала Мар’яна Гнатів