1 грудня, 2024
Зміна парадигми лікування пацієнтів високого та дуже високого кардіоваскулярного ризику: старт одразу з комбінації статин + езетиміб
Починаючи зі спільних рекомендацій Європейського товариства кардіології та Європейського товариства атеросклерозу з лікування дисліпідемій (2019), щодо контролю рівня холестерину ліпопротеїнів низької щільності (ХС ЛНПЩ) застосовується концепція «що нижче, то краще», яка насамперед стосується пацієнтів високого та дуже високого ризику (Mach F. et al., 2019).
Наріжним каменем ліпідознижувальної терапії (ЛЗТ) були, є і залишаються статини, яким притаманна не лише здатність знижувати рівень ХС ЛПНЩ та об’єм атером, а й низка плейотропних ефектів: протизапальна дія, покращення ендотеліальної функції, стабілізація атеросклеротичних бляшок (Oesterle A. et al., 2017). Однак, за даними дослідження DA VINCI, серед пацієнтів, які потребували вторинної профілактики, лише менше половини отримували високоінтенсивний статин у форматі монотерапії; з них лише близько 20% досягали зазначених у рекомендаціях цільових показників. Однак езетиміб було додано до лікування лише у 9% пацієнтів (Ray K.K. et al., 2020; Revankar S. et al., 2024). Сумну статистику підтверджують й інші автори: відповідно до аналізу даних 1,3 млн хворих, які отримували монотерапію статинами, цільових показників ХС ЛПНЩ досягали лише ≈30% (Allen J. et al., 2019).
Отже, більшість пацієнтів високого та дуже високого ризику не може досягти цільових показників ХС ЛПНЩ за допомогою монотерапії статинами, тому базовим правилом для таких осіб має стати комбінована ЛЗТ (Mach F. et al., 2019; Packard C.J. et al., 2021). Застосування комбінованої ЛЗТ у хворих найвищого ризику забезпечує значні клінічні переваги і є фармакоекономічно доцільним (Annemans L. et al., 2018). Останнє підтвердили і нещодавно опубліковані результати дослідження JaZ, відповідно до яких негайний початок лікування статином та езетимібом при госпіталізації пацієнтів з інфарктом міокарда (ІМ) з елевацією сегмента ST (STEMI) асоціювався з меншою частотою значущих кардіоваскулярних подій упродовж 2 років спостереження, отже, з меншими сумарними витратами на медичну допомогу (Haertel F. et al., 2024).
Слід зауважити, що покроковий підхід, запропонований у рекомендаціях Європейського товариства кардіології та Європейського товариства атеросклерозу з лікування дисліпідемій (2019), неминуче відтерміновує досягнення цільових показників ліпідного профілю, оскільки передбачає значну кількість поетапних кроків. Цьому можна запобігти, одразу призначаючи комбіновану терапію високоінтенсивним статином та езетимібом пацієнтам екстремально високого і дуже високого ризику (рис. 1). Після 3 місяців комбінованої терапії доцільно оцінити відповідь хворого на лікування та (за потреби) додати третій пероральний або ін’єкційний засіб. Така тактика дозволить зменшити кількість етапів ЛЗТ і збільшити частку пацієнтів, які досягнуть цільових показників. Дані досліджень підтверджують перевагу початку гіпохолестеринемічного лікування з комбінованої терапії, оскільки свідчать, що зв’язок між умістом ХС ЛПНЩ і кардіоваскулярними наслідками залежить не лише від величини зниження ХС ЛПНЩ, а й від його тривалості (Ray K.K. et al., 2024). Обсерваційні дослідження доводять, що стартове призначення комбінованої терапії дозволяє зменшити смертність, наприклад, у пацієнтів із гострим коронарним синдромом (ГКС) (Lewek J. et al., 2023).
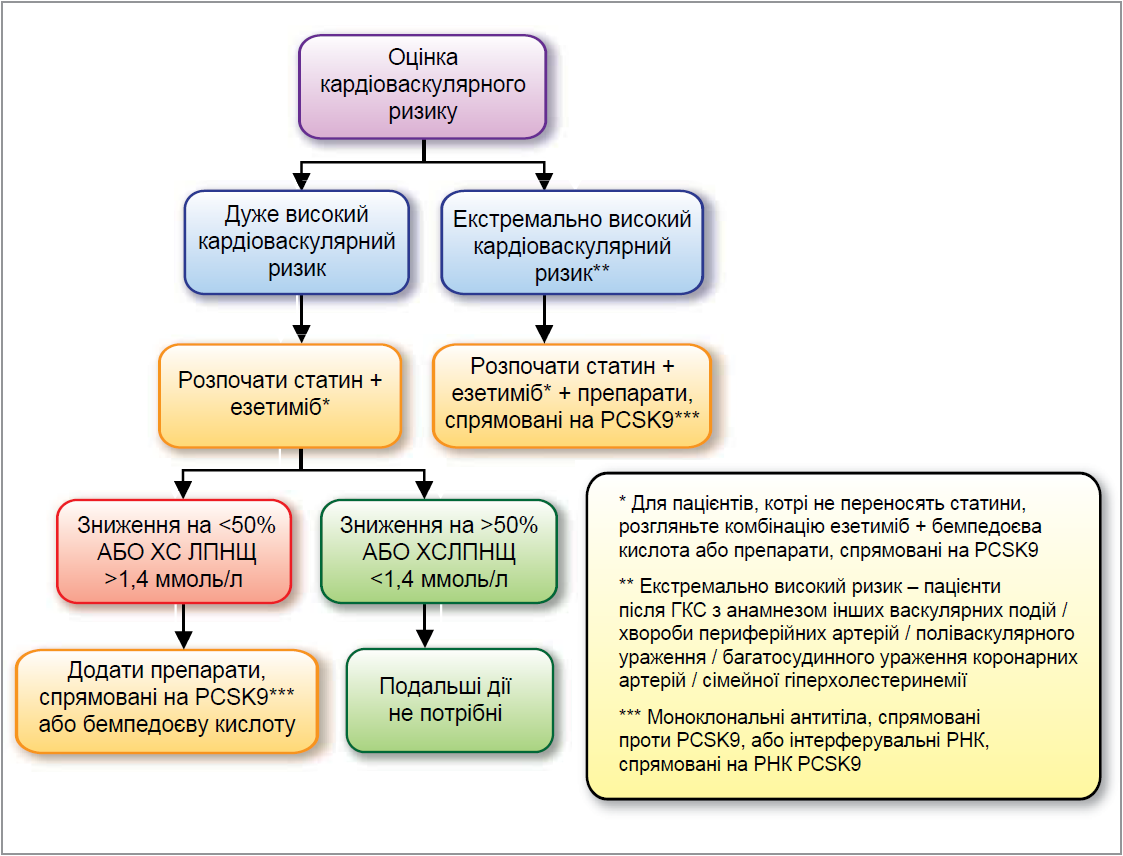 Рис. 1. Комбінована ЛЗТ як стратегія першої лінії для пацієнтів високого та дуже високого ризику (за Ray K.K. et al., 2021)
Рис. 1. Комбінована ЛЗТ як стратегія першої лінії для пацієнтів високого та дуже високого ризику (за Ray K.K. et al., 2021)
Примітка: PCSK9 – інгібітори пропротеїнової конвертази субтилізин-кексинового типу.
Усе більше як окремих наукових колективів, так і фахових товариств погоджуються, що прийшов час змінити парадигму ЛЗТ, визнавши переваги стартової комбінованої терапії у пацієнтів найвищого ризику, а також максимально раннє запровадження нестатинових ліпідознижувальних препаратів (Revankar S. et al., 2024).
На цьогорічному конгресі Європейського товариства кардіології було представлено аналіз даних дослідження SWEDEHEART (n=46 518), який доводить, що інтенсивне зниження рівня ХС ЛПНЩ одразу під час госпіталізації щодо ІМ через 1 рік забезпечує кращі клінічні наслідки, ніж застосування покрокового підходу (рис. 2).
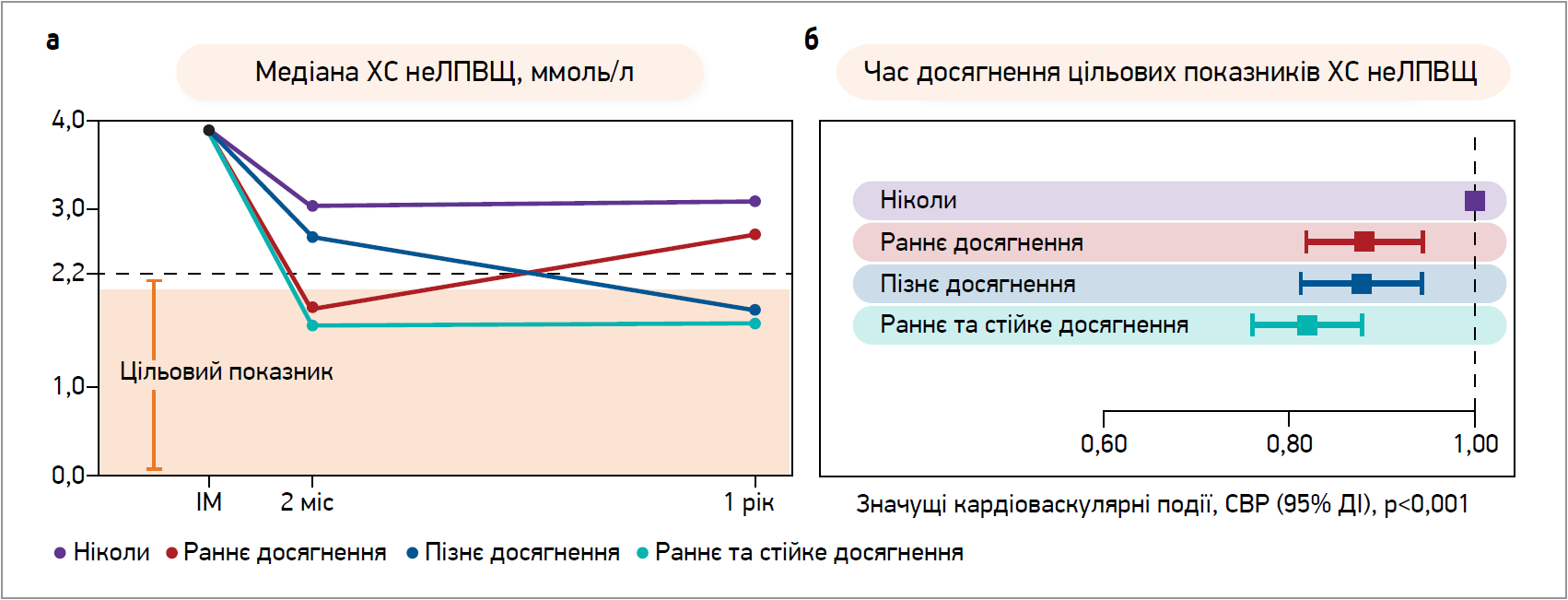 Рис. 2. Час досягнення цільових показників ХС неЛПВЩ і тривалість перебування в їхніх межах (а); відношення ризику значущих кардіоваскулярних подій (смерть від усіх причин, ІМ, ішемічний інсульт) (б)
Рис. 2. Час досягнення цільових показників ХС неЛПВЩ і тривалість перебування в їхніх межах (а); відношення ризику значущих кардіоваскулярних подій (смерть від усіх причин, ІМ, ішемічний інсульт) (б)
Примітки: СВР – стандартизоване відношення ризику; ДІ – довірчий інтервал.
Так, у пацієнтів, яким упродовж 2 міс після госпіталізації вдалося знизити ХС не ліпопротеїнів високої щільності (неЛПВЩ) на >2,2 ммоль/л, протягом року після ІМ спостерігався на 28% нижчий ризик значущих кардіоваскулярних подій. На думку авторів цього аналізу, не варто чекати контрольного візиту пацієнта, щоб додати езетиміб або інгібітори пропротеїнової конвертази субтилізин-кексинового типу (PCSK9). Натомість в осіб після ГКС, у пацієнтів з екстремально високим кардіоваскулярним ризиком і сімейною гіперхолестеринемією одразу слід розпочинати лікування з комбінації високоінтенсивного статину з езетимібом (Schubert J. et al., 2024).
Також під час проведення конгресу Європейського товариства кардіології (2024) відомий польський учений, член Міжнародної робочої групи експертів з ліпідології M. Banach представив дані польського реєстру пацієнтів після ГКС, відповідно до яких негайне призначення комбінованої ЛЗТ забезпечувало достовірно меншу смертність від усіх причин упродовж 3 років спостереження порівняно з високоінтенсивною монотерапією статином. Значуща відмінність між групами лікування фіксувалася вже через 52 дні.
Переваги комбінованого гіпохолестеринемічного лікування виявило і дослідження SANTORINI (n=9559), яке включало пацієнтів із високим та дуже високим кардіоваскулярним ризиком із 14 європейських країн. Протягом 1 року спостереження ескалація ЛЗТ проводилася в ⅓ пацієнтів. Серед осіб, які не отримували ЛЗТ на момент початку дослідження, монотерапія через 1 рік зумовила досягнення цільових показників ХС ЛПНЩ у 27,5% хворих, а комбінована терапія – в 39,9%. Схожий результат було отримано для осіб, які отримували ліпідознижувальні препарати на початку дослідження: через 1 рік застосування монотерапія забезпечила цільові рівні ХС ЛПНЩ у 25,5% учасників, а комбінована терапія – в 39,4% (Ray K.K. et al., 2024).
До популяції осіб дуже високого ризику належать пацієнти з анамнезом декількох значущих, зумовлених атеросклеротичними серцево-судинними захворюваннями, подій або однієї значущої події та декількох станів, асоційованих із високим ризиком (вік ≥65 років, гетерозиготна сімейна гіперхолестеринемія, сімейний анамнез черезшкірного втручання або аортокоронарного шунтування, цукровий діабет, хронічна хвороба нирок, куріння на цей момент, стійко підвищений уміст ХС ЛПНЩ ≥2,6 ммоль/л, незважаючи на вживання максимальних переносимих доз статину та езетимібу, застійна серцева недостатність) (Grundy S.M. et al., 2018). Запропоновано також вважати пацієнтами дуже високого ризику осіб із умістом коронарного кальцію >300 одиниць Агатстона або вище 75-го перцентиля для відповідної демографічної категорії (Lloyd-Jones D.M. et al., 2022). У разі високих показників коронарного кальцію (навіть у пацієнтів проміжного ризику) доцільно рано призначати комбіновану терапію (Revankar S. et al., 2024).
Езетиміб, схвалений для ЛЗТ у 2002 р., у формі монотерапії здатен знижувати рівень ХС ЛПНЩ на 20%. Дослідження EXPLORER показало, що застосування комбінації розувастатину (40 мг) та езетимібу (10 мг) у пацієнтів дуже високого ризику вже через 6 тиж знижувало вміст ХС ЛПНЩ на 70%; натомість монотерапія розувастатином забезпечувала зниження лише на 57%. Оптимального рівня ХС ЛПНЩ досягли 80% групи комбінованого лікування та 35% групи монотерапії (Ballantyne C.M. et al., 2007). Переваги комбінованого лікування статином та езетимібом значно перевищують просте зниження ліпідних показників. Така комбінація спроможна знижувати кардіоваскулярну смертність у пацієнтів, госпіталізованих щодо ГКС, а також покращує переносимість лікування в осіб, які не толерують статинотерапію. Так, під час проведення дослідження I-ROSETTE виявлено, що комбінація езетимібу та 5 мг розувастатину забезпечує зіставний зі 20 мг розувастатину ліпідознижувальний ефект (-55 проти -51%) (Hong S. et al., 2018). Схожі дані отримано і в дослідженні RACING (Kim B.K. et al., 2022).
Дані щодо ефективності комбінованої терапії підтримують і результати інтраваскулярного ультразвукового дослідження, які демонструють здатність комбінованої терапії не лише зупиняти прогресування атеросклерозу, а й зменшувати об’єм атероми значно потужніше, ніж монотерапія статином (78 проти 58%; p=0,004) (Tsujita K. et al., 2015). Цьогорічний метааналіз Y.-J. Zhang і співавт. продемонстрував, що комбінація статин + езетиміб знижує сумарний об’єм атером (отже, і загальний тягар атеросклерозу) потужніше, ніж монотерапія статинами.
Важливим контингентом для застосування комбінації статин + езетиміб є пацієнти з атеросклеротичними серцево-судинними захворюваннями та цукровим діабетом 2 типу. Незалежно від дози та типу застосовуваного статину систематичне додавання езетимібу дозволяє майже подвоїти кількість пацієнтів, які досягають цільового рівня ХС ЛПНЩ (Lavalle Cobo A. et al., 2024).
Нещодавно під час проведення обсерваційного дослідження виявлено, що стартове призначення комбінації статину та езетимібу дозволяє досягти достовірно нижчих показників смертності вже через 1 рік (5,9 проти 3,9%; p=0,041), а через 3 роки виразність ефекту виявилася ще потужнішою (10,2 проти 5,5%; p=0,024) (Lewek J. et al., 2023).
Незважаючи на те що дослідження однозначно доводять медичні та фармакоекономічні переваги стартового застосування комбінованого лікування в осіб високого та дуже високого ризику, впровадження цієї стратегії у реальну клінічну практику й досі є незадовільним. Імовірно, це обумовлено т. зв. клінічною інерцією – неспроможністю розпочати або інтенсифікувати лікування тоді, коли це потрібно.
Стартове застосування комбінації статин + езетиміб скорочує поетапний підхід до досягнення цільового рівня ХС ЛПНЩ на один крок, що значно прискорює отримання результату, отже, покращує кардіоваскулярні наслідки. Така стратегія є доцільною в пацієнтів високого та дуже високого ризику, які потребують не лише значного, а і якнайшвидшого зниження вмісту ХС ЛПНЩ. Ліпідознижувальні переваги комбінованої терапії реалізуються вже через 4-5 тиж (Kakara M. et al., 2014). Для подолання клінічної інерції слід підвищувати обізнаність лікарів-клініцистів із можливістю старту одразу з комбінації статин + езетиміб із метою пришвидшення досягнення цільових ліпідних показників і покращення прогнозу в пацієнтів найвищого ризику (Revankar S. et al., 2024).
В Україні розувастатин представлений, зокрема, європейським препаратом Розуліп® (фармацевтичний завод «Егіс», Угорщина) та комбінацією Розуліп® Плюс. Розуліп® наявний у дозах 10 та 20 мг, а Розуліп® Плюс передбачає комбінацію аналогічних доз із 10 мг езетимібу. З огляду на дані клінічних досліджень і новітні погляди на ЛЗТ у пацієнтів низького та середнього ризику доцільно застосування Розуліпу®, а у випадку високого і дуже високого ризику варто розпочати ЛЗТ одразу із Розуліпу® Плюс.
Підготувала Лариса Стрільчук
Медична газета «Здоров’я України 21 сторіччя» № 19/1 (581), 2024 р



